
Man schwebt inmitten eines grenzenlosen, dicht gedrängten Netzwerks aus blassblau leuchtenden Sauerstoffsphären, deren nächste Nachbarn in einem Abstand von nur 2,75 Ångström fast körperlich nah wirken – so nah, dass die Grenze zwischen dem eigenen Blickfeld und der umgebenden Materie vollständig aufgelöst scheint. Von jedem Sauerstoffkern strecken sich zwei weißlich glänzende Protonenfortsätze unter einem Winkel von 104,5° heraus, und zwischen benachbarten Molekülen spannen sich zartcyanfarbene Wasserstoffbrücken, die in einem Rhythmus von Pikosekunden reißen und neu entstehen – zu schnell für echte Bewegung, wahrnehmbar nur als ein dauerhaftes, leises Flimmern. Das gesamte Gitter atmet mit thermischer Unruhe: Jede Sphäre oszilliert mit feiner, schneller Amplitude, und diese Schwingung pflanzt sich als kollektives Zittern durch das Netzwerk fort, als hätte flüssiges Wasser bei 300 Kelvin einen eigenen molekularen Herzschlag. Bereits nach wenigen Moleküldurchmessern – jenseits von drei bis vier Nanometern – verdichtet sich die Szenerie zu einem tiefen Indigodunst aus überlappenden Elektronenwolken, sodass das visuelle Feld sich auf eine Handvoll vollständig aufgelöster Wassermoleküle beschränkt, bevor die Welt in transluzente Tiefe zerfließt. Diese scheinbar vertrauteste aller Substanzen offenbart sich auf dieser Ebene als ein fremdartig lebendiger Kristallkosmos ohne Horizont, ohne Boden, ohne Schwerkraft – nur das unaufhörliche, isotrope Pulsieren des Wasserstoffbrückennetzwerks, das in alle Richtungen gleichermaßen reicht.

Der Blick gleitet über eine endlose, gefrorene Ebene aus semitransparenten Sechsecken, die sich in einem präzisen Fischgrätmuster nach allen Seiten ausdehnen – flache aromatische Ringe, abwechselnd um etwa 55 Grad gekippt, wie Pflastersteine einer uralten Kathedrale aus Bernstein und Rauchquarz. Über und unter jeder Scheibe schwebt ein zarter Doppelschleier aus violett-goldenem Licht, die π-Elektronenwolke, die sich zu beiden Seiten der Molekülebene als hauchzarte Loben materialisiert und sich in den engen Zwischenräumen von kaum 3,5 Ångström zu einem gemeinsamen Leuchten verbindet – CH–π-Wechselwirkungen zwischen Ringkante und Ringfläche, die das gesamte Kristallgitter in geometrischer Disziplin halten. Das innere Licht ist golden und flach, wie eine Wintersonne tief hinter dem Gitter, und wirft lange Schattenstreifen über das Fischgrätmuster, während ferne Reihen identischer Moleküle in einem kontinuierlichen Bernstein-Violett-Dunst verschwimmen, als würde man durch ein riesiges facettiertes Mineral blicken. Bei 175 Kelvin ist das Kristallgitter nahezu unbeweglich, die Gitterschwingungen auf quantenmechanisches Zittern reduziert – und nur vereinzelte dunkle Lücken, vakante Gitterplätze, stören das sonst makellose periodische Mosaik, ihre Nachbarmoleküle leicht aus dem Lot geraten, ihre π-Halos dem Nichts entgegengeneigt wie Flammen im Zug.

Der Blick öffnet sich in einem schummrigen, wächsernen Raum, der sich in vollkommener bilateraler Symmetrie nach oben und unten erstreckt – man schwebt im absoluten Mittelpunkt einer DPPC-Lipiddoppelschicht, umgeben von einem dunkel-kohlegrauen Void, wo die Methylendgruppen der gegenüberliegenden Monolagen sich kaum berühren. Langsam steigen aus diesem öligen Nebel die silbergrauen Schäfte der gesättigten Fettsäureketten auf – jede ein Korridor aus dicht gepackten CH₂-Einheiten, gelegentlich unterbrochen von einem gelblich-grünen Knick einer Doppelbindung, die das Licht streut wie ein Gelenk aus warmem Bernstein. Weiter oben markiert eine durchscheinende Übergangszone aus glänzenden Glycerinrückgrat-Knoten die geochemische Grenze zwischen der unpolaren Innenwelt und der geladenen Außenwelt, eine Gesteinsschicht aus elektronendichten Estergruppen, so klar gezeichnet wie eine Sedimentlage im Querschnitt. Dann explodiert die Welt in Farbe: dicht gedrängte, orangeglühende Phosphatgruppen und himmelblau leuchtende Cholinköpfe werden von einem flimmernden, blau-weißen Wasserfilm überlagert, dessen Wasserstoffbrückennetzwerk sich in ständigem Aufbau und Zerfall befindet. Die gesamte Doppelschicht misst kaum vier Nanometer – und fühlt sich von innen an wie die Tiefe eines Ozeangrabens.

Der Besucher steht auf dem Boden einer engen Schlucht aus lebendiger Chemie: Links und rechts erheben sich bronzefarbene Deoxyribose-Pentagonringe in gleichmäßig gerippten Bögen, durchbrochen von rostorangen Phosphat-Tetraedern, deren wasserbefilmte Oberflächen das diffuse Blaulicht der Rille zerstreuen. Der Boden dieses Canyons ist aus horizontalen Schichten gestapelter Basenpaar-Scheiben gepflastert – blaugrünes Adenin gegenüber ocker-braunem Thymin, waldgrünes Guanin gegenüber lavendelfarbenem Cytosin –, jede Lage von einem haarfeinen π-Stapelspalt von 3,4 Ångström abgetrennt, einem Schatten so schmal wie das Unmessbare. Entlang der Phosphatwände zieht sich eine Perlenkette aus Wassermolekülen, jede durch Wasserstoffbrücken mit dem nächsten verbunden, ein biolumineszentes Ornament, das die negativ geladene Rückgratwand mit eisblauem Schimmer belegt. Die Atmosphäre hat Gewicht: ein elektrisch aufgeladenes, feuchtes Medium, in dem das elektrostatische Feld als kobaltblaue Lichtnebel sichtbar wird und alles Feste in einem ununterbrochenen thermischen Zittern zu stehen scheint – als könne die Geometrie des Augenblicks jeden Moment in eine neue Form fallen.

Der Blick führt entlang der zentralen Achse einer Alpha-Helix, einem der fundamentalsten Bauelemente des Lebens: eine rechtsgängige Spirale aus verketteten Aminosäuren, bei der jede Windung 3,6 Reste umfasst und eine Steigung von 5,4 Ångström aufweist. Die tiefroten Carbonyl-Sauerstoffatome und die bläulichen NH-Gruppen des Peptidrückgrats bilden eine skulpturale Innenwand, zusammengehalten durch Wasserstoffbrücken, die jeweils das vierte Residuum voraus verbinden – elektrostatische Fäden von 2,06 Ångström Länge, deren rosafarbenes Leuchten die gespeicherte Bindungsenergie sichtbar macht. Die leuchtend gelbgrünen Leucin- und Isoleucin-Seitenketten ragen wie kristalline Dornen radial nach außen, ihre unpolaren Oberflächen stoßen das umgebende Wasser ab und hinterlassen einen trockenen Schimmer inmitten des warmen, bernsteinfarbenen Lösungsmittels. Das gesamte Bauwerk flimmert in der thermischen Bewegung seiner Atome – jede Schwingung eingefroren in einem Augenblick von wenigen Femtosekunden –, während das blau-weiße Leuchten der Elektronendichte entlang jeder kovalenten Bindung den spiralförmigen Korridor von innen heraus erhellt, als trüge die Materie selbst ihr Licht.

Der Blick stürzt senkrecht in die kristallographische c-Achse des hexagonalen Eises Ih, und was sich offenbart, ist eine endlose Kathedrale aus Sechsecken – Ring um Ring aus Wassermolekülen, die sich in makelloser Symmetrie bis in eine blauschwarze Tiefe verlieren. Jedes Sauerstoffatom sitzt wie ein opalisierender Knoten an seinem Gitterplatz und ist über vier Wasserstoffbrücken von je 2,76 Å mit seinen Nachbarn verbunden, wobei der Tetraederwinkel von 109,5° die gesamte dreidimensionale Architektur bestimmt – eine Geometrie, die das Wasser zwingt, sich weniger dicht zu packen als flüssiges Wasser, was dessen anomale Dichte erklärt. An jedem dieser lumineszierenden Brücken hängt eine subtile Unschärfe: Das Proton ist nicht eindeutig lokalisiert, sondern existiert als probabilistischer Doppelschatten, der sichtbare Fingerabdruck der Pauling'schen Eisregeln, nach denen jedes Molekül genau zwei Protonen nah und zwei fern hält, ohne globale Ordnung zu erzwingen. Die hexagonalen Kanäle entlang der c-Achse öffnen sich als samtschwarze Schlünde struktureller Leere – keine Lücken aus Zufall, sondern geometrische Notwendigkeit, durch die das Gitter atmet. Bei −10 °C ist die thermische Energie noch groß genug, um die Konturen der fernsten Moleküle in einen türkis-indigo Schimmer aufzulösen, als würde das gesamte Kristallgitter in einer kollektiven Vibration unmerklich zittern.

Der Blick wandert von unten durch einen endlosen Wald aus gestapelten Coronenmolekülen, deren tief bernsteinfarbene aromatische Scheiben — jede knapp neun Ångström im Durchmesser — sich in einem regelmäßig hexagonalen Kristallgitter bis in einen warmen, dunstigen Fluchtpunkt nach oben erstrecken. Coronene, polyzyklische aromatische Kohlenwasserstoffe aus zwölf kondensierten Sechsringen, ordnen sich in organischen Kristallen durch π-π-Wechselwirkungen zu präzisen Säulen, wobei die Ebenenabstände von 3,4 Ångström — der klassischen van-der-Waals-Stapeldistanz konjugierter Systeme — dafür sorgen, dass die delokalisierten Elektronenwolken benachbarter Scheiben zu einem einzigen leuchtenden Membranring verschmelzen. Zwischen den Säulen füllt ein kühler grau-blauer Dunst den Raum: das volumetrische Abbild schwacher, richtungsloser van-der-Waals-Dispersionskräfte, die — ohne Ladung, ohne gerichtete Bindung — allein durch fluktuierende Dipolmomente die Kristallpackung zusammenhalten. Immer wieder zuckt ein elektrisch-oranges Aufleuchten durch eine Scheibengrenze: ein Polaron, ein durch Gitterverzerrung selbst eingefangener Ladungsträger, der durch thermisch aktiviertes Hopping von Scheibe zu Scheibe wandert und für den organischen Halbleitern typischen intermolekularen Ladungstransport sorgt. Man steht in einem Kathedralenschiff aus lebendigem Licht, in dem Größe keine menschliche Bedeutung mehr trägt — ein einziger dieser bernsteinfarbenen Ringe ist kaum breiter als zehn Kohlenstoff-Kohlenstoff-Bindungen hintereinander.

Der Blick reicht in einen Tunnel, dessen Wände sich wie das Innere einer lebenden Kathedrale um den Betrachter schließen – gerippte Spiralsäulen aus ribosomaler RNA wölben sich in Schichten aus dunklem Kobaltblau und tiefem Blaugrün, ihre Phosphat-Zucker-Rückgrate in enge Längsrillen gepresst, und die Geometrie des Raumes verengt sich voraus zu einer Engstelle von kaum zehn Ångström Durchmesser, einem molekularen Nadelöhr, durch das kein Atom ohne weiteres passt. In rhythmischen Abständen setzen Magnesiumionen grelle gelbweiße Lichtpunkte gegen die dunkle Phosphatmatrix, denn jedes zweifach positiv geladene Ion neutralisiert die elektrostatische Abstoßung benachbarter RNA-Stränge und macht den Tunnel überhaupt erst stabil genug, um ein naszierendes Polypeptid zu führen. Durch die Mitte dieses Kanals windet sich die frisch synthetisierte Peptidkette in warmem Bernsteinlicht, Aminosäure um Aminosäure aus dem peptidyltransferalen Zentrum darüber entlassen, stellenweise bereits zu ersten α-helicalen Windungen geordnet, deren Wasserstoffbrücken als hauchfeine Leuchtfäden aufblitzen. Am Rand des Tunnels versetzen tealfarbene Schimmer – flüchtige Signale der GTP-Hydrolyse – die molekulare Stille in Intervallen von Femtosekunden, und das gesamte Bild ist nicht von außen beleuchtet, sondern glüht von innen, gespeist allein durch die chemische Energie und das thermische Rauschen, das jeden Ångström dieses Raums durchdringt.
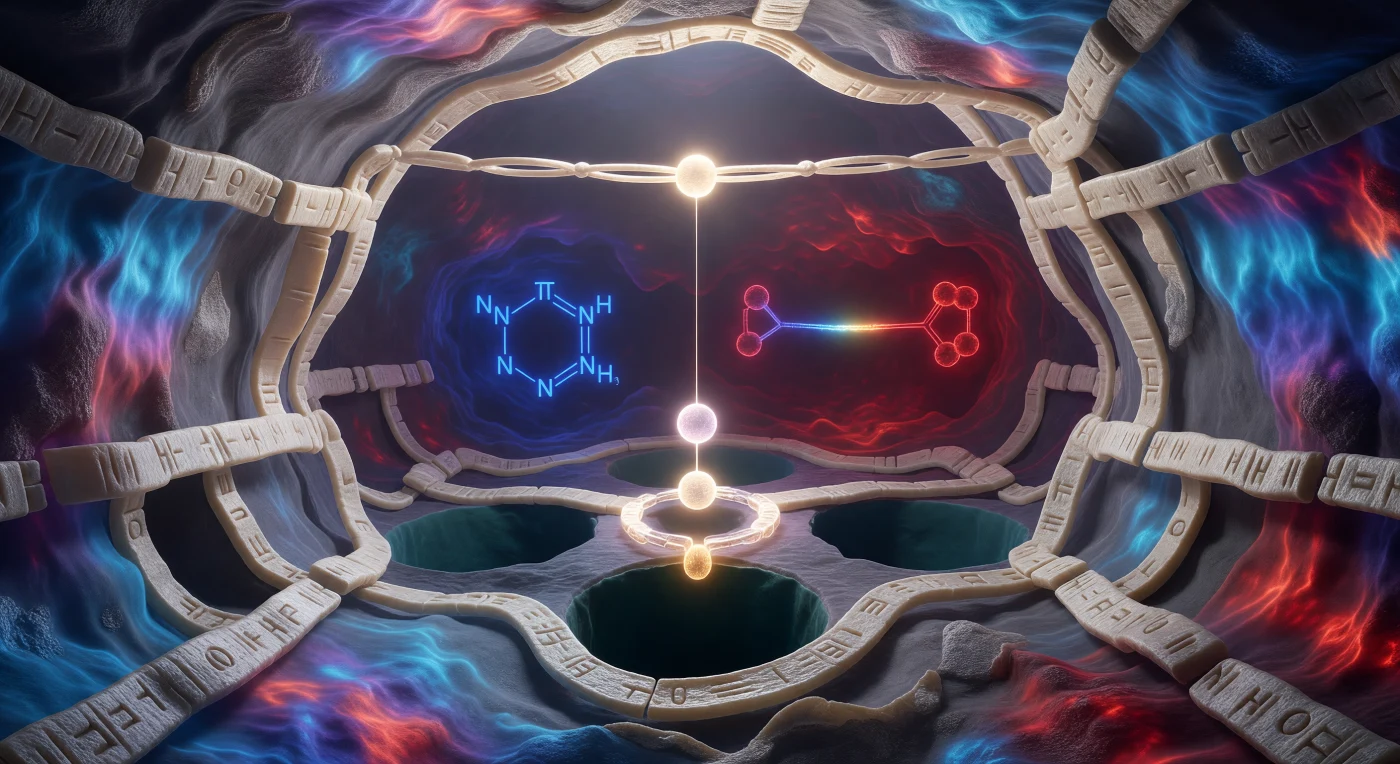
Wer an der Schwelle dieser molekularen Höhle steht, blickt in einen kaum fünfzehn Ångström weiten Kathedralenraum aus Protein — die Wände aus blassem Beta-Faltblatt wölben sich wie polierter Knochen, ihre Oberfläche von einer thermischen elektrostatischen Potentialkarte in ein kontinuierliches Farbenspektrum getaucht, das von kühlem Coelinblau über Violett bis in glutrotes Scharlach an den ladungsdichten Rückwänden zieht. Im Innern des aktiven Zentrums der Serinprotease Trypsin sind drei Residuen wie Altarbilder einer katalytischen Kathedrale angeordnet: das Hydroxyl-Sauerstoffatom von Serin 195 leuchtet in einem chirurgisch-weißen Goldton und richtet seine freien Elektronenpaare auf das Substrat, der Histidin-Imidazolring schwebt in elektrischem Kobaltblau als Protonenshuttle zwischen zwei Zuständen, und das Aspartat-Carboxylat pulsiert in tiefem Karmesin an der Rückwand — die drei Glieder eines Ladungs-Relais, das in Lichtgradienten allein geschrieben ist. Über dem Scheitel der Höhle spannt sich die spaltbare Peptidbindung des Substrats wie eine leuchtende Brücke, ihr Carbonyl-Kohlenstoff hängt in einem geometrisch erzwungenen Abstand von kaum drei Ångström über dem Serinoxygen — eine elektrostatische Spannung, die Reaktant und Produkt durch schiere Nähe trennt. Alles zittert: Bindungsschwingungen in der Größenordnung von Femtosekunden, Wasserstoffbrücken, die in Pikosekunden brechen und sich neu knüpfen, die van-der-Waals-Radien jedes Atoms als fühlbar körnige Topographie, die den Betrachter in einem Ausschlussvolumendruck einschließt, der weniger gesehen als gespürt wird.

An der Kante dieses suspendierten Graphenblattes trennt eine einzige Linie aus Kohlenstoffatomen – gerade einen Atomdurchmesser dick – zwei absolute Wirklichkeiten voneinander: auf der einen Seite das kalte Nichts des Vakuums, auf der anderen eine unendliche silberblaue Ebene aus hexagonalem Kohlenstoffgitter, das sich bis zu allen Horizonten erstreckt. Jeder der C-C-Bindungsabstände von 1,42 Å bildet einen Knotenpunkt im Geflecht, durch den das delokalisierte π-Elektronen-System wie ein luminöser Film oberhalb und unterhalb der Atomebene schimmert – ein metallischer Glanz, kalt und präzise wie poliertes Platin. Lange Biegewellen aus thermischen Phononenschwingungen – mit Wellenlängen von zehn bis hundert Nanometern – lassen die mathematisch flache Oberfläche sanft atmen, als läge sie zwischen Bewegung und Stille eingefroren. Inmitten dieser makellosen Symmetrie glüht ein Stone-Wales-Defekt warm orange heraus: Dort hat eine Bindungsrotation ein Fünfeck-Siebeneck-Paar erzeugt, dessen lokalisierte elektronische Zustände Energie konzentrieren und wie eine eingebettete Glut gegen das silberne Gitter leuchten, bevor die perfekte Sechseckordnung sich nach wenigen Ringabständen wieder durchsetzt.

Im Zentrum des Blickfelds brennt das Na⁺-Ion wie eine komprimierte Sonne – eine harte, goldweiße Sphäre kaum größer als eine Murmel, die keinen Wärmeglanz ausstrahlt, sondern elektrostatischen Druck, der den umgebenden Raum auf weniger als einem Nanometer zusammenzieht und jeden Grenzfläche in schneidender Schärfe enthüllt. Die sechs Wassermoleküle der ersten Hydratationshülle stehen in perfekter oktaedrischer Geometrie eingefroren, ihre Sauerstoffenden dem Ion zugewandt und in einem tiefen Cerulean-Violett leuchtend, wo die Elektronendichte im Feld der positiven Ladung konzentriert wird – ein Blaulicht, das keine Wärme kennt, sondern verstärkte Dipolausrichtung und beschränkte Wasserstoffbrückendynamik anzeigt. Der Abstand zwischen Ion und erster Hülle beträgt nur 2,36 Å, ein elektrisch gespannter Korridor, der bei dieser Skalierung wie ein glimmender Spalt aus reiner elektrostatischer Feldstärke wirkt, kaum breiter als das Nichts zwischen zwei Atomorbitalen. Dahinter weitet sich die zweite Hydratationshülle bei etwa 4,5 Å zu einem diffuseren Gürtel aus zwölf bis achtzehn teilweise ausgerichteten Molekülen, deren Ordnung schon von thermischen Stößen zernagt wird, bevor das Wasserstoffbrückennetzwerk des freien Wassers jenseits von 7 Å in ein dunkles, chaotisch flackerndes Tief-Cerulean zerfällt – ein ozeanisches Rauschen aus molekularem Lärm, das jede Erinnerung an die Ordnung des Ions ausgelöscht hat.

Im dichtesten Inneren eines gefalteten Proteins bewegt man sich durch ein lückenloses Mosaik aus Leucin-, Isoleucin- und Valin-Seitenketten, deren verzweigte Kohlenwasserstoffgerüste in warmem Bernstein- und Elfenbeinton leuchten und sich in C–C-Kontakten von 3,5 bis 4,0 Å berühren – eine Packungsdichte, die jener von geschliffenem Edelstein nahekommt und durch van-der-Waals-Wechselwirkungen zusammengehalten wird. Flache Phenylalanin-Ringe ordnen sich in versetzten Stapeln an, ihre delokalisierten π-Elektronen erzeugen ein kaltes, phosphoreszierendes Leuchten, während ein tiefes Blaugrün das bicyclische Indolringsystem eines Tryptophans markiert, dessen π-Elektronenwolke eine türkisfarbene Aura auf die benachbarten Ketten wirft. Ein vergrabener Methionin-Schwefel fängt das spärliche Licht und gibt es als scharfes Goldgelb zurück, ein metallischer Akzent inmitten der organischen Texturen. Am äußersten Rand der Wahrnehmung, kaum fünfzehn bis zwanzig Ångström entfernt, löst sich die enge Packung unmerklich auf: Durch die sich weitenden Zwischenräume dringt ein diffuser kühler Blaugrauschimmer herein – die hydrophile Proteinoberfläche und das wasserstoffbrückenvernetzte Bulk-Wasser jenseits der Proteinhülle, eine andere Welt, durch die hydrophobe Kernregion so vollständig versiegelt wie ein Fossil im Bernstein.

Die Oberfläche des Viruskapsids breitet sich in jede Richtung aus wie die Kruste eines kristallinen Miniaturplaneten – fünfblättrige Pentamere und sechsblättrige Hexamere pflastern das geschwungene Terrain in einer mathematisch strengen Symmetrie, deren leuchtend-weiße Immunodominanzschleifen sich über tiefblaue Rezeptorbindungsmulden erheben wie Gebirgskuppen über glaziale Seen. Dieses Gebilde ist kein starres Objekt, sondern ein T=3-Ikosaeder aus 180 identischen Hüllprotein-Untereinheiten, deren präzise verzahnte Kontaktflächen durch Salzbrücken gesichert werden – jene rot-blauen elektrostatischen Funken an den Nahtstellen zwischen Aspartat-Sauerstoff und Lysin-Stickstoff, die das gesamte 28 Nanometer große Gerüst mit einer Spannung durchziehen, die weder Schraube noch Klebstoff ersetzen könnten. Eine zwei bis drei Nanometer dicke geordnete Hydratationsschicht überzieht jede Erhebung und jede Vertiefung mit einem opalisierenden Schimmer, denn die Wassermoleküle sind hier nicht frei, sondern durch Wasserstoffbrückennetzwerke in quasikristalline Hüllen gebunden, die jede Proteinkontur getreulich nachzeichnen. Das wärmliche Bernsteinorange der hydrophoben Kontaktzonen zwischen den Untereinheiten erinnert daran, dass diese vergrabenen unpolaren Residuen energetisch unter latenter Spannung stehen – hinausgedrängt vom umgebenden Wasser, aber fest in das Innere des Verbandes gezogen, wo sie die Triebkraft des hydrophoben Effekts in strukturelle Stabilität verwandeln. Alles hier vibriert: Jede Bindung schwingt im Femtosekundenrhythmus, jede Seitenkette fluktuiert, und die gesamte Kapsidhülle atmet in thermischen Mikrobewegungen, die dem Terrain eine fast geologische Lebendigkeit verleihen – geduldig, präzise und von kolossal komprimierter Energie durchdrungen.

Der Blick führt direkt in die Achse einer Kollagen-Tripelhelix – drei ineinandergewundene Polypeptidketten in Bernstein, Tiefblau und Jadegrün schrauben sich in einem rechtsgängigen Supercoil in die Tiefe, während jede einzelne Kette für sich als linksgängige Polyprolin-II-Helix aufgebaut ist. Im Zentrum dieser molekularen Kathedrale berühren sich die Glycinreste der drei Stränge beinahe – mit einem Cα–Cα-Abstand von nur 3,9 Ångström trennt sie kaum mehr als ein einzelnes Wasserstoffatom. Nach außen ragen die pyrrolidinförmigen Ringe von Prolin und Hydroxyprolin in rhythmischer Abfolge hervor und verleihen der Oberfläche eine tiefe, rindenartige Textur, die an nanometerkleine Baumrinde erinnert. Zwischen den Strängen weben goldene Interchain-Wasserstoffbrücken und aquamarinfarbene Hydroxyprolin-Wasserbrücken ein sekundäres Netzwerk aus Licht und Bindungsenergie – ein in sich leuchtendes Geflecht, das die drei Helices in präziser geometrischer Registrierung hält. Die 8,7-Ångström-Helixwiederholung lässt in regelmäßigen Abständen eine vollkommene dreizählige Rotationssymmetrie aufblitzen, bevor die Struktur in warmem, molekularem Dunst in der Tiefe des Tunnels verblasst.

Der Blick fällt senkrecht in die Tiefenachse einer Amyloid-β-Fibrille – und was sich offenbart, ist keine biologische Struktur mehr, sondern eine Architektur des Unerbittlichen: Schicht um Schicht gestapelte β-Faltblätter recken sich in eine scheinbar unendliche Tiefe, jede Lage von der nächsten durch einen Abstand von nur 4,7 Ångström getrennt, einer Präzision, die eher an maschinelle Fertigung als an molekulare Selbstorganisation erinnert. Die goldenen Querstreben der Wasserstoffbrückenbindungen ziehen sich wie Sprossen einer nie endenden Leiter senkrecht zur Blickrichtung durch den Raum und verleihen diesem Tunnel aus Peptidketten eine fast liturgische Regelmäßigkeit. Im absoluten Zentrum des Abgrunds liegt der sterische Reißverschluss: ein samtschwarzer Spalt, in dem hydrophobe Seitenketten – Leucine, Isoleucine – so vollständig ineinandergreifen, dass kein einziges Wassermolekül eindringen kann, die molekulare Oberfläche poliert wie dunkler Basalt und von van-der-Waals-Kräften zusammengehalten wie eine trockene Steinmauer auf atomarer Ebene. Die äußere Mantelfläche der Fibrille hingegen schimmert blau-weiß in einer halbgeordneten Solvathülle, wo Wassermoleküle in Pikosekundengleichgewichten zwischen Flüssigkeit und Ordnung oszillieren und das Licht in ein nakreöses Glimmen zerstreuen. Was diese Landschaft so verstörend macht, ist die Erkenntnis, dass sie sich selbst gebaut hat – eine Schablone, die sich endlos reproduziert, Schicht für Schicht, mit derselben geometrischen Unerbittlichkeit rückwärts wie vorwärts durch die Zeit.
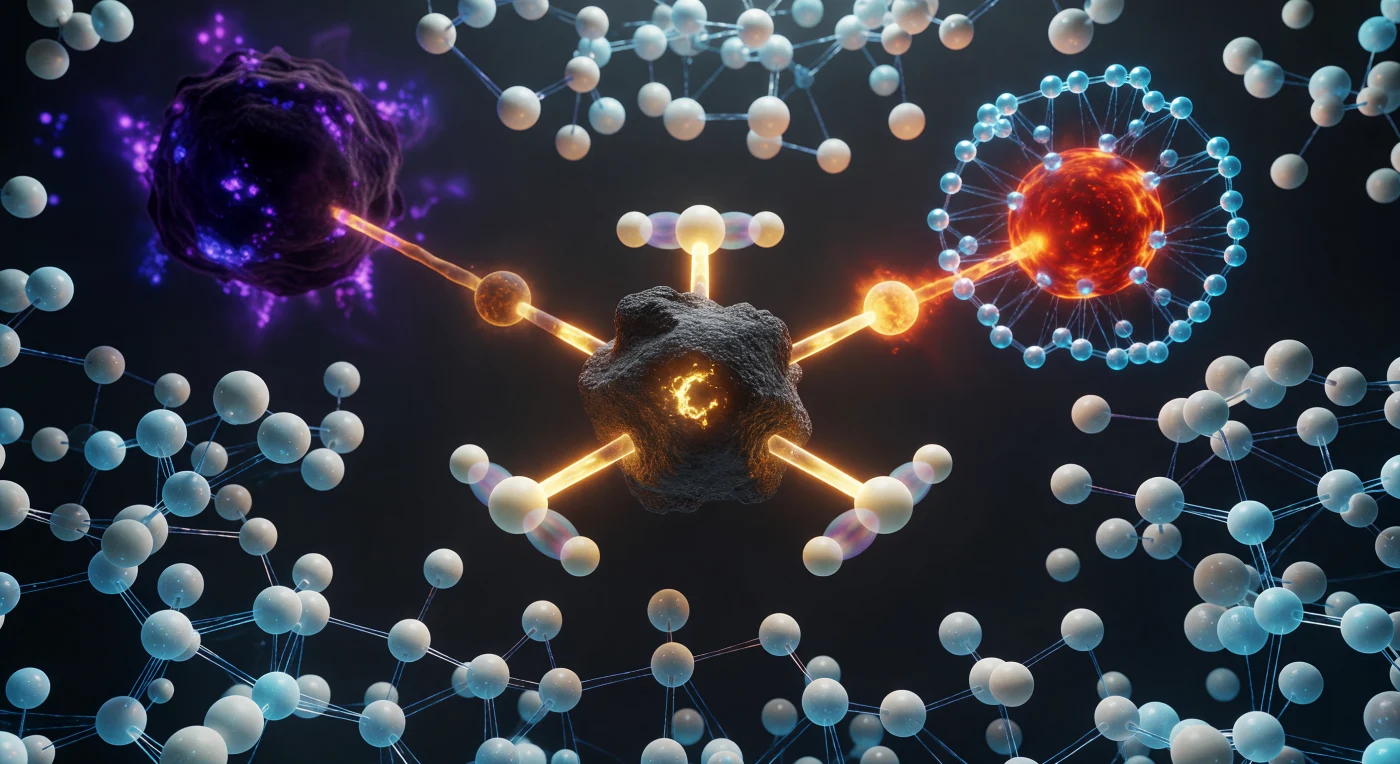
Im eingefroren Quantenaugenblick des Übergangszustands einer SN2-Reaktion schwebt das zentrale Kohlenstoffatom in geometrisch unmöglicher Pentakoordination — drei Wasserstoffatome spannen eine exakte trigonal-planare Anordnung mit 120°-Winkeln auf, während ein elektropositives Sauerstoffnukleophil von einer Seite in glühendem Rot-Orange auf 2,0 Å heranrückt und das massereich-violette Bromatom mit seiner diffusen Elektronenhülle auf 2,3 Å auf der gegenüberliegenden Seite entweicht, beide Partialbindungen in bernsteingoldenem Halbordnungsleuchten suspendiert. Diese lineare O···C···Br-Achse bildet die tektonische Wirbelsäule der gesamten molekularen Welt, während quantenmechanische Superposition die Wasserstoffatome als geisterhafte Doppelgänger ihrer invertierten Endpositionen erscheinen lässt — ein irisierendes Schimmern, das Tunnelwahrscheinlichkeit statt klassischer Lokalisation ausdrückt. Das umgebende polare Lösungsmittel ist keine Leere, sondern eine dicht gedrängte Gesellschaft von Wassermolekülen, deren Sauerstoffkerne in Eisblau aufleuchten und deren Wasserstoffbrückennetzwerk sich in cyan-weißen Filamenten sichtbar neu organisiert, da die umverteilende Partialladung des Reaktionszentrums elektrostatische Schockwellen durch jede Hydrathülle schickt. Das Licht dieses Ortes hat keine äußere Quelle — es emaniert aus den Ladungsumverteilungen selbst, aus der Quantenchemie der halbbrechenden Bindungen, die Bernstein, Violett und Kupferrot in ein komplexes inneres Leuchten verweben, das jede klassische Vorstellung von Molekülstruktur als statisches Objekt auflöst.

Du treibst lautlos durch einen elliptischen Kanal, der kaum breiter ist als ein einziges Molekül – die Wände aus unzähligen SiO₄-Tetraedern aufgebaut, deren blassgraue Siliziumzentren und leuchtendrote Sauerstoffbrücken eine sinusförmig gerippte Oberfläche formen, die sich mit kristalliner Präzision um dich schließt. Zehngliedrige Ringportale aus miteinander verzahnten Si-O-Si-Bindungen reihen sich in kaltem Blau-Weiß vor dir auf, während grelle weiße Punkte an den Aluminiumsubstitutionsstellen die hochreaktiven Brønsted-Säurezentren markieren – jeder einzelne ein lokalisiierter Reaktionsherd in einer sonst geometrisch makellosen Mineraloberfläche. Dreißig Ångström voraus öffnet sich das visuelle Herzstück der Szene: ein rechtwinkliger Tunnel-Kreuzungspunkt, an dem der sinusförmige Kanal senkrecht einmündet und eine zweite elliptische Öffnung in die Wand schneidet – jenes Fünf-Ångström-Nadelöhr, das über Diffusion und Selektivität in der heterogenen Katalyse entscheidet. Goldene, raumfüllende Kohlenwasserstoffmoleküle füllen den Kanal in fast perfektem Van-der-Waals-Kontakt mit der Porenwand – der winzige Spalt zwischen organischer Oberfläche und Sauerstoffgitter schwach blau schimmernd, als wären Londoner Dispersionskräfte sichtbar geworden.
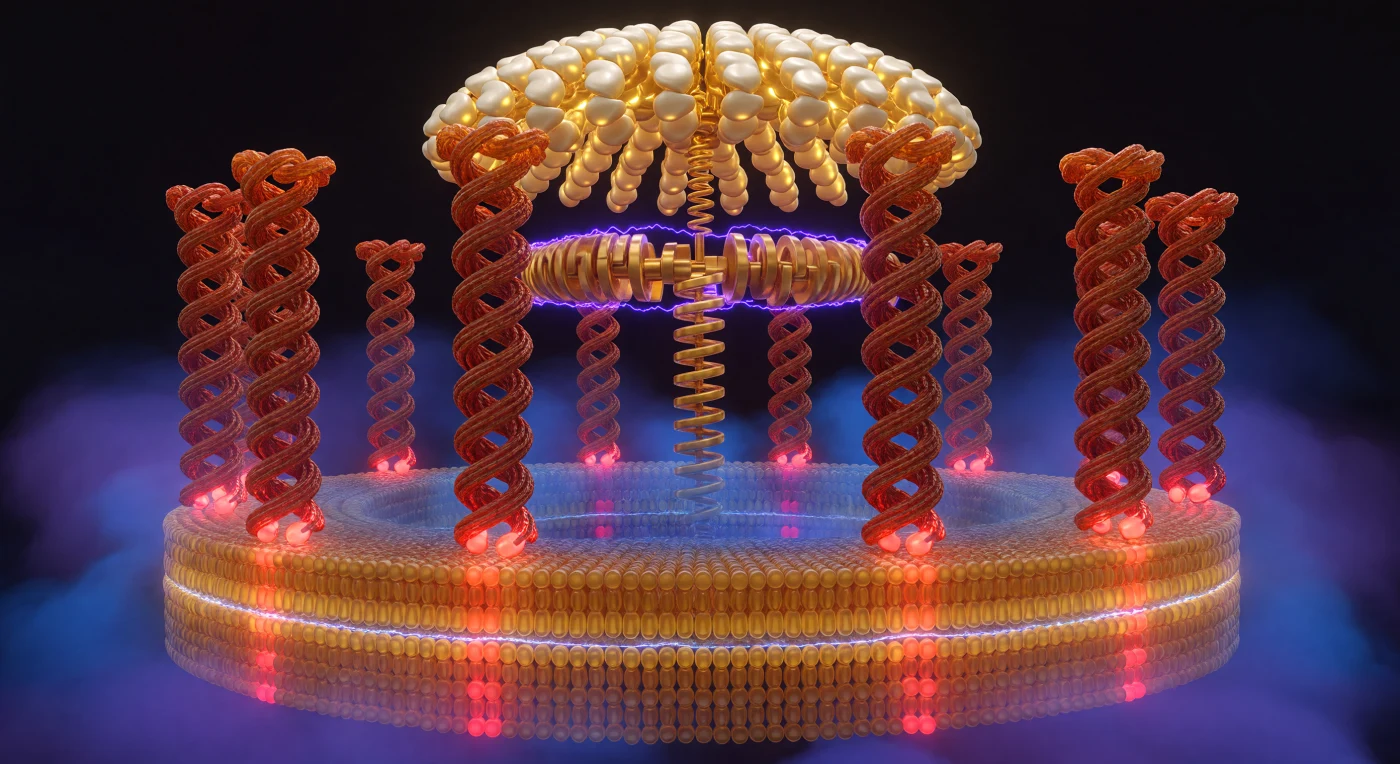
Im Inneren des c-Ring-Rotors der ATP-Synthase wölbt sich die Welt wie das Innere eines lebendigen Kolosseums: Zehn terrakottafarbene α-helikale Säulen erheben sich ringsum aus der Lipiddoppelschicht, deren äußeres Blatt in warmem Bernstein-Gold leuchtet und deren inneres Blatt in ein kühles Blau-Bernstein übergeht – eine so scharfe Grenzlinie wie eine Küstenlinie, an der Tempelstützen aus dem Wasser tauchen. An der Basis jeder Säule glüht ein einzelner Glutamatrest: die dem Protonenkanal zugewandten Reste brennen in leuchtendem Scharlachrot, elektrisch roh und deprotoniert, während jene im hydrophoben Membrankern zu einem gedämpften Ziegelrot verblassen – ein biologischer Rhythmus, wie Glut, die erlischt und wieder aufflammt. Das Spannungsgefälle der Protonenmotorischen Kraft von 150–200 Millivolt manifestiert sich nicht in Pfeilen oder Symbolen, sondern in der Qualität des Lichts selbst: Auf der einen Seite verdichtet sich ein schweres Kobaltviolett unter dem Gewicht akkumulierter Protonen, während es auf der anderen zu einem ruhigen Mitternachtsblau verblasst, als stünde die Atmosphäre kurz vor dem elektrischen Durchbruch. Darüber wölbt sich die F₁-Katalysekuppel wie ein Kathedralengewölbe aus Gold und Elfenbein, und die asymmetrische γ-Untereinheit – eine Kurbelwelle aus Protein – überträgt mit geometrischer Zwangsläufigkeit die Rotationsenergie der Protonenströmung in die chemische Bindungsenergie des ATP, eine Maschine, die seit vier Milliarden Jahren ohne Unterbrechung dreht.


















