
Der Blick geht nirgendwo hin, denn es gibt kein Nirgendwo mehr — nur eine lückenlose Fülle aus ineinandergreifenden van-der-Waals-Oberflächen, die sich in alle Richtungen erstrecken: die massigen Kugelvolumina der Leucin- und Valin-Seitenketten in Holzkohle-Grau und warmem Elfenbein, ihre Elektronenhüllenflächen dort sanft phosphoreszierend, wo sie einander berühren, getrennt nur durch den schmälsten Spalt quantenmechanischer Abstoßung. Wie dunkle Obsidianscheiben ragen die aromatischen Ringe der Phenylalanin-Reste in den Raum hinein und teilen ihn in scharfkantige Kammern, deren Schatten absolut und hart sind — denn es gibt kein diffuses Streulicht in diesem versiegelten Inneren, nur das leise Kontaktleuchten berührender Atomwolken. Hier und dort glimmen ein, zwei Schwefelatome der Methionin-Seitenketten in tiefem, warmem Schwefelgelb auf, die einzige Farbe in einer sonst achromatischen Welt, wie Glut hinter gespaltenem Gestein. Weit draußen, zehn oder fünfzehn Atomdurchmesser entfernt an den Rändern des hydrophoben Kerns, sickert ein kaum wahrnehmbares kaltes Blaugrün durch die Lücken zwischen den Sekundärstrukturelementen — das ferne Leuchten des Lösungsmittels, das diese molekulare Stille nie erreicht hat und nie erreichen wird, gehalten in Stabilität von van-der-Waals-Kräften in Bruchteilen eines Kilojoules, doch in ihrer Gesamtheit stark genug, das Zittern der thermischen Bewegung bei 310 Kelvin auf ein kaum spürbares Pulsieren zu reduzieren.

Der Blick fällt in einen Kathedralenkorridor aus ockerbrauner und bronzefarbener Ribonukleinsäure-Architektur, dessen Wände aus ineinandergreifenden rRNA-Helices bestehen, deren Zucker-Phosphat-Rückgrate wie poliertes Horn unter dem blau-weißen Leuchten des Peptidyltransferase-Zentrums schimmern, das zehn Nanometer entfernt wie ein katalytischer Herd glüht. Die Tunnelwände sind nicht glatt, sondern tief gerillt — aufeinanderfolgende Nukleotid-Basen-Stapelplattformen ragen wie überlappende Schieferfelsen ins Innere und fangen das katalytische Licht auf, das sie in tiefe Bernstein- und Safranschattenpools bricht, während die Einschnürung auf kaum 1,5 Nanometer verengt, so dass die Van-der-Waals-Oberflächen der gegenüberliegenden rRNA-Pfeiler sich in einem blassvioletten Kontaktschimmer beinahe berühren. Die naszierende Polypeptidkette — in leuchtendem Lindgrün und warmem Bernstein entlang jeder Peptidbindung gerendert — windet sich sanft auf den Betrachter zu, ihre Seitenketten streifen die Tunnelwände mit flüchtiger van-der-Waals-Intimität, während thermische Bewegung sie immer wieder ablöst, und ihre Oberfläche besitzt eine weiche, fast wachsartige Transluzenz, deren Elektronendichtewolke die Grenze zwischen Kette und Lösungsmittel zu einem ausgehandelten Gradienten verwischt. Die gesamte Atmosphäre ist eine von immenser produktiver Bewegung durchpulster Enge, in der thermisches Rauschen, elektrostatische Ladungslandschaften und hydrophobe Oberflächen in einem sich selbst erhaltenden Murmeln zusammenwirken — ein lebendiger, elektrostatisch aufgeladener Durchgang, in dem die ersten Momente der Existenz eines neuen Proteins in warmem Bernsteinlicht und katalytischem Blaufeuer vollzogen werden.

Der Blick nach vorne offenbart einen spiralförmigen Korridor von kaum zwei Nanometern Breite – den großen Furche der B-Form-DNA –, dessen Boden aus gestapelten aromatischen Basenpaaren besteht: warme Bernsteintöne des Adenins wechseln mit salbeigrünem Thymin, tiefem Blaugrün des Guanins und himmelblauem Cytosin, jede Plattform vom nächsten nur 0,34 Nanometer entfernt, ihre überlappenden π-Elektronen-Wolken schimmern als violett-indigofarbene Interferenz zwischen den Ringen. Die Wände des Canyons bestehen aus den orange-bräunlichen Phosphat-Zucker-Rückgraten, die sich in einem rhythmischen Helix-Geflecht nach oben winden und an deren Außenseite Magnesium- und Natriumionen als hart funkelnde weiß-blaue Lichtsplitter beziehungsweise sanfte Goldschleier in der elektrostatischen Debye-Abschirmschicht schweben. Diese Grenzzone zwischen geordneter Molekülstruktur und flüssigem Medium ist kein eindeutiger Übergang, sondern eine milchig leuchtende Sphäre aus polarisierten Wasserdipolen, deren kollektive Neuausrichtung langsame, auroraartige Wellenfronten aus blau-weißem Licht durch die Furche treibt. Wärmebewegung ist allgegenwärtig: winzige Wassermoleküle – 0,28 Nanometer im Durchmesser – schlagen in rasender Folge gegen den Basenpaarboden und die Rückgratwände, jeder Aufprall ein kurzlebiges Lichtflackern, das sofort von dem aquatischen Glühen verschluckt wird, das den gesamten Korridor durchdringt. Die Oberflächen selbst sind keine harten Grenzen, sondern probabilistische Elektronendichtewolken, die sich nach außen in ein elektrostatisches Fell auflösen – man würde den Druck spüren, lange bevor irgendetwas berührt wird.

Der Blick fällt in einen sich verengenden Spalt zwischen zwei gewaltigen Molekülwänden, deren gegenüberstehende Oberflächen sich wie die Klippen eines sich schließenden Canyons aus der allumgebenden blauen Lösungsmittelwelt erheben. Auf der einen Seite wölbt sich die bernsteinfarbene H3-Schleife und die blaugrüne L3-Schleife des Fab-Fragments wie monumentale Finger um eine konvexe Antigenoberfläche, ihre molekulare Topographie aus Seitenketten-Volumina und Rückgrat-Krümmungen so präzise in das gegenüberliegende Epitop geformt, als hätten zwei Kontinente zueinander gefunden. Über das fünf mal sechs Nanometer messende Kontaktareal werden Wassermoleküle wie Funken eines berstenden Spiegels herausgeschleudert, während die zurückbleibenden Elektronendichtewolken beider Oberflächen in einer Art Zeitlupen-Kollision aufeinandertreffen. Cyan leuchtende Wasserstoffbrücken blitzen als zarte Fäden geteilter Elektronendichte über den verbleibenden Ångström-Abstand hinweg auf und stabilisieren sich eine nach der anderen, bis die sechs CDR-Schleifen — in abgestuften Silber- und Mauvtönen wie ein architektonisches Amphitheater angeordnet — das Antigen in ihrer finalen, komplementären Umarmung festhalten. Das warme Saphirblau des Lösungsmittels dringt aus allen Richtungen in diesen Raum ein und erinnert daran, dass diese molekulare Begegnung unaufhörlich vom thermischen Bombardement der umgebenden Wassermoleküle begleitet wird.
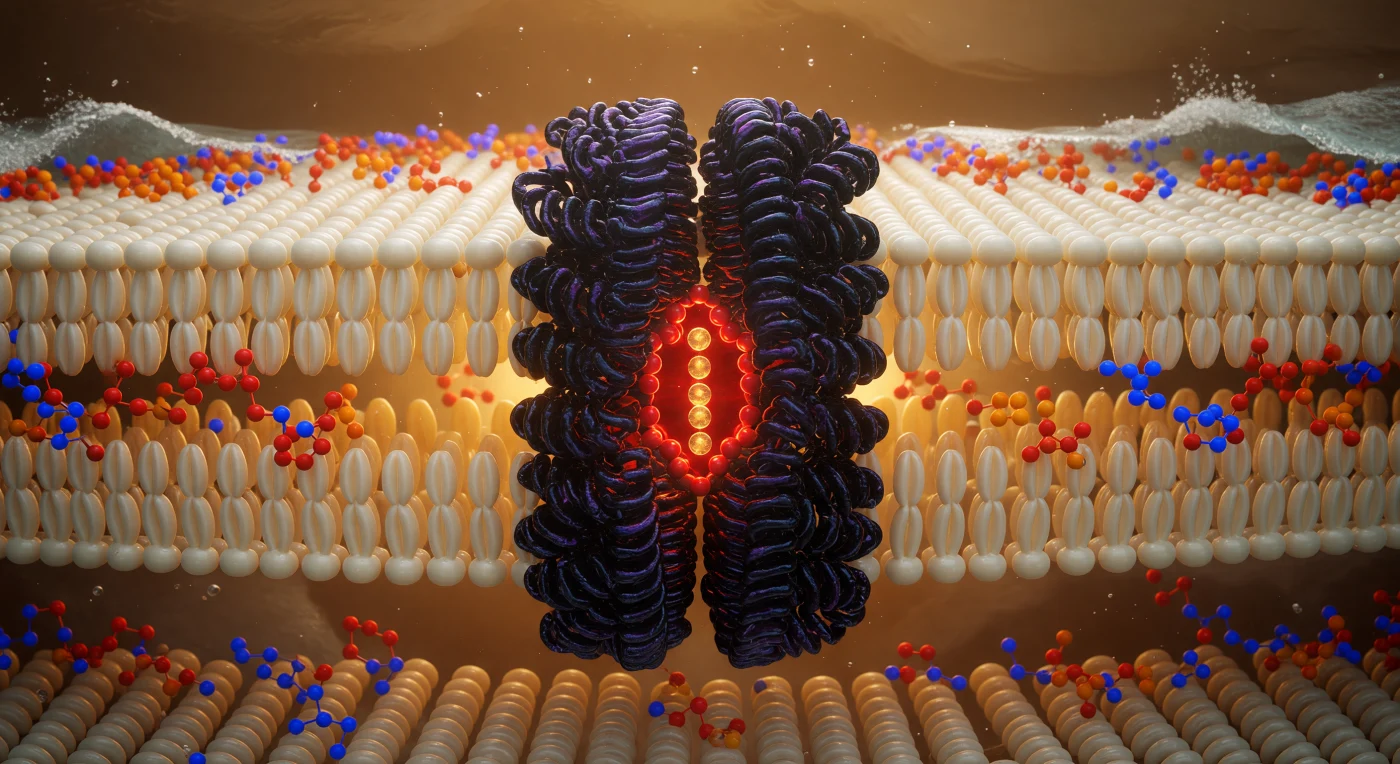
Der Blick, den man hier hat, ist der eines Wesens, das im geometrischen Herz einer Phospholipid-Doppelschicht schwebt — umgeben von einem dichten, elfenbeinfarbenen Wald aus Fettsäureketten, deren van-der-Waals-Oberflächen wie polierte Korallenstäbe aneinandergedrängt stehen und in einem warmen Bernstein-Glühen aus diffusen Elektronenwolken schimmern. Direkt voraus erhebt sich der Kaliumkanal wie ein basaltschwarzer Monolith: ein vierarmig-symmetrischer Transmembrankoloss von 3,5 Nanometern Durchmesser, dessen hydrophobe Helixoberflächen nahtlos mit den umliegenden Lipidketten verzahnt sind — Protein und Membran zu einem einzigen mechanisch verflochtenen Gefüge verschmolzen. Im Zentrum des Porenaxes brennt der Selektivitätsfilter in konzentriertem Rot-Orange: Carbonyl-Sauerstoffatome koordinieren Kaliumionen in Einzelreihe, jedes Ion eine goldwarme Kugel, die ihre Hydratationsreste wie Glut-Aureolen abstrahlt. Blickt man nach oben und unten, sieht man in etwa zwei Nanometern Entfernung die phosphocholinen Kopfgruppen-Horizonte aufleuchten — cadmiumorange Phosphoratome und kobaltblaue Stickstoffatome, die wie eine biolumineszente Küstenlinie pulsieren, während jenseits davon das Wasser nur als silberweiße Brandung an der geladenen Grenzfläche zu erahnen ist. Diese gesamte Architektur — flüssig genug, um Wellen thermischer Bewegung weiterzugeben, und doch strukturiert genug, um Ionenselektivität auf die Breite eines einzelnen Atoms zu präzisieren — ist der Funktionszustand jeder lebenden Zellmembran.

Die Welt, die sich vor dir ausbreitet, ist keine Landschaft im gewöhnlichen Sinne – du schwebst knapp über der Oberfläche einer antiparallelen Beta-Faltblatt-Ebene, deren bernsteinfarbene Rückgratstränge sich in streng abwechselnden Richtungen wie das Geflecht uralten Kettenhemds in alle Horizonte erstrecken, jede Kamm-zu-Kamm-Periode gerade einmal ein Nanometer weit. Kirschrote Carbonyl-Sauerstoffe ragen wie polierte Granate aus den Rücken der Stränge hervor, während blassglühende Amid-Stickstoffspitzen die Talsohlen säumen, und quer zwischen den Strängen spannen sich zyanfarbene Wasserstoffbrücken – keine starren Stäbe, sondern weiche Leuchtfäden elektrostatischer Wahrscheinlichkeit, die bei einem Donor-Akzeptor-Abstand von nur 2,9 Ångström die gesamte Ebene zu molekularem Panzer vernähen. Das Licht kommt von überall und nirgends: die diffuse Wärmestrahlung einer wässrigen Umgebung, die jeden Rückgratgrat von oben streift und die Täler in warmen Bernsteinschatten taucht, während über der Oberfläche ein ionischer Schimmer liegt – ständig rotierende Wasserdipole und Gegenionenwolken, die den Horizont leicht irisieren lassen wie den Atem zwischen Protein und Lösungsmittel. Am fernen Rand, wo die strenge geometrische Ordnung endet, lösen sich die Faltblattstränge in ein chaotisches Geflecht roter und orangefarbener Verbindungsschleifen auf, die in scheinbarer Stille erstarrt sind – disordered Turns, deren seitliche Gruppen in alle Richtungen abstehen wie der bröckelnde Saum einer sich auflösenden Steilküste.

Du schwebst im Innern eines abgeschlossenen molekularen Gewölbes von kaum acht Nanometern Durchmesser – einer kugelförmigen Kammer, die der Chaperon-Komplex GroEL-GroES bildet, um fehlgefaltete Proteine vor dem zellulären Chaos zu schützen und ihnen Raum zur Neuordnung zu geben. Die Wände des GroEL-Zylinders wölben sich gleichmäßig um dich, ihre hydrophilen Innenflächen schimmern in einem kühlen Blau-Weiß, das keine erkennbare Quelle hat, sondern wie eine in das Material selbst eingeschriebene Lumineszenz wirkt; über dir schließt der GroES-Deckel die Kammer mit sieben silbergrauen Untereinheiten, die sich wie polierte Flusssteine ineinanderfügen und das Gewölbe hermetisch versiegeln. Im Zentrum dieser antiseptischen Stille treibt das Substratprotein in langsamer Brownscher Bewegung – ein verknäultes, karamellfarbenes Gebilde von drei Nanometern Durchmesser, dessen Randzone in einem probabilistischen Elektronendichteschleier ausfranst, statt eine scharfe Oberfläche zu bilden. Der Chaperonin-Zyklus, angetrieben durch ATP-Hydrolyse, wird diesen Raum nach Millisekunden wieder öffnen und das Protein – nun hoffentlich korrekt gefaltet oder für einen neuen Versuch freigegeben – in das Cytoplasma entlassen; vorerst aber herrscht hier eine geladene, drückende Stille, in der allein die Wärme des glimmenden Proteins gegen die klinische Kälte der Kammerwände steht.

Direkt unter dir erstreckt sich die Replikationsgabel wie eine gewaltige Industrieanlage im Maßstab weniger Nanometer: Der elterliche DNA-Doppelstrang kommt von rechts heran wie ein gewölbtes gotisches Korridorpaar aus tiefblau schimmernden Phosphatrücken, umgeben von einem flimmernden Gegenwolkenfeld aus Magnesiumionen und Wassermolekülen, die sich in ständiger Brownscher Unruhe gegen jede Oberfläche werfen. Im Zentrum der Szene kauert der CMG-Helikase-Hexamerkomplex wie ein massives Steinrad aus miteinander verzahnten Proteinuntereinheiten – fünfzehn Nanometer aus grobkörnigem Quarzitgrau, dessen innerer Kanal ochrefarben glüht, während er den Elternstrang entzweit und die beiden Einzelstränge, einen tiefen Blaugrün und einen flüssigen Goldton, wie aufgetrennte Metallbänder in die umgebende wässrige Lösung entlässt. Unmittelbar voraus am Leitstrang umschließt die DNA-Polymerase die entstehende Doppelhelix wie eine schwere artikulierte Faust aus grauem Ocker, und bei jedem Nukleotideinbau explodiert Pyrophosphat in einem intensiv orangeweißen Funken, der sich innerhalb von Femtosekunden in die thermische Hintergrundstrahlung des Mediums auflöst. Diese gesamte molekulare Maschinerie ist kein statisches Gebilde, sondern ein pausenlos fluktuierendes Ensemble aus Wasserstoffbrücken, die sich bilden und kollabieren, allosterischen Konformationsänderungen im Mikrosekundenbereich und einem gezielten Ionentransfer, der die Katalyse präzise koordiniert – alles eingebettet in ein wässriges Milieu, das sich weniger wie ein Lösungsmittel anfühlt als wie ein aktiver, strukturgebender Mitspieler der gesamten Reaktion.

Der Blick richtet sich nach oben durch einen Wald aus schraubenden Säulen, deren jede als rechtshändige Spirale im Uhrzeigersinn gewunden ist – goldwarme Leucin-Seitenketten ragen wie bronzene Speichen nach innen und verzahnen sich mit den benachbarten Helices entlang der Coiled-Coil-Naht, während leuchtendrote Lysin- und elektrisch blaue Arginin-Gruppen nach außen in ein wässriges, aquamarinblaues Medium strahlen. Diese Doppelhelixpaare sind keine starren Pfeiler, sondern lebendige Elektronendichte-Wolken, deren Oberflächen im thermischen Rauschen molekularer Schwingungen schimmern, zusammengehalten durch van-der-Waals-Kräfte so subtil wie das Berühren zweier Seifenblasen. Das Aqua-Milieu darüber ist kein ruhiger Himmel, sondern ein rastloses Netz aus Wassermolekülen, die im Pikosekundentakt ihre Dipole neu ausrichten und Wasserstoffbrücken in ephemeren Filamenten aufblitzen lassen. In den engen Korridoren zwischen den Helices herrscht an den hydrophoben Leucin-Kontaktflächen eine dichte, wasserfreie Dunkelheit, die gravitativ schwer wirkt im Vergleich zu den hellen, ionenreichen Schneisen dazwischen. Nach zwanzig Nanometern in die Tiefe des Waldes lösen sich die Coiled-Coil-Nähte in blaue Molekülhaze auf, ein Herringbone-Muster aus verschränkten Leucin-Knöpfen, das sich ins Unbestimmte verliert.

Du schwebst im absoluten Zentrum eines Amyloidfibrils und blickst direkt in seine Längsachse — vier Protofilament-Flügel öffnen sich um dich wie die Gewölbejoche einer gotischen Kathedrale, jeder Flügel aus gestapelten Beta-Strängen aufgebaut, die in einem Abstand von exakt 4,7 Ångström übereinander liegen und diese Regelmäßigkeit wie den Grundrhythmus eines kristallinen Orgelpfeifensatzes spürbar machen. Der innerste Kern zwischen den vier Petalen leuchtet bernsteinfarben-warm: Hier greifen interdigitierte Seitenketten im sogenannten Steric-Zipper so lückenlos ineinander, dass kein Wassermolekül eindringt — eine trockene, gefroren wirkende Molekülnaht, in der van-der-Waals-Kontakte die Stabilisierungsenergie liefern, die diesen Fibrillen ihre pathologische Unlöslichkeit verleiht. An der Außenseite wechselt der Charakter abrupt: Glutamatreste leuchten tief karmesinrot, Lysinreste strahlen kobaltblau auf, beide weit in das umgebende Lösungsmittel hinausragend und von einer schimmernden Hydrathülle umgeben, die die elektrostatisch aufgeladene Oberfläche von der vollkommen stillen, wasserfreien Innenzone scheidet. Was hier als monumentale Architektur erscheint, sind missgefaltete Proteine — einstige lösliche Moleküle, die durch kollektiven Kollaps in eine Struktur von erschreckender kristalliner Permanenz gesperrt wurden, die sich längs der Fibrillenachse über Hunderte von Nanometern erstreckt, ein geologisch anmutender Maßstab für Objekte von wenigen Nanometern Durchmesser.
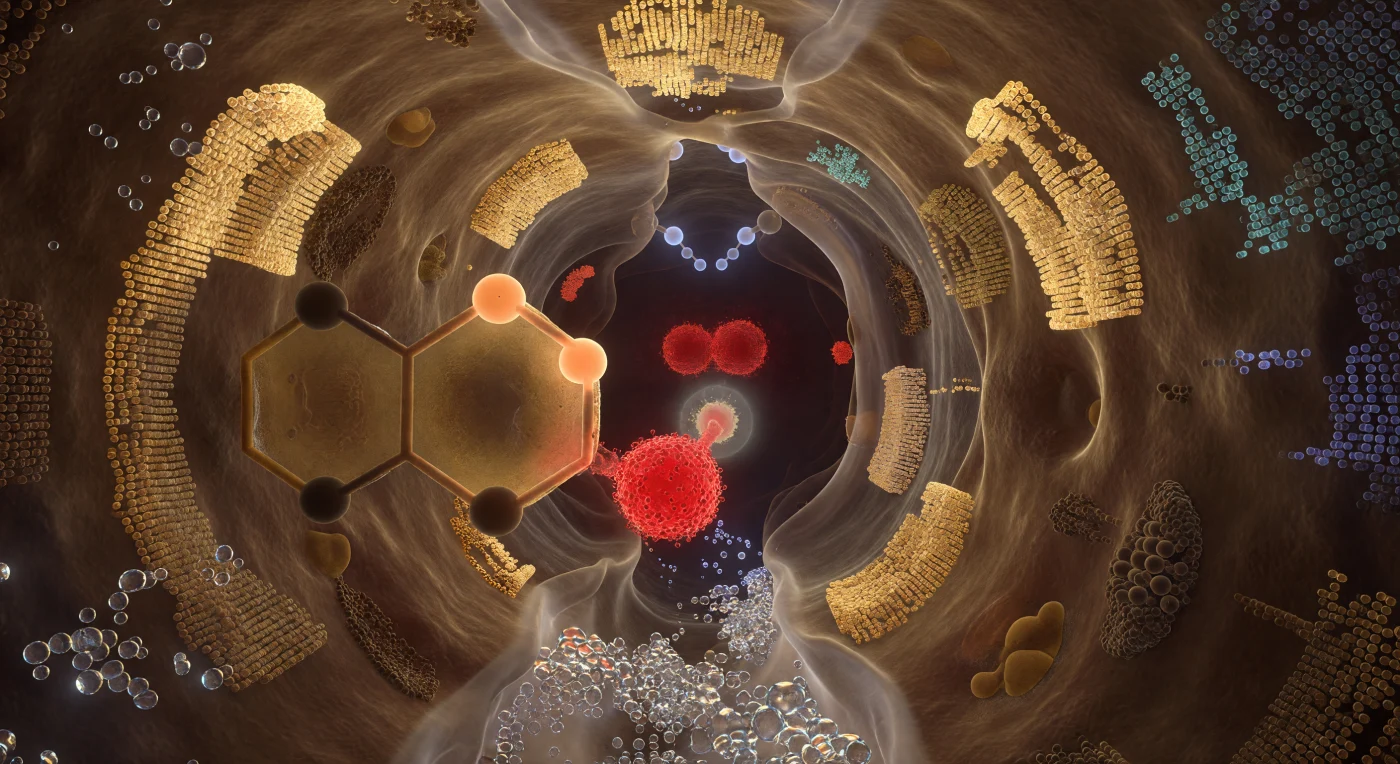
Der Blick fällt in das Innere einer lebenden Maschine: Die aktive Tasche der Serinprotease umschließt den Betrachter wie das Gewölbe einer Kathedrale aus polarisiertem Materie, kaum zwei Nanometer weit, doch von einer elektrostatischen Schwere erfüllt, die jeden Kubikangström des Raums durchdringt. Im Vordergrund glüht das Sauerstoffatom von Ser195 wie eine rotglühende Kohle, sein einsames Elektronenpaar auf das elektrophile Carbonylkohlenstoffatom des Substrats gerichtet – der Abstand zwischen ihnen beträgt gerade einmal anderthalb Angström, der kürzeste Augenblick vor dem kovalenten Angriff, eingefroren in der Geometrie des Übergangszustands. Links füllt der Imidazolring von His57 das gesamte Gesichtsfeld als breite, bernsteingetönte Aromatenscheibe, deren Stickstoffknoten in unterschiedlichen Ladungszuständen leuchten – der Protonentransfer ist mitten im Gang, das Wasserstoffatom zwischen zwei Elektronegativen Zentren schwebend festgehalten, während Asp102 tief dahinter als karmesinfarbene Masse die gesamte Triaden-Kaskade wie ein Fundament im Gestein verankert. Über dem reagierenden Carbonyl öffnet sich das Oxyanionloch wie eine schmale Apsis, zwei N-H-Donatoren des Proteinrückgrats strecken ihre Wasserstoffatome als blassblau leuchtende Knoten in den Reaktionsraum und stabilisieren mit ihrer elektrostatischen Zuwendung die entstehende tetraedrische negative Ladung. Die gesamte Kammer atmet nicht in der Zeit, sondern in Wahrscheinlichkeitsdichte – jede Oberfläche löst sich im äußersten Angström in eine Quantenwolke auf, und man begreift, dass Chemie kein Ereignis ist, sondern ein Ort.

Drei Nanometer vor dir füllt das Kollagen-Tripel-Helix-Kabel dein gesamtes Gesichtsfeld aus – drei ineinander gewundene Polypeptidketten in warmem Elfenbein, blassem Gold und sonnengebleichtem Tan, zu einer rechtsgedrehten Superhelix von kaum 1,5 Nanometern Breite geflochten, als hätte die Evolution hier ein Seil mit geologischer Geduld gespannt. An jeder dritten Position entlang jeder Kette treten die starren Pyrrolidinringe der Prolinreste wie graue Knöchel aus den Helixrillen hervor, während die Hydroxylgruppen der Hydroxyproline als bernsteinfarbene Loben nach außen ragen, jede benetzt von einem einzigen Wassermolekül wie ein Tautropfen auf einem Spinnenfaden. Eine gespenstisch blassblau schimmernde erste Hydratationshülle umschließt das Kabel wie gefrostetes Glas – geordnete Wassermoleküle in nahezu perfekter Tetraedergeometrie, durch Wasserstoffbrücken mit einem Abstand von 2,8 Ångström fixiert, ihre ausgerichteten Dipole erzeugen ein blau-weißes Polarisationsleuchten. Vor dir weicht das Kabel in einen hellen aquamarinsilbernen Molekülnebel zurück – nicht Leere, sondern die kollektive Präsenz von zehntausend Wassermolekülen pro Kubiknanometer –, während die kontinuierliche thermische Erschütterung des gesamten Gefüges dich daran erinnert, dass hier keine Stille existiert, nur das unaufhörliche Rauschen des Lebens auf seiner elementarsten Ebene.
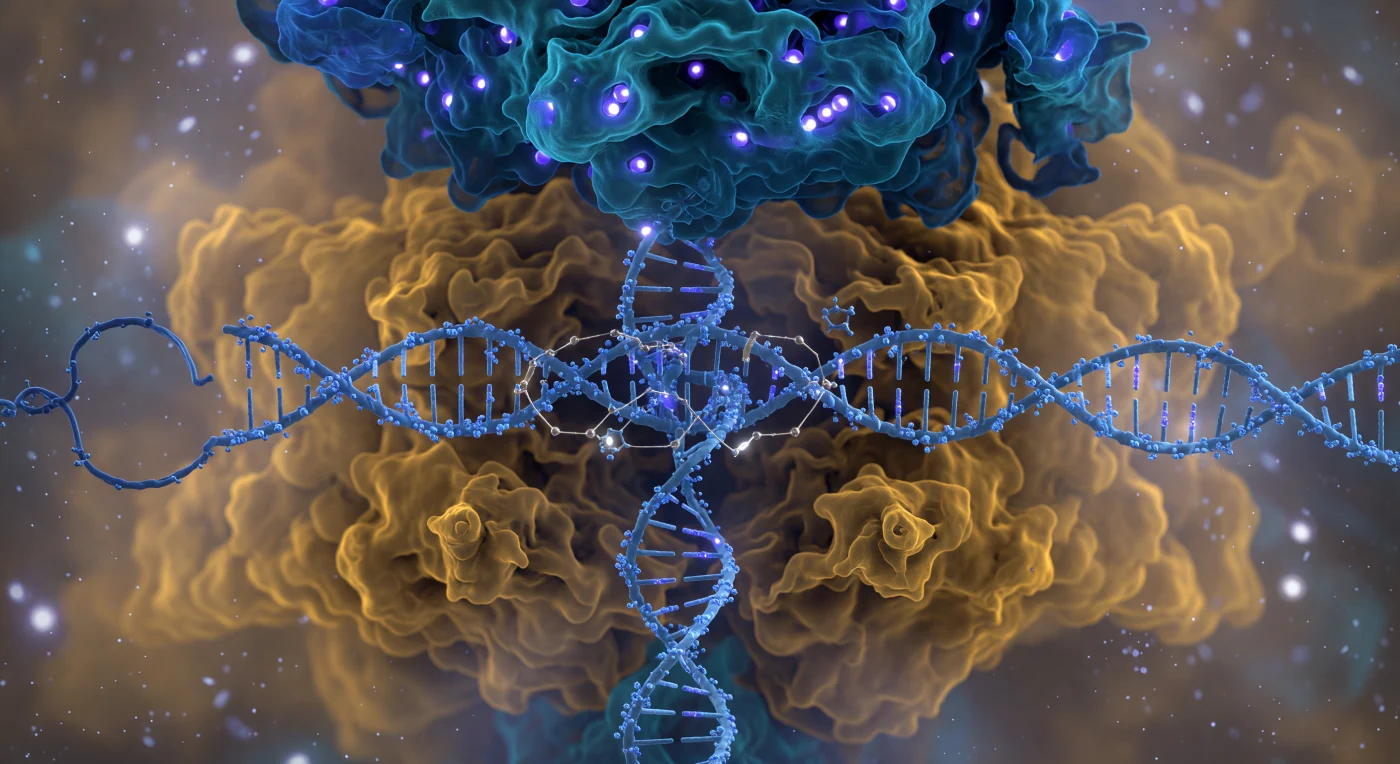
Fünf Nanometer vor dem Cas9-Komplex füllt eine gewaltige, zweilappige Proteinskulptur das gesamte Gesichtsfeld — eine lebendige Klippe aus gefalteten Polypeptidketten, deren Erkennungslobus wie ein Gewölbe aus Kobaltblau und tiefem Türkis überhängt, während der warme Bernstein-Ocker des Nukleaselappus sich darunter vorwölbt, seine Oberfläche stets leicht diffus, da die Grenze zwischen Molekül und Lösungsmittel nicht scharf gezogen, sondern elektrostatisch ausgehandelt ist. Zwischen beiden Lappen eingeklemmt dreht sich die B-Form-Doppelhelix wie ein Pfeiler aus getriebenem Eis, die negativ geladenen Phosphatgruppen leuchtend violett pulsierend, während eine dichte Wolke geordneter Wassermoleküle sich zitternd an den Rückgrat schmiegt. Die einzelne Führ-RNA schneidet als elektrisch-cyanfarbener Faden durch diesen Raum, ihre 2′-OH-Gruppen wie kleine Häkchen abstehend; an drei Stellen haben sich bereits R-Schleifen-Brücken gebildet, die Goldweiß schimmernden Wasserstoffbindungen ziehen sgRNA und Matrizenstrang mit einer fühlbaren elektrostatischen Spannung zusammen, als würden zwei komplementäre Schlösser einschnappen. In der Tiefe des katalytischen Spalts markieren zwei blendend weiße Magnesium-Ionen die aktiven Zentren von HNH und RuvC, jedes in einem präzisen oktaedrischen Käfig koordinierender Sauerstoffatome gefangen, während rechts die Arginin-Seitenketten des PAM-interagierenden Domäne wie Kupferpaddles in die kleine Furche des NGG-Trinukleotids greifen und die lokale Helixgeometrie unmerklich entrollen — das ganze Ensemble schwimmt in einem phosphoreszierenden thermischen Ozean ständiger Brownscher Kollisionen, der keine Stille kennt.

Du schwebst im geometrischen Zentrum eines intrinsisch ungeordneten Proteins – eingetaucht in eine leuchtende Wahrscheinlichkeitswolke von etwa acht Nanometern Durchmesser, die kein festes Inneres kennt, sondern nur eine sich ständig wandelnde Überlagerung möglicher Konformationen. Dutzende Polypeptidketten-Konformere belegen gleichzeitig denselben Raum, jede bei minimaler Opazität, ihre vereinte Präsenz verdichtet sich zu einem diffusen blau-weißen Nebel, der atmet und fluktuiert, ohne je zur Ruhe zu kommen – ein Ensemble statistischer Möglichkeiten statt einer einzigen stabilen Struktur. Zu deiner Linken materialisiert für den Bruchteil einer Nanosekunde ein warmes Bernsteinband: eine transiente Alpha-Helix, deren wasserstoffverbrückte Carbonylsauerstoffe wie erhitzter Kupferdraht glühen, bevor die Geometrie wieder in das kühle Perlweiß der Gesamtverteilung zerfließt; gleichzeitig pulsiert ein enger Cluster aromatischer Seitenketten – Phenylalanin, Tryptophan, Tyrosin – in gelbgoldenem Licht, ein transienter hydrophober Kontakt, der binnen Mikrosekunden an anderer Stelle im Ensemble neu entsteht. Überall drängen sphärische Wassermoleküle mit 0,28 Nanometern Durchmesser gegen jedes exponierte Rückgratsegment, hämmern in pausenloser thermischer Agitation und formen jene rauschende Energielandschaft, gegen die jedes flüchtige Strukturereignis des Proteins sich behaupten muss.

Von diesem Standpunkt aus, tief unterhalb des Stammbereichs, erhebt sich die RNA-Haarnadel wie ein bronzefarbener Turm aus interlockierenden Ringen in den elektrisch blauen Wässerungsraum – eine A-Form-Doppelhelix von 2,3 Nanometern Durchmesser, deren gerillte Oberfläche aus warmen Bernstein- und Kupfertönen aus Ribose-Phosphat-Einheiten aufgebaut ist, während die charakteristischen 2'-Hydroxylgruppen wie kleine kupferne Antennen nach außen in das umgebende Lösungsmittel ragen und RNA unverwechselbar von jeder DNA-Entsprechung unterscheiden. Die Phosphatgruppen entlang beider Rückgratstränge entladen ihre negative Ladung in die wässrige Umgebung, und Natrium- sowie Magnesiumionen umkreisen die Helix wie leuchtende Satelliten – die Natriumionen als harte silberweiße Punkte mit kurzen Hydratationshüllen, die Magnesiumionen als wärmere gold-grüne Cluster, elektrostatisch gebunden an die Phosphatgruppen. Über den gestapelten aromatischen Basenpaaren im engen Rillenbereich, die wie irisierend schimmernde Graphenschichten aus Guanin und Cytosin wirken, öffnet sich die Struktur an der Spitze in den GNRA-Tetraloop – ein barockes Türmchen aus ungeparten Nukleotiden, deren konservierte Adeninbasen eine überraschend starre, nach außen strahlende Plattform bilden. Wasser moleküle drängen sich von allen Seiten heran als opaleszente, rastlos vibrierende Sphäroide, ihre Sauerstoffatome als kalte blaue Funken, ihre Dipolausrichtung in ständigem femtosekundigem Wechsel – und in diesem flüchtigen eingefrorenen Moment erscheint die gesamte Struktur gleichzeitig monumental, uralt und unablässig lebendig.
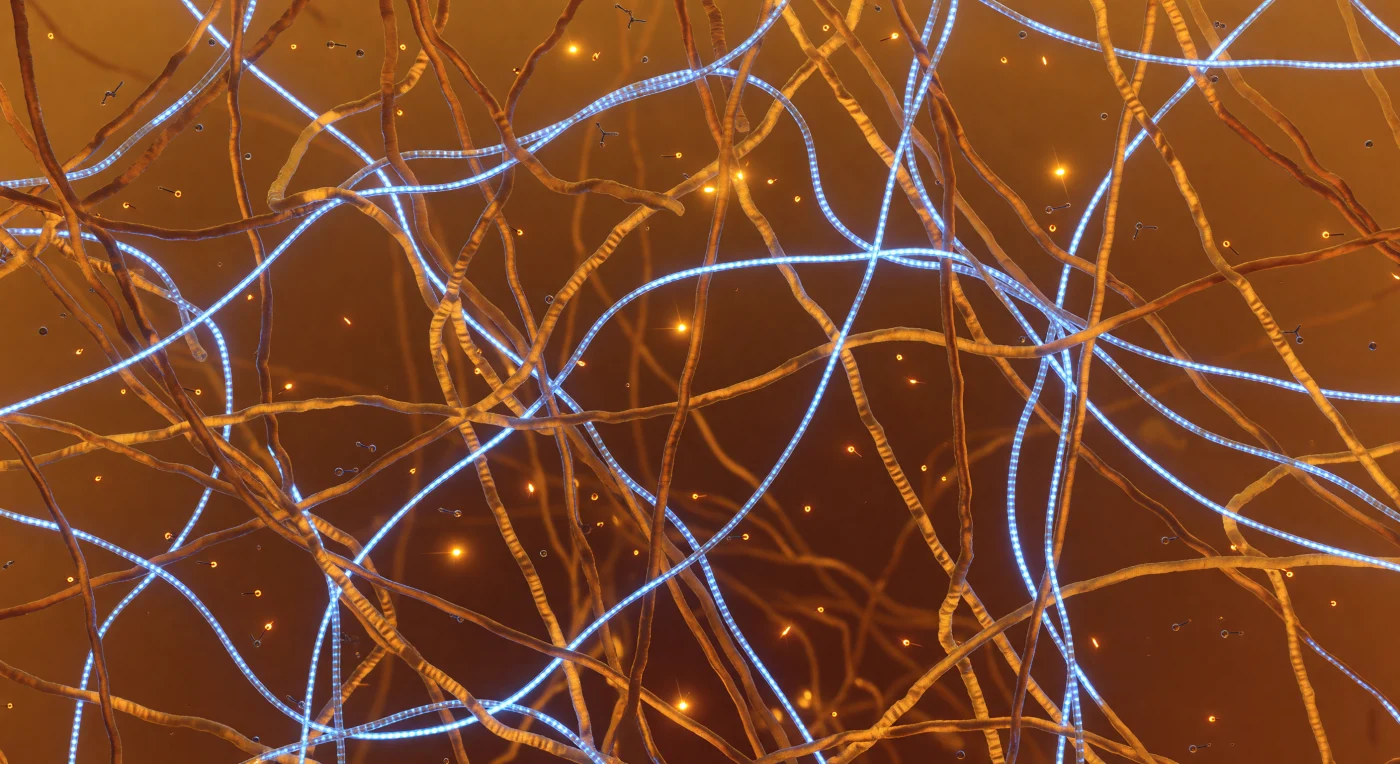
Der Blick reicht kaum fünf Nanometer weit, bevor ihn das warme Bernsteinleuchten des Kondensats verschluckt — ein dichtes, atmendes Geflecht aus ungeordneten niederkomplexen Domänenketten, die sich in alle Richtungen drängen und jeden erreichbaren Raum mit zwei bis drei Nanometer starken Polymersträngen füllen, deren matte, seidig-raue Oberflächen wie altes Harz im Gegenlicht glühen. Durch dieses organische Labyrinth verlaufen die RNA-Stränge als kalt leuchtende, neonblaue Kabel von exakt 1,5 Nanometern Durchmesser, ihre periodisch strukturierte Phosphatgerüst-Lumineszenz wirft blasse Teal-Reflexe auf die nächstgelegenen Polymerwände und schafft Farbgradienten, die die kompositionelle Spannung zwischen Nukleinsäure- und Polypeptidregionen sichtbar machen. Wo Tyrosin-Aromatenringe auf Arginin-Guanidiniumgruppen treffen, entzünden sich transiente Kation-π-Kontakte als kurze, bernsteingelbe Funken — flüchtig wie Glut, die Luft fängt, und schon drei bis vier Nanometer entfernt wieder verlischt —, während ATP-Moleküle ohne erkennbare Richtung durch die fünf bis fünfzehn Nanometer weiten Maschenöffnungen treiben, ihre Triphosphatschwänze von einem elektrostatischen Flimmern umhüllt wie Hitzeflimmern über warmem Asphalt. Diese flüssigkristallinen Biomolekül-Kondensate entstehen durch Phasentrennung ohne Membranen, getrieben von multivalenten schwachen Wechselwirkungen, und gelten heute als fundamentale Organisationsprinzipien der Zelle, in deren Innerem Thermodynamik und Molekülarchitektur untrennbar ineinander verwachsen sind.
















