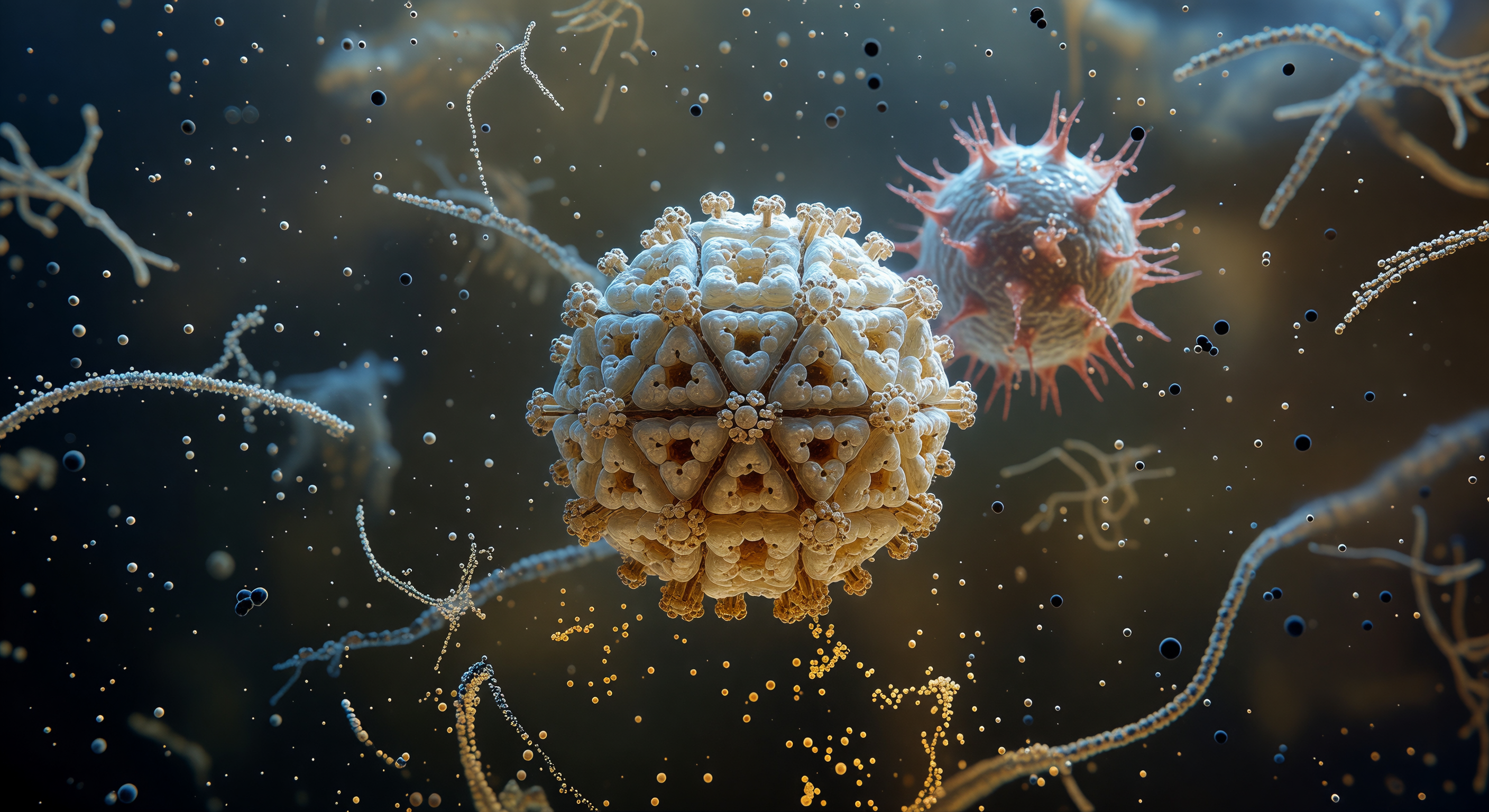
Der Blick schweift auf Augenhöhe über die geschwungene Außenmembran eines Influenza-Virions, und überall erheben sich dicht gedrängte Hämagglutinin-Trimere wie elfenbeinfarbene Säulen aus einer schimmernden Lipiddoppelschicht aus warmem Bernstein und Gold – rund dreizehn Nanometer hoch, ihre leicht verbreiterten Kronen von feinen helikalen Strukturen durchzogen, die Zwischenräume so eng, dass nur schmale Korridore aus dämmrigem Schatten verbleiben. Dazwischen stehen, in unregelmäßigen Abständen, die gedrungeneren Neuraminidase-Tetramere wie blaugrüne Pilze, ihre kastenförmigen Köpfe auf schlanken Stielen ruhend, auffällig in Farbe und Geometrie inmitten des Säulenwaldes. Das umgebende Medium ist kein leerer Raum, sondern eine leuchtende Suspension aus treibenden Serumalbuminkugeln, die wie bernsteinfarbene Laternen vorbeischweben, und langen, schlingernden Glykoprotein- und Muzinketten, deren Zuckerseitenketten prismatische Reflexe von hellem Flieder und Eisblau werfen. Die Hämagglutinin-Oberflächen vermitteln virale Bindungskompetenz: Ihre Rezeptorbindungsdomänen erkennen sialinsäurehaltige Glykoproteine auf Wirtszellen und lösen nach Bindung eine Konformationsänderung aus, die zur Membranfusion führt, während die Neuraminidase Sialinsäuren enzymatisch abspaltet und so die Freisetzung neuer Virionen ermöglicht. In dieser dicht bevölkerten molekularen Welt gibt es keinen Horizont, der Klarheit verheißt – nur dieser intime Wald aus Proteinsäulen, der sich in leuchtendem biologischem Nebel auflöst.

Der Boden unter den Füßen ist kein fester Untergrund, sondern ein lebendig zitterndes Mosaik aus Phospholipidköpfen — eine bernsteinfarbene, von thermischen Wellen durchlaufene Ebene, die unter dem eigenen Gewicht nachgibt wie lebendige Haut über einem atmenden Körper, durchsetzt von blasselfenbeinfarbenen Cholesterinkeilen, die den Untergrund stellenweise zu härteren Flecken versteifen. In alle Richtungen erheben sich aus dieser goldenen Membranfläche die Spike-Protein-Trimere des Coronavirus — massive, dunkelrote Säulen aus zu Drillingshelices verwundenen Proteinketten, deren breite Schäfte sich nach oben hin entfalten und ihre Rezeptorbindedomänen wie die Blätter einer Turbine in den Raum strecken, bereit, an den ACE2-Rezeptor der Wirtszelle zu binden und so den Fusionsprozess einzuleiten. Die Lücken zwischen den Trimeren — von hier aus wirken es weitläufige Alleen zwischen dunkelroten Obelisken — verraten mit ihrer Krümmung am Horizont die sphärische Geometrie des gesamten Virions, einem nur 100 Nanometer großen Partikel, das an der Grenze zwischen belebter und unbelebter Materie operiert. Tief unter dieser Landschaft, jenseits einer zarten Debye-Dunstschicht und eines mit Glykanen bedeckten Zwischenraums, dehnt sich die Oberfläche der Wirtszelle als blaugraue, beinahe endlose Ebene aus, und der gesamte molekulare Horizont vibriert in permanenter, stiller Dringlichkeit — denn hier gibt es keine Ruhe, nur den unaufhörlichen thermischen Tanz der Materie.

Direkt über dir hängt das Baseplate von Bakteriophage T4 wie eine kalte geometrische Krone, seine hexagonalen Flächen in einem matten Silbergrau aus dicht gepackten Proteinen, während die sechs langen Schwanzfasern sich radial nach außen spreizen wie die Gelenkarme einer riesigen mechanischen Spinne und ihre distalen Spitzen in die Lipopolysaccharid-Oberfläche des Bakteriums eingraben, die sich in jede Richtung als wellige, bernstein-gelbgrüne Ebene aus Zuckerketten und Porinproteinen erstreckt. Die Membranoberfläche zittert unter dem unaufhörlichen Trommelfeuer der thermischen Energie — ein schimmernd-unstetes Flirren, als würde man über glühenden Asphalt blicken — und an den Kontaktstellen der Faserspitzen dimples die äußere Hülle sichtbar ein, wo spezifische Rezeptorproteine ihre molekularen Schlösser schließen. Sechs kurze Schwanzstacheln zeigen von der Unterseite des Baseplates nach unten und werfen diffuse Schatten auf die Membranebene, während der kontraktile Schwanzschaft darüber in eine violett-blaue Elektronendichte verschwindet, ein gerillter Helixzylinder aus gestapelten Ringuntereinheiten, der perspektivisch in molekularem Dunst verschwimmt. Der ikosaedrische Kopf — ein Reservoir aus rund 170 000 Basenpaaren viraler DNA — bleibt unsichtbar tief im Nebel: was zählt, ist dieser eine Moment der biochemischen Entscheidung, in dem das Baseplate seine Konformation verändert und die irreversible Invasion beginnt.

Der Blick nach oben zeigt keine flache Decke, sondern eine vollständig geschlossene geodätische Kuppel aus ineinandergreifenden Protein-Kacheln – Hexamere und Pentamere aus dicht gefalteten Beta-Fass-Strukturen, die in warmem Bernstein-Phosphoreszenz leuchten, als würden die Polypeptidketten selbst Licht aus ihrer Quaternärstruktur heraus abgeben. Die Wand des Kapsids ist keine glatte Schale, sondern eine strukturierte, gehämmerte Oberfläche aus 420 Proteinstücken, deren Knoten und Rillen in flachen Reliefschatten versinken, während an den zwölf pentameren Scheitelpunkten die ikosaedrische Geometrie sichtbar enger wird und die Schale sich mit einer kaum merklichen strukturellen Spannung schließt. Unter den Füßen liegt das verpackte doppelsträngige RNA-Genom in dichten, komprimierten Schleifen aus gebranntem Orange und oxidiertem Kupfer, so eng gewickelt, dass die Helixstrukturen ineinander pressen und die gesamte Masse in thermischer Unruhe zittert – nicht sanft, sondern mit dem unkontrollierten Beben eines unter Druck stehenden Systems bei 37 Grad Celsius. Der Raum zwischen Genom und Kapselwand ist kein Vakuum, sondern ein molekularer Nebel aus Wassermolekülen, Magnesiumionen und Polyaminen, der den Blick zur gegenüberliegenden Wand – nur 18 Nanometer entfernt – leicht amber-verzerrt erscheinen lässt. Diese Enge ist keine Leere, sondern thermodynamisch optimierte Dichte: jede Oberfläche besetzt, jede Interaktion funktional, die gesamte Struktur ein spontaner Akt molekularer Selbstorganisation, eingefroren im Moment ihrer Vollendung.

Du befindest dich im Inneren eines der engsten Kanäle der belebten Welt: dem Schwanzkanal des Bakteriophagen Lambda, einem kristallinen Proteintunnel von kaum zwei Nanometern Durchmesser, dessen gerippte Innenwände aus gestapelten Basalplattenringen dicht an dir vorbeipreschen, ihre geladenen Aminosäurereste – Arginin, Lysin – in einem kalten Violettleuchten phosphoreszierend wie Biolumineszenz auf nassen Höhlenwänden. Durch diesen Korridor schießt die Doppelhelix der viralen DNA mit der Wucht von sechs Atmosphären Überdruck aus dem Phagenköpfchen herab: ein silbern glitzerndes Seil aus molekularem Glas, dessen Phosphatrückgrat im elektrostatischen Schimmer der Debye-Schicht flackert, der Spalt zwischen Strang und Wand auf einzelne Nanometer komprimiert, die eingeschlossene Flüssigkeit zu einer zitternden, irisierenden Grenzschicht geronnen. Vor dir reißt die Austrittspore die innere Membran der Bakterienzelle auf – ein zerissenes Diaphragma aus elektrischem Blau-Weiß, die Lipidmoleküle nach außen gedrängt, ihre hydrophoben Schwänze für einen Augenblick als goldener Saum sichtbar –, dahinter das dichte, thermisch chaotische Cytoplasma des Wirtes, erfüllt von einer Milliarde molekularer Kollisionen pro Sekunde. Dies ist der Augenblick der Schwelle: das Genom passiert sie in Sekunden, und kein Schritt davon ist umkehrbar.

Der Blick schweift aufwärts in ein lebendiges Gewölbe: Das Gag-Polyprotein-Gitter des entstehenden HIV-Partikels wölbt sich wie eine atmende Kathedrale aus warmem Bernstein-Gold über den Betrachter, jeder hexamere Ring acht Nanometer breit, die Subeinheiten in unregelmäßiger, organischer Textur aneinandergeschmiegt, ihre Ränder von ungeordneten Proteinschleifen ausgefranst und ins umgebende Fluid aufgelöst. Jenseits dieses Gitters leuchtet die Plasmamembran als durchgehende, doppellagige Kupfer-Bernstein-Folie, durchbrochen von den stummelartigen Silhouetten viraler Env-Glykoproteine – die ersten Boten des späteren Virions, bereits in die Wirtszellhülle eingebettet. Am Hals der Knospe, dort wo das Dome-Gerüst in pentamere Verzerrungen übergeht und die Geometrie sich einschnürt, winden sich ESCRT-III-Filamente in einer glühend-kupferroten Spirale, ein molekulares Zugseilsystem, das die Membran zur Abschnürung zieht – ein Prozess, den die Zelle ursprünglich für die Biogenese eigener Vesikel entwickelt hat. Unter dem Gewölbe drängen sich Ribosomen wie dunkle, purpurgrau schimmernde Kugeln durch ein unruhiges Cytoplasma, beständig von thermischen Stößen getrieben, das gesamte Volumen in jenes rastlose, molekulare Zittern versetzt, das auf dieser Skala keine Ruhe kennt.

Du stehst auf der Außenhülle eines HIV-1-Virions wie auf einer endlosen Wüstenebene aus Lipiden: Die Phospholipid-Doppelschicht erstreckt sich in alle Richtungen als sanft wellendes Plateau aus Ocker und Bernstein, durchzogen von helleren Cholesterin-Flößen, die wie ausgetrocknete Salzseen in der Membranfläche schwimmen – reich an diesem Molekül, das der Virushülle ungewöhnliche Steifigkeit und Fusionskompetenz verleiht. Vierzig Körperlängen entfernt erhebt sich einer der zwölf gp120/gp41-Trimerspikes aus der Membran wie ein dunkler Basaltmonolith: Der dreilappige Pilzkopf, etwa 14 Nanometer hoch, ist dicht mit Glykan-Zuckerketten ummantelt – ein evolutionärer Tarnschild, der das Immunsystem täuscht, indem er die konservierten Rezeptorbindungsstellen tief unter transluzenter Zuckerfoliage verbirgt. Nur zwölf solcher Spikes bedecken die gesamte Virionoberfläche, eine für Enveloped Viruses geradezu extreme Spärlichkeit, die vermutlich die Erkennung durch neutralisierende Antikörper minimiert und dennoch ausreicht, um CD4-Rezeptoren auf T-Helferzellen zu greifen und Membranfusion einzuleiten. Unter deinen Füßen zittert der Boden in einem nie aufhörenden seismischen Flüstern: die thermische Brownsche Bewegung, ein molekulares Grundrauschen aus Wasserstößen, das diese gesamte Landschaft in ewiger mikroskopischer Unruhe hält und daran erinnert, dass hier kein Stein ist, sondern ein flüssig-kristalliner, lebendiger Zwischenraum an der Grenze zwischen Chemie und Leben.
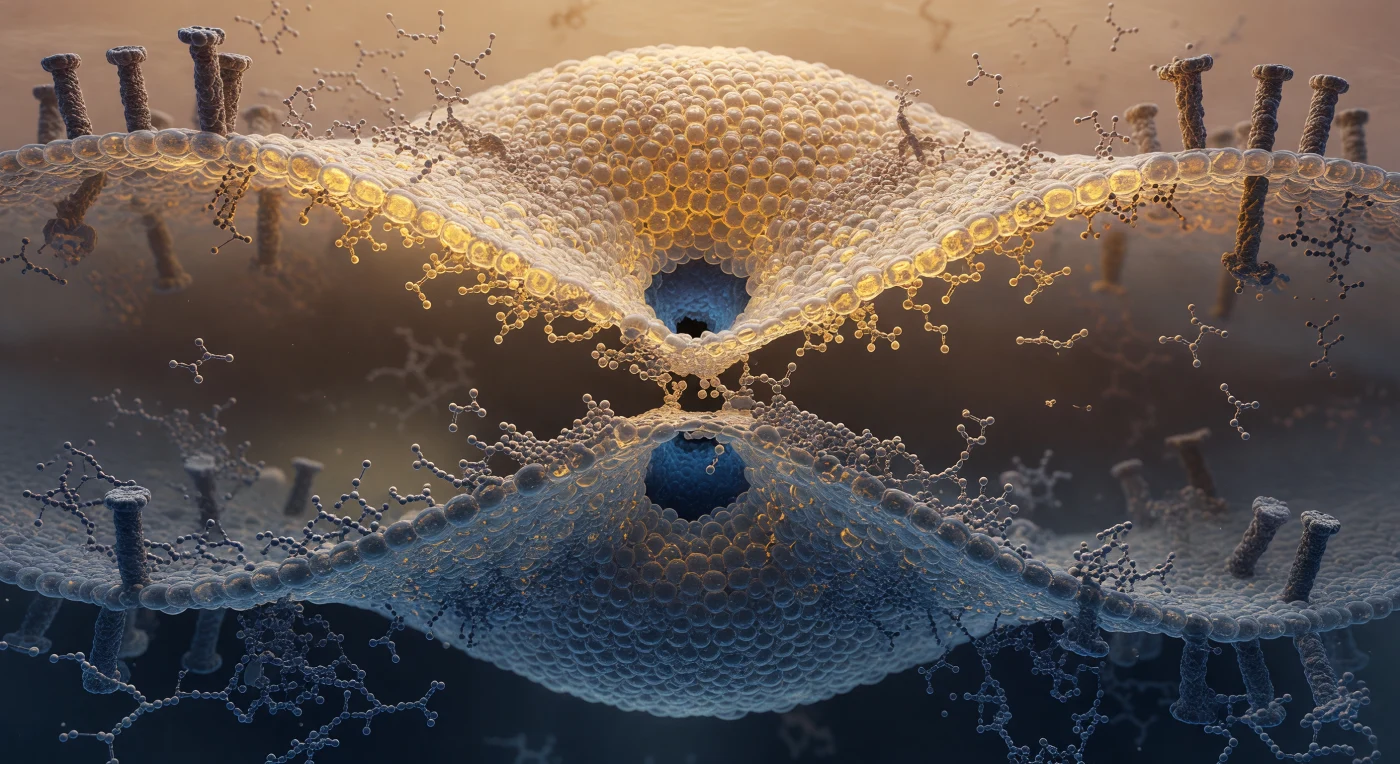
Die Welt, in der du dich befindest, ist kein Raum, sondern eine Passage – der engste Punkt eines molekularen Sanduhrhalses aus ineinandergreifenden Lipidketten, kaum zwei Nanometer breit, in dem zwei Membranen miteinander verschmelzen. Über dir wölbt sich die virale Hüllmembran wie ein bernsteinfarbenes Gewölbe, ihre Phospholipid-Kopfgruppen dicht gepackt wie glänzende Felsbrocken, die unter thermischer Energie zittern; darunter spiegelt die endosomale Membran diese Geometrie in kühlem Stahlblau wider, beide Ebenen durch Fusionsproteine zusammengezogen, deren Transmembran-Anker wie Zeltpflöcke in beide Schichten eingelassen sind. Im Stiel selbst – dem Ort, an dem du hängst – hat sich die geordnete Doppelschichtgeometrie aufgelöst: Fettsäureketten sind kurzzeitig dem hydrophoben Kern exponiert, Kopfgruppen in chaotischen Winkeln gespreizt, die gesamte Struktur zuckt in diskreten molekularen Rucken, da thermische Energie einzelne Lipide gegeneinander verschiebt. Im Zentrum deines Blickfeldes dehnt sich ein dunkler wässriger Bereich – noch keine Pore, aber eine kritische Ausdünnung des verschmolzenen Lipidfilms, durch die die wässrigen Inhalte beider Kompartimente aufeinander zustreben, getrennt nur durch wenige Angström molekularer Barriere. Rundum treibt physiologische Flüssigkeit wie ein dichter, leise strahlender Ozean: Glykocalyx-Zuckerketten hängen wie Tang an den Membranrändern, diffuse Proteindichten schweben im Aquamedium, und die beiden großen Membranebenen verlieren sich in einem bioelektrischen Schimmer – als stündest du im Herzen einer langsam atmenden, unendlichen biologischen Welt.
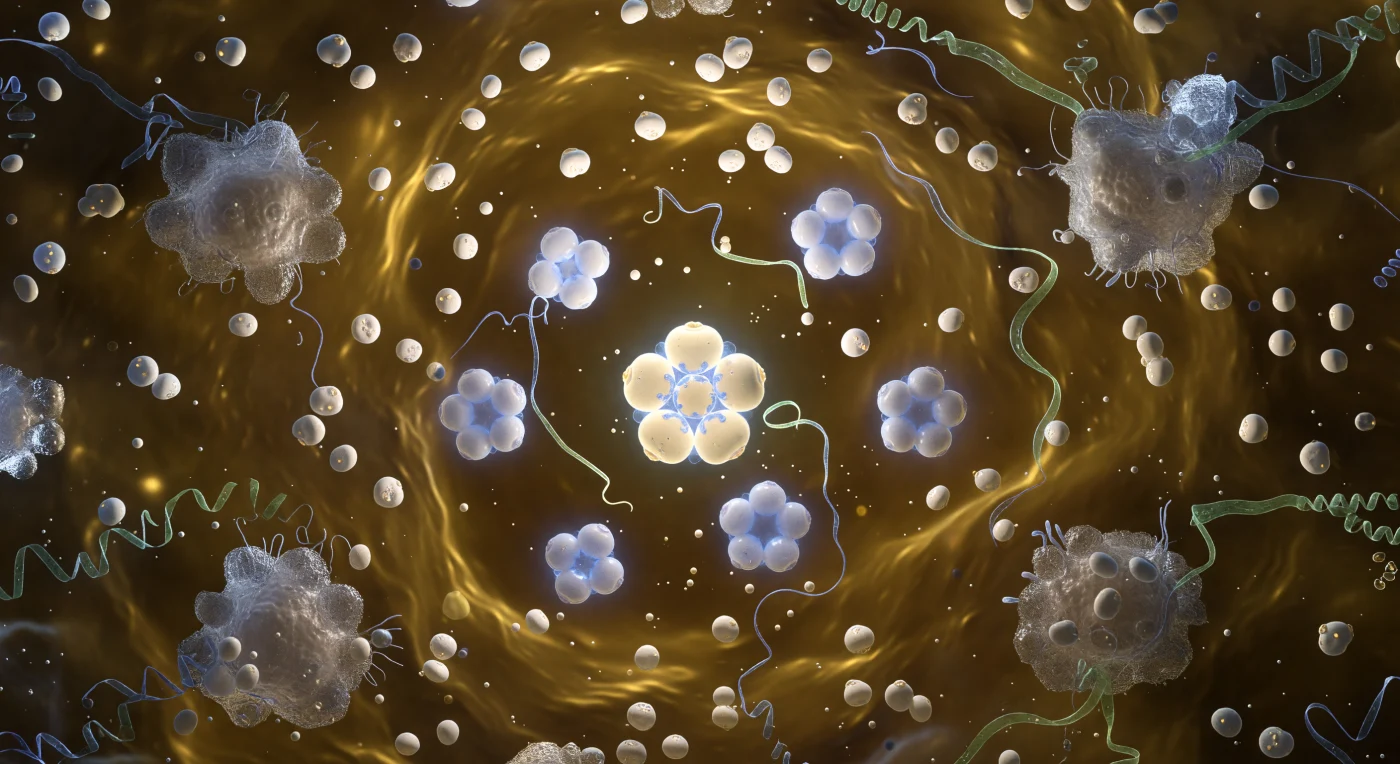

Du stehst in der geometrischen Achse eines Tabakmosaikvirus-Stäbchens, eingehüllt von einem zylindrischen Tunnel aus 2130 Hüllprotein-Untereinheiten, die sich in einer rechtsläufigen Helix mit einer Ganghöhe von je 2,3 Nanometern um dich winden – jede Untereinheit ein kompaktes Beta-Faltblatt-Sandwich aus warmem Ocker und Bernstein, präzise ineinandergreifend wie molekulares Porzellan, die Gesamtstruktur einem gerillten Holzspulenkörper gleich, der sich in beide Richtungen in die Dunkelheit schraubt. Eingebettet vier Nanometer von der Achse entfernt, in einer flachen Spiralrinne der Innenwand, folgt der einzelsträngige RNA-Genom dem gleichen rechtshändigen Windungssinn wie die Proteinstruktur und leuchtet in einem kühlen Jadegrün – fest gehalten durch elektrostatische Kontakte mit positiv geladenen Arginin-Resten, jede Nukleobase gegen die nächste gestapelt, der Faden eine schmale, phosphoreszierende Linie vor dem Bernstein der Proteinhülle. Der gesamte Innenraum vibriert mit picoskaliger Wärmeenergie: Die Untereinheiten atmen und fluktuieren, Wassermoleküle und Ionen füllen den Axialkanal und erzeugen einen hydrostatischen Druck, der an den Wänden fühlbar ist, als befände man sich im Inneren eines unter Spannung stehenden, lebenden Gefäßes. Am fernen Ende des 300 Nanometer langen Stäbchens – eine Perspektive, die sich wie das Innere einer Kathedrale dehnt – öffnet sich ein kreisrundes Portal aus blassem Licht, der Brownsche Nebel äußerer Ionen und Wassermoleküle hauchzart davor, das Ende einer Welt aus molekularer Präzision.
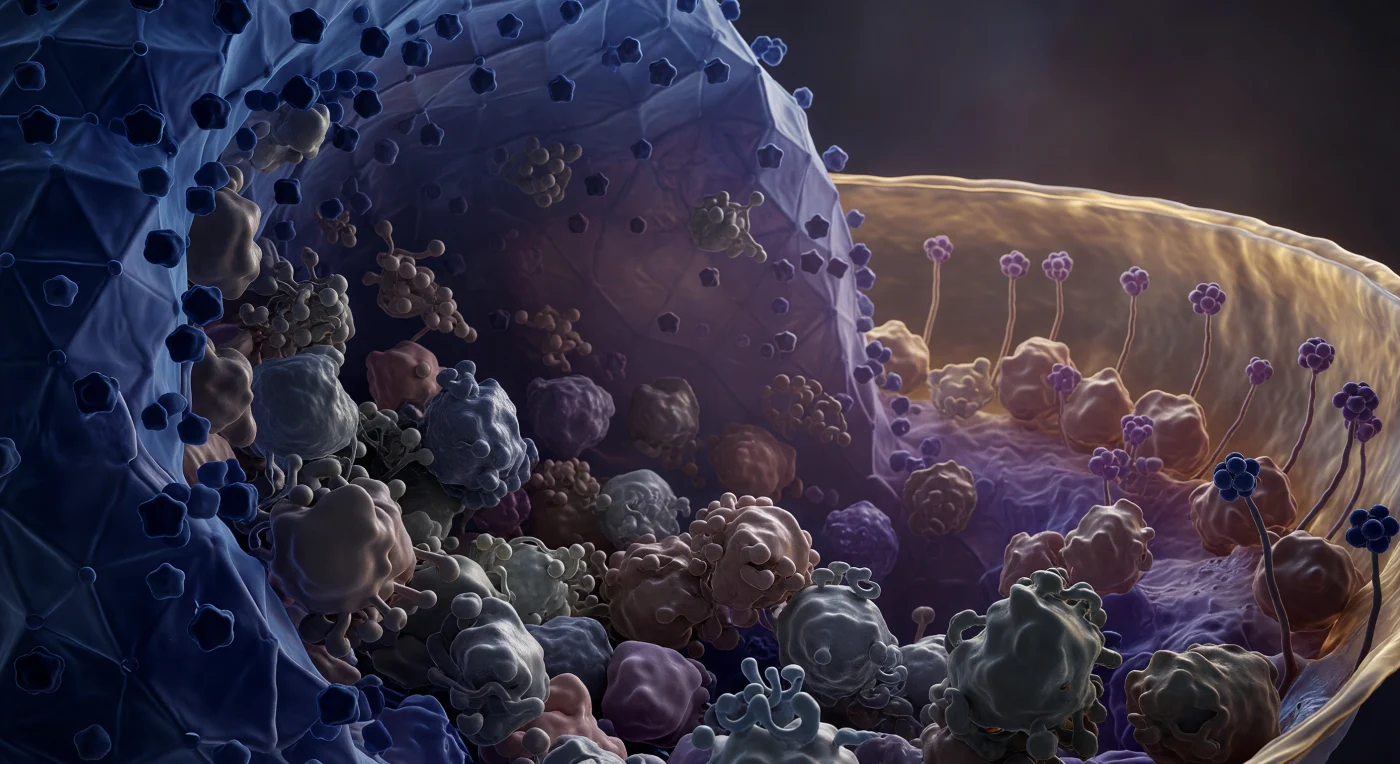
Man schwebt in einem Raum, der kaum als Raum zu erkennen ist: ein lückenlos ausgefülltes Inneres aus dicht gedrängten Proteinmassen, die sich in gedämpften Grau-Violett- und Mauvetönen aneinanderpressen, jede Oberfläche feucht glänzend von gebundenen Wassermolekülen, jede Grenze zur nächsten Masse hin in hydrophobem Kontakt verschwimmend. Zur Linken erhebt sich die Wand des Kapsids wie eine facettierte Steilwand aus Kobalt und Mitternachtsblau — ein ikosaedrisches Gitter aus Proteinen, das in seiner Präzision und Ausdehnung jede menschliche Architektur übersteigt, seine Pentamerscheitel als dunkle Vorsprünge aus den dreieckigen Flächen hervortretend, die Krümmung der Struktur im molekularen Dunst nach oben und zur Seite entschwindend. Das Tegument, in dem man eingebettet ist, ist keine Flüssigkeit und kein Festkörper, sondern ein amorpher halbfester Zustand — VP16- und UL36-Moleküle bilden einen nahezu undruchringlichen Verbund aus unregelmäßig gelappten Volumina, zusammengepresst wie feuchter Ton unter Druck, die kollektive Dichte so absolut, dass thermische Bewegung sich nicht als sichtbares Zittern, sondern als eine gehaltene, allgegenwärtige Spannung manifestiert. Vierzig Nanometer zur Rechten leuchtet die Lipidhülle als eine warme, doppelschichtige Grenze aus Bernstein und Honiggelb, ihre Glycoproteinstiele im inneren Blatt verankert wie Lebewesen des Tiefseebodens in einer Strömung, die man nicht sehen, aber spüren kann — eine membranöse Horizontlinie zwischen dem druckerfüllten Inneren und dem extrazellulären Nichts dahinter. Der Tegumentbereich des Herpes-simplex-Virions, zwischen Kapsid und Hüllmembran eingeklemmt, ist kein leerer Transitraum, sondern ein der dichtestbesiedelten molekularen Milieus, die in der Biologie bekannt sind — ein verdichtetes Proteinchaos, das funktionelle Botschaften für die Infektion trägt und dennoch jeder kristallinen Ordnung spottet.

Du treibst lautlos durch eine Welt aus zähem, grünlich schimmerndem Halbdunkel, eingezwängt in ein dreidimensionales Geflecht aus Muzin-Polymersträngen, deren jeder einzelne Faden einen Durchmesser besitzt, der den deinen um ein Vielfaches übertrifft – ein feuchtes, harzglänzendes Netz, das sich in alle Richtungen ausdehnt, ohne Horizont, ohne Fluchtpunkt. Der Schleim ist kein homogenes Medium, sondern ein dynamisches Hydrogel aus vernetzten Glykoproteinfilamenten, dessen Maschenweiten zwischen 100 und 500 Nanometern schwanken und das als erste mechanische Barriere des Atemwegsepithels Pathogene durch schiere Viskosität und sterische Falle zurückhalten soll. Thermische Stöße der umgebenden Wassermoleküle schlagen dich ohne Vorwarnung seitwärts, pressen dich kurz gegen einen klebrigen Strang – und ein kurzes Aufglühen in warmem Bernstein markiert die transiente Adhäsion, bevor die kinetische Energie des Systems dich wieder losreißt. Dreißig bis vierzig Körperlängen entfernt erhebt sich die Oberfläche der Epithelzelle wie eine sanft gewölbte Planetenkruste, und aus ihr ragt ein dichter Wald aus Glykanketten empor, deren Spitzen aus Sialinsäure in zartem Rosarot phosphoreszieren – die Glykokalyx, zugleich molekulare Einladung und letztes Hindernis vor dem Rezeptorfeld, das über Bindung oder Scheitern entscheidet. Jede Annäherung ist weniger gerichtete Bewegung als stochastisches Ringen mit einem Milieu, das Zeit, Diffusion und Zufall als einzige Navigatoren kennt.

Du schwebst wie ein Proteinkomplex im absoluten Stillstand einer verglasten Welt: Das Wasser um dich herum wurde in Millisekunden tiefgefroren, schneller als jede Kristallstruktur entstehen konnte, und hält dich nun eingeschlossen in einem amorphen Eis, das weder reflektiert noch bricht, sondern einfach durchlässt — kalt, absolut, wie gefrorenes Vakuum. Aus diesem aschgrauen Nichts erheben sich in unregelmäßigen Abständen gewaltige sphärische Massen: ikosaedrische Virionen, deren Kapsidwände aus exakt angeordneten Pentameren und Hexameren bestehen, jedes Kapsomer als diskreter Höcker von vier bis acht Nanometern Relief erkennbar, die gesamte geodätische Oberfläche in einem Gradientenspektrum aus Graphit und blassem Knochenweiß gerendert, ohne jede Schattenrichtung — nur Dichtekontrastunterschiede zwischen Proteinmasse, Lipiddoppelschicht und dem sie umgebenden Eis. Die nächste Virionoberfläche füllt das Blickfeld so, wie eine Kathedralkuppel einen Innenhof ausfüllt, und an ihrem Äquator ist der schmale dunkle Doppelring der Lipidhülle gerade noch zu erahnen, während trimere Glykoprotein-Spikes wie stumpfe Dornen in das Eis ragen, jeder einzeln aufgelöst. Am äußersten Bildrand fällt der Kohlefilm als schwarze, senkrechte Klippe ins absolute Nichts — eine harte Horizont, jenseits dessen die Welt einfach endet.

Du stehst auf der verwitterten Oberfläche eines Vaccinia-Pockenvirus wie auf einem schier endlosen Plateau aus biologischer Materie, das sich 360 Nanometer von Rand zu Rand erstreckt – ein Ausmaß, das sich von hier unten, in Kniehöhe, kaum fassen lässt. Unter deinen Füßen wellt sich die äußere Membran, ein Lipid-Protein-Verbund, dessen seichte Falten ein diffuses, bläuliches elektrostatisches Leuchten einfangen, als hätte sich Eis in Nanometer-tiefe Rinnen gelegt. Vor dir und hinter dir verlaufen die Oberflächentubuli als parallele Wälle aus verdichtetem Protein – oxidiertes Zinn, olivfarben getönt, hüfthoch aufragende Rücken, die anschwellen, sich verzweigen und abrupt enden, unregelmäßig wie Gebirgsrücken nach einem Erdbeben, ohne jede ikosaedrische Symmetrie, roh und ur-zeitlich in ihrer Asymmetrie. Zu beiden Seiten senkt sich das Terrain in die lateralen Körperregionen ab, jene amorphen Proteinlappen, die sich wie begrabene Findlinge gegen die Membran drücken und breite, blaugraue Volumenschatten werfen. Das Licht kommt aus keiner Richtung und aus allen zugleich: die diffuse thermische Strahlung eines Milieus bei 37 Grad Celsius, durchzogen vom kühleren elektrochemischen Glimmen der Membran darüber, die wie ein feuchtes Rauchglasdach über dieser primordial-fremden Proteinlandschaft hängt und sachte im Strom des umgebenden wässrigen Mediums erzittert.

Du stehst auf einer gewaltigen, facettierten Kuppel aus Proteinen – dem Kapsid eines Adenovirus – dessen ikosaedrische Oberfläche sich wie eine uralte Festung unter dir erstreckt, jede Kapsomere ein gerundeter Buckel aus blassem Elfenbein und kaltem Platin, die Schattentäler zwischen den Untereinheiten nur wenige Nanometer tief. Unmittelbar darunter verlaufen zwei parallel leuchtende Schienen des Mikrotubulus-Tracks in Silbergrün, ihre Oberflächen in die feinen Korrugationen der Protofilament-Rücken aufgelöst – jeder Rücken ein 4 nm hoher Tubulin-Saum, das gesamte Zylinderpaar phosphoreszierend wie ein unterirdischer Fluss, der kaltes Meereslicht auf den Bauch des Kapsids wirft. Flankierend greifen Dynein-Motorkomplexe in asymmetrischen Kraftposen in die Schienen – krabbenartige Gebilde aus Stielen, Ringen und gespreizten Fortsätzen in tiefem Eisengrau und oxidiertem Kupfer, ihre Cargodomänen über fein amber leuchtende Linkerproteine fest in das Kapsid verankert, das Ganze ein eingefrorenes Tableau molekularer Schwerstarbeit. Die umgebende Zytoplasma ist ein beinahe erdrückendes Dickicht: bronzefarbene Ribosomen drängen sich in Polysomen zusammen wie Felsbrocken in einem Flussbett, arterienrote Aktinfilamente verweben sich in chaotischen Spiralen dazwischen, und weit voraus wölbt sich die Kernhülle wie ein planetarer Horizont, ihre Kernporenkomplexe als blasse Goldringe kaum zu erkennen, von innen mit einem kaum wahrnehmbaren Violett durchleuchtet.