
Der Blick öffnet sich in ein architektonisches Labyrinth aus ineinandergreifenden Glykanketten, die sich in warmem Bernstein und gebranntem Sienna durch jeden Bildwinkel ziehen – halbdurchscheinend wie poliertes Horn, von innen schwach leuchtend, durch blassere Peptidbrücken in einem dreidimensionalen Geflecht außerordentlicher Dichte verankert. Dies ist die Peptidoglykanhülle von *Bacillus subtilis*, eine bis zu 80 Nanometer starke Schicht aus kovalent vernetzten NAG-NAM-Zuckersträngen, die der Zelle strukturelle Integrität verleiht und dem enormen osmotischen Innendruck von mehreren Atmosphären widersteht. Zwischen den Glykangerüsten weben sich Teichonsäureketten wie dunkelgrüne, leicht irisierende Vorhänge – anionische Polymere, die den elektrostatischen Charakter der Wandoberfläche regulieren und den Transport zweiwertiger Kationen wie Magnesium steuern. Tief unter dem Geflecht schimmert die innere Membran als warme, goldflüssige Phospholipidschicht, von der Wärme nach oben durch die Wandschichten abstrahlt, während am äußeren Rand die Glykanstränge dünner und ungeordneter werden und schließlich in ein kühles, blasses Blau des extrazellulären Wassers auflösen. In diesem Maßstab ist die Grenze zwischen Lebewesen und Umgebung keine Linie, sondern ein allmählich zerfransender Übergang aus Materie und Lösung.
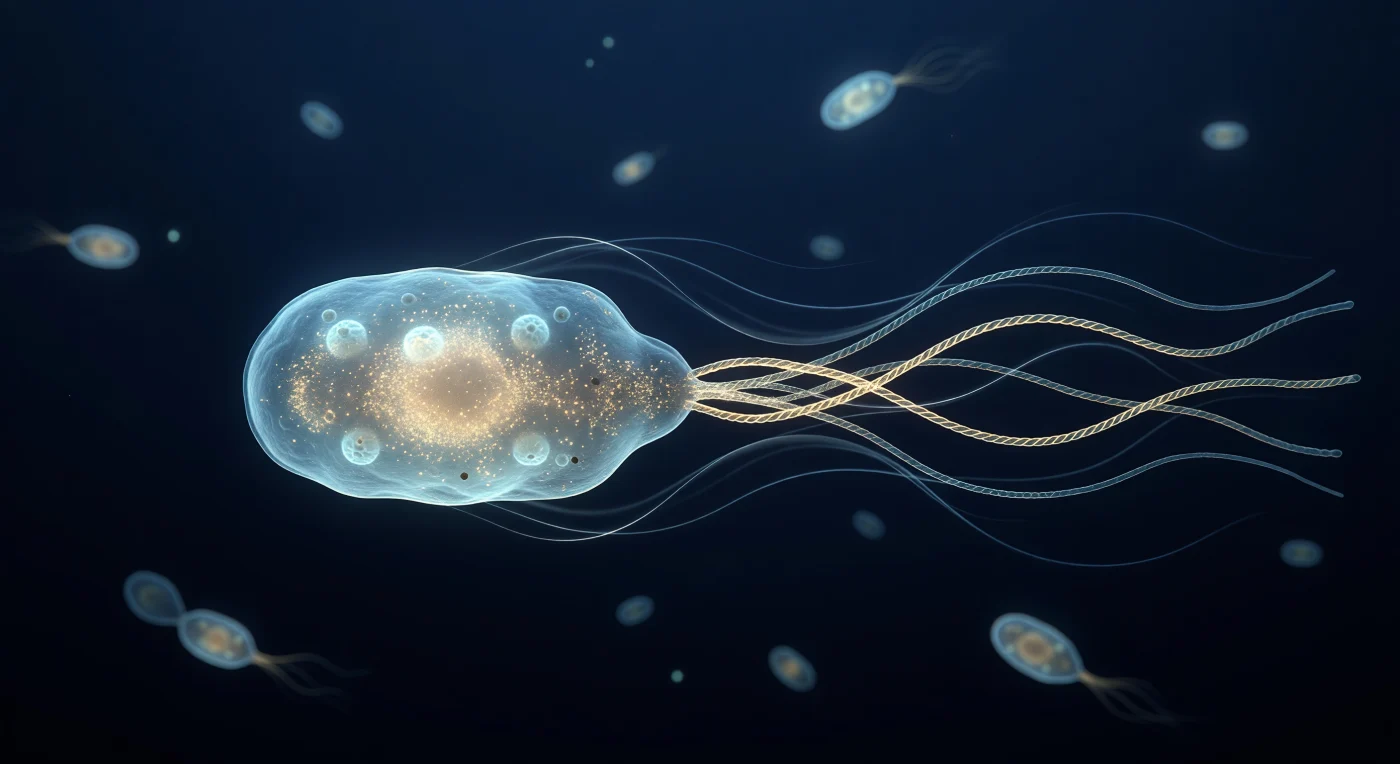
Im fahlen Schimmer des umgebenden Tiefblaus schwebt man knapp hinter dem Heck einer *Escherichia coli*-Zelle und blickt auf einen blasszyanen, ovalen Rumpf, dessen Außenmembran mit kaum erkennbaren Porin-Rosetten besetzt ist – winzige Trichter, die einen diffusen, kalten Schein einfangen, als ob ein phosphoreszierendes Licht tief im Inneren brennte. Vier blassgoldene Geißelfilamente haben sich hinter der Zelle zu einem einzigen superhelikalen Bündel zusammengeflochten, das sich mit einem warmen Bernstein-Glühen in das nachtblaue Wasser hineinverjüngt und von rotatorischer Bewegungsunschärfe umhüllt ist – das Ergebnis von Motorkomplexen im Inneren der Zellmembran, die mit bis zu dreihundert Umdrehungen pro Sekunde rotieren. Um dieses Bündel herum zeichnen feine silberblaue Schlieren geschwungene Bahnen vorwärts zur Zellhülle: vollkommen symmetrische, träge Strömungslinien, die das Regime extrem niedriger Reynolds-Zahlen sichtbar machen, in dem Viskosität regiert und Trägheit schlicht nicht existiert. Im Hintergrund treiben ein Dutzend weich unscharf gewordene Bakteriensilhouetten wie leuchtende Glut durch das Dunkel – nahe genug, um ihre Kapselschleier als zarte Silberringe zu erahnen, doch weit genug entfernt, um in reinem Bokeh zu verschwimmen und die gleichzeitige Intimität und ungeheure Dichte dieser flüssigen, molekular gewimmelten Welt zu bezeugen.

Im Inneren dieser winzigen Zelle schwebt man mitten in einer dichten, fraktalen Wolke aus dunkelblau glühenden DNA-Strängen, die sich in plektonemischen Superhelices winden und verzweigen, bis jede Sichtlinie nach wenigen hundert Nanometern in weichen Indigoschleiern versinkt. Die gesamte Chromosomen-DNA von *E. coli* – fast fünf Millionen Basenpaare, im gestreckten Zustand über einen Millimeter lang – ist hier in einen Raum von kaum einem Kubikmikrometer komprimiert, gefaltet und durch nucleoid-assoziierte Proteine wie HU und Fis in warmgelb leuchtenden Knoten an scharfen Biegungen fixiert, die wie Sternkonstellationen in einem Blaunebel erscheinen. Das kalte, selbstleuchtende Kobaltblau der DNA-Fasern durchdringt das gesamte Sichtfeld ohne harte Schatten, als würde biolumineszente Tinte langsam durch eisiges Wasser diffundieren. Am Rand dieser Nucleoid-Wolke, dort wo das Chromatin dünner wird und das Cytoplasma beginnt, hängen dunkelbraune Ribosomen-Granulate in losen Gruppen – leicht unscharf, von der gelatineartigen Viskosität des molekular überfüllten Cytoplasmas gebrochen –, und erinnern daran, dass Translation und Transkription in Bakterien räumlich kaum voneinander getrennt sind. Dieses überwältigende Labyrinth organisierter biologischer Materie, in dem kein leerer Raum existiert, ist kein Chaos, sondern eine präzise lebende Maschine, deren Architektur die Wellenlänge des sichtbaren Lichts selbst unterschreitet.

Der Blick gleitet über eine endlos wirkende, sanft wogende Ebene aus Lipopolysacchariden, deren Oberfläche in tiefem Blaugrün und warmem Gold schimmert – ein lebendiges Pflaster aus Lipid-A-Kristalldomänen, die unter dem diffusen Kryolicht mit irisierendem Kobalt und Aquamarin aufleuchten wie die Deckflügel eines Käfers im Zwielicht. In regelmäßigen Abständen von kaum zwanzig Nanometern durchbrechen Beta-Fass-Porin-Trimere diese flüssigkristalline Landschaft als obsidianschwarze Turmsäulen, ihre hohlen Innenräume senkrechte Schächte, die tief in die darunter liegende periplasmatische Welt führen. Das umgebende Medium ist kein leerer Raum, sondern ein dichter ionischer Brühe, in der elektrostatische Ladungswolken die Debye-Schicht über der Membranoberfläche zu einem silbrig schimmernden Schleier verdichten, der das von unten durch die Lipidschicht sickernde Biolumineszenzlicht in weiche Aureolen zerstäubt. Am linken Horizont erhebt sich der flagellare Basalkörper wie eine präzisionsgefertigte industrielle Konstruktion: konzentrisch gestapelte Proteindiscs aus L-, P- und MS-Ringen, die den Hook tragen, jener asymmetrische Proteinkrümmer, der sich in die ionische Ferne verliert und mit 100 bis 300 Umdrehungen pro Sekunde die gesamte Flagelle antreiben wird. Was sich hier als ruhige Landschaft darbietet, ist in Wirklichkeit thermisch erzitterndes Gewebe – jede Membranwelle ein Abbild der Brown'schen kT-Energie, die auf dieser Skala jede makroskopische Kraft weit überwiegt.

Der Blick öffnet sich in keine Richtung – stattdessen schließt sich die Welt aus jedem Winkel wie eine Kammer aus lebendigen Steinen, denn dicht gedrängte 70S-Ribosomen füllen das bernsteinfarbene Zytoplasma lückenlos, ihre dunkelgrauen Oberflächen durch Abstände von kaum fünf bis acht Nanometern getrennt, weniger Leerraum als dunkler Mörtel zwischen uraltem Mauerwerk. Polysomen-Ketten – sechs Ribosomen an einem kaum sichtbaren, cremefarbenen mRNA-Faden aufgereiht wie Perlen auf einer schlaffen Schnur – weben sich durch die mittlere Tiefe und verschwinden in einem warmen, harzigen Dunkel, das keine echte Distanz zulässt, sondern nur progressive Undurchdringlichkeit. Links überragt das GroEL-Chaperon wie ein versteinerter Baumstumpf die gesamte Ribosorenlandschaft: seine doppelringige Fassarchitektur aus tiefem Schiefergrau, die zentralen Höhle leicht heller und kühler, verleiht einer sonst isotropen Verdichtung eine fast architektonische Vertikalität. Das umgebende Medium ist kein Wasser – es liest sich als warmes, getrübtes Harz, gesättigt mit Makromolekülen in Konzentrationen jenseits dreihundert Milligramm pro Milliliter, ein Zustand, in dem Viskosität jede Bewegung bindet und Brownsche Stöße die einzige mechanisch spürbare Kraft bilden. Nur gelegentlich flammt ein GFP-markiertes Protein als smaragdgrüne Glut kurz auf, bevor es von einem weiteren Ribosom verdeckt wird und die warme Monochromie wieder geschlossen ist.

Der Blick fällt aus wenigen Mikrometern Höhe auf eine lautlose Metropolis, die nicht gebaut, sondern gewachsen ist: pilzförmige Mikrokolonie-Türme aus *Pseudomonas*-Zellen ragen in jadegrünem GFP-Leuchten empor, ihre gewölbten Oberflächen dicht mit einzelnen stäbchenförmigen Bakterien gepflastert, deren olivgrüne Körper sich wie Kacheln einer Kuppel aneinanderpressen. Zwischen den Türmen ziehen tintenschwarze Wasserkanäle mit hydraulischer Präzision hindurch – vom Strömungsdruck freigespülte Bahnen, die das lebende Gewebe in Quartiere gliedern und ein Flusssystem im Maßstab von Zehnteln eines Menschenhaares bilden. Das Zwischenraum-Gel aus extrazellulären Polysacchariden füllt die Lücken als bernsteinfarbene, leicht trübe Masse, in deren Tiefe ein warmes Orangeleuchten der Autofluoreszenz schwelt wie Glut unter grünem Blätterdach. Ganz unten, in den sauerstoffarmen Basalschichten reifer Türme, verraten verstreute Propidiumiodid-rote Signale abgestorbene Zellen, deren Membranen dem hypoxischen Schatten der eigenen Kolonie erlegen sind – korallrote Schlieren, durch die semitransparente Matrix hindurch sichtbar wie Feuer unter Eis. Die gesamte Szene dehnt sich zu einem Horizont, der in Zehnteln von Millimeterbruchteilen gemessen wird, und ist dabei so dicht, feucht und lebendig, als hätte eine Stadt beschlossen, aus sich selbst heraus zu wachsen.
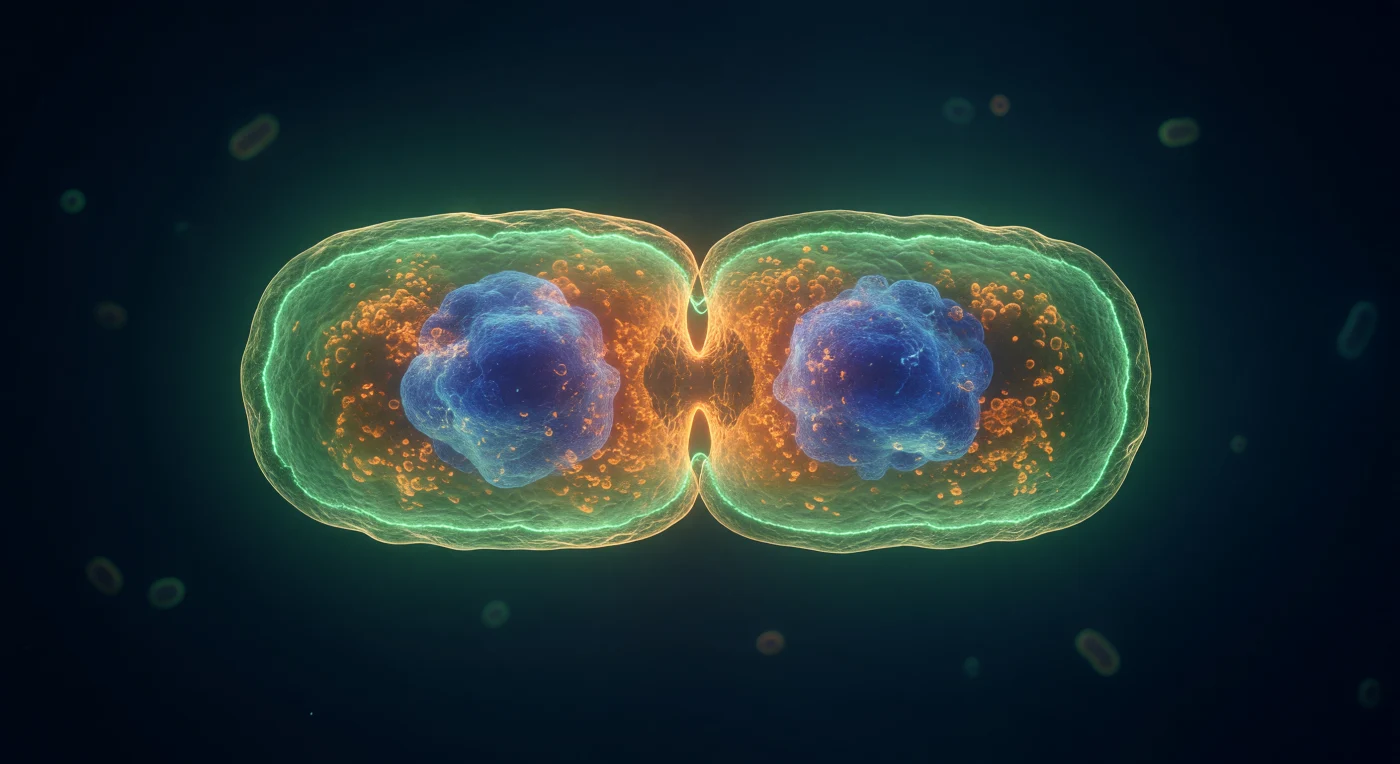
Wir schweben an der Äquatorialzone einer riesigen, schwach leuchtenden Welt — einer *Escherichia coli*-Zelle, die mitten in ihrer eigenen Teilung erstarrt ist. Der Zellkörper erstreckt sich in beide Richtungen wie ein transluzenter Pfeiler aus jadegrünem Licht, seine Oberfläche eine sanft schwingende Membran in warmem Bernsteinorange, das FM4-64-gefärbte innere Membrandoppel zeichnet die Einschnürung nach wie ein glühendes Klammernpaar, das die Einschnürung umrahmt. Genau an diesem Mittelpunkt — den gesamten Umfang der Zelle umspannend wie eine Krone aus lebendigem Feuer — brennt der FtsZ-Z-Ring in elektrischem GFP-Grün: ein durchgehend leuchtender Filamentring aus polymerisierten GTPase-Proteinen, die den bakteriellen Teilungsapparat orchestrieren und die Einschnürung aktiv vorantreiben, während sie mit der inneren Membran und Mureinsynthesekomplexen kooperieren. Durch die durchscheinende Zellwand hindurch leuchten in jeder entstehenden Tochterzelle dichte kobaltblaue Nukleoid-Massen — DAPI-gefärbte Chromosomenwolken, die sich bereits vollständig segregiert haben, getrieben von proteinhafter Kondensation und dem MukBEF-Komplex, eingebettet in ein granulares, bernsteinfarbenes Zytoplasma, das von dicht gepackten Ribosomen bei einer Konzentration von bis zu dreihundert Milligramm Protein pro Milliliter erfüllt wird. Der umgebende wässrige Raum verliert sich in einem fast lichtlosen Marineblau, in dem entfernte Bakteriensilhouetten das Grün des Z-Rings reflektieren — ein dramatisch ausgeleuchteter Moment molekularer Biologie, in dem wenige Sekunden Zellteilung wie geologische Zeit wirken.

Vor dir erstreckt sich die Magnetosomenkette wie ein Monument mineralischer Perfektion – fünfzehn pechschwarze, kubooktaedrische Magnetitkristalle hängen in einer unheimlich gleichmäßigen Linie, jeder etwa viermal so hoch wie du selbst, ihre facettierten Oberflächen werfen blau-violette Metallreflexe durch das trübe, bernsteinfarbene Cytoplasma, das von kaum aufzulösenden Ribosomen wie dunkle Kieselsteine durchsetzt ist. Jeder Kristall besteht aus biologisch synthetisiertem Magnetit – Fe₃O₄ –, gebildet in einer kontrollierten biomineralisierten Reaktion innerhalb der lipidumhüllenden Membranvesikel, die jeden Kristall wie ein gefrostetes Glasgehäuse umschließen und mit thermischer Undulation leise schwingen. Unterhalb der Kette verläuft das MamK-Filament als elektrokobaltblauer Proteinstrang, ein actinähnliches Zytoskelettgerüst, das die gesamte Kristallreihe gegen die viskose, gelartigen Cytoplasmaströmung verankert und dem Bakterium erlaubt, sich entlang geomagnetischer Feldlinien zu orientieren – ein Prozess namens Magnetotaxis. Die Innenmembran wölbt sich in der Ferne als schimmernde goldbraune Grenze, dahinter folgt ein kühler blaugrauer Periplasmastreifen, bevor die Welt im absoluten Dunkel des wässrigen Außenmediums endet. In diesem Reich regiert nicht die Schwerkraft, sondern die thermische Unruhe der Brownschen Bewegung, und jeder Molekülkomplex – jedes Ribosom, jeder Proteinkomplex in der Membran – zittert unaufhörlich im Takt des kT-Energierahmens.
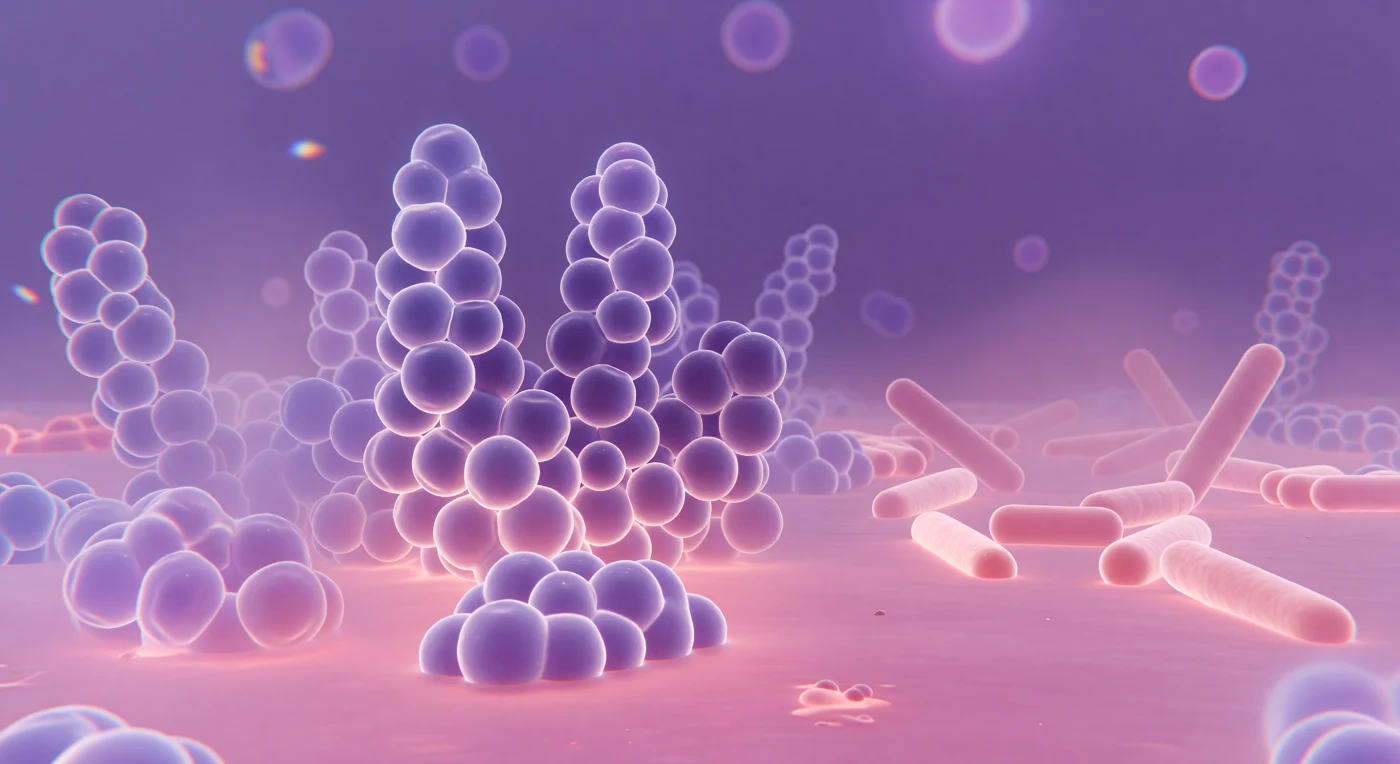
Der Blick fällt auf eine weite, in tiefes Violett getauchte Ebene, über die sich mächtige Kugelformen in dichten, traubenartigen Clustern türmen – Staphylococcus-aureus-Kokken, deren dicke Peptidoglykanwände den Kristallviolettfarbstoff der Gram-Färbung begierig aufgenommen haben und nun in sattem Blauviolett leuchten. Um den Äquator jeder Kugel, kaum größer als die Wellenlänge des sie beleuchtenden Lichts selbst, schimmert ein zarter Beugungshof wie ein blasser Violettkorona – ein physikalisches Zeugnis davon, dass hier die Grenzen der Lichtmikroskopie greifbar werden. Das Licht kommt von überall gleichzeitig, transmittiert durch ein wässriges Medium, das Oberflächen von innen heraus zum Leuchten bringt statt Schatten zu werfen, während der rosa Safranin-Gegenfarbstoff zwischen den Clustern wie rosafarbenes Glas in flachen Pfützen liegt. Nur wenige Körperlängen nach vorne lösen sich die violetten Formen in transparente Lavenderhalos auf, da die hauchdünne Fokusebene des Lichtmikroskops die Tiefenschärfe auf weniger als einen Mikrometer beschränkt und weiter entfernte Zellen zu Geisterumrissen verblasst. Rechts weichen die Kokkenburgen einem offenen Feld blass-rosafarbener Stäbchen – Escherichia coli –, deren Zellwände den Farbstoff kaum binden und die wie nebelverhüllte Monolithe auf einer rosa Salzebene liegen, ihre Enden leicht verwaschen, wo die Auflösung des Glases vor der Physik der Lichtwellen kapituliert.
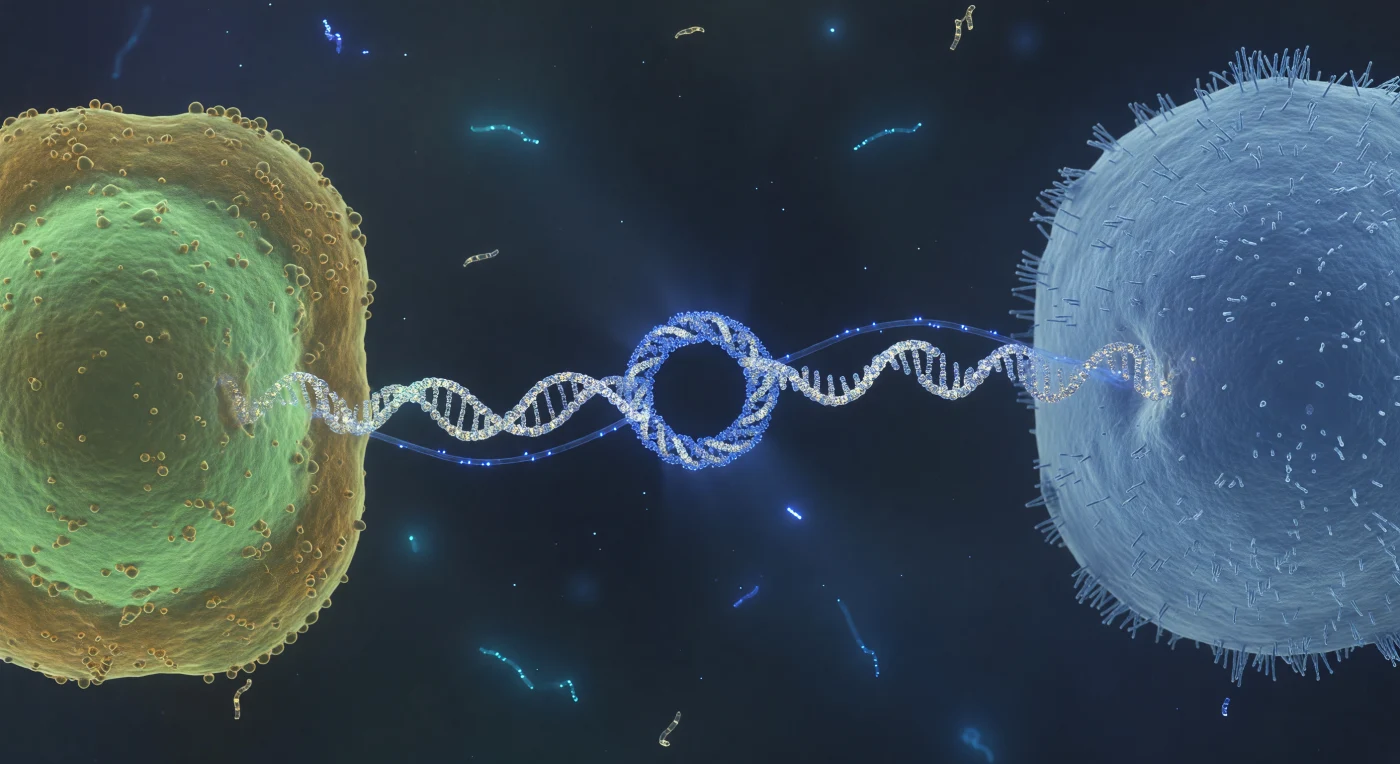
Zwischen zwei lebenden Zellen hängst du schwerelos in einem Flüssigkeitsraum, in dem die Schwerkraft keine Rolle mehr spielt und das Wasser sich anfühlt wie Sirup — du schwebst am Mittelpunkt eines Konjugationspilus, einem helicalen Proteinkabel von kaum 8 Nanometern Durchmesser, das sich gespannt zwischen einem grün leuchtenden Donor-Stäbchen zur Linken und einem matt-blauen Empfänger zur Rechten erstreckt. Dieser Pilus ist kein passiver Kanal, sondern eine dynamische Maschinerie aus ringförmig gestapelten Pilin-Untereinheiten, die aus den Zellhüllen hervorwächst, sich zurückzieht und dabei genetisches Material von einer Zelle in die andere überführt — ein horizontaler Gentransfer, der bakterielle Evolution in Echtzeit vollzieht. An der direkten Zell-Zell-Kontaktstelle verdichtet sich die Komposition in einem kreisrunden Kopplungsring von etwa 20 Nanometern Durchmesser, einem molekularen Andockapparat, durch den ein leuchtend blauer Einzelstrang-DNA-Faden pulsiert — nicht als diskretes Objekt, sondern als diffus glühender Lichtfaden, dessen Ränder sich in das umgebende wässrige Medium auflösen wie Glasfaserlicht im Nebel. Im fernen Hintergrund treiben cyanfarbene Geisterwischen — freie Plasmidbruchstücke, die unter dem unaufhörlichen Bombardement thermischer Stöße taumeln — und erinnern daran, dass dieser scheinbar stille Raum in Wahrheit von kinetischer Energie durchdrungen ist, einer unsichtbaren molekularen Unruhe, die hier, an dieser Skala, alles regiert.
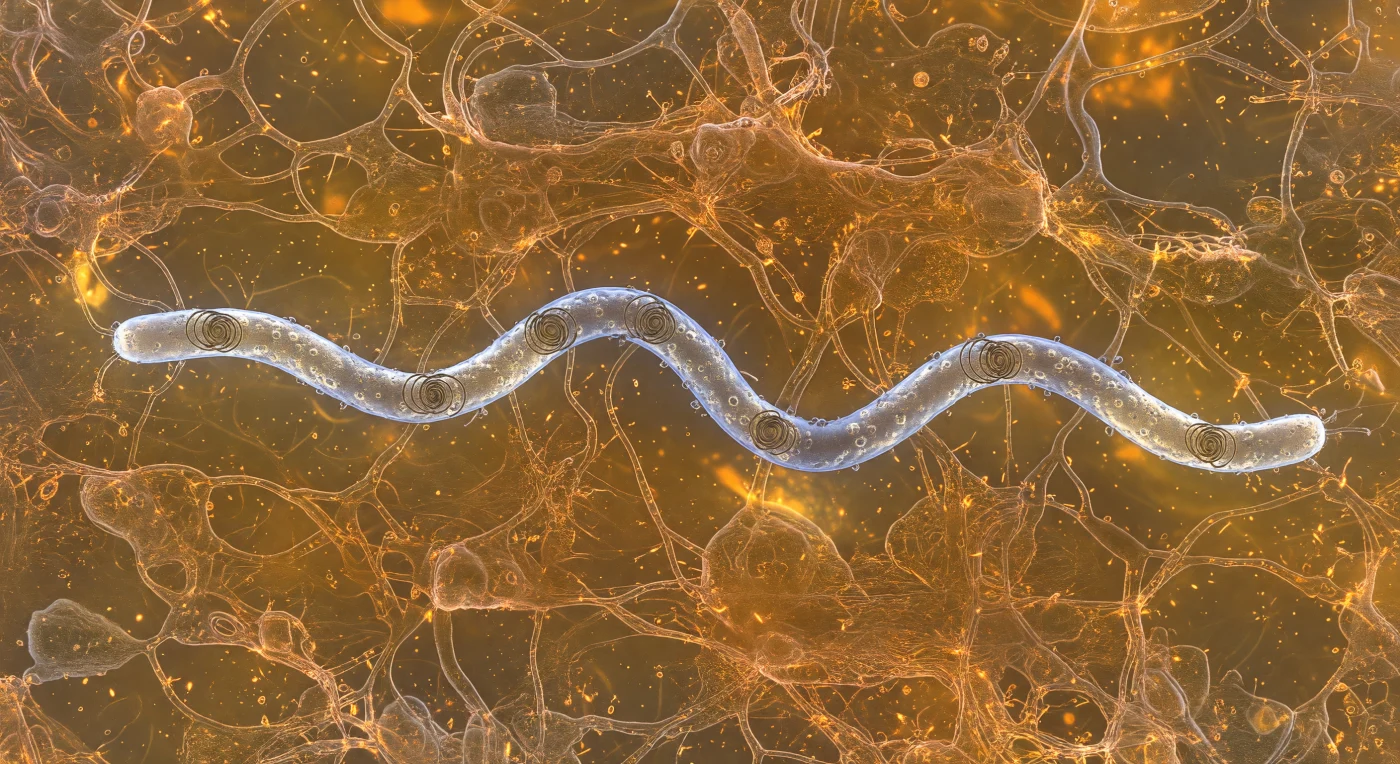
Man treibt reglos in einem dichten, bernsteinfarbenen Medium, das sich nach allen Seiten ausdehnt wie erhitztes Harz – ein Muzingel aus dem Innern eines biologischen Durchgangs, dessen Glycoprotein-Stränge als kupferfarbene, dreidimensionale Filigranfäden hängen und ein diffuses Leuchten ohne erkennbare Quelle zurückwerfen. Kaum fünf Mikrometer zur Linken durchschneidet ein *Borrelia burgdorferi*-Spirochät diese zähe Welt: ein achtzehn Mikrometer langes, silberblaues Korkenzieherband, das seine charakteristische Flachwell-Undulation mit mechanischer Präzision ausführt, während die periplasmatischen Flagellen als dunkel gewendelte Kabel unter der Außenmembran sichtbar bleiben – nie dem Medium ausgesetzt, doch die gesamte Zelle in ihre Wanderwelle biegend. Die Außenmembran, von Proteincluster-Knubbeln aufgeraut wie gehämmertes Platin, pariert das Polymer-Netzwerk bei jeder Bewegung in einem sanften V-förmigen Kielwasser, dessen einzelne Glycoprotein-Stränge im Ausweichen kurz goldkupfern aufblitzen, bevor sie sich hinter der Zelle wieder schließen. In diesem Regime winziger Reynolds-Zahlen spielt Schwerkraft keine Rolle; thermisches Rauschen und Viskosität bestimmen alles, und das Universum um diesen Erreger herum ist ein lebendiges chemisches Gedränge aus gelösten Molekülen, Membranvesikeln und vibrierendem Licht – eine Welt, in der die Wellenlänge des sichtbaren Lichts kaum größer ist als der Durchmesser der Zelle selbst.

Der Blick öffnet sich in das Innere einer lebenden Cyanobakterienzelle – ein weitläufiges Gewölbe aus parallelen Membranschichten, die sich in sanften Kurven in jede Richtung erstrecken und aus sich selbst heraus in tiefem Weinrot leuchten, als glühten unzählige Glutkerne knapp unterhalb ihrer wachsartigen, irisierenden Oberfläche. Dies sind die Thylakoidmembranen von *Synechocystis*, spezialisierte Lipiddoppelschichten, die in konzentrischen Lagen das gesamte Zellinnere durchziehen und in ihren Proteinkomplexen die Lichtenergie der Photosynthese einfangen – das warme Fluoreszenzlicht der Chlorophyllmoleküle in den Photosystemen I und II macht jede Membranoberfläche zu einer selbstleuchtenden Landschaft. Dicht gedrängte korallenfarbene Halbkugeln – die Phycobilisomen – überziehen die Membranen wie barocke Domkuppeln und leiten gesammeltes Licht mit einer Effizienz von nahezu hundert Prozent an die Reaktionszentren weiter, ihr warmes Bernsteinlicht mischt sich in den engen Lumenkorridoren zwischen den Schichten zu einem dichten, flüssig wirkenden Farbvolumen. Im freien Cytoplasma dahinter treiben ikosaedrische Carboxysomen wie mattierte Glaslaternen – facettierte Proteinhüllen von knapp 150 Nanometern Durchmesser, ihre Innenwände vollgepackt mit RuBisCO-Enzymen, dem Molekül, das CO₂ in organischen Kohlenstoff umwandelt, die erhöhte Konzentration des Gases im Inneren die Effizienz der Reaktion weit über das in freier Lösung Mögliche steigernd. Das gesamte Cytoplasma ist kein leerer Raum, sondern ein goldgelbes, von Ribosomen granuliertes Gel, das Wärme und Licht gleichermaßen speichert, während am äußersten Rand der Zelle ein blaugrüner Schimmer durch die Plasmamembran dringt – das leise Echo des Wassers, in dem diese ganze strahlende Welt schwimmt.
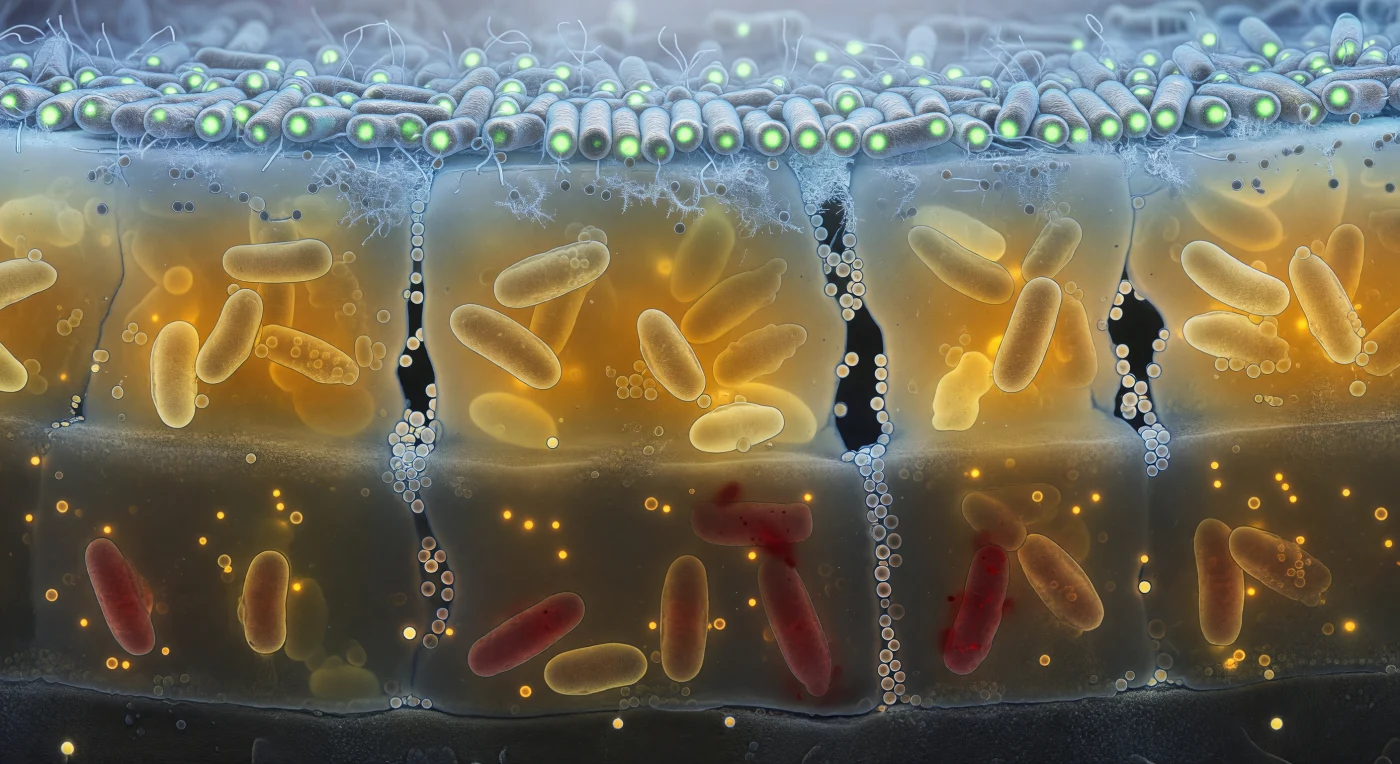
Der Blick fällt auf eine lebendige Gesteinsformation, die sich nicht aus Stein, sondern aus Bakterien zusammensetzt – ein 50 Mikrometer dicker Biofilm, aufgeschnitten wie ein Gebirgsquerschnitt, der drei leuchtende Provinzen übereinanderschichtet. An der Oberfläche drängen sich stabförmige Zellen Schulter an Schulter, ihre Membranen von einem kaltblauen Sauerstoffschimmer durchflutet, der GFP-Fluoreszenz in ein dichtes Feld eisgrüner Laternen verwandelt; Flagellen und extrazelluläre Fibrillen kristallisieren wie Reif auf Glas aus dem Licht heraus. Darunter verdickt sich die extrazelluläre polymere Substanz zu einem bernsteinfarbenen Harz, in dem metabolisch gestresste Zellen halb versinken, während dunkle Wasserkanäle – ausgekleidet mit schwebenden Membranvesikeln – senkrecht durch das gummiartige Gel schneiden und an Seifenblasen in zähflüssiger Stille erinnern. In der hypoxischen Tiefe löst Propidiumiodid die Membranen sterbender Zellen in ein schwaches Rotglühen auf, und der dunkle Mineraluntergrund – seine Oberfläche im Nanometerbereich aufgeraut, besetzt mit dauerhaft haftenden Pionierzellen – verankert das gesamte Gefüge wie ein Felsplateau, das eine Stadt aus Chemie trägt.

In absoluter Dunkelheit, die körperlich wirkt, schwebst du im Inneren eines einzelnen teilenden Bakteriums – dein gesamtes Blickfeld wird von der Geisterarchitektur einer einzigen Zelle eingenommen, rekonstruiert aus Tausenden einzelner Fluorophor-Lokalisierungen mit einer Präzision von zwanzig Nanometern. Vor dir beschreibt ein gebrochener Bogen goldgelber Leuchtpunkte den FtsZ-Ring am Zelläquator: kein geschlossener Kreis, sondern eine Folge diskreter Oligomer-Cluster, jede Lücke ein stummes Zeugnis der dynamischen Instabilität dieses Teilungsringes, der im Begriff ist, die Zelle in zwei Tochterzellen zu schnüren. Zu deinen Seiten ziehen sich zwei helicale Schienen kühler Cyan-Punkte in die Tiefe – das MreB-Aktinhomolog, dessen schraubenförmige Anordnung entlang der Zellachse die zylindrische Gestalt der Bakterienzelle mechanisch erzwingt und erhält. Über dir und unter dir wölbt sich ein dichtes, glutrot glühendes Gewölbe aus Membran-Lokalisierungen, so eng gedrängt, dass sie fast zu kontinuierlichen Bögen verschmelzen, und doch bleibt jeder Punkt ein für sich gewonnenes Photonenereignis. Die Tiefenkodierung verwandelt den Raum in einen thermischen Gradienten: nahe Moleküle brennen in warmem Bernstein, ferne verblassen durch Kupfer und Bronze bis hin zu kaltem Violett an den Zellpolen, sodass du im Inneren einer molekularen Entscheidung stehst – der Geometrie des Lebens selbst, kurz bevor es sich verdoppelt.
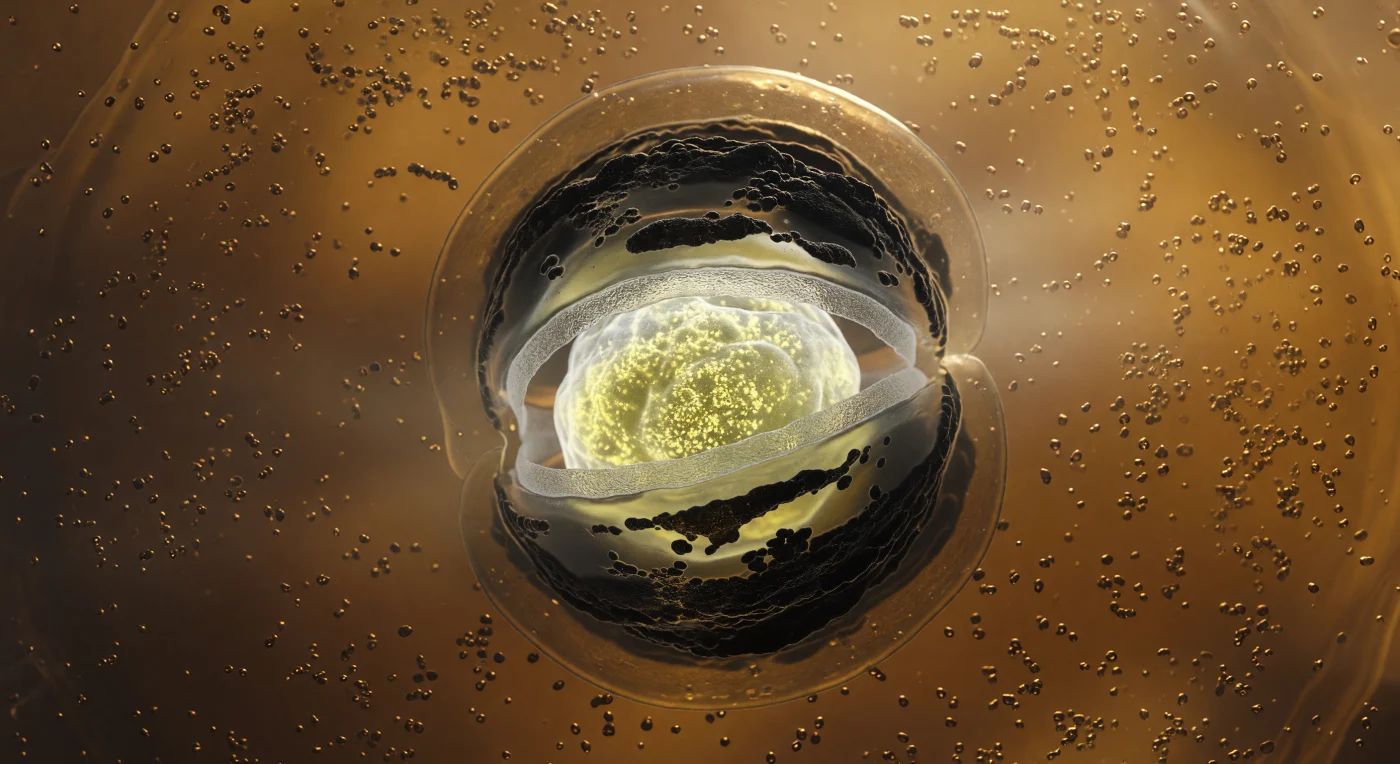
Im Inneren der Mutterzelle von *Bacillus subtilis* öffnet sich ein bernsteinfarbener Hohlraum, dessen warmes Licht von Millionen dichter Ribosomen-Granula aufgefangen wird – eine zähflüssige Welt, in der jedes schwebende Teilchen von der molekularen Viskosität des Zytoplasmas festgehalten wird, als hätte sich das Wasser selbst in Honig verwandelt. Im Mittelpunkt dieser Szenerie dominiert die Vorspore wie eine leuchtende Welt in der Welt: ein ovoides Gebilde, das von innen heraus kalt und mineralisch glüht, gespeist durch extrem dichte Kalzium-Dipicolinat-Ablagerungen und die kondensierte DNA, die von säurelöslichen Proteinen (SASPs) ummantelt ist und so vor dem Zerfall während der Reifung geschützt wird. Konzentrisch um diesen Kern legt sich ein zartes, milchig-graues Gerüst aus Peptidoglukan-Kortex wie mattgeschliffenes Glas, bevor dunkel polymerisierte Hüllproteine – SpoIVA und CotC – in matte, fast vulkanisch wirkende Schichten nach außen wachsen und das Licht des Inneren verschlucken. Was den Blick jedoch fesselt, ist die engulfierende Doppelmembran: zwei irisierend-glänzende Lipidschichten, die sich in einer dramatischen, phagozytoseartigen Umarmung um den Äquator der Vorspore krümmen, auf der Innenseite in warmem Amber leuchtend und auf der Außenseite in tiefes Kupferbraun schattierend, während das verbleibende Zytoplasma zwischen den Membranbögen langsam verdrängt wird und die Sporulation ihrem Abschluss entgegentreibt.

Der Blick nach oben offenbart einen geometrischen Koloss: Der ikosaedrische Kapsidkopf des T4-Phagen, gut hundert Nanometer breit, hängt wie ein gefacettierter Fremdkörper über der LPS-Oberfläche von *Escherichia coli*, seine kalten dunkelgrauen Flächen von feinen goldenen Kapsomernähten durchzogen, das Ganze in dem diffusen, quellenlosen Blaulicht tiefer wässriger Immersion gebadet. Sechs lange Schwanzfasern spreizen sich radial auf das türkis-goldene Lipopolysaccharid-Terrain hinunter, ihre rezeptorbindenden Proteinenden drücken sich in die Membranoberfläche wie Greiforgane eines präzisen molekularen Automaten – jeder Kontaktpunkt eine winzige mechanische Einbuchtung im Lipidblatt, sichtbar als leichte Verdichtung der LPS-Moleküle um jeden Auflagepunkt. Im Zentrum des Bildes hat die Schwanzröhre die Membran bereits durchstoßen: ein kaum drei Nanometer breiter Nanoporus, dessen Rand von leicht aufgeworfenen, ungeordneten Lipiden gesäumt wird, während das darunterliegende Periplasma als dunklerer Tealschatten durch den Einbruch schimmert. Durch diesen Kanal strömt ein blassblau-weißes Filament aus Einzelstrang-DNA – opaleszent wie Glasfaser in der Dunkelheit – vom Kapsid in die bakterielle Innenwelt hinein, getrieben vom osmotischen Druckgefälle einer Injektion, die in wenigen Sekunden das genetische Schicksal der gesamten Zelle neu schreiben wird. Im Hintergrund treiben zwei weitere Phagensilhouetten in der wässrigen Tiefe, ihre noch ausgestreckten Schwanzscheiden kalt silbern schimmernd – eine lautlose, unausweichliche Besetzung auf molekularer Ebene.
















