Confianza científica: Muy alto

El observador se encuentra suspendido en el interior de una muralla viviente, rodeado en todas las direcciones por una arquitectura densa y tridimensional de cadenas de glicano entrelazadas: largos bastones semitranslúcidos de ámbar cálido y siena tostada que se curvan suavemente y capturan la luz difusa a lo largo de su longitud, unidos entre sí por puentes peptídicos más cortos y pálidos —marfil desvanecido y oro polvoriento— que tejen una malla de extraordinaria compresión, como piedra antigua compactada durante eones. Esta es la pared de peptidoglicano de *Bacillus subtilis*, una bacteria Gram-positiva cuya muralla puede alcanzar entre 20 y 80 nanómetros de espesor y está compuesta por múltiples capas de glucanos de N-acetilmuramoil entrecruzados, una estructura que no solo da rigidez mecánica a la célula contra la presión osmótica interna —que puede superar varias atmósferas— sino que también define la identidad bacteriana ante el sistema inmune del huésped. Descendiendo entre los intersticios del andamiaje ambarino, cadenas de ácido teicoico caen en cortinas sinuosas de verde oscuro con destellos de teal, polímeros aniónicos que modulan la carga electrostática de la superficie y regulan el tráfico de iones y proteínas a través de la pared. Por debajo, apenas entrevista a través de la profundidad de la malla, la membrana plasmática se ondula como una lámina de aceite caliente, radiando un calor áureo hacia arriba, mientras que en la dirección opuesta el reticulado se deshilacha progresivamente hasta disolverse en la vasta y fría extensión azul pálido del entorno extracelular acuoso, donde el agua —gobernada a esta escala por la viscosidad y el movimiento browniano, no por la gravedad— aguarda como un océano difuso e indiferente.
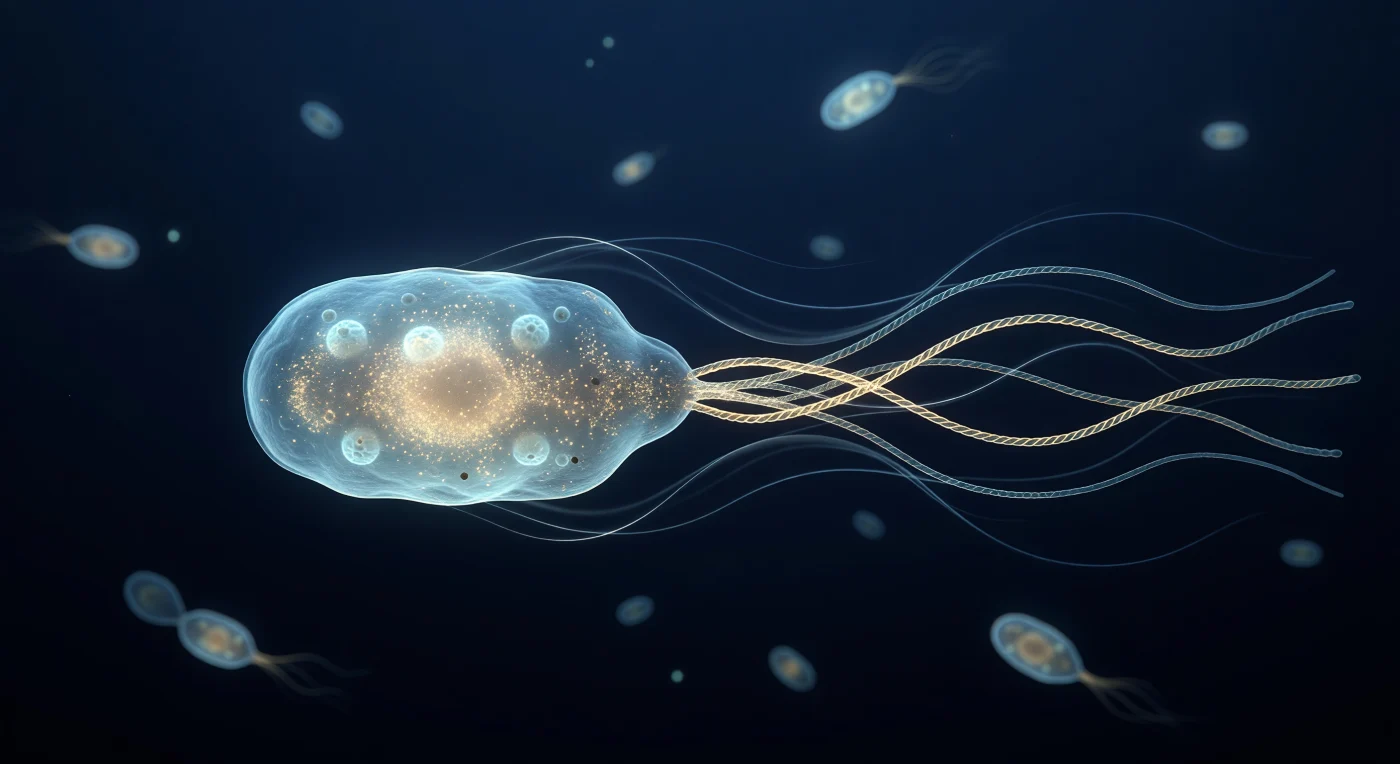
Te encuentras suspendido justo detrás de una célula de *Escherichia coli*, tan cerca que su cuerpo translúcido color cian pálido llena casi todo tu campo visual como el casco de una embarcación vista desde una pequeña lancha de remolque, con su membrana exterior trazando un fino ribete plateado donde la biología viva se separa del medio acuoso que la rodea. Detrás de ti —o más bien, detrás de la célula— cuatro filamentos flagelares de oro pálido se han trenzado en un único haz superhélico que gira en sentido antihorario a más de cien revoluciones por segundo, difuminándose en una cuerda iridiscente que se adentra en la oscuridad azul marino como un resorte en tensión disuelto en tinta. A esta escala la inercia no existe: el agua que te rodea se comporta como glicerina espesa, y el movimiento cesa de forma instantánea en cuanto la maquinaria rotante se detiene, de modo que cada trazo plateado-azulado que ondula hacia adelante —las líneas de flujo laminar de Stokes— es un testimonio visible de un mundo donde la viscosidad es la única ley mecánica que importa. En el interior de la célula, una neblina ámbar granulada delata decenas de miles de ribosomas apretujados en un citoplasma tan denso como un gel, mientras que en la lejanía azul oscura una docena de siluetas bacterianas fuera de foco flotan como brasas frías, sus halos capsulares captando la tenue luminiscencia molecular que, sin ninguna fuente identificable, parece emanar de la vida misma.

Flotas en el corazón de una bacteria viva, rodeado en todas las direcciones por una nube fractal de ADN superenrollado que llena el espacio como una nebulosa comprimida hasta el límite de lo concebible: gruesas cuerdas de doble hélice se trenzan sobre sí mismas en bucles plectonémicos que se ramifican una y otra vez, de un azul marino profundo en su núcleo más denso y de un cobalto suave y autoluminoso en los bordes, bañando el entorno en una radiance fría y omnidireccional, sin sombras duras, como tinta bioluminiscente disuelta en agua helada. A lo largo de cada curva pronunciada, pequeñas esferas proteicas de color amarillo cálido —las proteínas nucleoides HU y Fis— abrazan el ADN con precisión mecánica, plegando la fibra en pliegues agudos y devolviendo el azul circundante como destellos ámbar dorado, constelaciones diminutas distribuidas por todo el campo visual. El espacio entre las espiras no existe como vacío: un medio citoplasmático gelatinoso y translúcido —cargado de proteínas a concentraciones de cientos de miligramos por mililitro— actúa como un vidrio ahumado de aguamarina, borrando cualquier perspectiva limpia y disolviendo los bucles más distantes en planos sucesivos de índigo que se oscurecen hacia el azul-negro. En la periferia de la nube, donde el nucleoide cede terreno al citoplasma, esferas pardo oscuras y ligeramente desenfocadas marcan la presencia de ribosomas —máquinas de síntesis de proteínas de apenas veinte nanómetros— agrupados en la zona de transición entre el territorio del ADN y la cara interna de la membrana plasmática, recordando que este laberinto fractal, comprimido en menos de un micrómetro cúbico, no es una estructura inerte sino una máquina viva en pleno funcionamiento.

Te encuentras suspendido a apenas 150 nanómetros sobre la membrana externa de una *Escherichia coli*, y lo que se extiende ante ti no es una superficie inerte sino un paisaje biológico en perpetuo movimiento: una vasta llanura ondulante de lipopolisacáridos que oscila entre el verde azulado y el oro antiguo, cuyos largos brazos de oligosacáridos se mecen erguidos en el medio viscoso como algas en un mar sin viento, bañados en una luminiscencia fría y difusa que asciende desde las profundidades translúcidas de la bicapa lipídica. Cada veinte nanómetros aproximadamente, los trímeros de porinas en barril beta irrumpen desde la membrana como torres de obsidiana pulida, sus cavidades huecas perforando el plano en canales oscuros hacia el espacio periplásmico invisible más abajo, mientras entre ellos los parches cristalinos del Lípido A centellean con interferencia de fase en cobalto profundo, verde azumar y oro pálido, atrapados en ese estado liminal entre lo sólido y lo líquido cristalino. A la izquierda del horizonte curvado —porque incluso aquí la membrana se curva como la superficie de un pequeño planeta tibio— el cuerpo basal flagelar se eleva como una plataforma industrial de aros proteicos cromados, su gancho naciente desapareciendo en la bruma iónica del medio acuoso circundante, ese caldo denso de cargas electrostáticas donde la capa de Debye dispersa la luz ambiente en aureolas plateadas. Todo el mundo vibra con el ruido térmico de una bicapa lipídica que fluctúa millones de veces por segundo, un recordatorio de que esta quietud visual es ilusoria: estás dentro de una maquinaria viviente cuya escala hace que la gravedad sea irrelevante y donde el agua misma se comporta como miel espesa.

El espacio que te rodea no tiene horizonte: en todas las direcciones, esferas oscuras y compactas se apilan como adoquines húmedos de una calzada antigua, separadas únicamente por franjas de ámbar viscoso tan estrechas que parecen el mortero entre piedras milenarias, y el conjunto entero presiona desde todos los flancos con un peso casi geológico. Estas son las máquinas traductoras de la célula —ribosomas de 70S, cada uno apenas veinte nanómetros de diámetro—, y están tan concentrados en este citoplasma que la noción de espacio vacío ha desaparecido por completo, sustituida por una densidad de macromoléculas cercana a los 300 miligramos por mililitro, más cercana a una resina tibia que al agua. A media distancia, cadenas de polisomas atraviesan la escena como collares de perlas irregulares: seis ribosomas enhebrados en un filamento de ARN mensajero apenas visible, un hilo crema pálido que se curva bajo su propio peso molecular antes de disolverse en la penumbra marrón. A la izquierda, el complejo chaperonínico GroEL emerge como el tocón de un árbol petrificado, su arquitectura de doble anillo en gris pizarra dominando un cuadrante entero con la verticalidad de una columna entre adoquines. De vez en cuando, un destello verde esmeralda —una proteína etiquetada con GFP que pasa fugaz entre las esferas— es la única nota de color que interrumpe este universo monocromático y denso antes de ser engullida de nuevo por la oscuridad resinosa.

La mirada cae desde una altura de doce micrómetros sobre una metrópolis que jamás fue proyectada por ningún arquitecto: torres en forma de champiñón se elevan veinte, treinta, cuarenta micrómetros desde el sustrato, cada una irradiando una luminiscencia jade continua que proviene de proteínas fluorescentes expresadas en cada célula viva, y en sus superficies curvadas es posible distinguir, a pesar de la escala, los cuerpos cilíndricos individuales de las bacterias —varillas de cerámica húmeda apretadas unas contra otras como dovelas de una bóveda orgánica. Entre las torres, canales completamente oscuros surcan la matriz con una precisión casi hidráulica, corredores de agua que el propio flujo ha mantenido despejados y que actúan como sistema circulatorio de esta ciudad viviente, mientras el gel de polisacáridos extracelulares que ocupa los espacios intermedios se muestra ámbar translúcido, levemente autofluorescente en naranja, deformado en meniscos y superficies irregulares que hablan de deposición lenta y flujo viscoso a número de Reynolds infinitesimal. En las bases de las torres más maduras, donde el oxígeno no llega porque la propia colonia lo consume antes de que pueda difundir hacia el interior, manchas de rojo coral sangran a través de la matriz semitransparente —células cuyas membranas han cedido y cuyos ácidos nucleicos quedan teñidos desde dentro, brasas hipóxicas bajo un dosel verde. Todo el paisaje, desde el primer plano nítido hasta el horizonte disuelto en bruma de jade y ámbar, se extiende en silencio absoluto sobre una distancia que no llega al grosor de un cabello humano, y sin embargo contiene una arquitectura funcional completa: estructura, transporte, señalización y muerte.
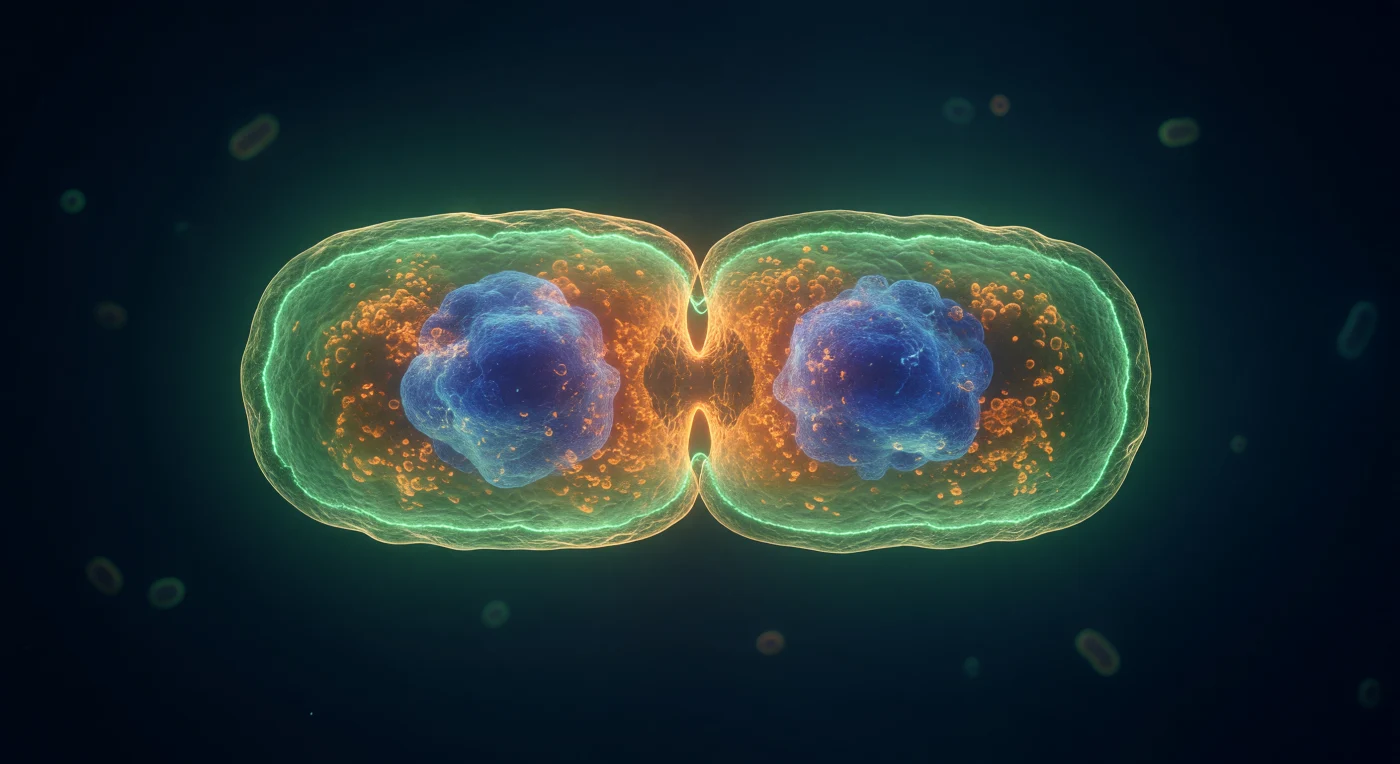
En este instante suspendido en el tiempo, el observador orbita el ecuador de una bacteria *E. coli* en el preciso momento de su escisión: el anillo FtsZ resplandece como una corona continua de verde eléctrico, una banda fluorescente de apenas doscientos nanómetros de ancho que ciñe la constricción en forma de reloj de arena como si una llama bioluminiscente hubiera encontrado la manera de doblarse sobre sí misma en geometría perfecta. Este anillo no es una estructura pasiva sino un andamio dinámico de protofilamentos de la proteína FtsZ —homóloga bacteriana de la tubulina eucariota— que polimeriza, se curva y genera fuerza de constricción mediante hidrólisis de GTP, coordinando desde el interior toda la maquinaria que tabicará la célula madre en dos hijas genéticamente idénticas. A través de la pared celular translúcida, de esa fina lámina dorada de peptidoglicano entretejido, se distinguen dos masas nucleoides teñidas de índigo cobalto, ya completamente segregadas hacia cada polo naciente, mientras el citoplasma intermedio hierve en silencio con una densidad ambarina de ribosomas empaquetados a concentraciones de varios cientos de miligramos por mililitro, un estado más próximo a un gel molecular que a una solución acuosa. En este régimen de bajos números de Reynolds, donde la viscosidad aplasta cualquier inercia y el movimiento browniano sacude sin cesar cada filamento proteico, la división celular no es un acto violento sino una constricción lentísima y orquestada con precisión molecular, un drama bioquímico que durará varios minutos antes de que el istmo naranja de la membrana interna —cuya doble curva enmarca el pinzamiento como un paréntesis luminoso— se cierre definitivamente y dos vidas independientes comiencen.

Ante ti se extiende la cadena de magnetosomas de *Magnetospirillum* como una avenida de monolitos minerales suspendida en un medio ámbar denso y turbio: quince cristales cúbicos negros como obsidiana, cada uno varias veces tu propia altura, dispuestos con una precisión geométrica que ningún proceso abiótico podría igualar. Su superficie facetada —magnetita pura, Fe₃O₄, sintetizada bajo control genético estricto dentro de vesículas lipídicas individuales— capta la luz difusa del citoplasma y la devuelve en destellos azul-violeta, como si cada mineral albergara su propia luminiscencia profunda. Este conjunto actúa como una brújula viva: la célula lo hereda, lo mantiene alineado a lo largo de su eje mayor gracias al filamento citosquelético MamK —visible aquí como un carril de cobalto eléctrico que ancla cada vesícula con precisión nanométrica— y lo utiliza para orientarse a lo largo de las líneas del campo geomagnético terrestre en un comportamiento llamado magnetotaxis. El citoplasma que te rodea no es un líquido sino un gel macromolecular opaco, sembrado de ribosomas que flotan y derivan en su agitación browniana incesante, la misma fuerza térmica que haría imposible cualquier movimiento dirigido si no fuera por los anclajes moleculares que mantienen esta arquitectura exactamente donde debe estar. Más allá de la membrana interna —esa frontera dorada que se curva alejándose en la penumbra— el mundo exterior no existe: solo oscuridad acuosa, campo magnético invisible, y la presión silenciosa de un entorno que esta célula lleva décadas aprendiendo a leer.
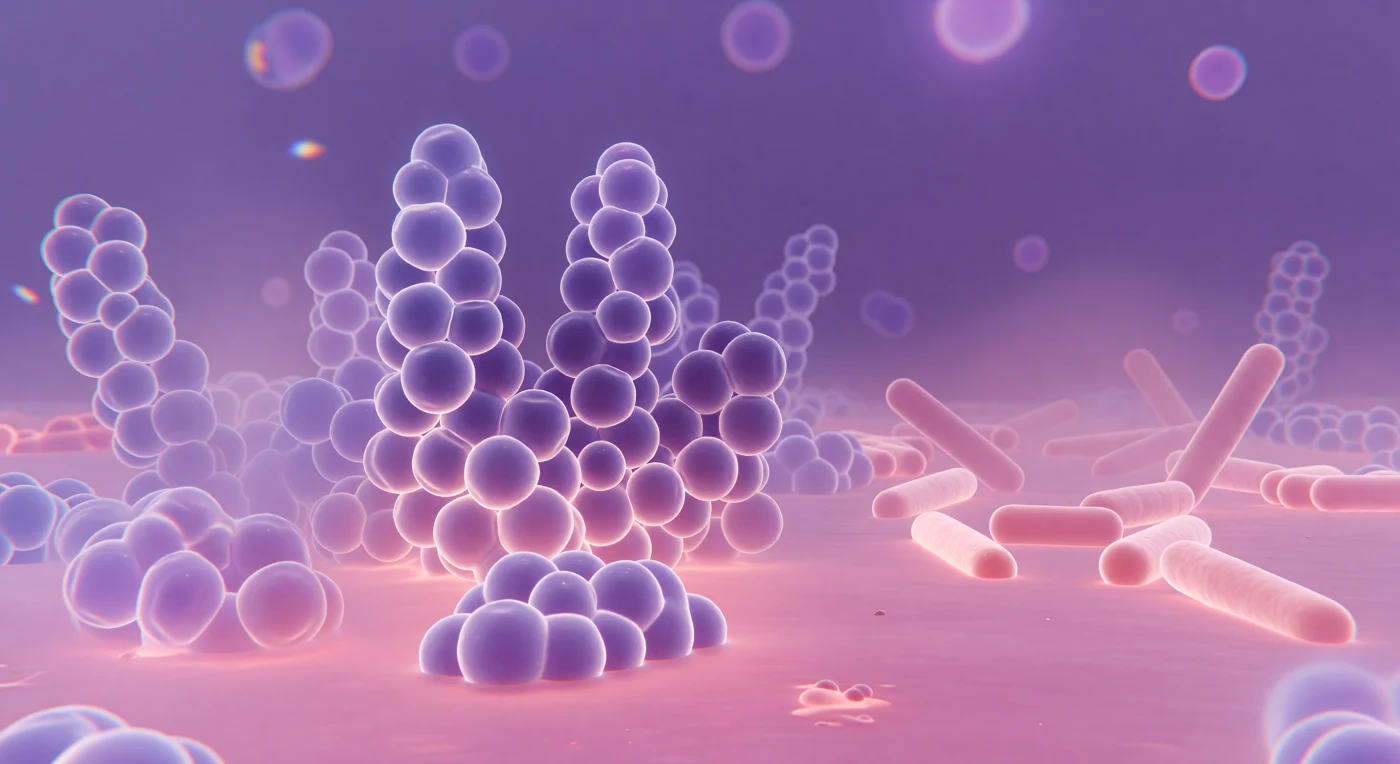
En este mundo teñido de violeta profundo y rosa empolvado, el observador se encuentra de pie ante colosales esferas de *Staphylococcus aureus* que se alzan en racimos apretados, cada una envuelta en una corona iridiscente donde la luz, cuya longitud de onda apenas supera el tamaño de las propias células, se dobla y se deshace en halos de difracción — un fenómeno físico que marca el límite absoluto de lo que el vidrio óptico puede revelar. La pared celular de estas bacterias Gram-positivas, saturada de cristal violeta atrapado en su gruesa malla de peptidoglicano de hasta 80 nanómetros de espesor, convierte cada esfera en una fortaleza de pigmento oscuro que contrasta con el baño rosado de safranina que cubre el suelo entre los clusters, señalando la presencia de bacilos Gram-negativos — formas elongadas de *Escherichia coli* — cuyos envolventes más delgados retienen apenas el contratinte, dejándolas en un tono melocotón suave. La profundidad de campo aquí es brutal en su estrechez: apenas unos nanómetros fuera del plano focal y las células se disuelven en fantasmas translúcidos, sus contornos sangrados en el halo lavanda circundante, recordando que este universo existe en capas simultáneas de materia viva que ningún microscopio óptico puede mostrar al mismo tiempo. La luz no proyecta sombras sino que emana desde abajo como a través de un cristal luminoso, impregnando cada superficie de una luminiscencia interior húmeda, la de un mundo donde la gravedad no existe, el agua se comporta como almíbar y cada molécula vibra con energía térmica suficiente para mover montañas a esta escala.
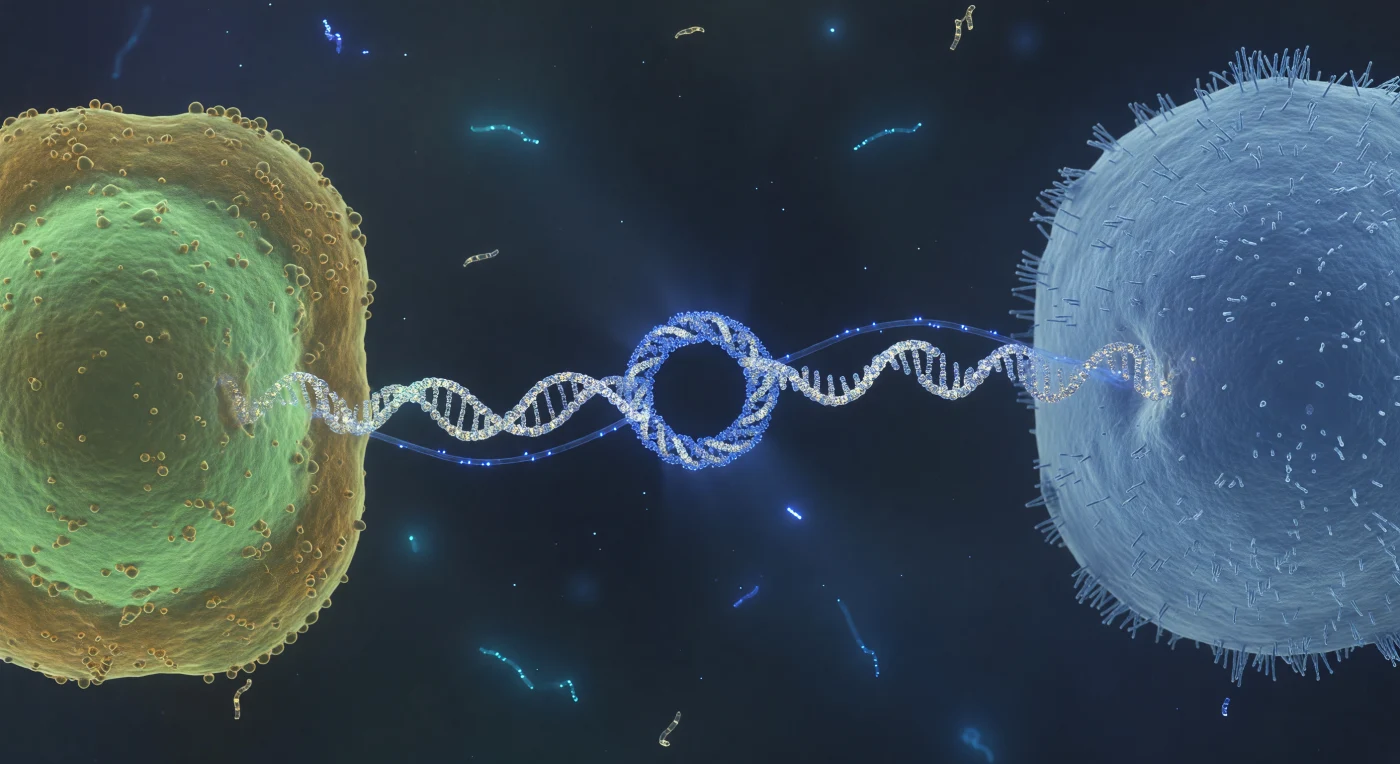
Suspendidos entre dos células bacterianas que se tocan en un silencio casi absoluto, contemplamos el puente de conjugación: un cable proteico helicoidal de apenas 8 nanómetros de anchura que se extiende tenso entre el cuerpo celular verde-celadón del donador —cuya membrana externa ondula como una lámina de ámbar salpicada de porinas— y la superficie azul pálido y erizada del receptor, un monolito cubierto de fimbrias como escarcha densa. En el punto de contacto directo entre ambas células, el poro conjugativo se materializa como un anillo oscuro y perfectamente circular de 20 nanómetros, orlado por un halo de densidad proteica que capta la luz ambiente como acero bruñido; es por aquí por donde el material hereditario cruza de un organismo a otro. A través del canal del pilus fluye un filamento de ADN monocatenario que pulsa con una luminiscencia eléctrica azul, difuminándose en sus bordes hacia el medio acuoso circundante como la luz que sangra por una fibra óptica, traduciendo en imagen visible un proceso que redefine el linaje genético de la célula receptora sin que medie ninguna reproducción. En el fondo oscuro del fluido —tan viscoso a esta escala que cualquier movimiento se detiene en el instante en que cesa la fuerza que lo produce— derivan como susurros de luz cian fragmentos de ADN libre, testimonio fantasmal de intercambios anteriores que el movimiento browniano dispersa sin destino en la penumbra del medio extracelular.
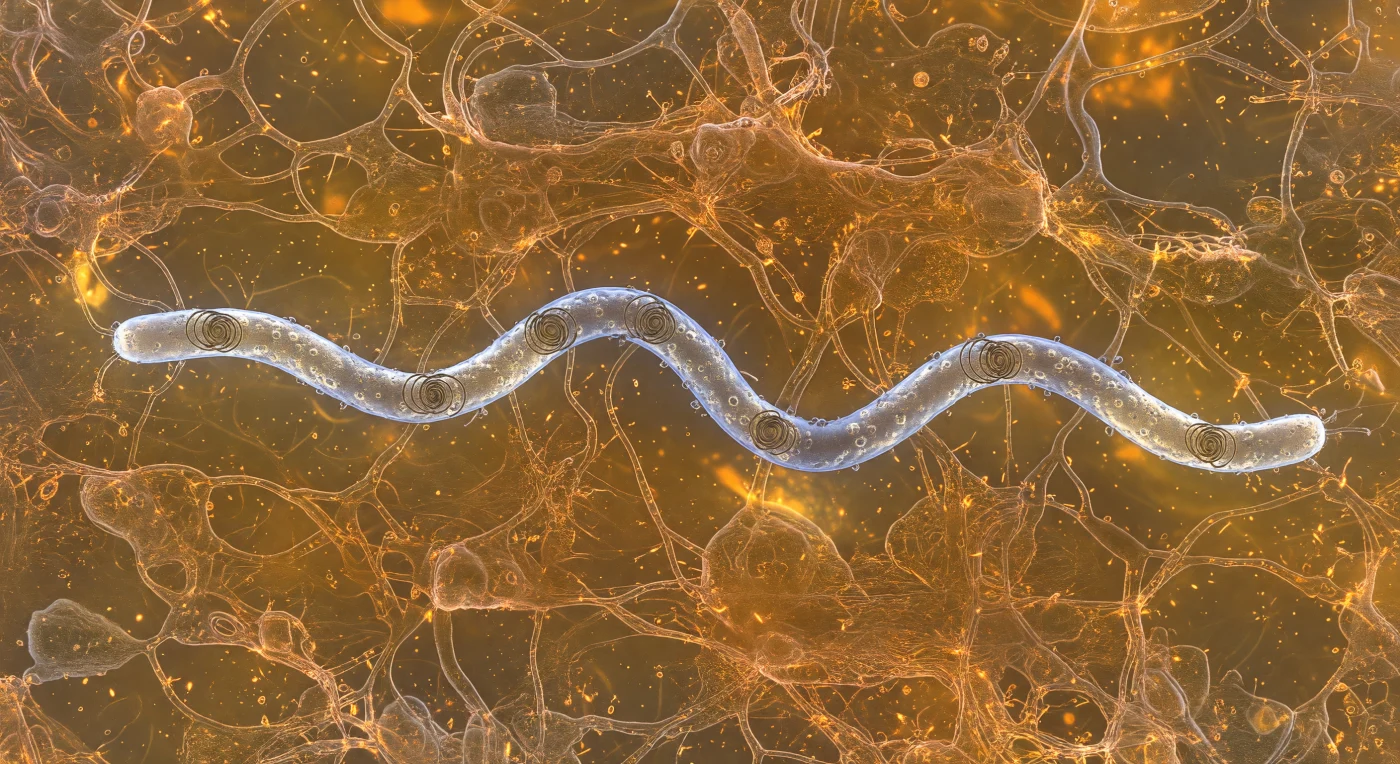
Suspendido en la misma dimensión que el ser vivo más estudiado y menos visto, el observador flota en una matriz de mucina que se extiende como ámbar tibio iluminado desde adentro, donde filamentos de glucoproteína tejen una red tridimensional de cobre y oro que atrapa la luz difusa del propio medio biológico. A apenas cinco micrómetros a la izquierda, *Borrelia burgdorferi* avanza con precisión mecánica: su cuerpo helicoidal de dieciocho micrómetros ejecuta una undulación de onda plana impulsada por flagelos periplásmicos —cables helicoidales confinados bajo la vaina exterior— que nunca tocan el medio pero deforman toda la célula en una ola viajera, un mecanismo evolutivo perfeccionado para atravesar medios viscoelásticos de bajo número de Reynolds donde el agua se comporta como jarabe espeso y el movimiento cesa en el instante en que cesa la fuerza. La membrana externa de la bacteria devuelve la luminiscencia ambiental como un frío destello plateado e iridiscente, con cada clúster de proteínas de superficie visible como una pequeña protuberancia sobre una lámina de platino trabajado en espiral, mientras los extremos de la espiroqueta parten la red de polímeros en una estela en V que se cierra lentamente detrás de ella como una ola de sirope en cámara lenta. El mundo entero —confinado, cálido, químicamente activo— es una solución densa donde la gravedad ha dejado de existir y el movimiento browniano sacude cada partícula con la misma energía que mueve moléculas, recordando al observador que la vida, en su escala más antigua, ocurre en un universo gobernado por la viscosidad y el azar térmico.

Desde el interior de una *Synechocystis* viva, el mundo se despliega como una catedral de membranas paralelas que se curvan hacia el infinito en todas direcciones, cada superficie ardiendo con una luminiscencia carmesí profunda que emana de los complejos de clorofila enterrados en la bicapa lipídica, bañando el citoplasma ámbar en tonos borgoña e rojizos que se intensifican en los estrechos corredores luminales, pasillos de apenas unos nanómetros de ancho llenos de un fluido viscoso dorado-jade que conduce la luz como niebla volumétrica. Las superficies membranales no son lisas sino densamente encostradas con ficobilisomas hemisféricos de color naranja coral y amarillo azafrán —complejos antena que capturan fotones y los transfieren a los fotosistemas embebidos en la membrana—, apretados uno contra otro como cúpulas barrocas que dispersan halos ámbar lateralmente, convirtiendo cada calle entre membranas en un túnel de color estratificado y pulsante. Flotando en el espacio citoplasmático más allá del sistema tlacoide, los carboxisomas —cápsulas proteicas icosaédricas de unos 150 nanómetros de diámetro— se ciernen como linternas de marfil pálido y translúcido, sus interiores repletos de RuBisCO compactado que fija el CO₂ en condiciones de concentración controlada, cada una facetada y parcialmente iluminada por el resplandor rojo de las membranas vecinas. El citoplasma entre todas estas estructuras no está vacío sino que es una resina ámbar granular y translúcida, atestada de ribosomas que crean una textura fina como arena dorada en suspensión, mientras que en el límite curvo más lejano de la célula una neblina azul-verde suave sangra a través de la membrana plasmática, recordando que este universo autodiluminado de superficies radiantes y geometrías flotantes cabe por completo en el ancho de una décima parte de un cabello humano.
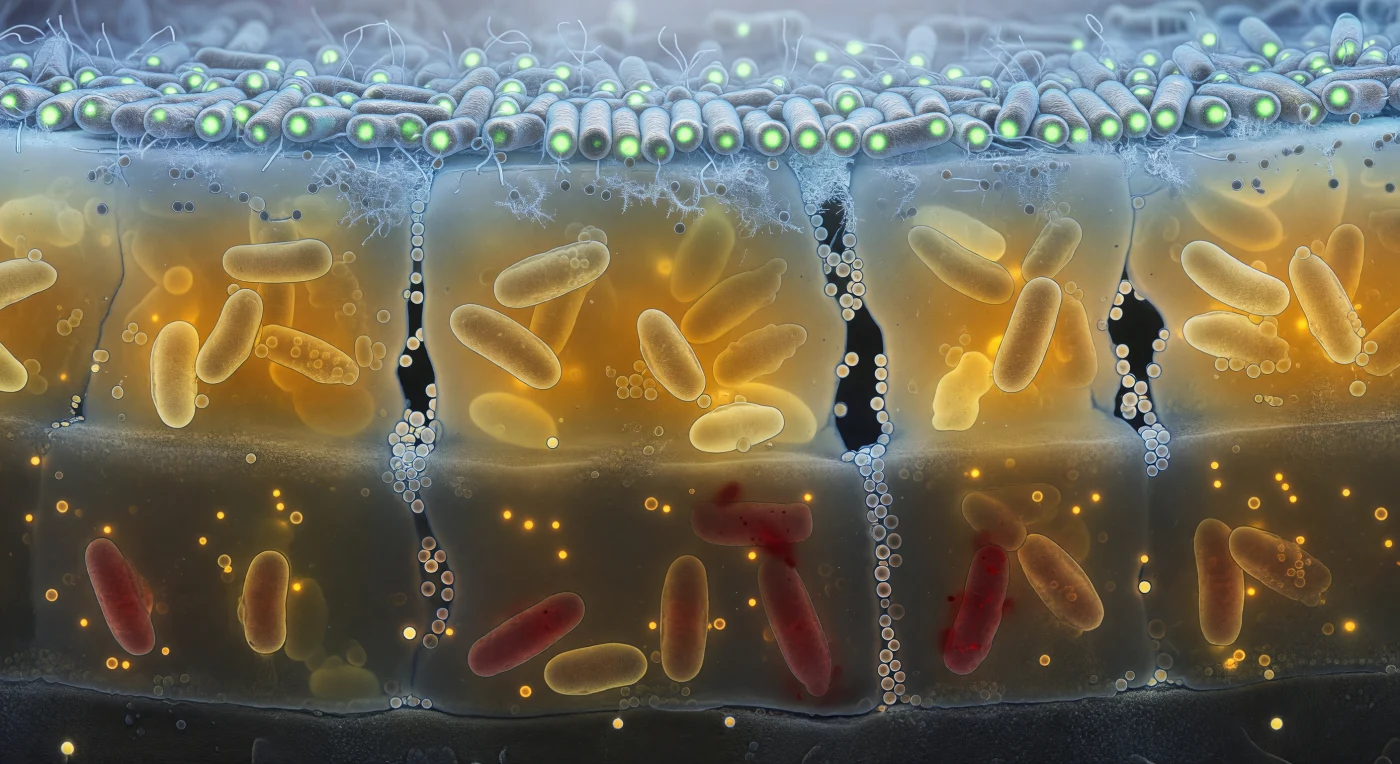
El observador se encuentra dentro de un corte vertical a través de una arquitectura viva estratificada, un mundo de apenas cincuenta micrómetros de espesor que se despliega como un cañón geológico con su propia luminosidad interna. En el estrato superior, los bastones bacterianos se aprietan en filas densas y ordenadas, sus membranas bañadas por una neblina azul-blanca que desciende desde la interfaz con el medio oxigenado, convirtiendo cada célula en un farol verde frío gracias a la fluorescencia de GFP; aquí el oxígeno es abundante, el metabolismo activo y los filamentos del glicocálix se extienden entre célula y célula como escarcha sobre vidrio. Más abajo, la sustancia polimérica extracelular —esa resina ámbar-translúcida secretada colectivamente por la colonia— absorbe y dispersa la luz, atrapando células metabólicamente estresadas en una matriz viscoelástica surcada por canales de agua oscuros y vacíos que actúan como vías de difusión para nutrientes y señales quórum. En el fondo hipóxico, casi sin oxígeno disuelto, el rojo tenue del ioduro de propidio tiñe las membranas comprometidas de las células muertas o moribundas, mientras vesículas de membrana —esferas perfectas de apenas unos cientos de nanómetros— flotan inmóviles en el medio viscoso como bioluminiscencia de aguas profundas, testigos de un ciclo continuo de muerte, lisis y reciclaje de nutrientes que alimenta las capas superiores. El plano del sustrato ancla todo desde abajo, rugoso a escala nanométrica, con las primeras células adheridas de manera irreversible mediante adhesinas, recordando que lo que parece un paisaje mineral es en realidad el punto de partida de toda esta arquitectura bacteriana vertical y autoorganizada.

De pie en la oscuridad absoluta de una reconstrucción STORM, el ojo no encuentra reposo en ningún horizonte continuo: solo puntos de luz discreta suspendidos en el vacío, cada uno el registro exacto de una única molécula fluorescente recuperada del ruido óptico. Un arco quebrado de manchas dorado-ambarinas dibuja el anillo de FtsZ en la cintura ecuatorial de la célula, una guirnalda incompleta cuya curvatura implica un círculo perfecto de casi cien longitudes de cuerpo de diámetro, proteínas divisoras que se agrupan en parches oligoméricos mientras la célula ensaya la decisión de partirse en dos. A ambos lados, dos series helicoidales de puntos cian-blanco frío trazan el andamiaje citoesquelético de MreB a lo largo del eje celular, raíles bioluminiscentes que se enroscan lentamente hacia la profundidad axial, mientras miles de puntos rojo-naranja forman el contorno de la membrana plasmática —tan densos que casi se funden en arcos continuos de brasa, y sin embargo cada uno permanece un nodo discreto e irrepetible. La codificación de profundidad convierte el interior de la célula en un gradiente térmico: las moléculas más cercanas arden en ámbar cálido y las más alejadas se enfrían hasta un violeta bruñido, como si uno estuviese de pie en el ecuador de un planeta molecular cuyos polos permanecen perpetuamente congelados, noventa por ciento del campo visual vacío absoluto y negro, porque así es la verdad de la materia a esta escala.
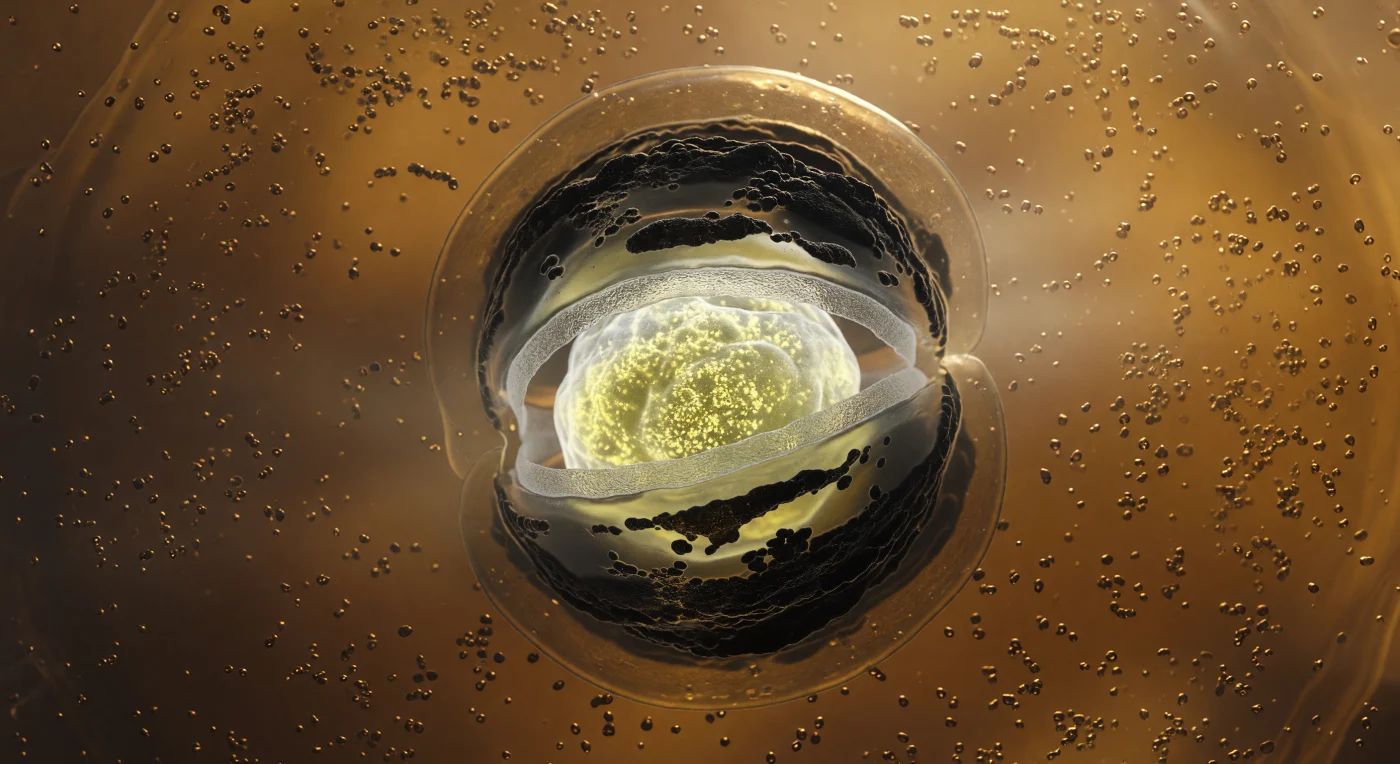
El observador se encuentra suspendido en el interior de una célula madre de *Bacillus subtilis*, rodeado por una caverna ámbar de citoplasma viscoso cargado de ribosomas que flotan como granos de arena húmeda en una miel tibia —un medio donde las fuerzas de inercia son insignificantes y toda materia queda atrapada en la resistencia del fluido, gobernada por el movimiento browniano más que por cualquier impulso dirigido. En el centro, la forespore irradia una luminosidad frío-mineral: los depósitos de calcio-DPA y el ADN condensado recubierto de proteínas SASP forman un núcleo denso más allá de cualquier estado biológico ordinario, envuelto sucesivamente por una delgada corteza de peptidoglicano que dispersa esa luz interior como vidrio esmerilado, y luego por capas concéntricas de proteínas de cubierta —SpoIVA, CotC— que polimerizan en arcos oscuros y casi mates que absorben la luz como roca volcánica enfriándose. Lo que verdaderamente detiene la mirada es la membrana envolvente: una doble lámina lipídica que se curva con dramatismo extremo alrededor del ecuador de la forespore en un abrazo fagocítico, sus dos superficies iridiscentes separadas apenas por un espacio periplásmico angosto, iluminadas desde dentro por el resplandor dorado-ámbar y ensombrecidas por fuera en un marrón cobrizo profundo. El citoplasma ribosomal, progresivamente excluido a medida que el engullimiento se acerca a su conclusión, llena el volumen restante con una neblina proteica semiopaca que difumina cada borde más allá de unos pocos cientos de nanómetros en un desenfoque suave, íntimo, irrevocablemente biológico.

El observador flota a ochenta nanómetros sobre la membrana externa de *Escherichia coli*, inmerso en un crepúsculo acuoso sin fuente luminosa definida, donde la vasta llanura de lipopolisacáridos se extiende en todas las direcciones como un continente de oro oxidado y verde azulado, interrumpida por los porines que emergen de la bicapa como chimeneas volcánicas rodeadas de un halo de luminiscencia electrostática. Directamente sobre esta superficie, el bacteriófago T4 desciende con la solemnidad silenciosa de un cuerpo celeste: su cápside icosaédrica de cien nanómetros de anchura —faces oscuras de gris metálico surcadas por costuras doradas donde los capsómeros encajan con precisión geométrica— eclipsa el horizonte superior mientras sus seis fibras de cola se despliegan radialmente hacia la membrana, presionando con sus dominios de unión al receptor como patas de un insecto arcaico que toma tierra sobre un terreno desconocido, deformando localmente la hoja lipídica en suaves depresiones de presión mecánica. En el centro exacto de la escena, el tubo de aguja ya ha perforado la membrana creando un poro de apenas tres nanómetros, cuyo borde muestra lípidos levemente desordenados y un patrón radial de tensión mecánica; desde la cápside desciende por ese conducto un hilo de ADN monocatenario de un blanco azul opalescente, liberado bajo presión osmótica hacia el espacio periplásmico como información genética en cascada. En el fondo acuoso, dos fagos adicionales flotan en la penumbra azul-grisácea con sus vainas de cola aún sin contraer y brillantes como plata fría, silhouetas de una ocupación silenciosa e inexorable que recuerda que en este mundo dominado por el ruido térmico, la gravedad es irrelevante y toda interacción se mide en longitudes de enlace molecular.
















