Confiance scientifique: Très élevé

Le regard se perd dans une architecture d'une densité vertigineuse : des chaînes glycaniques d'ambre et de sienna brûlé s'entrelacent en un maillage tridimensionnel compact, reliées par de courts ponts peptidiques couleur ivoire qui verrouillent l'ensemble en une maçonnerie organique d'une rigidité extraordinaire — c'est la paroi peptidoglycanide de *Bacillus subtilis*, épaisse de plusieurs dizaines de nanomètres, conférant à cette bactérie à Gram positif sa résistance mécanique face à une pression osmotique qui, à cette échelle, équivaudrait à plusieurs atmosphères. Entre les travées de glycanes se glissent des rideaux sinueux d'acides téichoïques vert forêt, polymères anioniques dont la charge électrostatique régule le passage des ions et des antibiotiques à travers ce labyrinthe. Plus bas, partiellement voilée par la profondeur du réseau, la membrane plasmique ondule comme une nappe d'huile chaude baignée d'or ambré, ses complexes protéiques enchâssés apparaissant comme de petites îles sombres dans le flux lipidique. Vers le haut, la trame se défait progressivement, les derniers brins de glycane se dissolvant en filaments fantomatiques avant de s'ouvrir sur l'immensité froide et bleutée du milieu extracellulaire, où la chaleur ambrée de la paroi cède la place à une lumière pâle et diffuse venue de nulle part.
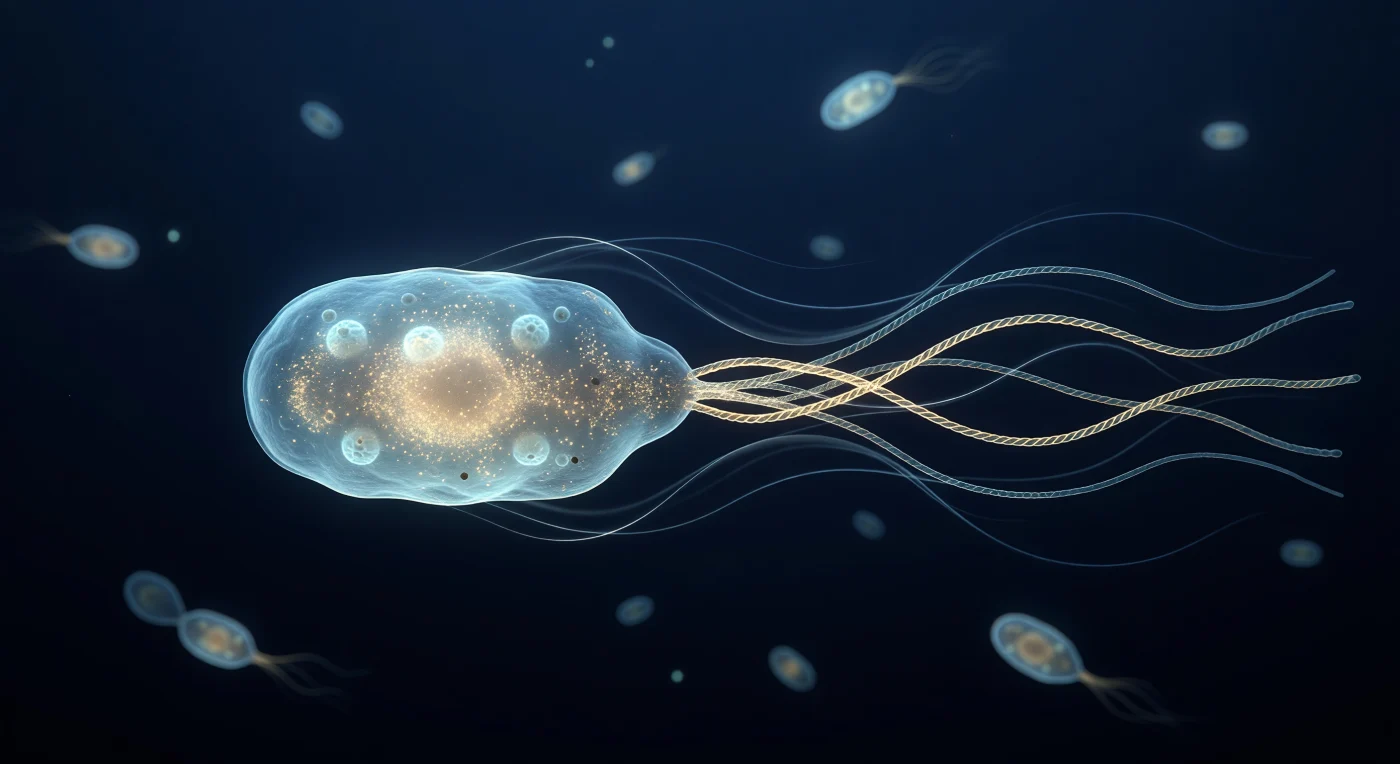
Vous vous trouvez suspendu dans le sillage immédiat d'une cellule d'*Escherichia coli*, si proche que son corps cylindrique translucide, d'un cyan pâle lumineux, occupe tout le centre de votre champ visuel comme la coque d'un submersible vu depuis une embarcation de remorquage — sa membrane externe scintille d'un fin liseré argent-bleu et ses porines y creusent de minuscules fossettes qui captent une lueur froide et phosphorescente, tandis que le cytoplasme intérieur se révèle comme un halo ambré et granuleux, dense de dizaines de milliers de ribosomes. Derrière la cellule, quatre filaments flagellaires se sont tressés en un faisceau superhélical unique, ce câble doré-ambré pivotant en sens inverse des aiguilles d'une montre à plusieurs centaines de tours par seconde, enveloppé d'un voile de flou cinétique qui trahit une rotation dont la puissance moléculaire semble disproportionnée à la taille infime des moteurs qui la génèrent. Dans ce régime de Stokes où le nombre de Reynolds avoisine dix puissance moins quatre, l'inertie n'existe plus : de délicats filaments volumétriques argent-bleu s'incurvent en arcs parfaitement symétriques depuis le faisceau vers la cellule, traçant dans le liquide les lignes de courant laminaires d'un monde où la viscosité est souveraine et où chaque mouvement s'arrête instantanément dès que la rotation cesse. En arrière-plan, une douzaine de silhouettes bactériennes fantômes dérivent dans le bleu nuit profond comme des braises suspendues, leurs halos capsulaires réduits à de purs disques de lumière diffuse, comprimés par la profondeur de champ en une intimité vertigineuse où quelques longueurs de cellule suffisent à dissoudre la matière vivante dans le bokeh de l'abîsse aqueux.

Au cœur d'une cellule d'*E. coli*, le regard plonge dans un univers sans horizon libre : des câbles d'ADN bleu marine s'enroulent sur eux-mêmes en supercoïles plectonémiques, se ramifiant en géométries fractales qui occupent chaque direction du champ visuel, sans jamais laisser apparaître le moindre couloir ouvert. Le long de chaque boucle, de minuscules nodules jaune-blanc — les protéines nucléoïde-associées HU et Fis — s'accrochent aux courbures les plus serrées, renvoyant une lueur ambrée chaude qui contraste avec la radiance cobalt froide et omnidirectionnelle émanant des fibres d'ADN elles-mêmes, comme une encre bioluminescente diffusant dans une eau glaciale. L'espace entre les boucles, à peine quelques dizaines de nanomètres de cytoplasme visqueux et macromoléculairement encombré, prend la qualité d'un verre aquamarine fumé, transformant les plans successifs en nappes d'indigo de plus en plus sombres. À la périphérie de ce nuage dense, là où le nucléoïde se raréfie, de sombres sphères brun-noir — les ribosomes — flottent en agrégats lâches dans une zone de transition légèrement moins comprimée, à peine nets, dissous dans le halo réfractif du milieu gélatineux. L'ensemble évoque l'intérieur d'une nébuleuse compressée à l'extrême : un espace où la notion de vide n'existe pas, où chaque ligne de regard se perd dans une nouvelle couche de matière vivante organisée à l'échelle du nanomètre.

Suspendu à seulement 150 nanomètres au-dessus de la surface d'*Escherichia coli*, le regard plonge sur une plaine ondulante d'une complexité vertigineuse : la membrane externe d'une bactérie Gram-négative vivante, dont les fluctuations thermiques soulèvent le lipopolysaccharide en vagues lentes et majestueuses, comme la surface d'une planète minuscule baignée d'une lumière de cryo-aube bleue et dorée. Toutes les vingt nanomètres environ, des trimères de porines bêta-barrel percent la membrane comme des tourelles d'obsidienne aux parois cannelées, leurs canaux intérieurs s'enfonçant en puits sombres à travers le feuillet lipidique vers le monde périplasmique en contrebas. Entre ces bastions protéiques, des domaines cristallins de Lipide A forment des pavages iridescents — cobalt profond là où deux phases se chevauchent, vert aquamarine où la lumière froide frappe une surface plane —, leur texture évoquant l'aile d'un coléoptère figée à la limite du cristal liquide. À l'horizon incurvé, le corps basal du flagelle s'élève comme une installation industrielle de précision biologique : ses anneaux protéiques empilés avec une régularité chirurgicale traversent la membrane en colonnes concentriques, son crochet nascent se perdant dans la brume ionique diffuse qui filtre au-dessus de ce monde électrostatiquement chargé.

Dans ce monde sans horizon ni vide, le regard ne trouve aucun refuge : des milliers de ribosomes 70S s'entassent comme des galets de basalte dans toutes les directions, séparés par des interstices si étroits qu'ils ressemblent moins à de l'espace qu'à du mortier sombre entre des pierres jointives, et le milieu qui les unit n'est pas de l'eau mais une résine ambrée tiède et visqueuse, saturée de macromolécules à une concentration de trois cents milligrammes par millilitre, rendant la notion même de solution aqueuse presque abstraite. Des chaînes polysomales traversent le champ comme des colliers de perles irrégulières, six ribosomes enfilés sur un filament d'ARN messager à peine visible, crème pâle contre le fond brun, ployant sous leur propre poids moléculaire avant de disparaître dans l'opacité résineuse au-delà de quelques longueurs de ribosome. À gauche, un chaperon GroEL en double anneau s'impose comme le tronc fossilisé d'un arbre immense, sa cavité centrale légèrement plus lumineuse et fraîche ouvrant une respiration verticale dans l'écrasement isotrope des sphères. Par intermittence, un éclair vert émeraude — une protéine marquée à la GFP — traverse brièvement la monochromie chaude avant d'être de nouveau occulté, seule ponctuation de couleur dans cette densité géologique où la profondeur ne se lit pas par la distance mais par l'assombrissement progressif vers un brun-noir d'encre.

Le regard plonge vers le bas selon un angle oblique, survolant une métropole silencieuse dont les tours ont poussé plutôt qu'été construites : des microcolonies en forme de champignons s'élèvent du substrat en spires jade luminescentes, chacune portant à sa surface des cellules bactériennes en forme de bâtonnets disposées en rosettes denses, leurs corps olivâtres pressés les uns contre les autres comme des tuiles sur une coupole, chaque individu ne mesurant qu'un à quelques micromètres de long. Entre ces édifices vivants, un réseau de canaux d'eau parfaitement noirs découpe la matrice extracellulaire de polysaccharides — un gel translucide couleur ambre, légèrement autofluorescent en orange chaud, que le courant hydraulique a sculpté avec une précision remarquable, assurant la distribution en oxygène et nutriments à l'ensemble de la communauté. Ce biofilm mature de *Pseudomonas* constitue une architecture collective régulée par le quorum sensing, où chaque tour représente des milliers de cellules clonales coordonnées dans une structure tridimensionnelle fonctionnelle dotée d'une division du travail spatiale. Au pied des spires les plus hautes, là où l'oxygène ne pénètre plus, des lueurs rouge corail trahissent des cellules hypoxiques en train de mourir dans l'ombre de leur propre colonie — rappel que même dans cette cité du vivant, les couches profondes sacrifiées soutiennent l'exubérance verte du dôme supérieur.
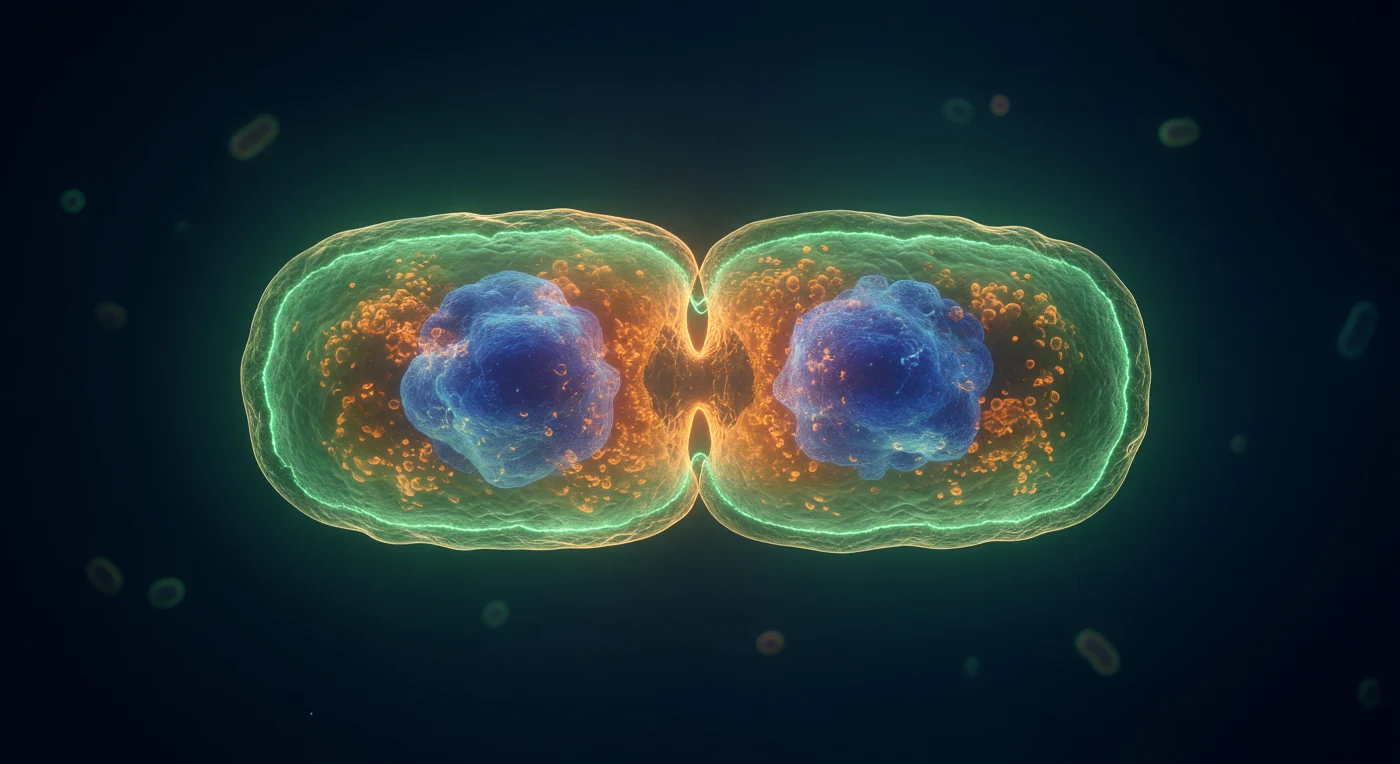
Nous orbitons à l'équateur d'une cellule d'*Escherichia coli* saisie au paroxysme de sa division, suspendue dans un milieu aqueux quasi-obscur comme un astre isolé dans l'espace profond — le corps cellulaire s'étire de part et d'autre en un cylindre translucide d'à peine deux micromètres de diamètre, ses membranes teintées d'orange chaud par le FM4-64 dessinant la double courbe d'un étranglement en sablier qui se resserre lentement sous la pression coordonnée de centaines de filaments protéiques. Là, ceinturant la totalité de la circonférence avec la précision d'une suture moléculaire, l'anneau Z de FtsZ brûle en vert GFP électrique — une bande fluorescente de deux cents nanomètres à peine, composée de protofilaments GTPasiques qui se polymérisent et se dépolymérisent en continu, générant la force mécanique nécessaire pour pincer la cellule en deux enfants identiques. À l'intérieur, visible à travers la paroi translucide comme des nébuleuses aperçues derrière du verre dépoli, deux masses nucléoïdes bleu cobalt DAPI ont achevé leur ségrégation, chacune tirée vers un pôle par le système de partition Min et les forces d'entropie de confinement, tandis que le cytoplasme environnant — une résine ambrée et granuleuse saturée de ribosomes à trois cents milligrammes de protéines par millilitre — transmet la lumière intérieure comme une lanterne biologique. Dans ce régime de très faible nombre de Reynolds où l'inertie n'existe pas et où l'agitation thermique gouverne chaque molécule, ce moment de clivage ne dure que quelques minutes, mais il condense l'intégralité du programme de réplication de la vie procaryote en un seul instant d'une beauté presque géologique.

Devant vous, la chaîne de magnétosomes de *Magnetospirillum* se déploie comme une colonnade minérale suspendue dans un brouillard ambré et grouillant, chacun des quinze cristaux cuboctaédriques de magnétite s'élevant à plusieurs fois votre hauteur, leurs surfaces facettées renvoyant des éclats bleu-violet dans la masse semi-opaque du cytoplasme. Ces cristaux de Fe₃O₄ sont le résultat d'une biominéralisation contrôlée gène par gène — leur taille et leur forme remarquablement uniformes, comprises entre 35 et 120 nanomètres, témoignent d'une régulation moléculaire d'une précision presque cristallographique, chaque minéral enveloppé dans sa propre vésicule lipidique dont la bicouche frémit doucement sous l'agitation thermique. Sous la rangée entière court le filament MamK, rail cytoplasmique d'un bleu électrique intense, polymère protéique analogue à l'actine qui maintient l'alignement de la chaîne le long de l'axe cellulaire, transformant cette assemblée de minéraux en un véritable compas biologique capable de percevoir le champ magnétique terrestre. Tout autour, des ribosomes denses comme des graviers sombres dérivent lentement dans le gel cytoplasmique — à cette échelle où la viscosité écrase la gravité et où le mouvement brownien secoue chaque granule, la cellule entière ressemble moins à un récipient qu'à un réacteur chimique vivant, sa membrane interne dorée se courbant à la périphérie vers l'obscurité absolue du milieu aqueux extérieur.
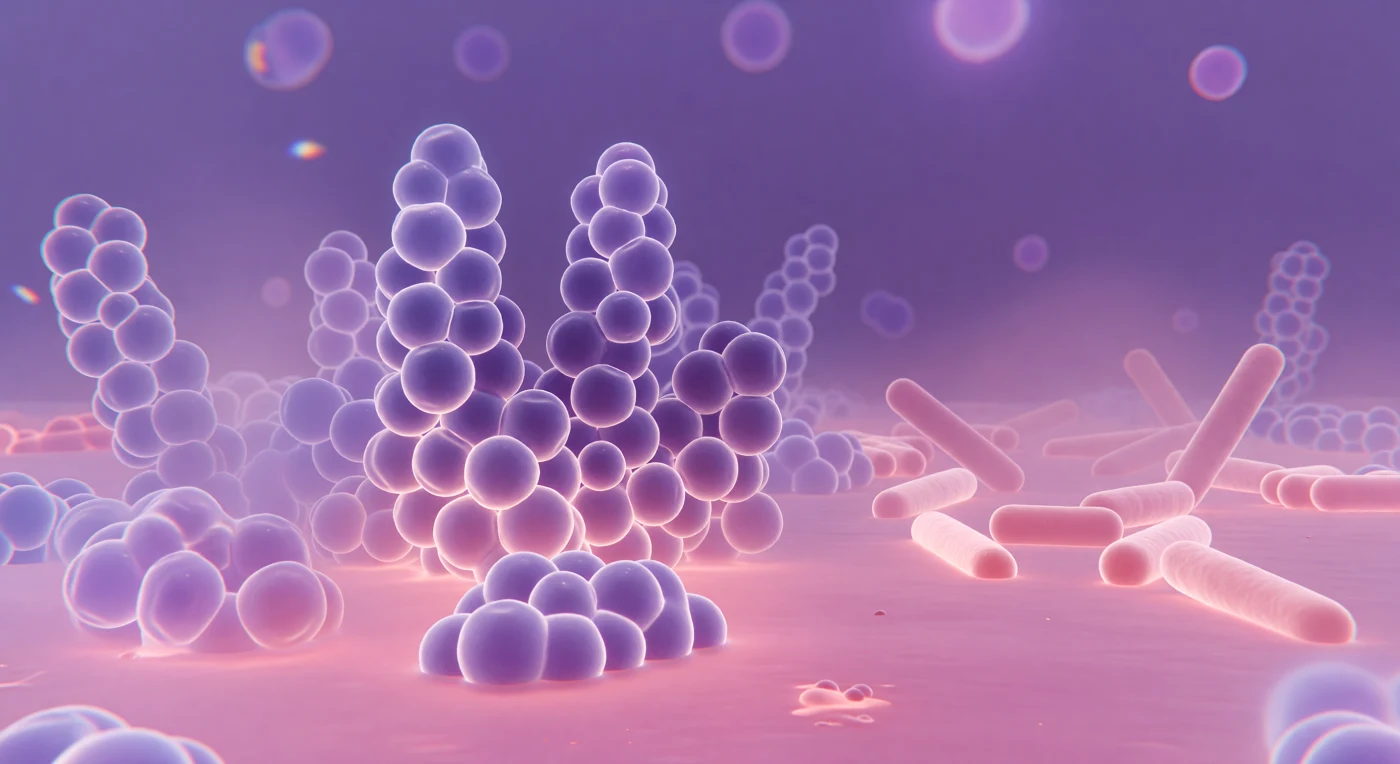
Sur cette plaine baignée d'une lumière violette et rose diffuse, le regard plonge dans un monde saturé par les teintes profondes du violet cristal, là où des sphères colossales s'agglomèrent en grappes denses — des *Staphylococcus aureus* dont les parois épaisses en peptidoglycane ont avidement retenu le colorant primaire de la coloration de Gram, trahissant ainsi leur nature Gram-positive. Autour de chaque globe, une couronne irisée tremble doucement, halo de diffraction né du fait que la longueur d'onde de la lumière visible approche les dimensions mêmes des cellules, portant la résolution optique à sa limite physique absolue. À droite, sur un fond de rose safranin chaud comme du verre teinté, des bâtonnets plus pâles — des bacilles Gram-négatifs comme *Escherichia coli* — absorbent moins le colorant, leur enveloppe plus mince et leur membrane externe en lipopolysaccharide ayant libéré le violet lors du rinçage à l'alcool, ne retenant que la contrecoloration rose. La profondeur de champ s'effondre en quelques longueurs de cellule : les formes hors foyer se dissolvent en fantômes translucides aux contours lavande, et des franges chromatiques bleues et ambrées couronnent les bords du champ, rappel poétique des imperfections inhérentes aux lentilles de verre qui seules permettent d'entrevoir cet univers invisible.
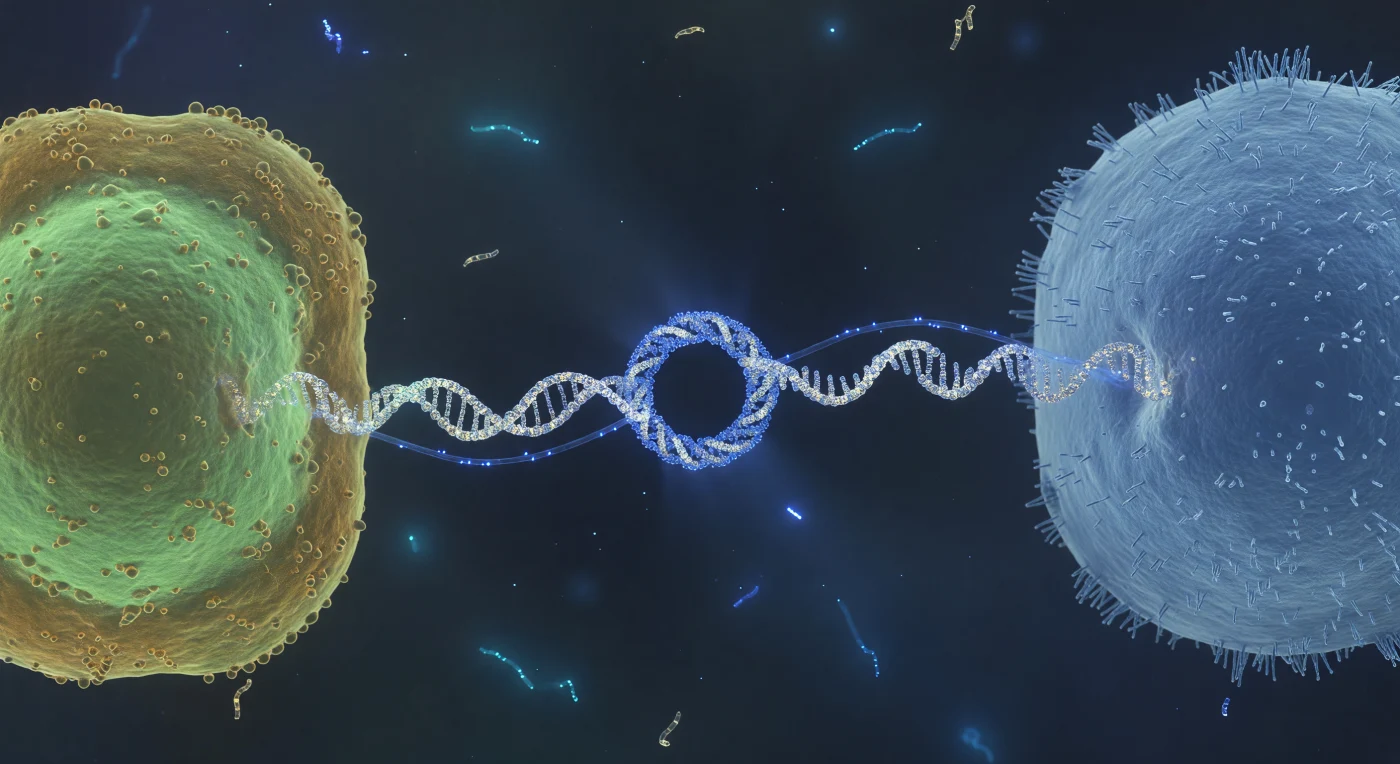
Au cœur d'un espace aqueux presque immobile, le regard se pose à mi-chemin d'un pont de conjugaison : un câble de piline hélicoïdal, blanc-or et iridescent, s'étire avec une tension précise entre deux immenses corps cellulaires, l'un baigné d'un vert céladon froid de fluorescence GFP, l'autre dressé comme un monolithe bleu poudre hérissé de fimbriae. À l'endroit où les deux membranes se rejoignent, le pore conjugatif s'ouvre comme un anneau d'obscurité parfaite de vingt nanomètres, cerclé d'un halo d'acier bleu, point de contact silencieux entre deux génomes distincts. À travers le canal du pilus pulse un filament d'ADN simple brin électrique, fil lumineux aux contours diffus qui saigne sa lumière azurée dans le milieu environnant comme une fibre optique sous tension, portant avec lui une information héréditaire d'une cellule à l'autre. Le milieu n'est pas vide : une légère brume d'ions dissous et de débris macromoléculaires trouble le fond bleu-noir, traversé par endroits de fantômes cyan — fragments d'ADN libre dérivant sous l'agitation brownienne, témoins muets d'autres transferts avortés ou accomplis. Ce transfert horizontal de gènes, omniprésent dans les populations microbiennes, est l'un des moteurs majeurs de la plasticité génomique bactérienne, propageant en quelques dizaines de minutes des résistances aux antibiotiques ou de nouveaux métabolismes à travers des communautés entières.
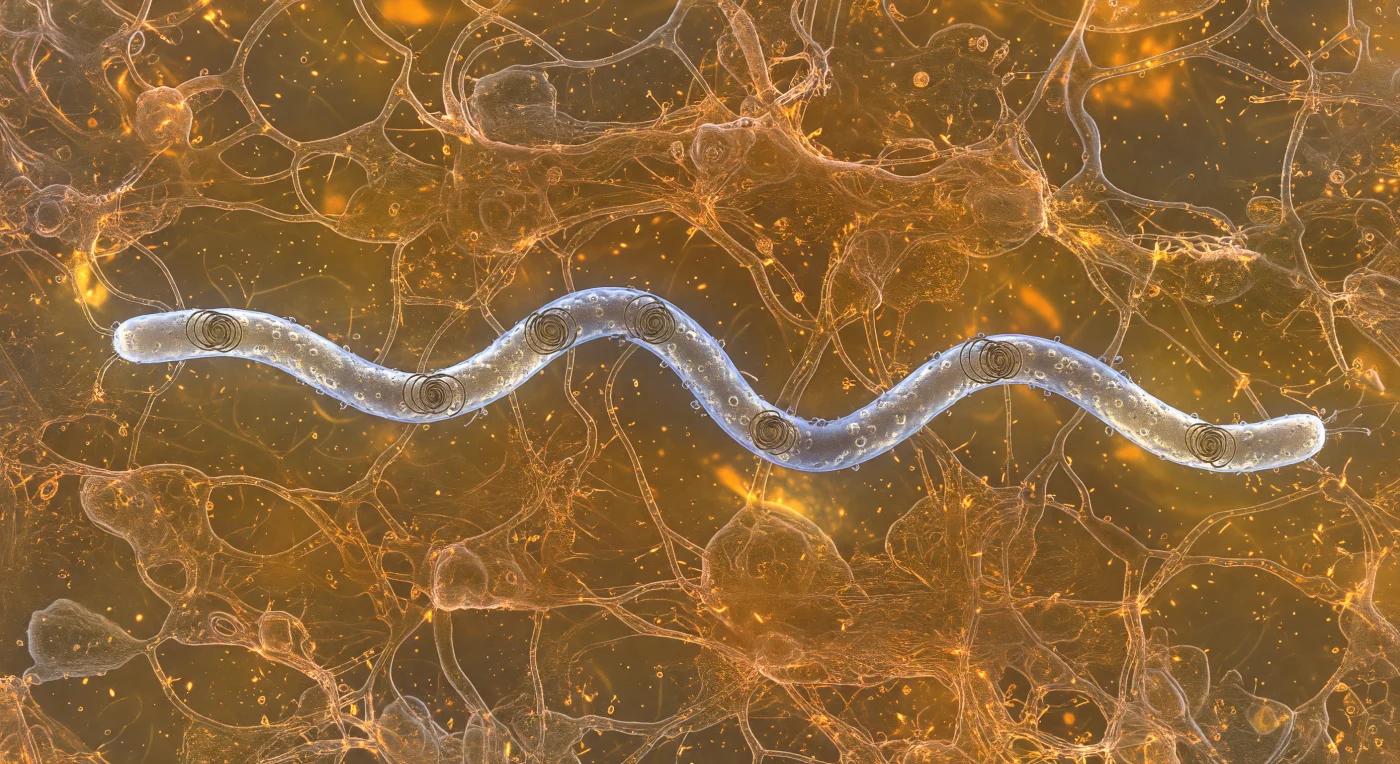
Suspendu dans cet ambre visqueux où chaque filament de glycoprotéine capte et renvoie une lueur diffuse, vous assistez au passage d'une *Borrelia burgdorferi* dont la spirale argentée fend la matrice mucinique avec une précision presque métronome — dix-huit micromètres de membrane externe gainée d'une iridescence froide, là où les protéines de surface forment un relief discret de bosses et de nodules sur ce qui ressemble à du platine martelé en hélice continue. La propulsion de la bactérie ne dépend d'aucun flagelle externe : ce sont les flagelles périplasmiques, confinés sous la gaine protectrice comme des câbles sombres torsadés contre la face interne de la membrane, qui imposent à l'ensemble du corps cellulaire son onde plane caractéristique, stratégie mécanique propre aux spirochètes pour progresser dans des milieux viscoélastiques où un flagelle nu se trouverait immédiatement immobilisé par la résistance du gel. Le sillage en V qui s'ouvre dans le réseau polymère — les brins de mucine s'écartent lentement, réfléchissent la lumière à de nouveaux angles avant de se refermer en cuivre-or derrière la cellule — illustre le régime hydrodynamique à très faible nombre de Reynolds où l'inertie est nulle et où chaque mouvement cesse instantanément si la force qui le génère s'interrompt. À cette échelle, la frontière entre le vivant et son milieu devient poreuse : de minuscules vésicules membranaires larguées par la bactérie diffusent dans le gel comme des halos réfractifs à peine perceptibles, tandis que la profondeur de champ se dissout dans un brouillard ambré, rappelant que cet espace confiné, dense et chimiquement actif constitue l'environnement quotidien d'un pathogène capable de déjouer les défenses immunitaires de l'hôte.

À l'intérieur de *Synechocystis*, le regard s'ouvre sur une cathédrale vivante de membranes thylakoïdes concentriques qui s'étendent en arcs parallèles vers chaque horizon, leurs surfaces brûlant d'une luminescence cramoisi profond — la fluorescence de chlorophylle rayonnant depuis le cœur même des bicouches lipidiques, comme des braises enfouies sous une peau translucide. Chaque feuillet membranaire est couvert d'une colonnade baroque de phycobilisomes hémisphériques couleur corail et safran, antennes photocollectrices qui captent et redistribuent la lumière rouge en halos ambrés se fondant les uns dans les autres, tandis que les corridors luminaux entre les membranes — couloirs liquides comprimés à quelques nanomètres de largeur — pulsent d'un or pâle tirant vers le jade. Dans l'espace cytoplasmique ouvert au-delà de la pile thylakoïde flottent des carboxysomes icosaédriques, coques protéiques d'environ 150 nanomètres de diamètre, semblables à des lanternes en ivoire givré dont l'intérieur laiteux trahit la présence des molécules de RuBisCO concentrées à l'intérieur pour fixer le CO₂ atmosphérique. Le cytoplasme ambiant n'est pas un vide mais une résine dorée et grumeleuse, chargée de ribosomes qui confèrent au milieu une texture granulaire continue, et la lumière dans cette scène entièrement auto-illuminée glisse du rouge profond des membranes vers l'ambre du cytoplasme puis vers la lueur bleu-vert diffuse de la paroi cellulaire distante — un univers à la fois immense et intime, structuré par la répétition architecturale de surfaces rayonnantes s'incurvant à l'infini.
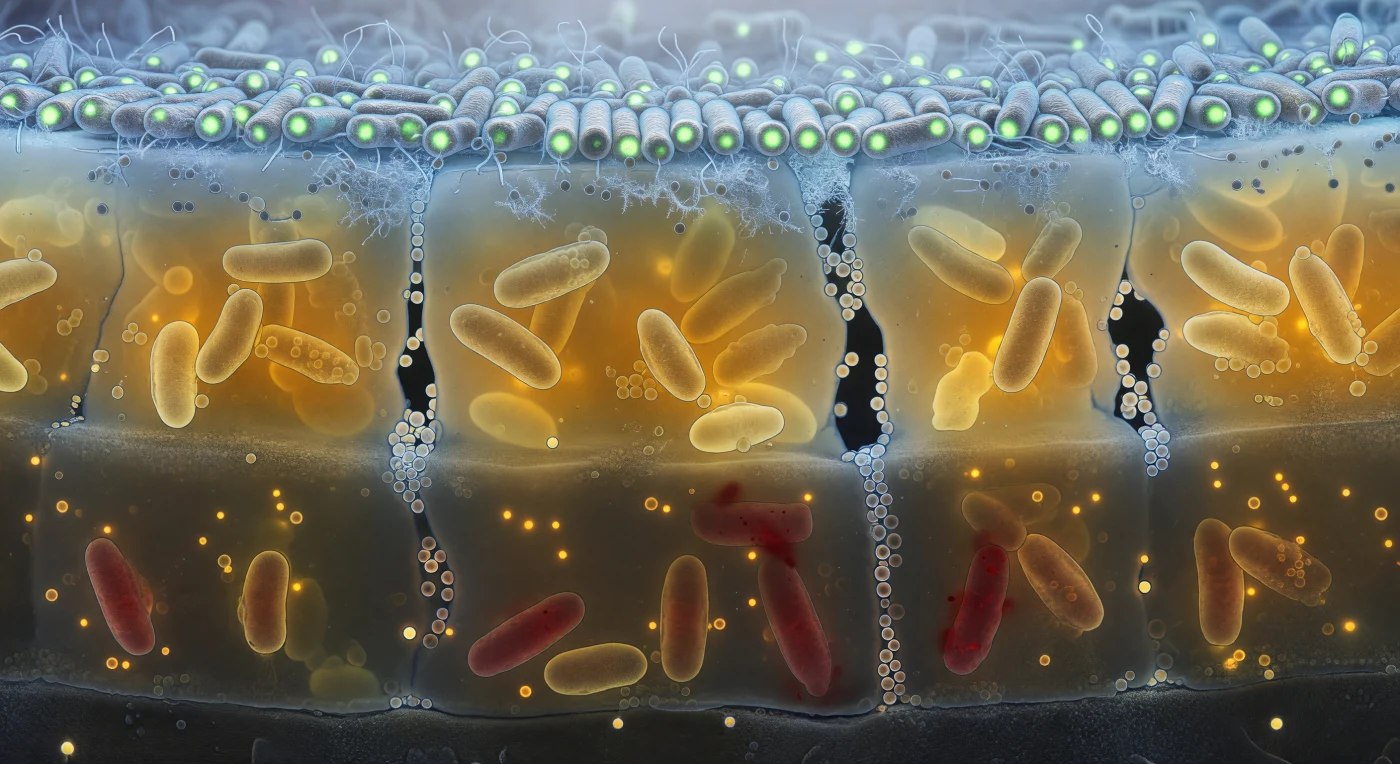
Face à cette coupe verticale d'un biofilm vivant, le regard plonge dans un empilement de trois mondes distincts qui évoquent les strates d'une géologie animée : une canopée vert-froid où des bacilles ordonnés en rangs serrés scintillent sous la lumière bleue qui filtre depuis la surface oxygénée, une zone intermédiaire ambrée où la substance polymère extracellulaire emprisonne des cellules jaunissantes dans une résine translucide parcourue de canaux sombres porteurs de vésicules membranaires, et une fondation rouge sombre peuplée de cellules mortes aux membranes perméabilisées, ancrées sur un substrat minéral gris à peine visible. Ce que l'on observe n'est pas un diagramme mais la réalité physique d'une communauté bactérienne structurée, où le gradient d'oxygène — matérialisé par une brume bleue lumineuse s'éteignant progressivement vers le bas — détermine le destin métabolique de chaque cellule selon sa position dans l'épaisseur du film. La substance extracellulaire, mélange de polysaccharides, de protéines et d'ADN extracellulaire, n'est pas un simple ciment inerte : elle régule la diffusion des nutriments, piège l'eau, crée une mémoire collective de la colonie et protège les cellules profondes des agressions chimiques venues de l'extérieur. Immergé dans cette section, on perçoit l'architecture d'une ville microscopique dont chaque quartier vit selon ses propres règles, la lumière elle-même servant d'indicateur chimique de la frontière entre le vivant actif et la mort lente.

Dans la nuit absolue d'une reconstruction STORM, vous flottez à l'intérieur même d'une bactérie en cours de division, entouré d'une constellation de points lumineux discrets qui matérialisent, pour la première fois, la vérité moléculaire d'une cellule vivante à une précision inférieure à vingt nanomètres. Devant vous, un arc brisé de touches dorées-ambrées trace l'anneau de FtsZ à l'équateur cellulaire — non pas un cercle continu, mais une phrase aux lettres manquantes, chaque tache gaussienne représentant un oligomère isolé d'une protéine dont la polymérisation orchestre la constriction et la division de la cellule. Sur vos flancs, deux réseaux hélicoïdaux de points bleu-cyan froid cartographient le cytosquelette de MreB, cette actine bactérienne qui guide la machinerie d'insertion du peptidoglycane et maintient la forme cylindrique de la cellule, tandis qu'un millier de points rouge-orangé dessinent avec une densité presque continue la membrane plasmique au-dessus et en dessous de vous, frontière vivante où résident les chaînes respiratoires et les moteurs ATP synthase. Le codage de profondeur axiale transforme cet espace en gradient thermique — l'ambre chaud des molécules proches cède progressivement au violet froid des molécules lointaines — rappelant que la troisième dimension est ici mesurée non pas en mètres mais en dizaines de nanomètres, chaque point étant l'empreinte d'un seul fluorophore capturé dans l'obscurité optique avant d'être reconstitué en coordonnée précise dans l'espace.
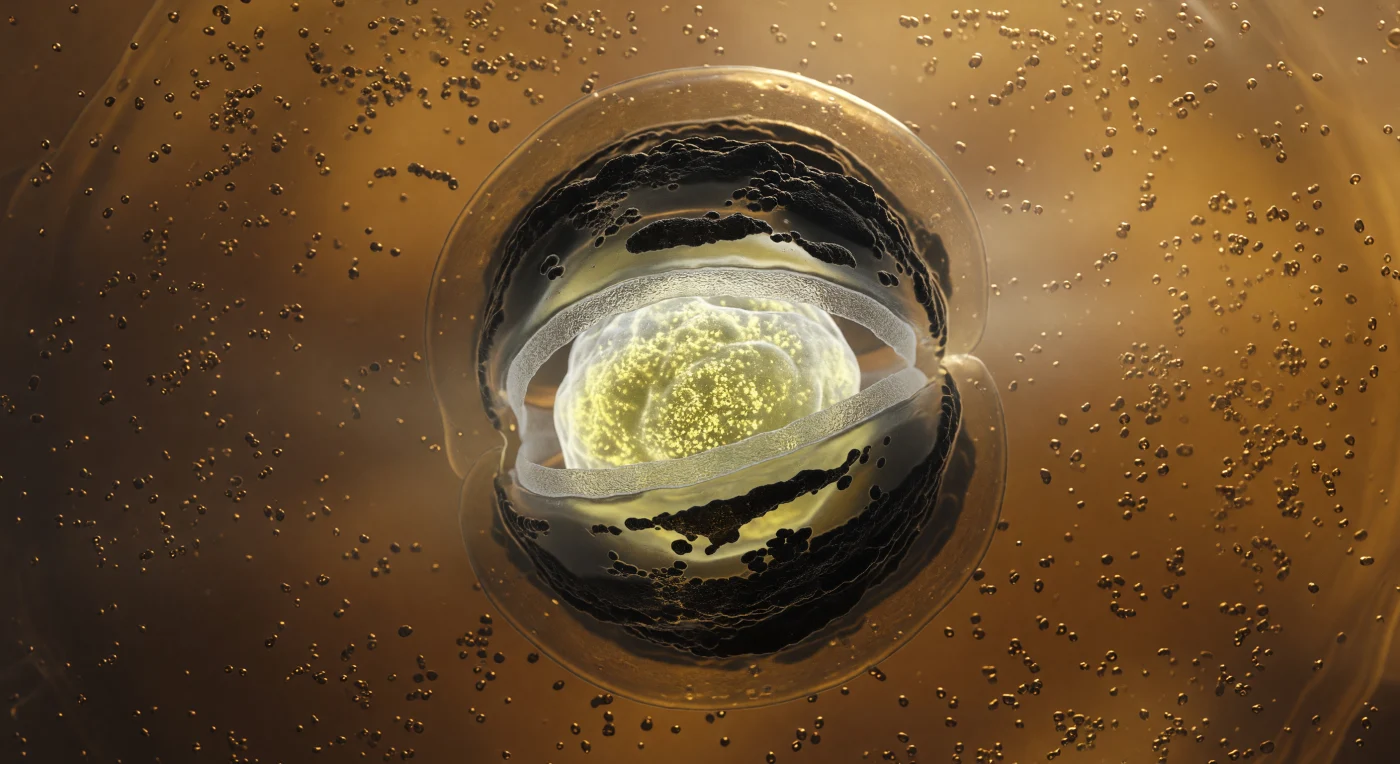
Au cœur de la cellule mère, l'œil est immédiatement capturé par la présence lumineuse du préspore : une sphère ovoïde suspendue dans le cytoplasme ambré, irradiant une lueur froide et minérale née de l'accumulation d'acide dipicolinique chélaté au calcium et d'un ADN condensé à une densité extrême par les protéines SASP, comme si un astre de poche brûlait en silence au centre d'une caverne organique. Autour de ce noyau, un anneau de cortex peptidoglycanique grisâtre — matière structurelle, poreuse et réfractive comme du verre dépoli — encercle le cœur lumineux, pendant que les couches protéiques SpoIVA et CotC se polymérisent en voûtes sombres et matte qui absorbent la lumière plutôt qu'elles ne la réfléchissent, comparables à une lave refroidissant en coulées concentriques. Ce qui saisit véritablement, c'est la membrane d'engulfment elle-même : cette double feuille lipidique qui se courbe en une étreinte phagocytaire d'une précision moléculaire, ses deux feuillets nacrés séparés par un étroit espace périplasmique, avançant millimètre biologique par millimètre biologique pour refermer le préspore dans un cocon membranaire — processus guidé par des ATPases et des protéines de guidage comme SpoIIIE, dans un milieu cytoplasmique si dense en ribosomes que la lumière ambrée s'y diffuse comme à travers une résine vivante. L'ensemble de cette scène se déroule dans un régime de bas nombre de Reynolds où le temps semble suspendu, chaque granule immobile dans sa viscosité, tandis qu'en son centre, la future spore accumule silencieusement les armes de sa résistance au monde extérieur.

Depuis quatre-vingts nanomètres au-dessus de la membrane externe d'*Escherichia coli*, la surface s'étend comme un continent minéral et vivant — une plaine de lipopolysaccharides teintée de bleu-vert et d'or oxydé, parsemée de trimères de porines qui émergent comme des cheminées hydrothermales cerclées d'une faible lueur électrostatique, le tout baigné dans la lumière diffuse et froide du milieu aqueux environnant. Dominant le cadre supérieur, le capside icosaédrique du phage T4 descend avec la lenteur silencieuse d'un corps céleste en approche terminale — cent nanomètres de faces sombres délimitées par de fines lignes dorées là où les capsomères s'assemblent en géométrie précise, ses six longues fibres caudales contractées s'évasant vers la surface comme les membres d'un insecte ancien dont chaque pad de liaison appuie dans la feuille lipidique en y creusant une légère déformation mécanique. Au centre exact de la scène, le tube caudal a déjà percé la membrane en un pore de trois nanomètres à peine, dont le rebord lipidique désordonné révèle la violence nanométrique de l'intrusion, tandis qu'un filament d'ADN simple brin — opalescent, bleu pâle, lumineux comme une fibre optique dans les ténèbres — s'écoule en continu du capside vers le périplasme sous la pression osmotique accumulée. Dans le fond aqueux, deux phages supplémentaires flottent en silhouettes argentées, gaines caudales encore non contractées, leurs têtes icosaédriques à peine visibles dans la brume volumétrique bleue-grise — témoins immobiles d'une occupation biologique aussi précise qu'inexorable.
















