Affidabilità scientifica: Molto alto

Ci si trova immersi nel cuore della parete cellulare di *Bacillus subtilis*, sospesi all'interno di un'architettura biologica densa come pietra antica: catene glicosidiche ambrate e color avorio si intrecciano in una rete tridimensionale di straordinaria complessità, tenute insieme da ponti peptidici trasversali che saldano l'intera struttura in una maglia capace di resistere a pressioni osmotiche di diversi bar. Tra i pilastri della rete scivolano le catene di acido teicoico, polimeri anionici di verde scuro che si muovono come alghe in una corrente impercettibile, modulando il pH locale e il passaggio di ioni attraverso questo labirinto molecolare spesso tra i venti e gli ottanta nanometri. Più in basso, oltre la profondità del reticolo, la membrana plasmatica appare come una distesa fluida di fosfolipidi ambra, interrotta da complessi proteici che mediano il trasporto di nutrienti e la catena respiratoria — un confine caldo e dinamico tra citoplasma gelificato e protezione strutturale. Verso l'alto, il reticolo si allenta progressivamente: i filamenti si fanno più radi, sbiadiscono nel pallore traslucido e si dissolvono infine nell'ambiente acquoso extracellulare, un vuoto freddo e bluastro dove le forze elettrostatiche e il moto browniano dominano ogni interazione, e dove la luce non trova più la corda tesa di una struttura, ma solo l'assenza di essa.
Sospesi appena dietro la poppa di una cellula di *Escherichia coli*, il corpo traslucido color ciano pallido occupa il centro del campo visivo come lo scafo di un vascello osservato da una scialuppa di rimorchio: la sua superficie non è liscia, ma percorsa da una corrugazione sottile dove le rosette poriniche captano una luce bioluminescente diffusa, mentre il citoplasma interno svela una nebbia ambrata densa di migliaia di ribosomi che sfumano in perle scure verso i poli cellulari. Dietro di noi, quattro filamenti flagellari si sono intrecciati in un unico fascio superelicoidale che si assottiglia nel blu notte del mezzo acquoso, ruotando a centinaia di rivoluzioni al secondo con una sfocatura rotazionale che ne rivela la torsione come una molla d'oro pallido impressa nella luce laterale. Attorno al fascio, il liquido stesso porta testimonianza visibile del flusso di Stokes laminare: delicati veli argento-azzurri si incurvano verso il corpo cellulare in archi perfettamente simmetrici, là dove l'inerzia è inesistente e la viscosità governa ogni movimento come una forza assoluta. In questo universo intimo e pressurizzato, dove la lunghezza d'onda della luce visibile è paragonabile alle dimensioni della cellula stessa, il moto browniano fa fremere ogni superficie e l'unica illuminazione è il freddo autorisplendere della biologia molecolare al lavoro.

Sospesi al cuore di una cellula di *E. coli*, lo sguardo non trova mai il vuoto: in ogni direzione si estende una nebulosa compatta di DNA a doppia elica intrecciato in supercoil plectonemici, corde di un blu marino scurissimo che si biforcano e si riavvolgono su sé stesse in geometrie frattali, riempiendo ogni piano visivo come un labirinto senza pareti né uscite. Lungo ogni curva acuta della fibra, piccole perle giallo-ambra — le proteine nucleoide-associate HU e Fis — stringono e piegano il DNA con un contatto meccanico preciso, restituendo nel loro riflesso un calore dorato che contrasta la fredda luminescenza cobalto che emana dai filoni stessi, diffondendosi verso l'esterno come inchiostro bioluminescente nell'acqua buia. Questo intero ambiente è compresso in un volume di circa un micron cubico, dove la molecola di DNA di *E. coli* — lunga circa 1,5 millimetri se distesa — è ripiegata migliaia di volte grazie all'azione delle topoisomerasi e di proteine strutturali, formando quella nuvola densa e organizzata che i biologi chiamano nucleoide. Ai margini della nuvola, dove il DNA si dirada e il citoplasma comincia ad affermare la propria identità, granuli scuri e sferici — i ribosomi, densi come cinders e appena fuori fuoco nella foschia rifrangente del mezzo gelificato — stazionano in aggregati lenti, separati dal nucleo dal principio di esclusione macromolecolare che impedisce loro di penetrare nella regione più affollata. L'intera scena vibra di un'eloquenza silenziosa: non c'è quiete né spazio libero, solo la pressione organizzata di una macchina vivente che funziona senza sosta in un dominio dove la gravità è irrilevante e il moto termico governa ogni cosa.

Ci si trova sospesi a brevissima distanza da una pianura vivente che si estende fino a un orizzonte lievemente curvato, come la superficie di un pianeta minuscolo e caldo: quello che si vede è lo strato più esterno di una cellula batterica gram-negativa, la membrana esterna rivestita di lipopolisaccaridi le cui lunghe catene oligosaccaridiche oscillano verticalmente nel mezzo viscoso come alghe in un mare senza vento, tingendo il paesaggio di turchese profondo e oro antico. Ogni venti nanometri circa, trimeri di porine a barile beta erompono dalla pianura come torri di ossidiana levigata, i loro canali interni oscuri che scendono come pozzi verticali attraverso il doppio strato lipidico verso il mondo periplasmico sottostante, mentre tra di esse le placche cristalline di Lipide A formano mosaici iridescenti che variano dal cobalto all'acquamarina secondo l'angolo della luce fredda diffusa che filtra dal basso attraverso la membrana stessa. All'estrema sinistra, il corpo basale di un flagello s'innalza dall'orizzonte come una torre di perforazione industriale, i suoi anelli proteici sovrapposti con precisione chirurgica, il gancio nascente che si incurva verso l'alto e scompare nella foschia ionica del mezzo acquoso. L'intera scena è immersa in una luminosità glaciale e diffusa, quella luce bioluminescente che trasuda verso l'alto attraverso lo strato lipidico translucido e ammorbidisce ogni ombra, donando a questo paesaggio molecolare la quiete luminosa di una baia artica fotografata all'alba.

Ci si trova sospesi nell'ambra densa del citoplasma batterico, appena oltre il margine fibroso del nucleoide, e il campo visivo è interamente occupato da ribosomi 70S che si stipano come ciottoli di una pavimentazione antica, separati da interstizi di soli cinque o dieci nanometri colmi di un gel macromolecolare opaco, caldo come resina, nel quale non esiste traccia di spazio libero. Attraverso questa densità granulare si snodano catene polisomiali come collane di perle irregolari, sei ribosomi infilati lungo un filamento di mRNA appena percettibile — un filo color crema che si incurva sotto il proprio peso molecolare prima di dissolversi nella nebbia bruna del fondo — a testimoniare la traduzione simultanea e incessante che avviene in ogni punto di questo ambiente. A sinistra, lo chaperonino GroEL si erge come il tronco pietrificato di un albero colossale: la sua architettura a doppio anello in ardesia scura, con la cavità centrale leggermente più luminosa, domina un intero quadrante della scena con una verticalità quasi architettonica che fa apparire i ribosomi circostanti poco più che briciole. Di tanto in tanto, una proteina marcata con GFP lampeggia come una brace smeraldo nell'uniformità monocromatica dell'ambra — un istante di colore subito occultato dal passaggio di un'altra sfera scura — ricordando che in questo spazio non esiste quiete, solo un affollamento molecolare in movimento perpetuo alimentato dall'energia termica in assenza di qualsiasi influenza della gravità.

Lo sguardo precipita dall'alto in un paesaggio che non ha nulla da invidiare a una città vista dall'elicottero, eppure l'intera distesa si misura in decine di micrometri: torri a fungo di colonie di *Pseudomonas* si ergono dal substrato irradiando una luce jade-GFP continua e viscerale, le loro cupole più alte dissolvendo il verde saturo verso un viridiano profondo lungo i gambi, mentre sulle superfici curve si distinguono i singoli bastoncelli cellulari disposti come mattonelle su una volta, ciascuno un frammento lucente di ceramica bagnata. Tra le torri, canali d'acqua neri e anecoidali tagliano la scena con la precisione idraulica di fiumi scavati dall'erosione, i loro bordi segnando una transizione netta tra la massa biologica verde e il vuoto assoluto al centro, dove la corrente ha ripulito ogni traccia di matrice. L'interstizio tra struttura e struttura è colmato da un gel di polisaccaridi extracellulari color ambra traslucido, caldo e vagamente autofluorescente in arancione, che cola tra le torri come caramello viscosissimo depositato per accumulo lento e flusso denso — la firma materiale di un biofilm maturo in cui la comunità batterica ha letteralmente costruito il proprio ambiente. In profondità, sotto la volta verde delle colonie più sviluppate, chiazze di rosso corallo smorzato emergono dagli strati basali: cellule morte per ipossia, le cui membrane cedute lasciano entrare il propidio ioduro e tradiscono, attraverso il polisaccaride semitrasparente, il destino di chi vive nell'ombra della propria metropoli biologica.
Orbitando all'altezza dell'equatore di questo mondo cilindrico largo meno di un micrometro, il visitatore si trova sospeso attorno a un'*Escherichia coli* colta nell'istante preciso della sua scissione: la cellula si estende in entrambe le direzioni come una cattedrale translucida di ambra e giada, mentre al centro la costrizione a clessidra è cinta da un anello di fuoco verde-GFP, la proteina FtsZ polimerizzata in un filamento continuo largo appena duecento nanometri che orchestra l'intero processo divisionale reclutando gli enzimi necessari alla sintesi del setto. La membrana interna, marcata dalla sonda FM4-64, disegna una doppia curva arancione che segue fedelmente l'indentatura, mentre all'interno del corpo cellulare trasparente i due nucleoidi segregati brillano come nebulose cobalto — masse di DNA compattate da proteine NAP e prive di un vero nucleo membranoso, già distribuite nelle due cellule figlie nascenti dalla forza combinata di diffusione entropica e sistemi di segregazione attiva come *parABS*. Il citoplasma tra le due metà non è uno spazio vuoto ma un materiale denso e viscoso, saturo di ribosomi da venti nanometri che conferiscono all'interno la consistenza ottica di una resina d'ambra illuminata dall'interno, un oceano molecolare in cui la gravità non conta nulla e il moto browniano governa ogni scala di energia. Nell'oscurità navy del mezzo acquoso circostante, la luce diffusa dall'anello Z si propaga come un'aureola di bioluminescenza spaziale, isolando questo dramma nanometrico su un palcoscenico biologico sospeso nel tempo.

Davanti a voi si erge una fila di quindici cristalli cubottaedrici di magnetite, ciascuno alto circa quattro volte la vostra statura, che si allunga nell'oscurità ambrata del citoplasma come un monumento minerale di precisione geologica: le loro superfici sfaccettate, nere come ossidiana, catturano la luce diffusa e restituiscono riflessi blu-violacei che attraversano il mezzo cellulare denso di ribosomi. Ogni cristallo è avvolto da una sottile vescicola lipidica — un involucro perlaceo e leggermente traslucido che ondeggia per agitazione termica, conferendo a ciascun corpo minerale un alone quasi fantasmatico — e insieme costituiscono i magnetosomi di *Magnetospirillum*, organelli unici in grado di allineare la cellula ai campi magnetici terrestri come un ago di bussola biologico. Al di sotto della catena corre il filamento proteico MamK, un'impalcatura citoschelettrica simile all'actina che pulsa di un blu cobalto elettrico, tenendo l'intera struttura cristallina in posizione contro le correnti invisibili del moto browniano che scuotono continuamente i ribosomi circostanti come sassolini in un liquido viscoso. Più lontano, la membrana interna si incurva come la volta di una caverna umida, il suo strato bilipidico dorato costellato di complessi proteici, oltre il quale la parete cellulare cede all'oscurità assoluta dell'ambiente acquoso esterno, dove i campi magnetici che orientano questa meravigliosa architettura non hanno né forma né colore.
Ci si trova in piedi sulla soglia di una pianura immersa in una luce violacea densa e nebbiosa, dove enormi sfere di colore viola scuro si ergono in grappoli compatti come architetture organiche, le loro superfici lisce e leggermente deformate nei punti di contatto, circondate da un alone di diffrazione iridescente che tradisce la natura stessa della luce quando incontra forme grandi quanto la propria lunghezza d'onda. Queste strutture sono cellule di *Staphylococcus aureus*, batteri Gram-positivi la cui spessa parete di peptidoglicano trattiene avidamente il cristalvioletto della colorazione di Gram, trasformandosi in torri viola-indaco che dominano il paesaggio. Il suolo attorno ai grappoli è inondato di un caldo rosa safranina, un controstagno che penetra solo dove la parete batterica non ha opposto resistenza al decolorante, formando un piano traslucido come vetro rosa che riflette caustica luminosità. A destra, forme cilindriche di un rosa polveroso — bacilli Gram-negativi la cui membrana esterna di lipopolisaccaride ha ceduto il violetto al lavaggio — giacciono oblique come monoliti nella foschia, i loro bordi sfumati dall'inevitabile resa dell'ottica quando la risoluzione tocca il suo limite fisico. La profondità di campo è impietosamente sottile: le cellule fuori piano si dissolvono in fantasmi lavanda, e ai margini estremi del campo visivo sottili anelli cromatici di blu e ambra coronano le forme sfocate, testimonianze oneste dell'imperfezione del vetro e di un mondo esplorato fin dove la luce stessa cede.
Sospesi nel quasi-immobile silenzio di uno spazio acquoso a bassissimo numero di Reynolds, siamo al centro di un atto di scambio genetico orizzontale tra due cellule batteriche: il pilo coniugativo si tende come un cavo di proteine elicoidali — largo appena 8 nanometri — tra la cellula donatrice a sinistra, che diffonde una luce celadone dal GFP intracellulare, e la cellula ricevente a destra, monolite blu-cipria la cui superficie è irta di fimbrie come una brina proteica. Al punto di contatto diretto tra le membrane, l'anello coniugativo si apre come un'oscurità perfettamente circolare del diametro di 20 nanometri, orlata da un alone grigio-acciaio di densità proteica — un portale molecolare costruito da entrambe le cellule, encastrato nelle rispettive bilanciature lipidiche. Attraverso il canale del pilo scorre un filamento di DNA a singolo filamento che appare come una luminescenza azzurra elettrica pulsante, i cui margini sfumano nel solvente come la luce fuoriesce da una fibra ottica in tensione, trasferendo informazione genetica da un organismo all'altro in un senso che la selezione naturale ha affinato in miliardi di anni. Sullo sfondo buio e lattiginoso di ioni disciolti e detriti macromolecolari, spiriti cianotici di frammenti di DNA libero derivano sotto il bombardamento browniano come filamenti dimenticati, testimoni silenziosi di un'intimità molecolare che ridefinisce i confini stessi dell'individualità biologica.
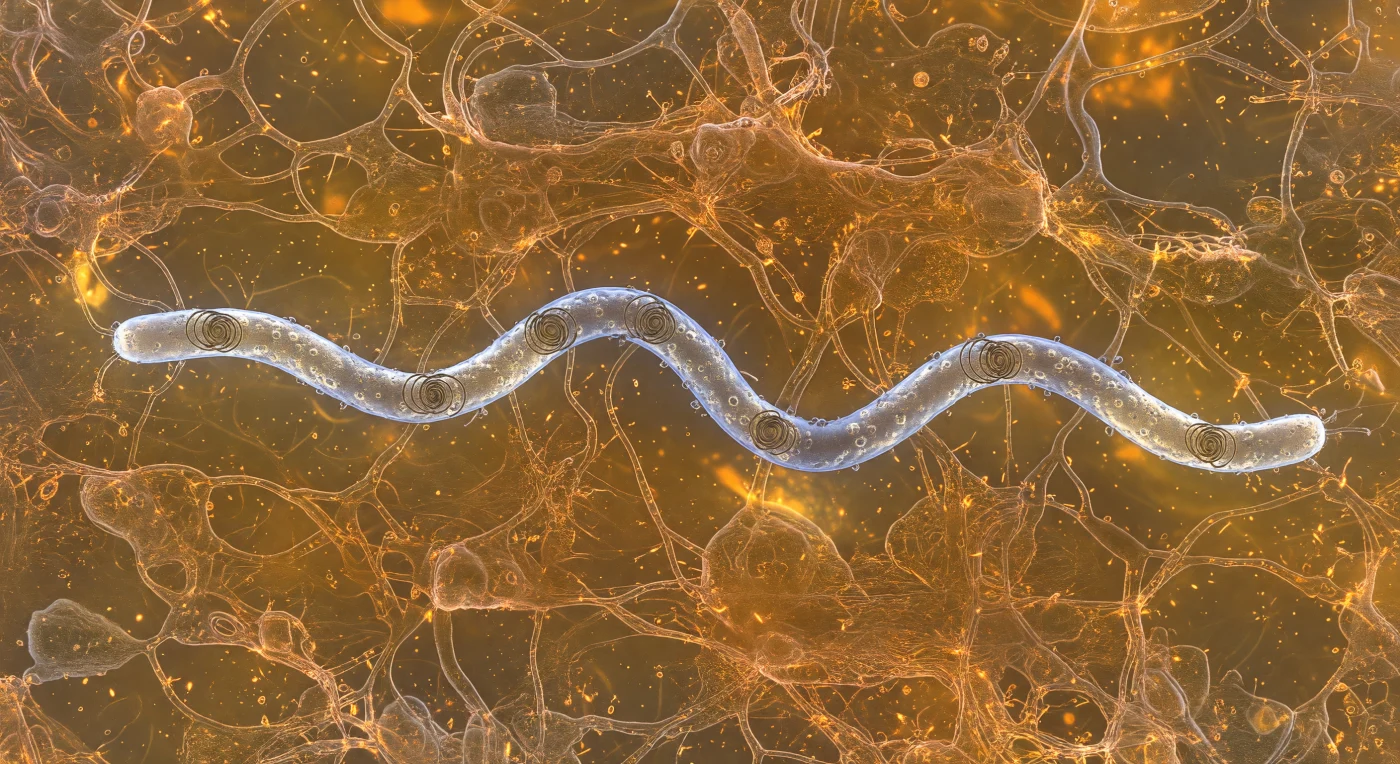
Sospeso nell'ambra viscosa del gel di mucina, il tuo sguardo è catturato dalla presenza di un'entità in movimento a soli cinque micrometri di distanza: una *Borrelia burgdorferi*, spirochete responsabile della malattia di Lyme, che si fa strada attraverso la matrice fibrosa con un'ondulazione piatta e meccanicamente precisa, il suo corpo elicoidale lungo diciotto micrometri avvolto in una guaina di membrana esterna che restituisce il calore ambrato dell'ambiente come un freddo bagliore argenteo iridescente. Sotto quella membrana, invisibili al mezzo circostante ma appena percettibili come cavi elicoidali scuri che premono dall'interno, i flagelli periplasmici ruotano nel loro spazio confinato, generando l'onda viaggiante che spinge l'intera cellula in avanti senza mai esporre i loro filamenti al gel — un meccanismo propulsivo unico tra i procarioti, perfettamente adattato a navigare ambienti viscoelastici come il muco connettivale o il liquido sinoviale dell'ospite. La matrice di mucina che ti circonda non è un semplice fluido: è una rete tridimensionale di glicoproteine intrecciate, ciascuna fune di polimero capace di deformarsi e riformarsi, e il V-wake che la spirochete apre al suo passaggio — filamenti di rame dorato che si incurvano verso l'esterno e lentamente si richiudono — rivela la natura viscoelastica di questo materiale biologico, né liquido né solido, ma entrambe le cose simultaneamente. A questa scala, la gravità è irrilevante e il moto Browniano impone il proprio disordine su ogni particella granulare sospesa nel caldo bagliore onnidirezionale, rendendo ogni istante un equilibrio dinamico tra caos termico e propulsione batteriologica millimetrata.

Ci si trova all'interno di un batterio vivo — *Synechocystis*, una cianobatterio d'acqua dolce — immersi in un mondo di membrane parallele che si curvano lontano in ogni direzione come le navate di una cattedrale in fiamme, le loro superfici che ardono di una luminescenza cremisi profonda generata dai pigmenti clorofilliani incorporati nel doppio strato lipidico, ciascun fotone emesso testimonianza silenziosa della fotochimica che trasforma la luce solare in energia chimica. Le membrane tilacoidi di questo organismo procariotico non sono segregate in cloroplasti come nelle cellule vegetali, ma formano lamelle concentriche libere nel citoplasma, le loro superfici incrostate di complessi ficobilisonici — antenne raccoglitrici di luce color arancio corallo, strutture proteiche elaborate che captano lunghezze d'onda inaccessibili alla clorofilla e le trasferiscono ai centri di reazione con efficienza quantistica quasi perfetta. Nel citoplasma ambrato che circonda le membrane fluttuano gusci icosaedrici carboxisomici, poliedri traslucidi di centocinquanta nanometri costruiti da proteine di rivestimento capaci di concentrare l'anidride carbonica intorno agli enzimi RuBisCO intrappolati all'interno, aggirando così la loro imbarazzante tendenza a legare ossigeno invece di carbonio. L'intera scena è autoluminosa — nessuna fonte di luce esterna penetra significativamente a questa scala — e il gradiente cromatico dall'intenso rosso delle membrane all'ambra del citoplasma fino al verde-azzurro della periferia cellulare mappa fedelmente la chimica stessa di questo microorganismo che da tre miliardi di anni ossigena il pianeta.
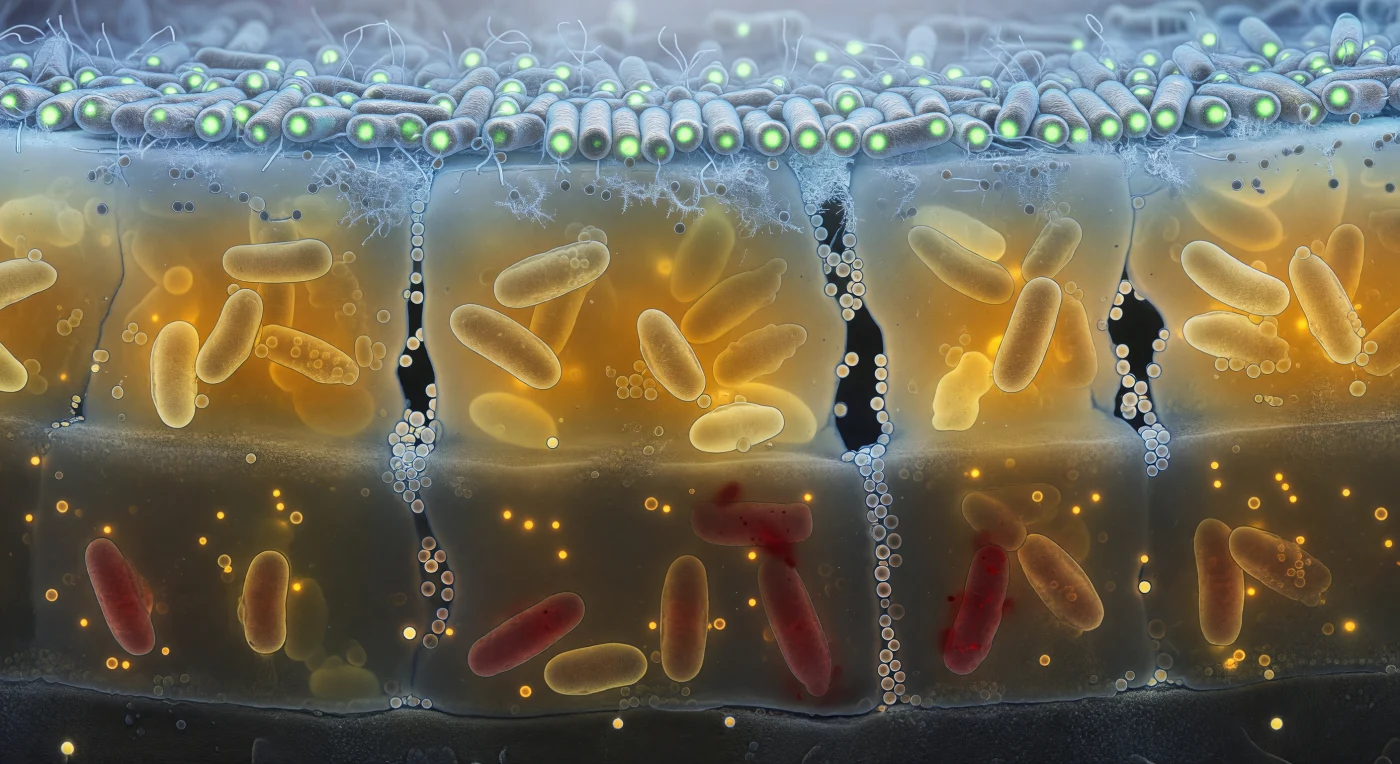
La sezione verticale di un biofilm di cinquanta micrometri si apre davanti all'osservatore come la parete di un canyon geologico vivente, stratificata in province luminose distinte: in alto, una fitta canopia di cellule a bastoncino compatte irradia una fredda luce verde-blu dove l'ossigeno disciolto penetra dall'esterno, trasformando ogni membrana tesa in una lanterna fluorescente. Scendendo, la sostanza polimerica extracellulare si addensa in una resina ambrata e traslucida che ingloba cellule metabolicamente stressate dal colore giallo-verde, mentre canali idrici vuoti e scuri tagliano la matrice come fessure in un sasso bagnato, le loro pareti ornate di vescicole di membrana che galleggiano immobili come bolle di sapone sospese nel tempo. Nella fondazione ipossica più profonda, il rosso fioco del propidio ioduro tinge i cadaveri batterici di una luce da fondale abissale, le loro membrane permeabili che cedono il contenuto cellulare in una colata arancione che intorbida la matrice circostante. L'intera struttura è tenuta insieme dal gradiente di ossigeno stesso, un alone luminoso blu che brucia in superficie e si spegne progressivamente verso il substrato minerale grigio-scuro su cui le prime cellule si sono saldate in modo irreversibile, fondendo chimica e architettura in un ecosistema autonomo spesso quanto un capello è largo cento volte meno.

Ci si trova sospesi nell'oscurità assoluta di una ricostruzione STORM, immersi nell'architettura molecolare di un unico batterio in divisione: attorno a voi, costellazioni di punti luminosi discreti occupano il vuoto con la precisione calibrata di localizzazioni singole di fluorofori, ognuna un evento fotonico strappato al rumore ottico. Un arco spezzato di punti giallo-ambrati traccia l'anello di FtsZ all'equatore cellulare — non un cerchio continuo, ma una frase con lettere mancanti, la cui curvatura suggerisce una circonferenza perfetta che si estende per decine di lunghezze corporee nell'oscurità. Ai lati, due elici aperte di punti ciano-freddo definiscono l'impalcatura di MreB lungo la lunghezza della cellula, mentre migliaia di punti rosso-arancio formano una volta e un pavimento curvi che delineano la membrana con precisione sub-diffrattiva, così fitti da sfiorare la continuità eppure rimasti, ciascuno, un nodo distinto e tremante di intensità. La codifica cromatica della profondità assiale trasforma l'intero volume in un gradiente termico: le molecole più vicine ardono di un ambra ricco e saturo, mentre quelle che si allontanano lungo l'asse polare si raffreddano progressivamente fino a un violetto livido, come se si stesse in piedi all'equatore di un pianeta molecolare i cui poli fossero perennemente gelati — un pianeta vivo, che sta decidendo di dividersi.
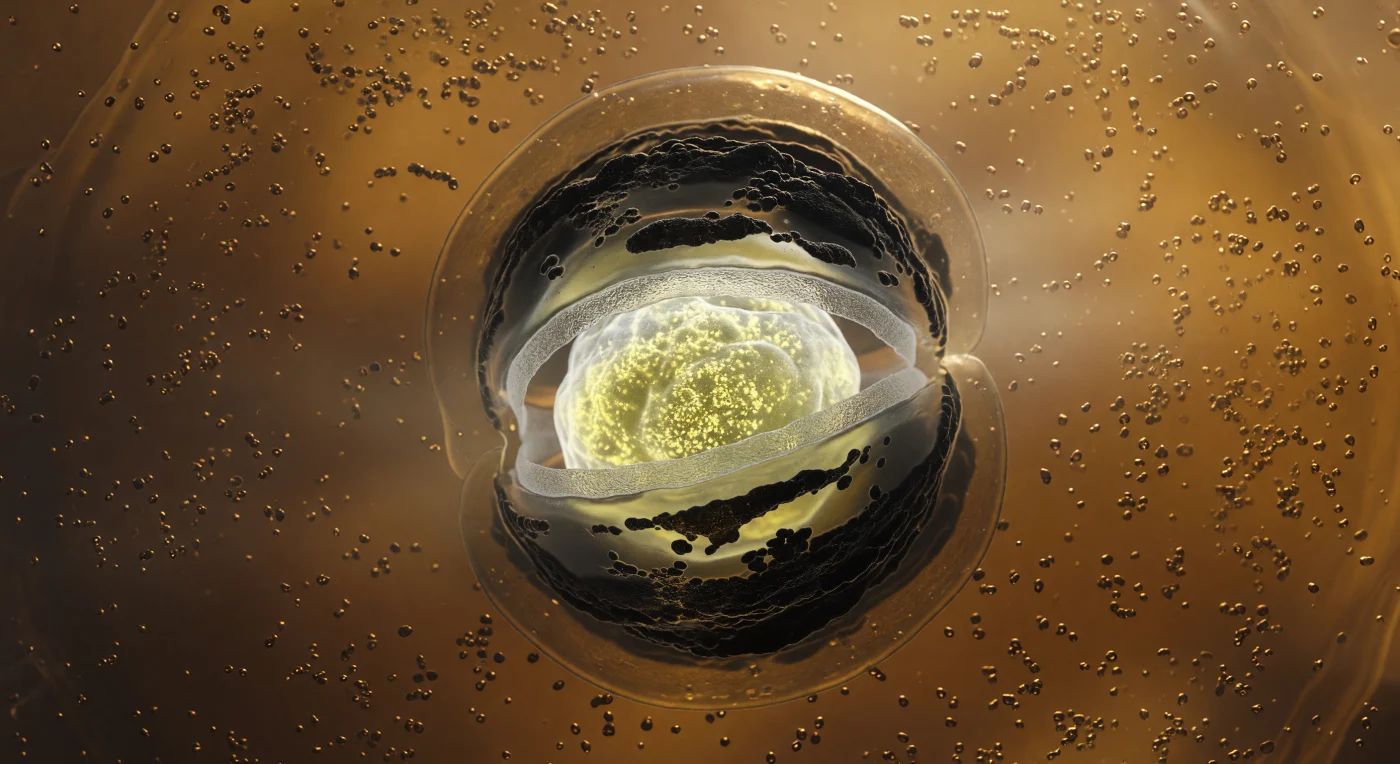
Al centro di questa caverna ambrata si erge la forespore come un mondo nel mondo: una massa ovoidale illuminata dall'interno da una luminescenza giallo-bianca quasi minerale, generata dai depositi ultra-densi di calcio-DPA e dal DNA condensato rivestito di proteine SASP, compresso oltre ogni limite biologico ordinario all'interno di un compartimento che misura appena pochi centinaia di nanometri. Attorno a quel nucleo incandescente, un sottile anello di corteccia peptidoglicana grigio-pallido disperde la luce come vetro smerigliato, mentre strati concentrici di proteine del rivestimento — SpoIVA e CotC — si polimerizzano in superfici quasi opache, scure come roccia vulcanica raffreddata, assorbendo la luce invece di rifletterla. La membrana che avvolge la forespore costituisce l'elemento più drammatico della scena: un doppio foglio lipidico che piega con curvatura estrema attorno all'equatore della forespore in un abbraccio fagocitico, le sue due superfici quasi iridescenti separate da uno stretto spazio periplasmico, illuminate sul lato interno dall'oro caldo della forespore e immerse nell'ombra ramata sul lato del citoplasma materno. L'intera caverna è densa di ribosomi che catturano la luce come sabbia bagnata sotto un'illuminazione dorata fioca, il citoplasma — viscoso come miele tiepido a numero di Reynolds quasi nullo — esclude lentamente ogni molecola residua mentre l'engulfment si avvicina al completamento, sfumando ogni profilo lontano in una nebbia proteica biologicamente intima.

La superficie che si estende sotto il punto di osservazione appartiene alla membrana esterna di *Escherichia coli* — un foglio lipopolisaccaridico asimmetrico largo diversi micrometri, la cui topografia molecolare ondeggia sotto la pressione termica costante dell'acqua circostante, i trimeri di porina emergono come torri scure coronate da un tenue alone elettrostatico color ambra. Sopra questo paesaggio, una particella di fago T4 scende in silenziosa occupazione: la testa icosaedrica di circa cento nanometri di diametro — grigio scuro con sottili linee auree lungo le giunture tra capsomeri — esercita una presenza gravitazionale illusoria in un regime fisico dove la gravità è irrilevante e ogni movimento è governato dalla fluttuazione termica e dalle forze di van der Waals. Le sei fibre caudali lunghe e articolate si aprono radialmente sulla superficie teal-oro come zampe di un insetto antico, ciascun pad di legame al recettore imprimendosi nell'LPS con una deformazione locale visibile, mentre il tubo ago ha già perforato la membrana in un poro di pochi nanometri, il bordo lipidico sollevato e disordinato a indicare la prima rottura dell'integrità della barriera. Da quel punto di penetrazione sale — o meglio scende — un filamento luminoso di DNA a singolo filamento, pallido bianco-azzurro come fibra ottica nell'oscurità acquosa, spinto dalla pressione osmotica accumulata nel capside verso il perioplasma sottostante, dove inizierà il dirottamento dell'intera macchina biosintetica batterica. Sullo sfondo, due faghi ancora in fase pre-contrazione fluttuano nella foschia blu-grigia del mezzo acquoso, le loro guaine caudali d'argento freddo a ricordare che questo non è un evento isolato, ma l'inizio di un'occupazione molecolare silenziosa e inesorabile.
















