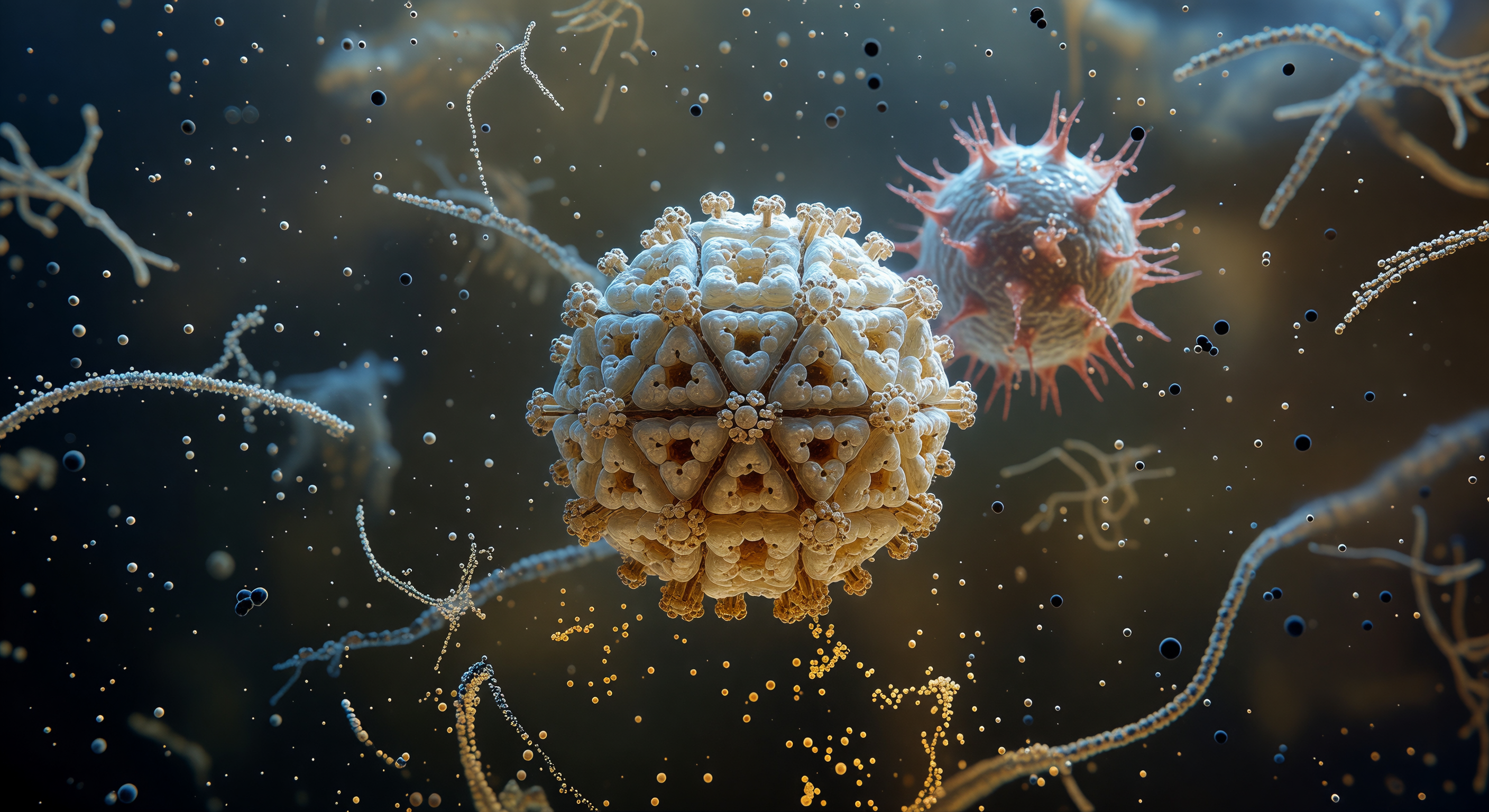
Confianza científica: Alto

En esta deriva a ras de superficie, el mundo entero se reduce a una llanura membranosa de ámbar cálido que se curva suavemente hacia un horizonte borrado por la niebla, y desde ella emergen cientos de trimeros de hemaglutinina como columnas de marfil —cada uno formado por tres hélices alfa entrelazadas que ascienden unos trece nanómetros— lo bastante apretados entre sí para que los espacios que los separan sean apenas corredores en penumbra. Entre esos pilares uniformes, los tetrámeros de neuraminidasa irrumpen como setas achaparradas de un teal profundo, sus cabezas boxeadas captando la iluminación difusa de manera distinta y subrayando así la complejidad funcional de esta cubierta viral: mientras la hemaglutinina se une a los receptores de ácido siálico de la célula huésped, la neuraminidasa los escinde para liberar los viriones recién formados. El medio que rodea la escena no es vacío sino una suspensión densa y luminosa de macromoléculas —glóbulos de albúmina sérica que derivan como linternas translúcidas de ámbar, cadenas de glicoproteínas y hebras de mucina que ondean como algas en corriente lenta— todo ello agitado de manera continua e invisible por el movimiento browniano térmico, esa violencia molecular constante que a esta escala equivale a una tormenta perpetua. La visibilidad se extingue a pocas filas de distancia, donde el bosque de pilares se disuelve en una neblina opalescente de blanco y ámbar frío, convirtiendo este espacio de apenas decenas de nanómetros en un universo claustrofóbicamente rico, sin cielo discernible ni horizonte despejado, sólo la intimidad sofocante de una selva proteica que respira a escala cuántica.

El suelo bajo los pies es una llanura ámbar y oro fundido que ondula con lentitud térmica, una membrana lipídica doble tan densa y continua que parece pavimento vivo, interrumpida aquí y allá por cuñas pálidas de colesterol que endurecen el terreno a su alrededor y por una neblina electrostática azul-blanca que flota a ras de superficie donde se concentran los grupos fosfato cargados. Desde esta planicie se elevan en todas direcciones los trímeros de proteína Spike del SARS-CoV-2, columnas de veinte nanómetros de altura en rojo oscuro y carmesí, cada una formada por tres cadenas proteicas enrolladas sobre sí mismas con una precisión biomecánica extraordinaria, sus dominios de unión al receptor desplegados en la cima como las palas abiertas de una turbina esperando el contacto con la célula huésped. La curvatura del virión completo se percibe en el horizonte lejano, traicionando la geometría esférica de todo el conjunto, mientras que hacia abajo, separada por un espacio cargado de iones y moléculas pequeñas, la membrana de la célula huésped se extiende como una inmensa llanura gris-azul cubierta de glucanos ramificados que ascienden como cristales de escarcha. Nada aquí permanece quieto: los sacudones brownianos del agua sacuden continuamente cada estructura, y las propias puntas de las espículas oscilan en una urgencia molecular silenciosa que lo impregna todo, recordando que este paisaje existe suspendido entre el estado de vida y el de mera química organizada.

Estás aplastado contra la llanura de la membrana externa bacteriana, mirando hacia arriba mientras la plataforma basal del bacteriófago T4 desciende sobre ti como una corona hexagonal de acero frío, sus seis caras facetadas captando la luminiscencia violeta-azulada del entorno acuoso en destellos de beta-láminas empaquetadas con precisión de ingeniería. La superficie de lipopolisacáridos se extiende en todas las direcciones como una vasta planicie ámbar y verde bilioso, estremecida por la percusión incesante del ruido térmico, sus cadenas de azúcares y proteínas porinas elevándose como rocas en una costa antigua mientras los seis filamentos caudales largos del fago se despliegan hacia afuera en un patrón estelar, sus puntas distales ya hundidas en la membrana a distancias enormes, ancladas a receptores específicos de LPS en el evento de reconocimiento molecular más íntimo y devastador que pueda existir. Por encima de la plataforma basal, la vaina contráctil helicoidal asciende en perspectiva hacia un punto de fuga, sus anillos estriados perdiéndose en la neblina molecular índigo antes de que la cabeza icosaédrica —depositaria de un genoma de 170 kilobases de ADN de doble cadena— emerja apenas como un fantasma facetado desde la densidad electrónica circundante. Todo el coloso, de unos doscientos nanómetros de altura, se mantiene en un equilibrio tremebundo justo antes del evento irreversible: la contracción de la vaina en milisegundos que empujará el tubo central a través de la membrana e inyectará el genoma viral en el citoplasma bacteriano, sellando el destino de la célula huésped.

Te encuentras en el corazón geométrico de una catedral molecular, encerrado dentro de una cápside del virus de la hepatitis B cuya arquitectura icosaédrica se despliega en todas las direcciones como una bóveda de piedra biológica de apenas 36 nanómetros de diámetro. Las paredes curvas están construidas de tejas proteicas hexaméricas y pentaméricas cuyas estructuras en barril beta emergen 4 o 5 nanómetros de la superficie interior, bañadas en una fosforescencia ámbar dorada que no proviene de ninguna fuente externa sino de la propia arquitectura cuaternaria, acumulándose en las concavidades entre capsómeros y revelando cada cresta y cada surco como si la estructura entera fuera una formación mineral iluminada desde adentro. Bajo tus pies, el genoma de ARN bicatenario se enrosca en masas densas de bucles color cobre quemado, comprimidos hasta el punto en que los surcos helicoidales apenas se distinguen en el entramado, y toda esa masa tiembla con agitación térmica a frecuencias imposibles de percibir conscientemente, micro-oscilaciones que recorren los filamentos como estremecimientos lentos a través de un resorte comprimido. El espacio intermedio entre el genoma y la pared no está vacío: una niebla molecular de agua, iones de magnesio y poliaminas llena ese interior, ejerciendo sobre ti una presión térmica aleatoria y simultánea desde todos los ángulos, porque a esta escala el agua a 37 grados no es un fluido sereno sino un entorno de violencia cinética constante. La geometría icosaédrica lo envuelve todo sin concesiones: no existe ninguna superficie plana ni ningún horizonte, solo la curvatura continua de una esfera perfecta construida por automontaje termodinámico, en la que cada nanómetro cuadrado de superficie interior cumple una función estructural precisa, sin nada decorativo, sin nada desperdicado.

Te encuentras atrapado dentro del canal de cola del bacteriófago lambda, un túnel proteico de apenas dos nanómetros de diámetro cuyas paredes te rozan por todos lados, formadas por anillos apilados de proteína de la placa base cuya superficie interna reluce con una luminiscencia violeta fría, el resplandor de los residuos cargados de arginina y lisina que revisten el cilindro como líquenes bioluminiscentes en una caverna submarina. El ADN bicatenario erupciona a tu lado como una cuerda de cristal plateado, impulsado por seis atmósferas de presión liberadas desde la cabeza del fago en lo alto, su esqueleto de fosfato centelleando en la penumbra mientras los surcos mayor y menor de la doble hélice pasan a velocidad catastrófica y el fluido confinado entre el ADN y las paredes cargadas apenas ocupa unos pocos nanómetros, vibrando como una capa de Debye iridiscente e inestable. Ante ti, el poro de salida se abre en la membrana interna bacteriana como una apertura luminosa de azul eléctrico, los lípidos del bícapa desplazados hacia afuera como un diafragma roto con un flequillo dorado pálido de colas hidrofóbicas expuestas, y más allá comienza el citoplasma de la bacteria —una oscuridad densa y seething, apenas iluminada por el calor difuso de mil millones de colisiones moleculares por segundo. Este es el instante irreversible en que el genoma abandona un recipiente para invadir otro, la información cruzando el umbral entre dos formas de existencia.

Des de l'interior d'una beina viral en formació, la volta de proteïnes Gag s'estén per sobre com una catedral de mel viva, cada anell hexamèric de vuit nanòmetres traçant amb precisió extraordinària la geometria d'un bastidor que s'autoconstrueix en temps real gràcies a interaccions termodinàmiques espontànies. La membrana plasmàtica, just al damunt del reticle, emana una llum ambre càlida —les dues fulles lipídiques prou resoltes com per entreveure els primers espiells d'Env inserits com bolets foscos retroil·luminats, marcadors de la futura infectivitat del virió. Al coll de constricció que delimita el perímetre del cúpol, els filaments d'ESCRT-III s'enrotllen en una hèlix metàl·lica d'aspecte rogenc, una maquinària cel·lular segrestada pel virus per executar la separació final de la membrana —un tall que alliberarà la partícula immadura a l'espai extracel·lular. A sota, el citoplasma s'estén com un univers dens i agitat: globus de ribosomes, cadenes d'ARN vibrant per la violència tèrmica del medi aquós, i centenars de proteïnes en col·lisió constant, tot plegat en un remolí molecular que recorda que fins i tot l'acte de néixer, a aquesta escala, és indistingible del caos.

Te encuentras de pie sobre la superficie exterior de un virión de VIH-1, y lo que se extiende ante ti es una llanura interminable de membrana lipídica —ocre cálido, ámbar profundo, siena quemada en el horizonte— que ondula con suaves marejadas térmicas como dunas animadas por un calor invisible, cada cabeza fosfatídica visible como un adoquín tenuemente luminoso bajo tus pies, los cristales de colesterol formando islas crema más rígidas en ese mar de oro fluido. Esta membrana no es una superficie inerte sino un sistema vivo en constante movimiento browniano: las moléculas lipídicas intercambian posiciones en microsegundos, generando un temblor sísmico que nunca cesa, el ruido de fondo termal de todo lo vivo a escala nanométrica, donde el agua circundante golpea la superficie con una energía comparable a la de una tormenta a escala humana. A unos cuarenta cuerpos de distancia, una de las doce espículas triméricas gp120/gp41 se alza como un monolito oscuro de basalto —catorce nanómetros de altura, corona trilobulada cubierta de cadenas de glicanos que la coronan como musgo bioluminiscente azul-verde—, una estructura extraordinariamente solitaria en esta vasta sabana curvada, porque el VIH-1 despliega apenas doce de estas torres sobre toda su superficie, una densidad casi absurdamente escasa comparada con la mayoría de los virus envueltos. Esta esparsidad no es un defecto sino una estrategia evolutiva de evasión inmune: menos espículas significa menos dianas para los anticuerpos neutralizantes, y cada una de esas torres está además blindada por ese escudo de glicanos que la hace casi invisible al sistema inmunitario del huésped.
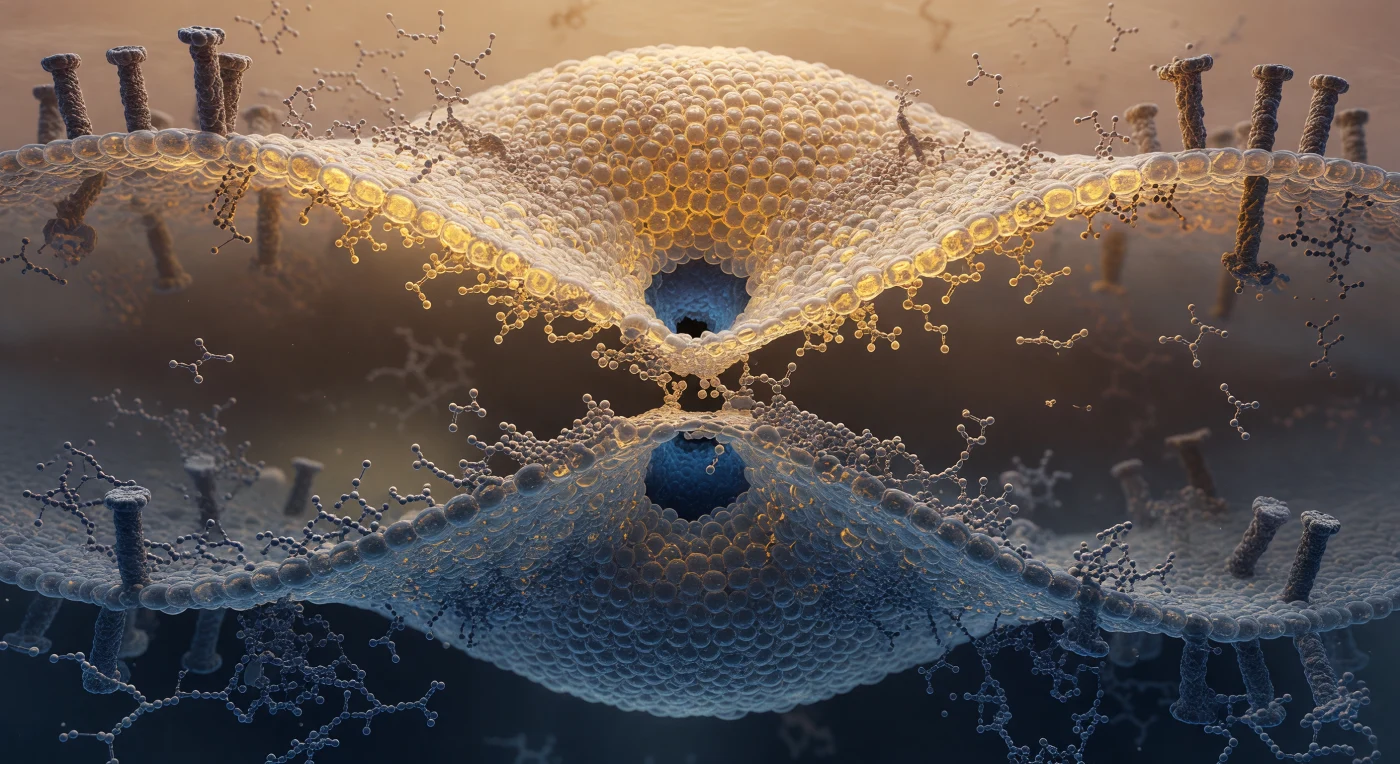
En este instante, te encuentras suspendido en la garganta de dos nanómetros de un tallo de hemifusión, el punto exacto donde dos mundos membranosos han abandonado su geometría ordenada para fundirse en una sola capa continua de lípidos entrelazados. Por encima, la bicapa viral se arquea como una bóveda de ámbar oscuro, sus cabezas fosfolipídicas —cada una del tamaño de un peñasco a esta escala— apiñadas en filas relucientes que tiemblan con violencia térmica discreta, sacudidas por la energía cinética del medio acuoso circundante; por debajo, la membrana endosomal replica esa geometría en azul acero y gris pizarra, sus leaflets curvándose hacia ti como el fondo de un océano frío e iluminado desde ninguna parte. Las proteínas de fusión viral, ancladas en ambas membranas como pilares irregulares hundidos en tierra blanda, han tensado toda esta arquitectura hasta el punto de ruptura, y en el centro mismo de tu campo visual una región de lípido estirado hasta el límite cede lentamente: el agua del interior viral y la del lumen endosomal empujan hemisferios oscuros y teñidos de azul contra los últimos angstroms de barrera molecular, anunciando el poro acuoso que, en fracciones de segundo, unirá irreversiblemente dos compartimentos que hasta hace un instante eran mundos separados.
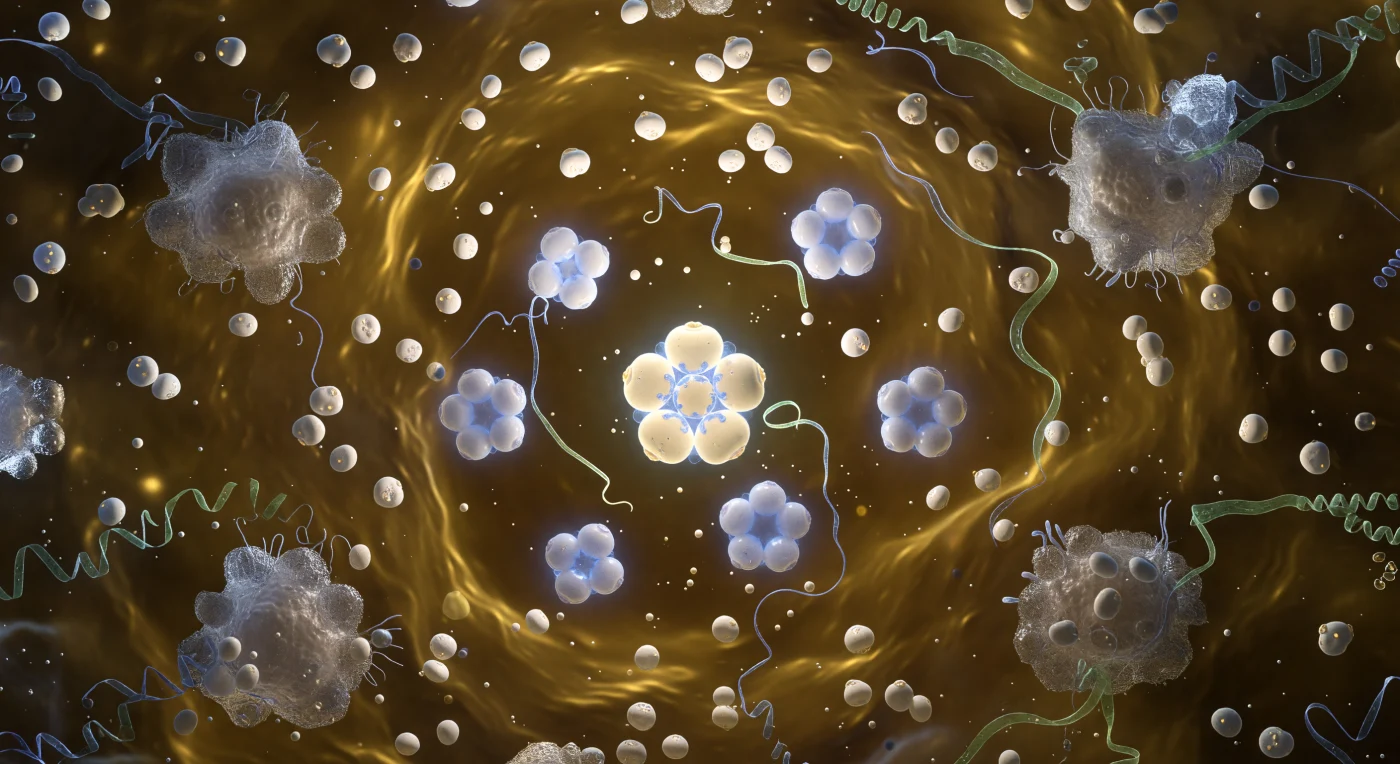

Te encuentras suspendida en el eje central de una vara del Virus del Mosaico del Tabaco, dentro de un túnel cilíndrico de apenas cuatro nanómetros de diámetro, cuyas paredes ascienden en una espiral dextrógira de 2130 subunidades proteicas entrelazadas con precisión matemática: cada subunidad es una lámina beta compacta de color ocre y ámbar cálido, sus aristas curvadas encajando en ángulos exactos para formar una hélice acanalada y corrugada que se pierde hacia arriba y hacia abajo en la penumbra con la regularidad de un mecanismo de relojería molecular. Incrustado en el surco interior de la pared proteica, a cuatro nanómetros del eje, el genoma de ARN de cadena sencilla serpentea como un hilo fosforescente de verde jade, sus nucleótidos apilados uno contra otro y abrazados electrostáticamente por residuos de arginina cargados positivamente en la cara interna de las proteínas de cubierta, una doble espiral en miniatura que sigue con fidelidad absoluta el sentido de la hélice que la contiene. Al mirar hacia el extremo lejano de la varilla —trescientos nanómetros en términos absolutos, pero a esta escala una perspectiva que se extiende como la nave de una catedral— el túnel se estrecha hasta una abertura circular de luz fría y pálida, un portal distante velado por la niebla browniana de moléculas de agua e iones que presionan desde el exterior. Las propias paredes proteicas vibran con oscilaciones picoscópicas, cada subunidad respirando y flexionándose en su lugar, y esa agitación térmica colectiva recorre la superficie acanalada como un temblor casi imperceptible, recordando que esta máquina molecular no está quieta: humea con energía cinética en el límite mismo de su estabilidad estructural.
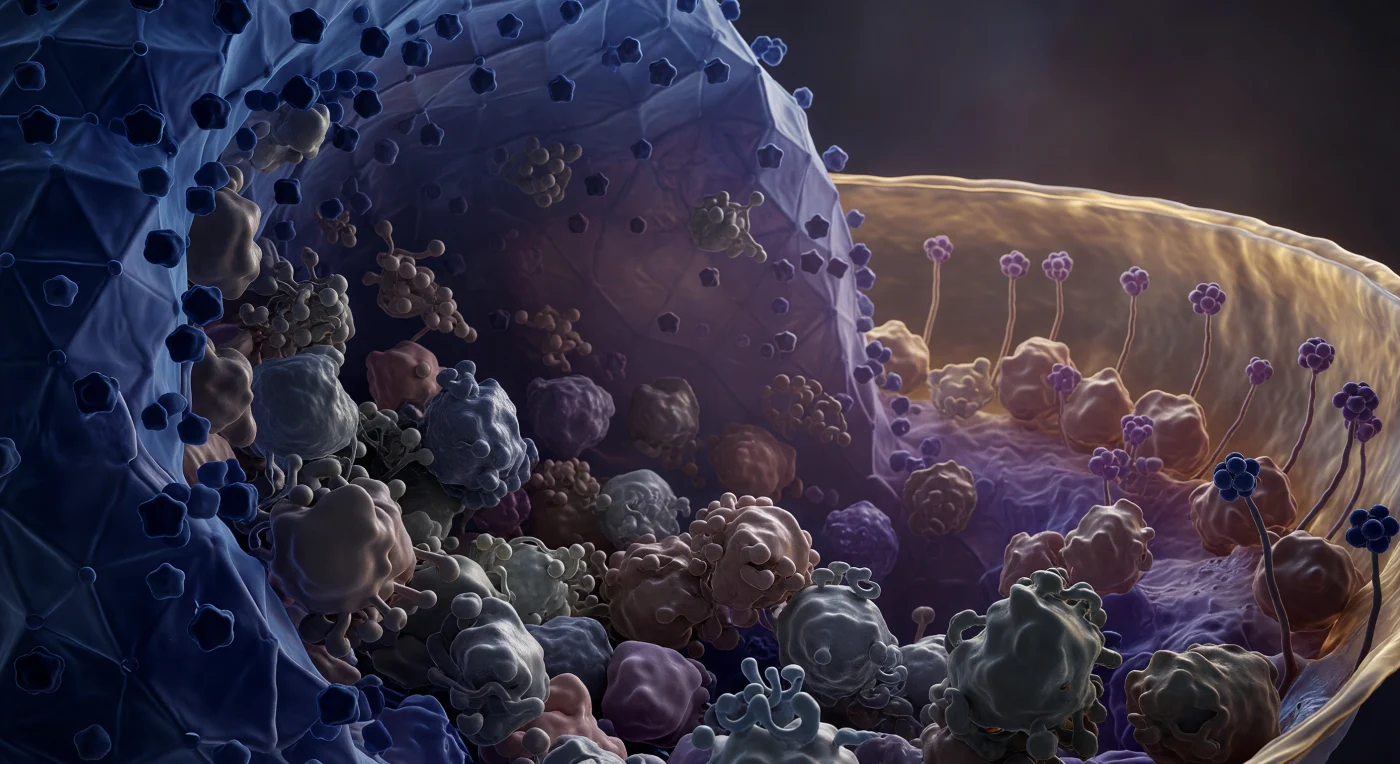
Te encuentras suspendido en el interior del tegumento de un virión del herpes simple, atrapado entre dos arquitecturas colosales que se curvan fuera de tu campo visual en ambas direcciones. A tu izquierda, la pared capsídica icosaédrica se alza como un acantilado facetado de cobalto profundo y azul medianoche, sus caras trianguladas emergiendo como una geometría geodésica alienígena de proporciones inmensas, con los vértices pentaméricos sobresaliendo como protuberancias oscuras que emiten una luminiscencia fría y difusa. A tu derecha, apenas cuarenta nanómetros de distancia que a esta escala equivalen a un horizonte lejano, la bicapa lipídica de la envuelta ondula en una franja doble de ámbar y oro miel, sus glucoproteínas ancladas meciéndose como flora abisal en una corriente imperceptible. Entre estas dos paredes, el tegumento te rodea con una densidad casi asfixiante: masas proteicas lobuladas e irregulares —VP16, UL36 y docenas de otras proteínas aún mal caracterizadas— se aprietan unas contra otras en grises violáceos y mauves polvorientos, sus superficies brillantes por el agua de hidratación, sus bordes difuminados donde los contactos hidrofóbicos fusionan una molécula con la siguiente hasta que ningún volumen cúbico permanece vacío. Este tegumento amorfo, único entre los virus animales, no es un espacio de tránsito sino una maquinaria comprimida: transporta factores de transcripción como VP16 directamente al núcleo de la célula infectada, y su vibración térmica constante —cada superficie temblando levemente contra su vecina— no es ruido sino la energía cinética misma de la vida molecular mantenida en un instante de tensión congelada.

Te encuentras suspendido en una jungla molecular de color verde ámbar que se cierra desde todas direcciones, atrapado en una red tridimensional de cadenas de mucina —polímeros glucoprotéicos entrelazados que forman un gel viscoso cuya malla varía entre 100 y 500 nanómetros de anchura— mientras sacudidas brutales de Brownian motion te arrojan lateralmente sin previo aviso, pues a esta escala el agua no es un fluido suave sino un medio térmicamente violento donde la energía cinética de cada molécula resulta enorme respecto a tu masa. A treinta o cuarenta longitudes de cuerpo por delante, la superficie de la célula epitelial asciende como una pared planetaria de color gris verdoso iridiscente, desde la cual emerge un bosque denso de cadenas de glicanos del glucocáliz cuyos extremos cargados de ácido siálico brillan con una fosforescencia rosa-magenta, estructuras que el virus debe penetrar o sortear mediante interacciones electrostáticas y enlaces de hidrógeno para alcanzar sus receptores de membrana. Ocasionalmente, un golpe térmico te aplasta contra una hebra pegajosa de mucina y el punto de contacto florece en un halo cálido color ámbar —una adhesión transitoria mediada por fuerzas de van der Waals y puentes de hidrógeno— antes de que la energía térmica rompa el vínculo y la cadena se aleje vibrando. Este trayecto a través del moco, un mecanismo de defensa de la mucosa respiratoria, puede inmovilizar o retardar indefinidamente a los viriones, filtrándolos antes de que jamás alcancen el epitelio subyacente.

Te encuentras suspendido en el interior de una película de hielo vítreo de setenta nanómetros de grosor, inmovilizado en fracción de milisegundo junto a todo cuanto te rodea, atrapado en una pausa absoluta donde la termodinámica molecular ha quedado congelada en plena violencia. Ante ti, masas esféricas de arquitectura icosaédrica emergen del sustrato grisáceo con la claridad implacable que solo el contraste electrónico puede otorgar: sus superficies se articulan en arreglos de cápsomeros pentagonales y hexagonales, cada protuberancia una colina de cuatro a ocho nanómetros de relieve, los espigos glucoproteicos de algunas partículas proyectándose hacia el hielo como coronas de espinas romas resueltas individualmente en su estructura trimérica. La paleta del mundo carece de todo cromatismo: sólo ceniza, grafito, hueso pálido y la oscuridad absoluta del borde del carbono fotorado que corta el horizonte como un acantilado geológico, el agujero del sustrato abriéndose en una nada perfecta y sin fondo. La escala se impone por proporción pura: el virión más próximo llena el campo visual como una cúpula catedralicia llena un patio interior, su pared capsídica —una doble banda oscura de cuatro a diez nanómetros de grosor— separando la densidad proteica del núcleo genómico del hielo estéril e infinito que lo envuelve.

De pie sobre la vasta superficie del virus vaccinia, el suelo bajo tus pies es una extensión de membrana suavemente arrugada de proteínas y lípidos, color gris verdoso con tintes de peltre oxidado, que se extiende en todas direcciones como una meseta de materia biológica casi plana pero de geometría caprichosa, sin ninguna de la elegancia geométrica icosaédrica que caracteriza a otros virus. Ante ti se elevan crestas paralelas de túbulos superficiales —estructuras de proteína comprimida que corren en filas aproximadamente alineadas pero irregulares, bifurcándose y terminando de forma abrupta, dejando entre ellas hondonadas donde se acumula una luminiscencia azul-blanca de origen electrostático, producto de la concentración de iones cerca de la membrana exterior cargada. A ambos lados, el terreno desciende hacia las regiones de los cuerpos laterales, lóbulos amorfos de material proteico que presionan hacia afuera contra la membrana como peñascos enterrados bajo una lona, proyectando sombras volumétricas de un gris-azulado profundo en una luz difusa que no proviene de ninguna fuente concreta sino del propio calor bioquímico del entorno a 37°C. Por encima, la membrana exterior —una bicapa lipídica de apenas nanómetros de grosor— se comba y ondula como un toldo traslúcido de vidrio ahumado, su cara interior reluciente como hielo glacial pálido, mientras que en el medio acuoso que lo rodea, masas globulares de proteínas derivan con lentitud imperceptible, sus desplazamientos gobernados enteramente por la difusión browniana en un entorno donde la viscosidad hace imposible cualquier movimiento inercial. Este es el poxvirus: el más complejo y extraño de los virus conocidos, una partícula asimétrica y primordial cuya arquitectura irregular —registrada hoy con resolución casi atómica gracias a la criomicroscopía electrónica— encierra en apenas 360 nanómetros de anchura la maquinaria genética capaz de replicarse de forma casi autónoma dentro de la célula huésped.

Estás suspendido sobre la superficie de una fortaleza molecular en movimiento: la cápside icosaédrica de un adenovirus, cuyas facetas de proteína marfil y platino frío se extienden bajo tus pies como los adoquines de una ciudadela antigua, transportada a lo largo de dos raíles fosforescentes de verde mar que son los microtúbulos del citoesqueleto, cada uno resuelto en crestas de protofilamentos de apenas 4 nm de altura, arquitectura tubular construida por dímeros de tubulina ensamblados con precisión cuasi-cristalina. A los flancos, complejos de dineína —motores moleculares de unos 15 nm, hierro gris y cobre oxidado, con anillos inclinados y apéndices articulados como cangrejos atrapados en mitad de su golpe de potencia— sujetan el vientre de la cápside a través de proteínas enlazadoras que pulsan en ámbar, arrastrándonos activamente hacia el núcleo celular cuya pared oscura y colosal domina el horizonte, salpicada de complejos de poro nucleares como iris de oro pálido apenas resueltos. El espacio circundante es una jungla de densidad aplastante: ribosomas broncíneos de 25 nm se agrupan en polisomas a lo largo de hilos invisibles de ARNm, mientras filamentos de actina en rojo arterial se entrelazan entre ellos con su doble hélice apenas perceptible, todo ello sacudido sin tregua por la violencia térmica del agua circundante, donde cada colisión de molécula de solvente es un terremoto a esta escala y la frontera entre materia viva e inerte se disuelve en pura geometría y fuerza.