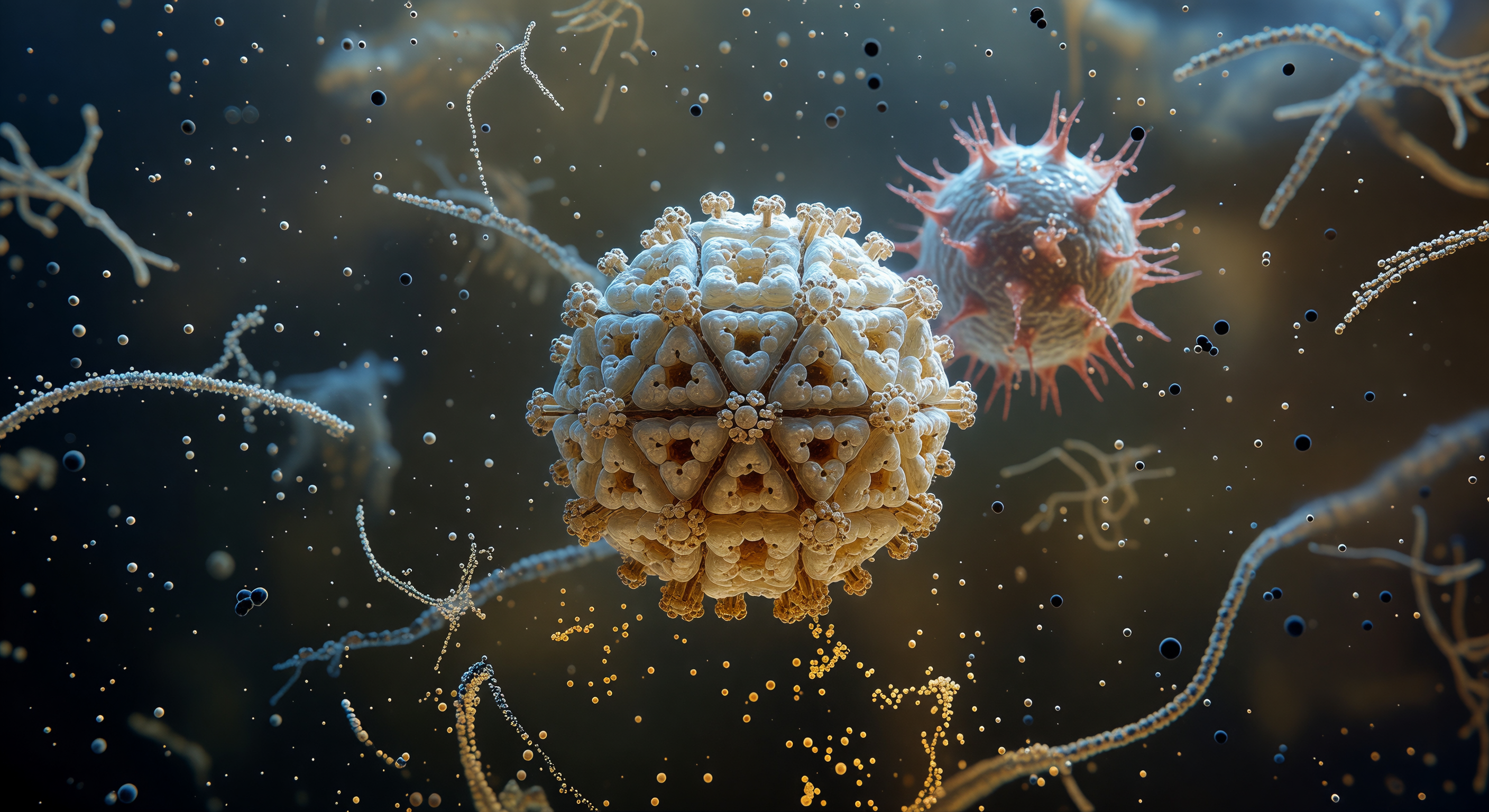
Affidabilità scientifica: Alto

La superficie del virione dell'influenza si estende in ogni direzione come una pianura ambrata e ondulante, ricoperta da una foresta fitta di colonne d'avorio — le trimere dell'emoagglutinina, ciascuna alta circa tredici nanometri, si ergono serrate con le loro corone glicoproteiche leggermente rigonfie, separate da corridoi stretti dove il doppio strato lipidico affiora appena in bagliori dorati. Tra questi pilastri si distinguono, a intervalli irregolari, le tetramere della neuraminidasi, più basse e tozze, con le teste appiattite di un verde-azzurro intenso che catturano la luce diffusa in modo diverso dal bianco osseo circostante, punteggiando la scena come funghi solitari in un bosco fitto. Il mezzo extracellulare non è vuoto ma un'atmosfera densa e luminosa: globuli di albumina sierica derivano come lanterne ambrate e traslucide, mentre lunghe catene di glicoproteine e filamenti di mucina ondeggiano nella distanza media come alghe in una corrente silenziosa, rifrattendo riflessi prismatici di lilla pallido e azzurro ghiaccio. La nebbia proteica si addensa rapidamente con la profondità, e già dopo poche file di colonne le strutture si dissolvono in una foschia opalescente dove solo i contorni fantasma sopravvivono, rendendo questo mondo claustrofobicamente intimo, senza cielo, senza orizzonte libero, senza via di fuga — solo la foresta molecolare che recede nel bagliore biologico.

Ci si trova sulla superficie esterna di un virione di SARS-CoV-2, in piedi sul foglietto esterno del doppio strato lipidico, un piano ondulante di ambra e oro che si increspa in lente onde termiche come una pelle viva tesa su qualcosa che respira, disseminato di cunei d'avorio di colesterolo che irrigidiscono localmente il terreno viscoso attorno ai loro punti d'inserzione. Da questa pianura emergono in ogni direzione le proteine spike trimeriche — colonne torreggianti di cremisi scuro e rosso sangue, alte venti nanometri, con radici ancorate nella membrana che ne distorcono e sollevano il bordo lipidico, i loro fusti scanalati che si allargano salendo fino a sbocciare in cima in tre domini di legame aperti verso l'alto come pale di una turbina in attesa, presentando le loro superfici di riconoscimento al vuoto sovrastante. Tra una colonna e l'altra si aprono corridoi di quindici nanometri di bilayer libero — strade larghe tra obelischi monolitici che si ripetono fino a un orizzonte curvo, tradendo la geometria sferica dell'intero virione. In basso, lontana, la membrana cellulare ospite si distende come una pianura grigio-azzurra ricoperta di glicani ramificati come cristalli di brina, mentre sopra le spike si apre il vuoto extracellulare in un blu notte quasi assoluto, e l'intero paesaggio vibra in uno stato di silenziosa, incessante urgenza molecolare.

Sei disteso contro la superficie della membrana esterna di un batterio, schiacciato tra le catene di lipopolisaccaridi che si innalzano intorno a te come massi su una pianura di ambra e verde bile, mentre l'intera distesa trema di rumore termico, un'agitazione continua e percussiva che fa tremolare l'orizzonte come aria sopra asfalto rovente. Sopra di te, scendendo direttamente dall'alto e occupando quasi tutto il campo visivo, il basale esagonale del batteriofago T4 si avvicina come una corona geometrica di sessanta nanometri, le sue sei facce lucidate in un'architettura proteica grigio-argento con una sottile luminescenza viola-blu dove i foglietti beta impaccati rifrangono il bagliore diffuso dell'ambiente acquoso circostante. Sei fibre caudali lunghe si dispiegano verso l'esterno a raggiera come le zampe articolate di un enorme ragno meccanico, i loro apici distali che già affondano nella membrana a centinaia di nanometri di distanza, agganciandosi con precisione assoluta agli specifici recettori di zucchero LPS in un riconoscimento molecolare irreversibile. Al di sopra del basale, il guaine contrattile elicoidale sale verso un punto di fuga lontano, striata di anelli sovrapposti in acciaio e blu freddo, fino a dissolversi nella nebbia indigo prima ancora che la testa icosaedrica diventi visibile — solo il suo vertice inferiore emerge fantasmatico dalla foschia, a ricordare che questo colosso da duecento nanometri sta per compiere il gesto per cui esiste, iniettare il proprio genoma attraverso una delle membrane più difese della biosfera.

Vi trovate al centro geometrico di una cattedrale molecolare: la capside del virus dell'epatite B, una sfera icosaedrica di circa 36 nanometri di diametro il cui numero di triangolazione T=7 impone alle 420 subunità proteiche una logica geodetica inflessibile, con dodici vertici pentamerici che chiudono la geometria sferica come chiavi di volta e fasce di esameri che rivestono ogni faccia triangolare con protuberanze beta-barrel alte 4-5 nanometri, il tutto avvolto in una fosforescenza ambrata diffusa che sembra emanare dalla struttura quaternaria stessa. La parete curva si estende in ogni direzione senza interruzione, bronzo martellato e corallo fossilizzato fusi in un'unica superficie biologica dove ogni nanometro quadrato è occupato da texture funzionale: nessun piano piatto, nessun orizzonte, soltanto la volta geodetica che si incurva sopra e attorno a voi nel caldo alone delle catene polipeptidiche compresse. Sotto i vostri piedi, il genoma a dsRNA riempie lo spazio disponibile in densi grovigli di arancione bruciato e rame ossidato, le eliche compresse le une contro le altre così strettamente che i solchi minori e maggiori si confondono nella massa, mentre l'intero aggregato trema di agitazione termica a frequenze impercettibili ma inesorabili, ogni filamento che oscilla come una molla compressa percorsa da scosse lente. Lo spazio tra il genoma e la parete proteica non è vuoto: una nebbia molecolare di acqua, ioni magnesio e poliamine riempie il mezzo acquoso a 37°C, trasformando ogni contatto in un potenziale evento di legame e il semplice esistere a questa scala in un'immersione nella violenza termica casuale dell'universo biologico.

Sei dentro il corridoio più stretto dell'universo biologico: un cilindro di soli due nanometri di diametro, rivestito di anelli proteici cristallini che proiettano sulle pareti una luminescenza violacea fredda — il bagliore delle cariche elettrostatiche di residui di arginina e lisina, ordinati con la precisione di una struttura a raggi X. Attraverso questo tunnel, il DNA a doppio filamento del batteriofago lambda ti sfreccia accanto come una fune di vetro argentato, spinto da una pressione interna di sei atmosfere accumulata nella testa del fago: il filasso vibra termicamente mentre riempie quasi per intero il canale, lasciando tra sé e le pareti cariche uno spessore di pochi nanometri in cui il campo elettrostatico trema come un miraggio sul asfalto rovente. Davanti a te, il poro d'uscita squarcia la membrana interna batterica in un'apertura elettrica di luce blu-bianca, con le molecole lipidiche scacciate verso l'esterno come un diaframma lacerato, i loro gruppi idrofobici brevemente esposti come un alone dorato attorno alla breccia. Oltre quella soglia luminosa inizia il citoplasma — un'oscurità brulicante e irrisolvibile, densa di collisioni molecolari, il luogo dove il genoma virale compie il passo irreversibile da una cellula all'altra, trasformando in pochi secondi il destino di un intero organismo.

Alzando lo sguardo dall'interno di questa cupola nascente, si osserva una volta proteica che si arcua come la navata di una cattedrale vivente: il reticolo di poliproteine Gag forma una tessellatura esagonale color oro antico, ogni anello esamericale largo circa otto nanometri, le cui superfici granulari e lievemente irregolari tradiscono la natura biologica di questa architettura in continuo assemblaggio. La membrana plasmatica oltre la faccia esterna del reticolo irradia un calore ambrato — una doppia lamina lipidica appena risolta come un velo di rame bruciato, punteggiata dagli spike Env virali come funghi scuri retroilluminati da un'incandescenza interna tutta molecolare. Al collo della struttura, dove la geometria esagonale cede a distorsioni pentameriche che stringono il bordo del domo, i filamenti di ESCRT-III si avvolgono in una spirale elicoidale color rame opaco — macchinario cellulare dirottato dal virus per tagliare la propria via di fuga per scissione della membrana. Sotto, il citoplasma si estende come un sottomondo oscuro e affollato, dove globuli ribosomiali da cinque a venticinque nanometri si addensano in catene torbide, filamenti di RNA derivano come ragnatele luminescenti, e la violenza termica del moto browniano agita ogni elemento in un tremito perpetuo, rendendo palpabile la densità termodinamica di questo spazio dove ogni collisione molecolare è un potenziale evento chimico.

Ci si trova in piedi sulla superficie esterna di un virione di HIV-1, e la membrana lipidica si distende in ogni direzione come una pianura desertica senza fine, ondulata da lenti moti termici che fanno oscillare i gruppi testa dei fosfolipidi — visibili come selciato luminoso sotto i piedi — in un continuo rimescolamento viscoso percepibile come impercettibili tremori del suolo. A una quarantina di lunghezze corporee di distanza, uno dei dodici spigoni trimerici gp120/gp41 si erge dalla membrana come un monolite di basalto scuro, alto circa il doppio della propria statura, la sua corona a tre lobi avvolta in un alone di catene glucidiche traslucide color verde-azzurro che ne corona la sommità come muschio bioluminescente, mentre intorno alla base trema una penombra elettrostatica — il layer di Debye — che distorce l'atmosfera ionica come aria calda sopra il deserto. L'HIV-1 porta in media soltanto undici-dodici di questi trimeri sulla sua superficie, una densità straordinariamente bassa rispetto ad altri virus rivestiti, evoluta probabilmente per sfuggire alla sorveglianza anticorpale: ogni spike è un'isola isolata in una vastità di membrana ricca di colesterolo, separata dalla successiva da distanze enormi a questa scala. Il cielo sopra di sé è una sospensione densa di molecole d'acqua e ioni che si legge come una foschia ambrata calda, e la superficie sotto i piedi vibra in piccoli impulsi casuali e inarrestabili — il bombardamento browniano — un sisma molecolare che non si organizza mai in una direzione, fedele testimonianza di un mondo governato dall'energia termica e non dalla forza muscolare.
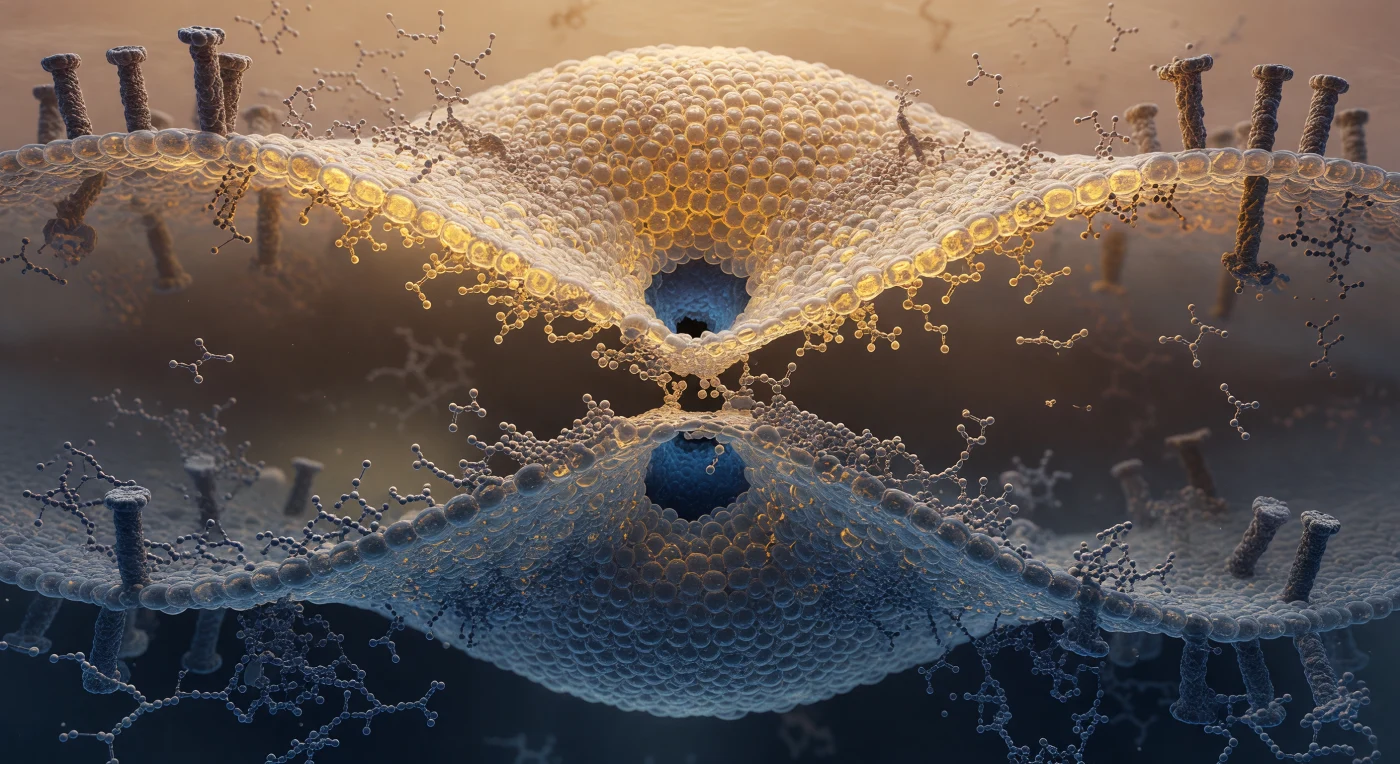
Ci si trova sospesi nel punto esatto in cui due universi di membrana si toccano per la prima volta: sopra, la volta ambrata del doppio strato virale si curva verso il basso in una cascata di sfere fosfolipidiche serrate come selciato antico, ciascuna visibile come un boulder traslucido che trema di energia termica; sotto, la membrana endosomiale risponde con la stessa geometria molecolare immersa in toni di acciaio freddo e grigio ardesia, come se filtrasse una luce di acque profonde. Tra questi due piani curvi si stringe lo stalo di emifusione: un collo di clessidra largo appena due nanometri dove la doppia architettura dei bilayer è collassata in un unico monostrato continuo, le catene idrofobiche degli acidi grassi intrecciate in un groviglio caotico, i gruppi testa fosforilici sparsi in una corona disordinata attorno alla vita della struttura con una lucentezza semitrasparente, quasi organica, quasi ferita. Ai margini del campo visivo, le proteine di fusione virale emergono come colonne irregolari affondate simultaneamente in entrambi i leaflet, tenendo in tensione l'intera geometria come picchetti piantati in terra morbida, mentre frammenti di catene glicosiliche e densità proteiche fluttuano nel mezzo acquoso circostante come alghe in una corrente lentissima. Al centro, dove l'occhio cerca un varco, il lipide si è assottigliato fino all'inverosimile: due emisferi acquosi — l'interno virale e il lume endosomiale — premono l'uno verso l'altro attraverso gli ultimi ångström di barriera molecolare, un poro scuro che non è ancora un foro ma una promessa di fusione, il momento in cui due mondi separati stanno per diventare uno solo.
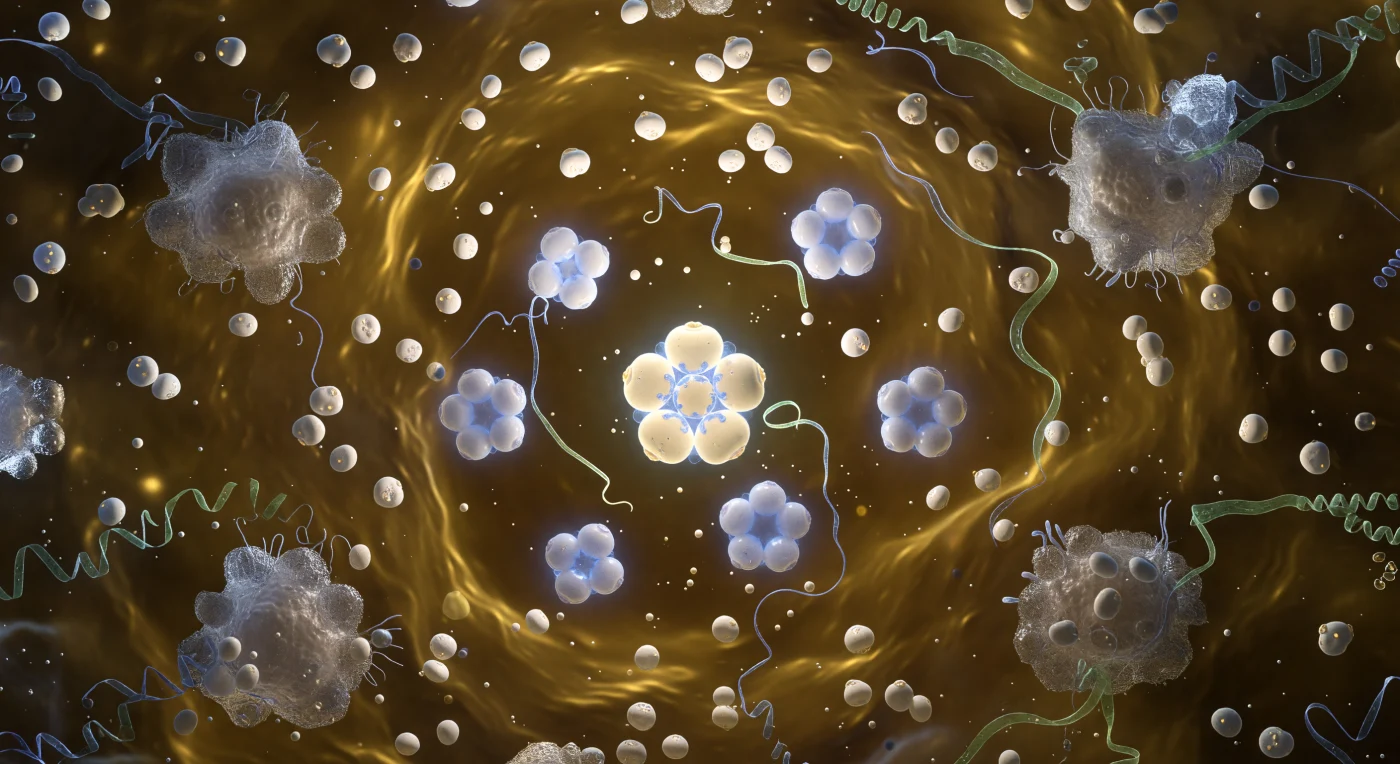

Ti trovi sospeso al centro geometrico di una delle macchine molecolari più eleganti della natura: il capside del virus del mosaico del tabacco, un cilindro lungo trecento nanometri le cui pareti sono costruite da 2130 subunità proteiche che si avvolgono in un'elica destrorsa con precisione assoluta, ogni subunità un compatto sandwich di beta-foglietti color ocra e ambra che si incastra con le adiacenti formando un tunnel costolato di quattro nanometri di diametro, simile a una bobina di porcellana molecolare illuminata dall'interno da una luce calda e diffusa. A quattro nanometri dall'asse centrale, incassato in uno scanalatura che percorre tutta la spirale, il genoma a RNA singolo filamento corre come un filo fosforescente di verde giada, trattenuto in un abbraccio elettrostatico da residui di arginina sulla superficie interna delle proteine, ogni nucleotide impilato sul successivo con fedeltà assoluta alla geometria elicoidale del capside che lo avvolge. Le pareti stesse non sono immobili: ogni subunità respira e flette sotto la pressione termica dell'ambiente, producendo un fremito appena percettibile su tutta la superficie costolata, mentre il canale assiale è affollato di molecole d'acqua e ioni che premono dall'esterno con una pressione che si avverte più che si vede. Guardando verso l'estremità opposta del cilindro, la prospettiva si allunga come la navata di una cattedrale, e il tunnel si restringe in un portale circolare di luce pallida e fredda, lontano trecento nanometri in termini assoluti ma qui percepito come un orizzonte remoto, velato dalla nebbia browniana di un ambiente che vibra instancabilmente al limite della stabilità strutturale.
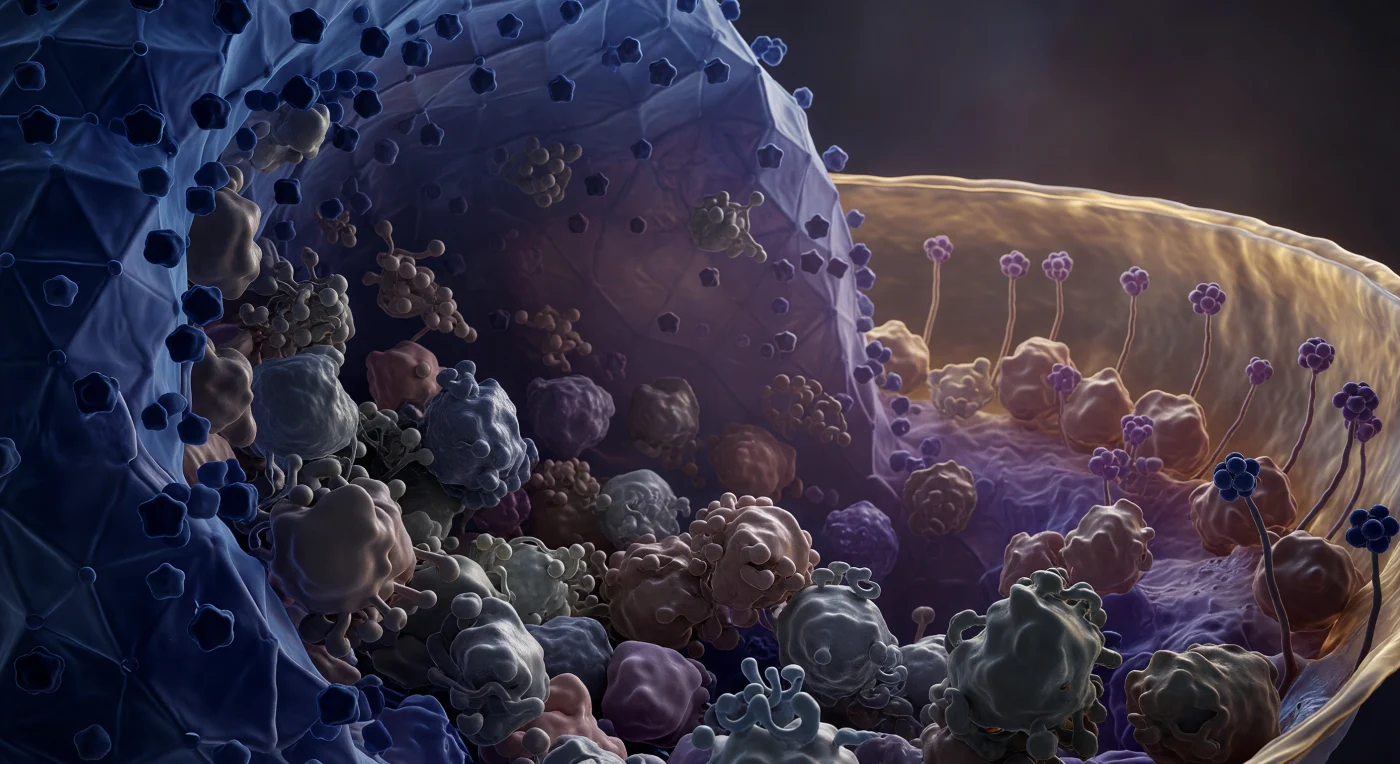
Ti trovi sospeso nell'oscurità compressa del tegumento, lo strato proteico amorfo che occupa i quaranta nanometri tra la parete capsidica e l'involucro lipidico dell'herpes simplex virion. Attorno a te si accalcano masse lobate di VP16 e UL36, proteine irregolari dalla superficie traslucida e umida che si premono l'una contro l'altra senza lasciare alcun corridoio libero, ogni volume molecolare reclamato in una densità quasi soffocante di contatti idrofobici e legami non covalenti. Alla tua sinistra, la parete del capside icosaedrico si erge come una scarpata di cristallo cobalto, le sue facce triangolate che curvano verso l'alto e scompaiono nella nebbiolina molecolare, i vertici pentamerici sporgenti come torrette di un paesaggio alieno e geometrico generato dall'identica logica della simmetria matematica che governa ogni virione della famiglia Herpesviridae. A destra, a soli quaranta nanometri di distanza — una distanza percorribile in pochi battiti termici — l'envelope lipidico ondeggia come un orizzonte ambrato, il suo doppio foglietto risolvibile a questa scala come due bande distinte di oro e miele che tremano sotto la pressione costante del moto browniano, con gli steli glicoproteici ancorati alla faccia interna come flora abissale in una corrente impercettibile. L'intera scena è pervasa da una tensione irriducibile: il tegumento non è ordinato né cristallino, ma una massa amorfa e semi-solida la cui architettura è determinata non dal design ma dall'equilibrio caotico di forze di van der Waals, repulsioni steriche e fluttuazioni termiche che scuotono ogni superficie con un'energia di circa quattro piconewton per nanometro.

Ci si trova sospesi in un intrico soffocante di cavi polimerici color verde-ambra, le catene di mucina che si intrecciano in ogni direzione formando una rete tridimensionale irregolare con maglie larghe tra i cento e i cinquecento nanometri, abbastanza strette da sfiorare i fianchi ad ogni scossone termico impresso dalle molecole d'acqua circostanti. Il moto browniano non è una vibrazione delicata: a questa scala il calore è violenza pura, scarti laterali improvvisi e rimbalzi contro i filamenti adesivi che lasciano per un istante un alone ambrato caldo prima che l'energia termica strappi via il contatto. La mucosa delle vie aeree è un ecosistema biochimico denso — le glicoproteine muciniche, altamente glicosilate e cariche negativamente, formano un gel viscoelastico che costituisce la prima barriera difensiva dell'epitelio respiratorio, capace di intrappolare e rallentare i patogeni prima ancora che raggiungano la superficie cellulare. In lontananza, a trenta o quaranta lunghezze di corpo, la membrana plasmatica dell'epitelio si incurva come un pianeta di colore teal scuro, dalla cui superficie si erge la foresta del glicocalice: catene di glicosamminoglicani e glicoproteine che oscillano sotto la spinta del moto termico, le loro punte di acido sialico che pulsano di un rosa fosforescente, residui chimici cruciali che molti virus respiratori riconoscono come recettori d'ingresso. Tra la giungla di mucina in cui si è immersi e quella soglia luminosa si distende un gradiente di complessità molecolare crescente, un paesaggio che a questa scala appare smisurato come un continente, eppure misura meno di un micrometro.

Sospeso nell'immobilità assoluta di un oceano vetrificato in millisecondi, ti trovi circondato da masse sferiche di proporzioni cattedrali: virioni icosaedrici inglobati nel ghiaccio amorfo, le loro superfici che presentano capsomeri esagonali e pentagonali con una nitidezza allucinante, ogni rilievo da quattro a otto nanometri leggibile come una sequenza di creste e canyon in puro contrasto elettronico. L'illuminazione non ha direzione né fonte cromatica — solo densità, convertita in gradiente dal carbone grafite al grigio cenere al bianco osseo dove il film di ghiaccio si assottiglia fino a quasi nulla — e le regioni più dense di proteina affondano nel nero assoluto mentre il ghiaccio stesso legge come un tono d'argento uniforme, né riflettente né rifrangente, semplicemente trasmissivo come vuoto solidificato. Sulle particelle più vicine, un sottile doppio anello scuro tradisce la presenza del doppio strato lipidico che avvolge alcune di esse, e dalla superficie di queste protrudono spike glicoproteici trimerici — corone di spine ottuse individualmente risolte — separati l'uno dall'altro da distanze che a questa scala equivalgono a pianure di ghiaccio sterile. Al margine del campo visivo, il bordo del foglio di carbonio crolla come una scarpata geologica in un abisso di nero assoluto, il confine netto di un mondo in cui ogni moto browniano è stato arrestato a metà traiettoria, ogni ione bloccato nella posizione esatta che occupava nel momento in cui la temperatura è precipitata abbastanza velocemente da sconfiggere l'ordine cristallino stesso.

Ti trovi sulla superficie di un mattone di vaccinia, un paesaggio di proteina grigio-verdastra che si estende per 360 nanometri da un bordo all'altro come un altopiano desertico quasi piatto, le cui creste parallele di tubuli superficiali si ergono all'altezza della vita in filari di corda proteica compressa dal colore dello stagno ossidato. Sotto i tuoi piedi, la membrana esterna è morbidamente increspata — un composito lipoproteico che cattura una luce diffusa e azzurrina nelle sue pieghe poco profonde, ciascuna intaccatura una piccola ravina in un terreno coriaceo dove l'accumulo di cariche elettrostatiche fa brillare dolcemente pozze di luminescenza bianco-glaciale. Ai lati, il terreno scende verso le regioni dei corpi laterali, lobi amorfi di materiale proteico che premono dall'interno contro la membrana come massi sepolti sotto una tela cerata, proiettando ombre volumetriche di un grigio-teal profondo in un'illuminazione che non ha sorgente singola ma nasce come bagliore termico aggregato di un ambiente a 37°C. Sospese nel mezzo acquoso viscoso sovrastante, masse proteiche globulari derivano con lentezza impercettibile, la loro presenza tradita da sottili onde di pressione nelle pieghe della membrana — nessuna simmetria icosaedrale qui, nessuna geometria ripetuta, solo l'architettura irregolare e primordiale di una delle particelle biologiche più complesse e ancestrali che la natura abbia mai prodotto.

Sospesi sulla superficie di un'antica fortezza molecolare, osservate come la geometria icosaedrica del capside adenovirale si distenda sotto di voi in un mosaico di capsomeri d'avorio pallido e platino freddo, ciascuno un nodo proteico denso che cattura la luce bioluminescente diffusa nell'ambiente circostante. Direttamente sotto, due binari paralleli di microtubulo si estendono verso un orizzonte lontano, le loro creste di protofilamenti di tubulina che emanano un bagliore fosforescente verde-azzurro, architettonici nella loro imponenza, come cavi di un ponte sospeso osservati dagli occhi di un insetto. Complessi di dineina affiancano il percorso in pose asimmetriche di forza meccanica — forme simili a granchi in grigio ferro e rame ossidato, i cui domini di legame al carico aggrappano il ventre del capside attraverso proteine linker che ardono di ambra, trascinando l'intera struttura verso la vasta parete oscura dell'involucro nucleare che curva attraverso il campo visivo come un pianeta, punteggiata dai complessi del poro nucleare in oro pallido. Intorno a tutto questo, il citoplasma è una giungla di densità schiacciante: ribosomi in bronzo antico ammassati in polisomi, filamenti di actina rosso arterioso che si intrecciano a spirale come coralli illuminati da una luce cremisi abissale, ogni superficie una potenziale reazione, ogni contatto un evento di legame in un universo governato non dalla gravità ma dalle forze di van der Waals e dall'agitazione termica incessante.