
Você existe no coração geométrico de uma proteína globular, comprimido no interior de um núcleo hidrofóbico onde nenhuma molécula de água jamais penetrou — um espaço definido não pelo vazio, mas pela matéria maciça das cadeias laterais de leucina, valina e fenilalanina compactadas a 75% de densidade, cujas superfícies de contato de van der Waals se tocam sem se fundir, separadas apenas pela repulsão quântica mais fina que a física permite. A caverna imediata é geológica na sua geometria: esferas cinzento-carvão e marfim quente pressionam umas contra as outras como pedras fluviais perfeitamente encaixadas, cada superfície subtilmente fosforescente com a sua própria densidade electrónica, projetando halos de contato pálidos onde duas nuvens atômicas se roçam, enquanto os anéis aromáticos da fenilalanina cortam o espaço como discos de obsidiana escura, as suas sombras absolutas e nítidas numa escuridão que não conhece luz difusa. Dispersos pela matriz, dois ou três átomos de enxofre da metionina captam o mínimo de luminescência existente e devolvem-no como um brilho âmbar-amarelado profundo — pontuações de calor biológico num mundo de outra forma acromático, como brasas vistas através de pedra fendida. Muito além, a dez ou quinze diâmetros atômicos de distância, a compactação afrouxa imperceptivelmente e uma fria luz azul-aquosa filtra-se pelas fissuras entre os elementos de estrutura secundária, o assinatura distante do solvente bulk que envolve a proteína — chegando ao núcleo como bioluminescência filtrada por metros de oceano imóvel, sugerindo profundidade e encerramento sem jamais iluminar coisa alguma, enquanto as vibrações térmicas a 310 Kelvin percorrem a estrutura como um pulso lento e sub-angstrom através de cada superfície em contacto.

O observador encontra-se suspenso na boca do túnel de saída peptídico do ribossoma, olhando para o interior de um corredor de arquitetura ribonucleica em tons de ocre e bronze queimado, cujas paredes são formadas por hélices de RNA ribossomal entrelaçadas — plataformas de empilhamento de bases nucleotídicas projetam-se para o interior como lajes de ardósia sobrepostas, cada uma com apenas alguns ångströms de largura, suas faces aromáticas captando a luminescência azul-branca que emana do centro peptidil transferase dez nanômetros à frente, como uma fornalha catalítica rodeada por pilares radiais de rRNA que lançam sombras profundas em âmbar e índigo. No ponto de constrição, o túnel estreita-se a apenas 1,5 nanômetros, onde as superfícies de van der Waals dos pilares opostos quase se tocam, suas névoas de densidade eletrónica interpenetrando-se numa franja de contacto violeta pálido, enquanto moléculas de água em vibração térmica ensombreiam o meio da cena numa neblina translúcida e tremulante. Uma cadeia polipeptídica nascente avança em direção ao observador desde a fornalha catalítica, o seu esqueleto alternando entre verde lima luminoso e âmbar quente ao longo de cada ligação peptídica, com cadeias laterais hidrofóbicas que roçam fugaz e intimamente as paredes estriadas de rRNA antes de serem retiradas pelo movimento térmico da própria cadeia. Nos relevos das paredes, halos de contra-iões — magnésio e potássio encaixados nas reentrâncias do sulco maior — brilham como pontos especulares de luz prateada, cada um envolto na sua própria camada de moléculas de água orientadas, lembrando que cada superfície aqui é probabilística e dinamicamente viva. Esta passagem molecular não é uma estrutura estática, mas um canal eletrostaticamente carregado e em respiração contínua, onde o ruído térmico, os gradientes de carga e os efeitos hidrofóbicos colaboram no transporte silencioso dos primeiros momentos de existência de uma nova proteína.

Você voa por um corredor em espiral com menos de dois nanómetros de largura, as paredes a curvar-se para dentro de ambos os lados como gargantas de uma catedral em miniatura, construídas não de pedra mas de densidade eletrónica probabilística que se recusa a ter contornos nítidos. O chão da canelura maior da dupla hélice de DNA em conformação B é um mosaico de plataformas aromáticas empilhadas — âmbar quente da adenina, verde-sálvia suave da timina, azul-teal profundo da guanina, azul-celeste da citosina — separadas por apenas 0,34 nanómetros cada uma, com as suas nuvens de eletrões π a sobreporem-se num brilho translúcido violeta-índigo que pulsa entre os andares como interferência quântica visível. As paredes da canelura erguem-se como railings de fosfato-açúcar, laranja-bege e ligeiramente translúcidos, percorridos por contra-iões em suspensão — magnésio como faíscas branco-azuladas intensas envoltas em conchas de moléculas de água orientadas, sódio como halos dourado-pálido à deriva na névoa eletrostática — enquanto a camada de Debye confere ao espaço além das margens carregadas uma luminosidade leitosa e auroral de azul suave. O bombardeamento térmico das moléculas de água omnipresentes enche o corredor com um tremor constante, cada colisão uma centelha de luz branca rapidamente engolida pelo brilho aquoso ambiente, e à frente a hélice espirala suavemente para a direita, os seus andares de bases a desaparecerem em perspetiva numa sucessão decrescente de âmbar, teal, azul e verde, tudo capturado na quietude cristalina de um único femtossegundo.

O visitante paira a apenas dois nanómetros da zona de contacto, suspenso entre dois mundos de densidade electrónica que se aproximam como continentes em colisão lenta — de um lado, o corpo maciço do fragmento Fab em cinzento-prateado, com a sua arquitectura de folha beta a erguer-se como uma muralha de cristas laminares, e do outro, a superfície convexa do epítopo antigénico em tons de ocre e terracota, moldada com precisão complementar para receber os loops CDR que se avançam. Os seis loops da região hipervariável — o H3 em âmbar arqueado com confiança, o L3 em verde-azulado serpenteando por baixo, os restantes quatro em prateados e mauves surdos — formam uma cúpula arquitectónica que fecha em redor do epítopo como dedos de uma mão imensa, definindo uma zona de contacto de cinco por seis nanómetros onde a exclusão de moléculas de água transforma superfícies antes hidratadas em faces nuas de nuvem electrónica. As moléculas de água expulsas dispersam-se como faíscas de espelho partido, cada dipolo assimétrico captando a luz ambiente azul-cianótica num clarão branco antes de se dissipar no solvente circundante, enquanto pontes de ligação de hidrogénio em ciano se consolidam uma a uma como fios luminescentes entre as superfícies em aproximação — manifestações visíveis da entropia de desolvatação e da complementaridade electrostática que governam a especificidade de reconhecimento molecular com constantes de dissociação que podem atingir valores picomolares. Este abraço molecular, filtrado pela luz difusa e volumétrica do solvente aquoso como no fundo de um oceano translúcido, não é estático: cada superfície vibra com flutuações térmicas na escala dos picossegundos, e é precisamente da tensão entre o bombardeamento browniano omnipresente e a geometria de encaixe precisa que emerge a estabilidade do complexo imunológico.
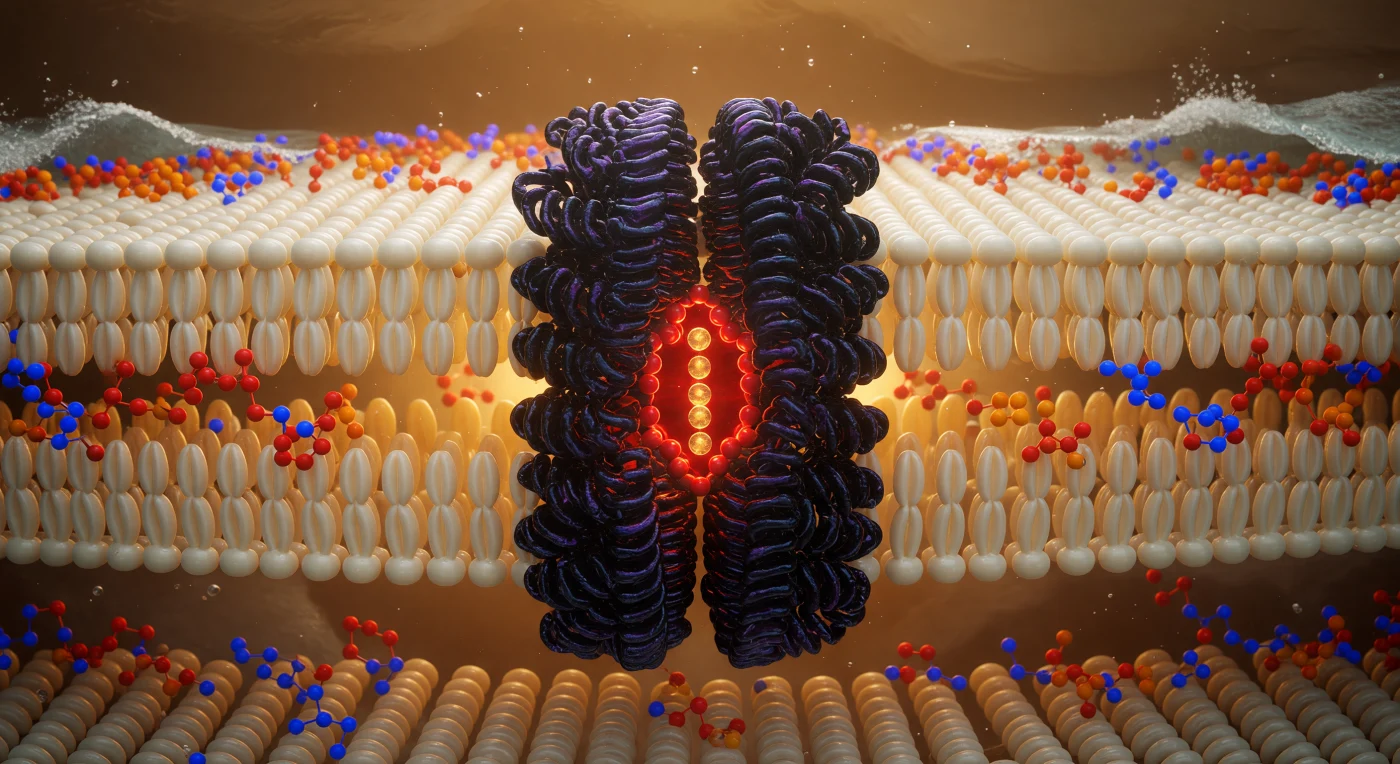
Você se encontra suspenso no plano médio de uma bicamada fosfolipídica, a dois nanômetros de cada interface aquosa, envolto por uma floresta densa de cadeias de ácidos graxos que se estendem em todas as direções como cilindros de marfim polido, aquecidos por um brilho eletrostático difuso proveniente das nuvens eletrônicas de cada átomo vizinho. O interior hidrofóbico da membrana é governado por forças de van der Waals e pela exclusão entrópica da água, criando um ambiente de viscosidade oculta e movimento térmico constante, onde as cadeias carbonadas vibram e ondulam em escalas de picossegundos sem nunca se dissolverem no caos. Emergindo desta neblina âmbar diretamente à sua frente, o canal de potássio KcsA ergue-se como uma coluna de basalto de simetria quádrupla, com cerca de 3,5 nanômetros de diâmetro, suas hélices transmembranares entrelaçadas aos lipídios circundantes por resíduos hidrofóbicos que formam uma interface proteína-membrana mecanicamente coesa e termodinamicamente estável. No eixo central da proteína, o filtro de seletividade arde em vermelho-alaranjado concentrado — um anel preciso de oxigênios carbonílicos que coordena íons potássio em fila única, despindo-os de sua hidratação e reconstituindo-a com geometria atômica de precisão angstrom, selecionando K⁺ contra Na⁺ com fidelidade iônica que nenhuma engenharia humana ainda igualou. Acima e abaixo, as camadas de cabeças polares da fosfocolina pulsam como horizontes luminosos de cor saturada — fósforos alaranjados, nitrogênios cobalto-azuis, oxigênios carmesim — separando este mundo interior aquecido e silencioso do tumulto aquoso que pressiona a membrana de fora como oceano contra um recife.

Você está suspenso a poucos centímetros acima de uma planície corrugada que se estende até todos os horizontes — uma folha beta antiparalela vista em intimidade atómica, as suas cristas de cor âmbar-pergaminho alternando de direção com a precisão geométrica de uma cantaria milenar, cada intervalo de crista a crista correspondendo a apenas um nanómetro de distância real. As pontes de hidrogénio ciano cosem lateralmente os fios adjacentes como filamentos fantasmagóricos de probabilidade eletrostática, cada um emitindo um suave brilho aguamarino onde as nuvens eletrónicas do dador e do aceitador se sobrepõem a uma distância de 2,9 ångströms, tecendo coletivamente a planície numa armadura molecular. Oxygens carbonilo cor de cereja sobressaem do cume de cada crista como granadas polidas incrustadas em osso antigo, enquanto as pontas de amida brancas alinham os vales — pálidas e ligeiramente luminosas contra o ocre quente do esqueleto peptídico — e o conjunto inteiro poderia ser engolido por um único glóbulo vermelho do sangue. Na periferia distante da folha, as corrugações ordenadas dissolvem-se num novelo caótico de alças vermelhas e laranja — regiões de turn desordenadas que parecem ter sido surpreendidas a meio de uma flutuação térmica, os seus contornos irregulares marcando a fronteira entre a arquitetura proteica e a névoa azul-acinzentada do meio aquoso. Acima da superfície, uma cintilação iónica subtil revela nuvens de contra-iões e dipólos de água em reorientação constante, tornando o horizonte ligeiramente iridescente, como se a fronteira entre a proteína e o solvente respirasse.

Você flutua no interior de uma câmara esférica com cerca de oito nanómetros de diâmetro, as paredes de GroEL curvando-se em torno de si em todos os sentidos como o interior de uma pérola oca — superfícies de resíduos hidrofílicos que irradiam uma luminescência fria de azul-branco de forma radialmente simétrica, enquanto a cúpula de GroES sela o topo em sete subunidades prateadas encaixadas como pedras polidas por um rio. No centro desta câmara de dobragem molecular, a três metros de distância em escala subjetiva, uma proteína substrato mal dobrada deriva em suspensão browniana — uma massa enovelada de fita de caramelo quente colapsada sobre si mesma, emanando um brilho âmbar orgânico que contrasta com a frieza assética das paredes que a encerram. Este é o interior do complexo chaperonina GroEL-GroES, uma máquina molecular que as células utilizam para ressgatar proteínas mal dobradas: após a encapsulação, mudanças conformacionais alostéricas dependentes de ATP remodelam as paredes internas, criando um ambiente hidrofílico isolado onde a proteína substrato pode tentar dobrar-se corretamente, isolada de interações inespecíficas com o citoplasma circundante. A névoa translúcida que espessa junto às paredes carregadas e se adelgaça em direção ao centro não é um efeito de iluminação, mas a expressão visível da hidratação diferencial e dos gradientes eletrostáticos que tornam esta câmara num laboratório molecular de precisão atómica.

Você paira a apenas cinco nanômetros acima do garfo de replicação, suspenso num meio aquoso denso e levemente luminoso onde moléculas de água vibram como fantasmas azul-esbranquiçados em constante colisão térmica — não há gravidade, apenas o bombardeio perpétuo do movimento Browniano. Diretamente abaixo, o complexo CMG helicase se impõe como uma roda de pedra quartzítica, quinze nanômetros de subunidades proteicas interligadas que forçam a abertura da dupla hélice parental, cujas colunas de fosfato azul-escuro chegam pela direita como um corredor gótico iridescente antes de se desfazerem em dois filamentos-molde: um em verde-azulado profundo e outro em âmbar-dourado fundido, ambos oscilando nas correntes Brownianas enquanto os pares de bases se separam numa franja probabilística acompanhada de um breve clarão dourado pálido libertado pela ruptura das pontes de hidrogênio. À frente no filamento líder, a DNA polimerase crava-se como um punho articulado de pedra cinza-ocre, e em cada evento de incorporação de nucleotídeo o pirofosfato é expelido numa explosão de luz laranja-branca intensa — um fenômeno termicamente equivalente à energia liberada pela hidrólise do ATP, dissipando-se em femtossegundos no halo aquoso circundante. Iões de magnésio faíscam como pontos de prata nos canais eletrostáticos do sítio ativo, enquanto proteínas de ligação de filamento simples derivam ao longe como medusas translúcidas, mantendo os moldes expostos estáveis numa forquilha que avança a cerca de mil pares de bases por segundo, copiando fielmente a informação genética num processo que nunca cessa enquanto a célula vive.

Você está de pé no interior de uma floresta de colunas helicoidais que se erguem ao redor em espirais de sentido horário, cada pilar com apenas 1,2 nanómetros de diâmetro e seis nanómetros de altura, as suas superfícies polidas como âmbar fossilizado com sulcos atómicos que captam uma luz difusa em alternâncias de ouro quente e bronze profundo. Os resíduos de leucina projetam-se para o interior como raios de carga, encaixando-se nos das hélices vizinhas ao longo da costura de coiled-coil, onde as forças de van der Waals mantêm os pilares em contacto íntimo numa zona de sombra âmbar seca, inteiramente excluída de água. Para o exterior, as cadeias laterais de lisina estendem os seus braços flexíveis em carmim saturado e as de arginina pulsam em azul elétrico, os seus grupos guanidínio irradiando halos eletrostáticos difusos para o meio aquoso envolvente, um céu cerúleo translúcido agitado pelo bombardeamento incessante de moléculas de água que colidem e se reorientam em intervalos de picossegundos, tornando o espaço aberto num aerogel luminoso que oscila entre o aquamarino e o prateado. A vinte nanómetros de distância a floresta dissolve-se numa névoa molecular suave de cinzento-azulado, as costuras das coiled-coils traçando linhas diagonais serpenteantes que desaparecem em indistinção, enquanto as colunas mais próximas impõem a sua textura hiper-real — cada oxigénio carbonílico do esqueleto peptídico uma pequena reentrância escura, cada ligação N–H um nó luminoso — vibrando com a energia térmica intrínseca que nunca cessa a esta escala.

Você está suspenso no centro exato do eixo de uma fibril amiloide, olhando diretamente para o túnel que se estende por centenas de nanômetros à sua frente, onde quatro protofilamentos se abrem em simetria perfeita como as pétalas de uma flor arquitetónica de aço — cada uma com cerca de 3 nanômetros de largura, suas paredes de folhas beta empilhadas com uma precisão absolutamente implacável de 4,7 ångströms entre cada camada, um ritmo tão regular que ecoa a frequência fundamental de uma estrutura cristalina. O núcleo entre os protofilamentos incandece em âmbar-dourado, onde cadeias laterais interdigitadas se encaixam com tolerância próxima de zero e ausência quase total de moléculas de água, formando um fecho estérico de ordem molecular que rivaliza com qualquer sólido inorgânico em termos de compactação e permanência. Na periferia de cada pétala, resíduos de glutamato surgem como afloramentos carmesins eletricamente carregados enquanto lisinas azul-cobalto estendem os seus braços alquílicos para a névoa dielétrica do solvente, criando uma fronteira eletrostática agitada que contrasta violentamente com o silêncio absolutamente seco do interior. Estas fibrilas — estruturas que emergem do colapso irreversível de proteínas outrora solúveis, associadas a doenças como Alzheimer e Parkinson — representam um dos estados mais estáveis que a matéria proteica pode atingir, uma catedral molecular congelada cuja simetria e ordem superam as de muitos cristais naturais.
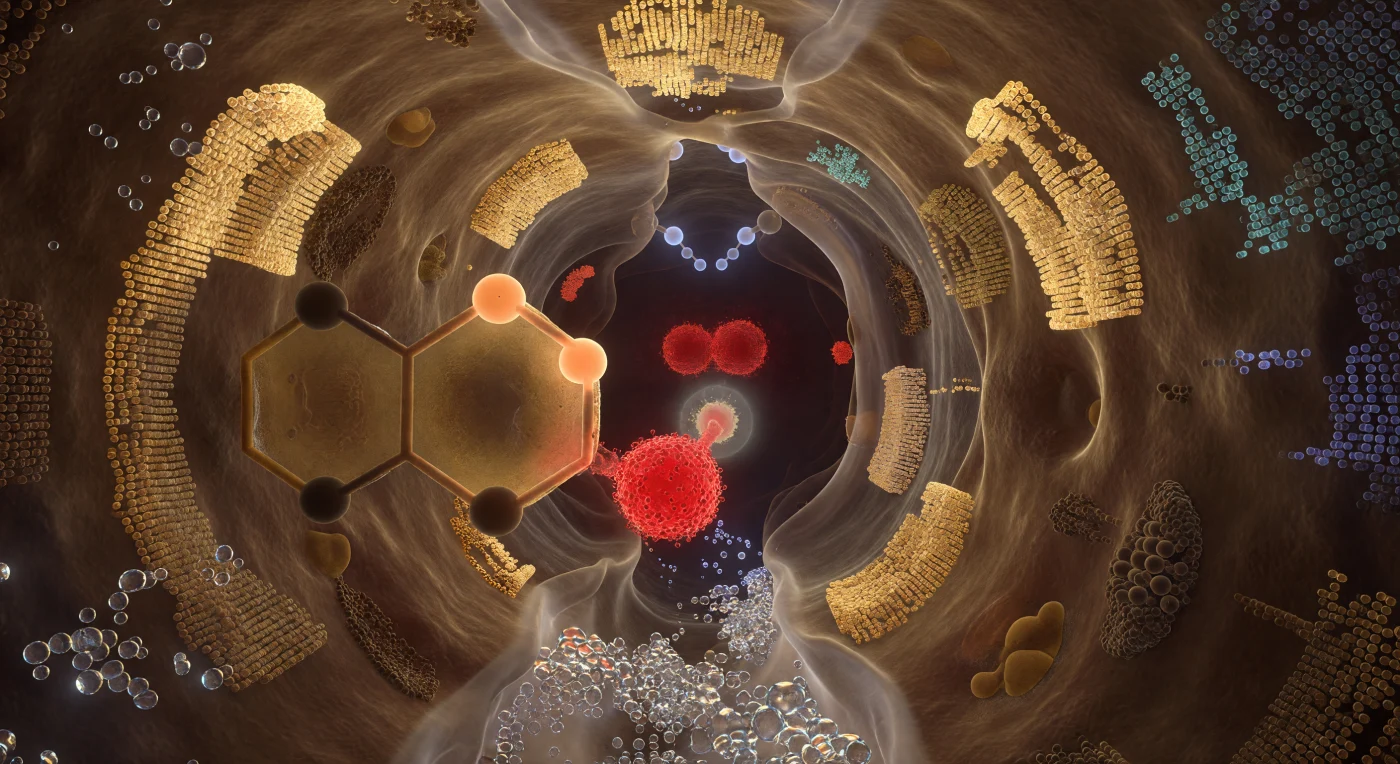
Você está de pé no interior de uma câmara não mais larga do que alguns diâmetros atômicos, curvada ao seu redor como uma catedral esculpida em âmbar vivo e sombra profunda — as paredes proteicas sobem em superfícies ondulantes de material semitranslúcido, densamente compactado pelo encaixe de van der Waals de centenas de cadeias laterais, e moléculas de água enormes reluzem na entrada como contas de vidro irregular, girando em caos térmico a centenas de metros por segundo. No centro da câmara, a tríade catalítica da serina protease domina o espaço com a gravidade de marcos geológicos: o oxigênio da Ser195 arde como brasa suspensa a apenas 1,5 Å do carbono da ligação a ser clivada, enquanto o anel imidazólico da His57 preenche seu campo de visão esquerdo como um painel de vitral âmbar, com um próton congelado a meio caminho entre seus dois nitrogênios em apricot luminoso, e o carboxilato da Asp102 pulsa ao fundo como uma névoa granada de carga negativa que ancora todo o relé como raízes na rocha. Acima do carbono carbonílico do substrato, o buraco do oxiânion abre-se como uma alcova abobadada, dois doadores N-H projetando seus hidrogênios como nódulos azul-pálido que convergem sobre o intermediário tetraédrico nascente com luz eletrostática fria e branca. Toda a câmara respira não em tempo, mas em densidade probabilística — cada superfície dissolve-se em sua última camada de angström numa névoa quântica de probabilidade eletrônica, tornando este lugar simultaneamente sólido e espectral, congelado no instante preciso em que a química acontece.

Você flutua a apenas três nanómetros do cabo de colagénio, tão perto que a sua superfície ocupa toda a largura do seu campo de visão — três cadeias polipeptídicas entrelaçadas em marfim quente, ouro pálido e bronze desbotado, torcidas numa superhélice direita de apenas 1,5 nanómetros de largura, com a paciência de uma corda trançada ao longo de eons geológicos. A cada terceira posição ao longo de cada cadeia, os anéis pirrolidínicos rígidos da prolina emergem como nós acinzentados e achatados, enquanto os grupos hidroxilo da hidroxiprolina projectam-se para o exterior como gotas de âmbar húmido, cada um retendo uma única molécula de água como orvalho num fio de seda — estas interacções não são ornamentais, são a própria razão pela qual a tripla hélice resiste à tração mecânica dos tecidos conjuntivos, dos tendões e da pele. Envolvendo o cabo como vidro fosco, a primeira camada de hidratação organiza moléculas de água em geometria tetraédrica quase perfeita, com espaçamentos de 2,8 ångströms entre pontes de hidrogénio, formando uma bainha azul-cristalina que separa a estrutura do solvente turbulento circundante. O cabo recua para centenas de nanómetros à sua frente, dissolvendo-se numa névoa aquamarina luminosa de dez mil moléculas de água por nanómetro cúbico, atravessada por nuvens âmbar de contra-iões hidratados que orbitam o esqueleto carregado — um corredor molecular que se estende, aparentemente infinito, até aos limites da visibilidade nesta escala.
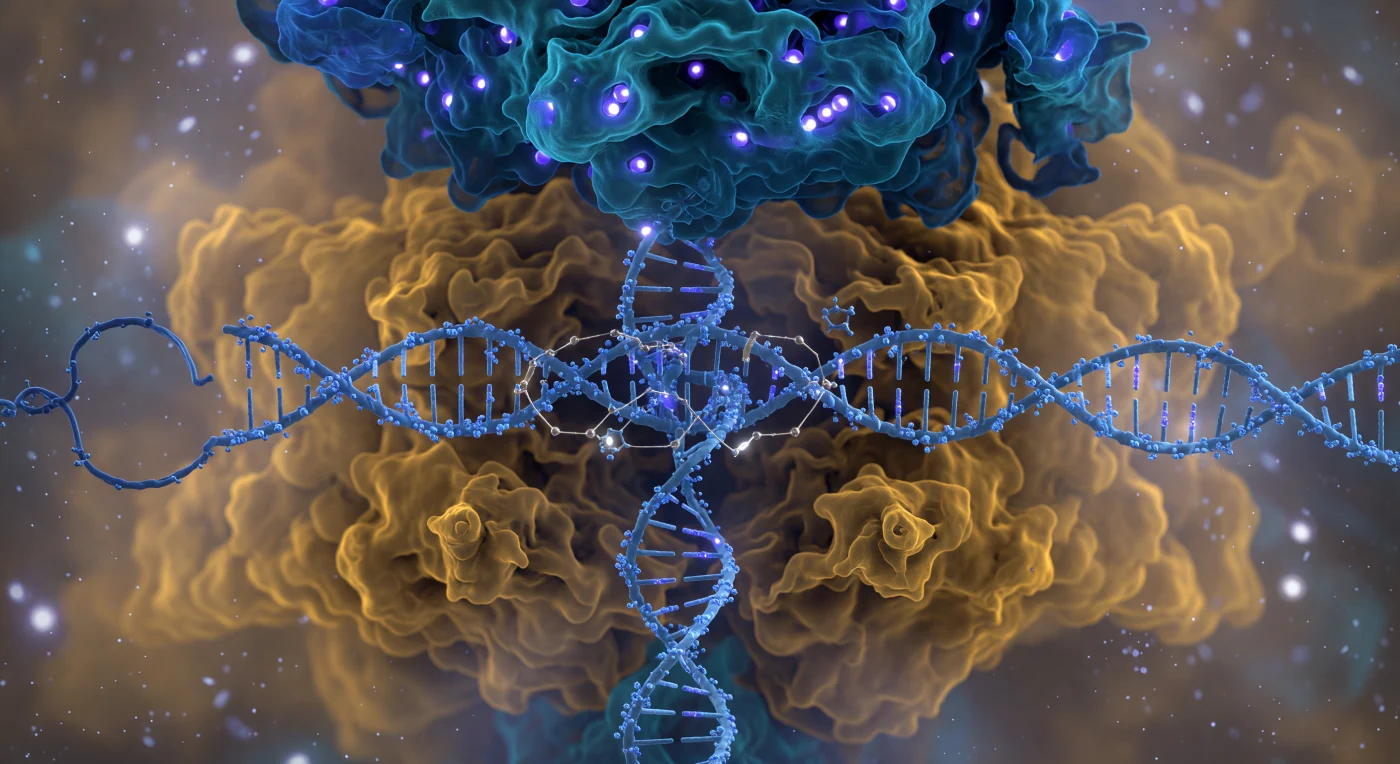
Você está suspenso a apenas cinco nanômetros da face frontal do complexo Cas9, e a proteína preenche todo o seu campo de visão como uma falésia viva — o lobo de reconhecimento acima em cobalto e azul-teal, um cofre de hélices-alfa que emite uma bioluminescência interior como se canais de ligações de hidrogênio carregassem luz própria, enquanto o lobo nuclease abaixo incha em âmbar e ocre quente, sua superfície perpetuamente difusa onde a fronteira entre proteína e solvente é negociada por nuvens de densidade eletrônica que nunca se resolvem em arestas fixas. Entre os dois lobos, a dupla hélice de DNA atravessa o espaço como uma coluna de corda torcida em azul-gelo, o esqueleto fosfato faiscando com carga negativa violeta enquanto moléculas de água se agrupam ao longo dele como satélites trêmulos que dispersam luz pálida em todas as direções — e o RNA-guia elétrico-ciano corta essa geometria como uma fibra mais irregular, seus grupos 2′-OH projetando-se como ganchos microscópicos, com três pontes R-loop já formadas à sua frente, cada par de bases unido por fios de ouro-branco que você percebe tanto como visão quanto como tensão eletrostática. À direita, o domínio de interação com o PAM insere dois resíduos de arginina na goteira menor do trinucleotídeo NGG como dedos sentindo uma fechadura, seus grupos guanidínio brilhando em cobre-laranja quente enquanto distorcem localmente a geometria da hélice, e no fundo da fenda entre os lobos, os íons de magnésio dos sítios ativos HNH e RuvC resplandecem como pontos brancos incandescentes, cada um em uma gaiola octaédrica de oxigênios coordenados — o complexo inteiro suspenso num oceano térmico de turbulência iônica constante, onde o limite entre molécula e solvente dissolve-se em névoa fosforescente de profundidade molecular infinita.

Você se encontra suspenso no coração geométrico de uma proteína intrinsecamente desordenada, imerso numa nuvem de probabilidade luminosa de cerca de oito nanómetros de diâmetro — não uma estrutura, mas uma sobreposição viva de dezenas de confórmeros da cadeia polipeptídica, cada um transparente como névoa, os seus contornos de densidade eletrónica sobrepostos em azul-branco difuso que respira e muda sem nunca se fixar. As proteínas intrinsecamente desordenadas existem precisamente neste estado de ambiguidade funcional: sem uma conformação nativa estável, o seu espaço conformacional é um ensemble contínuo amostrado em nanossegundos, onde a própria falta de ordem é biologicamente essencial para a interação com múltiplos parceiros e para a regulação celular. Uma fita âmbar aquece subitamente à sua esquerda — uma alfa-hélice emergindo do ruído estocástico, os seus oxigénios carbonílicos ligados por pontes de hidrogénio por um breve instante antes de se dissolverem novamente na névoa pérola, enquanto um aglomerado de resíduos aromáticos pulsa a amarelo-dourado como brasas sob cinza, um mínimo energético hidrofóbico transitório que se reformará noutro ponto do ensemble em microssegundos. Em toda a parte, moléculas de água de 0,28 nanómetros pressionam cada segmento exposto da cadeia numa jostling perpétua de esferas translúcidas, o seu calor térmico sendo o ruído de fundo contra o qual cada evento estrutural fugaz compete — o solvente não é aqui um cenário, mas o agente activo que esculpe, desestabiliza e remodela continuamente esta arquitectura de possibilidade.

De baixo, a visão é esmagadora: uma torre helicoidal de cor bronze-âmbar ergue-se verticalmente pela névoa azul elétrica do ambiente aquoso, os seus sulcos e cristas captando uma luz difusa que parece filtrar de muito longe acima, como se estivéssemos no sopé de uma catedral gótica de proporções impossíveis. Esta estrutura é um hairpin de RNA — uma única cadeia de ácido ribonucleico que dobra sobre si mesma, formando um duplex em hélice A com aproximadamente 2,3 nm de diâmetro e 3,5 nm de altura, mais compacta e inclinada do que a hélice B do DNA, com cada unidade de ribose-fosfato revestida por grupos 2'-OH que se projectam para o exterior como antenas de cobre aquecido, conferindo ao RNA a sua identidade química distinta. As moléculas de água manifestam-se como esferóides opalescentes em agitação incessante, os iões de sódio atravessam o campo visual como pontos prateados e brilhantes, enquanto os iões de magnésio mais pesados pairam próximos do esqueleto fosfatado em aglomerados luminosos dourado-esverdeados, todos mantidos por laços electroestáticos invisíveis que estabilizam a estrutura contra a repulsão mútua dos grupos fosfato carregados negativamente. No ápice, a tetraloop GNRA abre-se como um torreão barroco de nucleótidos não emparelhados, as suas bases de adenina empilhadas e contraventadas numa plataforma surpreendentemente rígida que capta a luz ambiente em tons dourados mais quentes. O mundo inteiro treme a ritmos de femtossegundos, mas este instante cristalizado revela a perfeição estrutural desta molécula — monumental, antiga e viva.
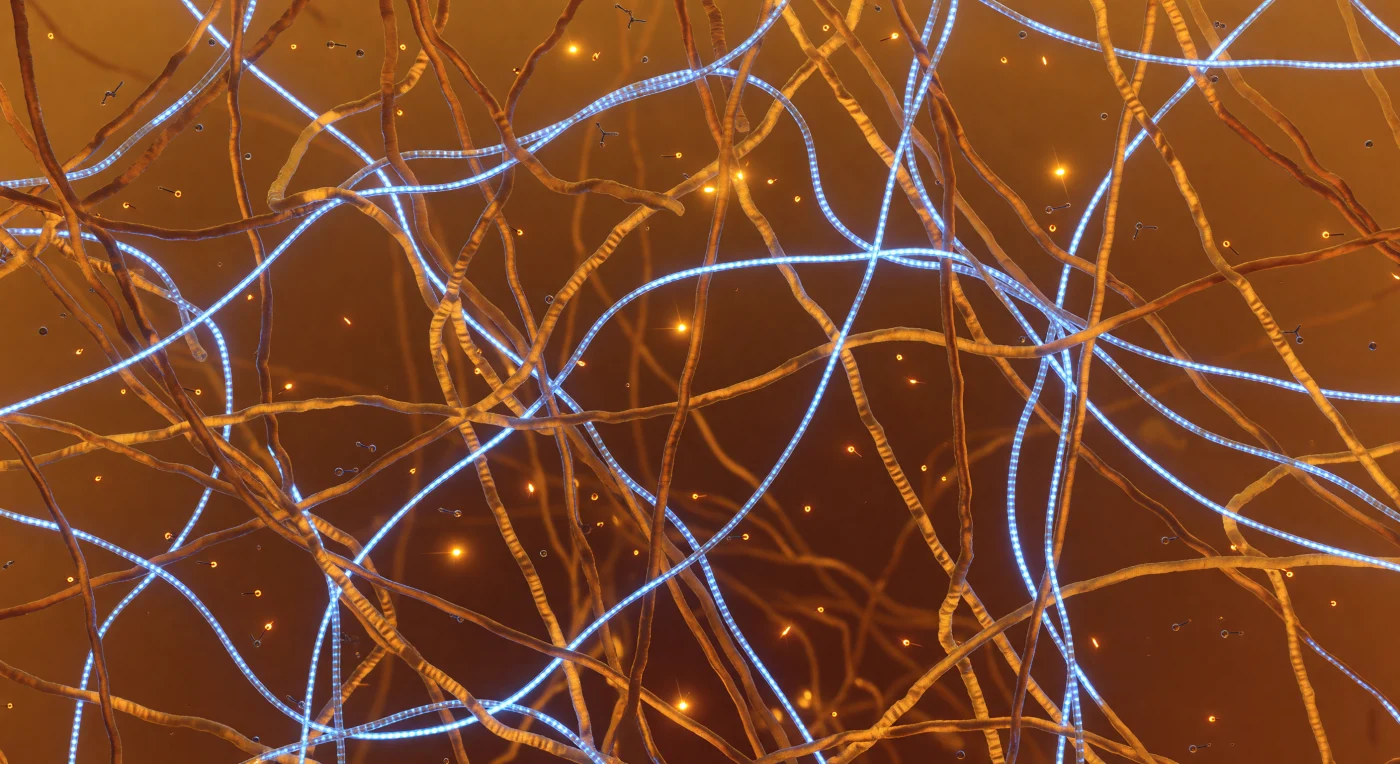
O observador encontra-se suspenso no interior de um condensado proteico-RNA, envolvido por uma malha densa e orgânica de cadeias polipeptídicas desordenadas que preenchem cada volume disponível com cordas ambarinas de dois a três nanómetros de espessura — domínios de baixa complexidade que se enovelam e entrelaçam sem geometria regular, mantidos em proximidade não por estrutura terciária estável mas pela física de separação de fase, onde flutuações de concentração locais estabilizam um estado condensado distinto da solução aquosa circundante. Onde resíduos de tirosina e arginina se aproximam em contactos cation-π transitórios, surgem faíscas de âmbar fundido que se apagam em frações de nanossegundo, cada evento uma troca electrostática efémera que contribui colectivamente para a coesão viscoelástica do condensado sem estabelecer ligações covalentes permanentes. Através desta rede atravessam filamentos de RNA com 1,5 nanómetros de diâmetro, emitindo uma luminescência azul-branca estruturada que revela o empilhamento periódico das bases a 0,34 nanómetros de intervalo, cabo a cabo de informação genética navegando por entre poros de cinco a quinze nanómetros que se abrem e fecham à escala dos microssegundos conforme a malha proteica flutua termicamente. Moléculas de ATP derivam por difusão de Brown através dessas clareiras, invisíveis à distância mas quimicamente ubíquas, enquanto o campo de profundidade colapsa a menos de oito nanómetros em todas as direções, dissolvendo-se numa névoa âmbarina uniforme que é, em si mesma, o sinal de que este interior condensado não tem fronteiras percecionáveis a partir de dentro — apenas densidade, calor eletrostático e o pulso silencioso de ligações a formar-se e a desfazer-se na escuridão molecular.
















