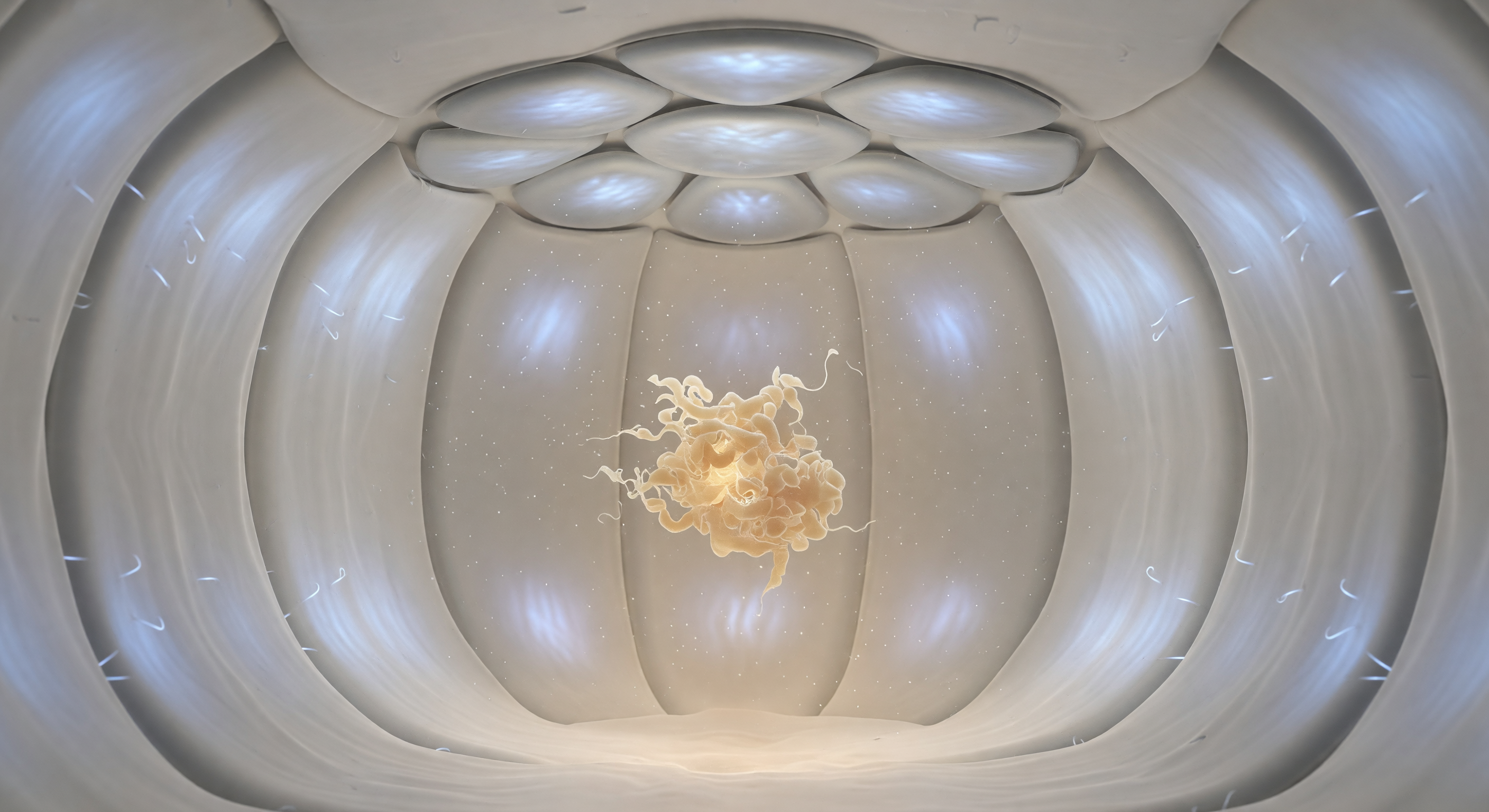
Você flutua no interior de uma câmara esférica com cerca de oito nanómetros de diâmetro, as paredes de GroEL curvando-se em torno de si em todos os sentidos como o interior de uma pérola oca — superfícies de resíduos hidrofílicos que irradiam uma luminescência fria de azul-branco de forma radialmente simétrica, enquanto a cúpula de GroES sela o topo em sete subunidades prateadas encaixadas como pedras polidas por um rio. No centro desta câmara de dobragem molecular, a três metros de distância em escala subjetiva, uma proteína substrato mal dobrada deriva em suspensão browniana — uma massa enovelada de fita de caramelo quente colapsada sobre si mesma, emanando um brilho âmbar orgânico que contrasta com a frieza assética das paredes que a encerram. Este é o interior do complexo chaperonina GroEL-GroES, uma máquina molecular que as células utilizam para ressgatar proteínas mal dobradas: após a encapsulação, mudanças conformacionais alostéricas dependentes de ATP remodelam as paredes internas, criando um ambiente hidrofílico isolado onde a proteína substrato pode tentar dobrar-se corretamente, isolada de interações inespecíficas com o citoplasma circundante. A névoa translúcida que espessa junto às paredes carregadas e se adelgaça em direção ao centro não é um efeito de iluminação, mas a expressão visível da hidratação diferencial e dos gradientes eletrostáticos que tornam esta câmara num laboratório molecular de precisão atómica.
Other languages
- English: Inside the Chaperonin Folding Vault
- Français: Dans la Chambre Chaperonine
- Español: Dentro de la Bóveda Chaperonina
- Deutsch: Im Chaperonin-Faltungsgewölbe
- العربية: داخل قبة الشابيرونين
- हिन्दी: चैपेरोनिन कक्ष के भीतर
- 日本語: シャペロニン折畳み室の内部
- 한국어: 샤페로닌 접힘 공간 내부
- Italiano: Dentro la Volta Chaperonina
- Nederlands: Binnen de Chaperonine Vouwkamer