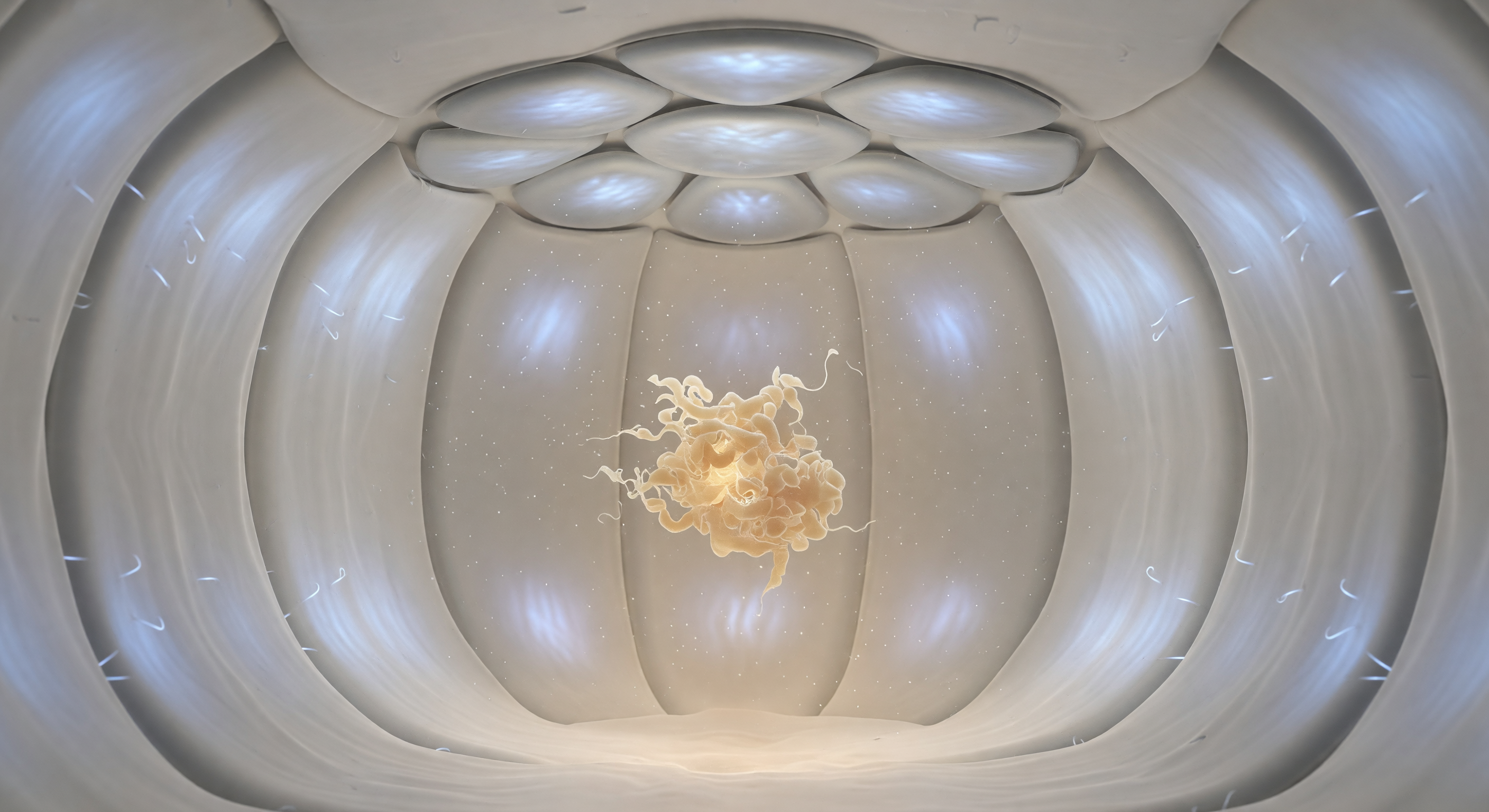
Du schwebst im Innern eines abgeschlossenen molekularen Gewölbes von kaum acht Nanometern Durchmesser – einer kugelförmigen Kammer, die der Chaperon-Komplex GroEL-GroES bildet, um fehlgefaltete Proteine vor dem zellulären Chaos zu schützen und ihnen Raum zur Neuordnung zu geben. Die Wände des GroEL-Zylinders wölben sich gleichmäßig um dich, ihre hydrophilen Innenflächen schimmern in einem kühlen Blau-Weiß, das keine erkennbare Quelle hat, sondern wie eine in das Material selbst eingeschriebene Lumineszenz wirkt; über dir schließt der GroES-Deckel die Kammer mit sieben silbergrauen Untereinheiten, die sich wie polierte Flusssteine ineinanderfügen und das Gewölbe hermetisch versiegeln. Im Zentrum dieser antiseptischen Stille treibt das Substratprotein in langsamer Brownscher Bewegung – ein verknäultes, karamellfarbenes Gebilde von drei Nanometern Durchmesser, dessen Randzone in einem probabilistischen Elektronendichteschleier ausfranst, statt eine scharfe Oberfläche zu bilden. Der Chaperonin-Zyklus, angetrieben durch ATP-Hydrolyse, wird diesen Raum nach Millisekunden wieder öffnen und das Protein – nun hoffentlich korrekt gefaltet oder für einen neuen Versuch freigegeben – in das Cytoplasma entlassen; vorerst aber herrscht hier eine geladene, drückende Stille, in der allein die Wärme des glimmenden Proteins gegen die klinische Kälte der Kammerwände steht.
Other languages
- English: Inside the Chaperonin Folding Vault
- Français: Dans la Chambre Chaperonine
- Español: Dentro de la Bóveda Chaperonina
- Português: No Interior da Câmara Chaperonina
- العربية: داخل قبة الشابيرونين
- हिन्दी: चैपेरोनिन कक्ष के भीतर
- 日本語: シャペロニン折畳み室の内部
- 한국어: 샤페로닌 접힘 공간 내부
- Italiano: Dentro la Volta Chaperonina
- Nederlands: Binnen de Chaperonine Vouwkamer