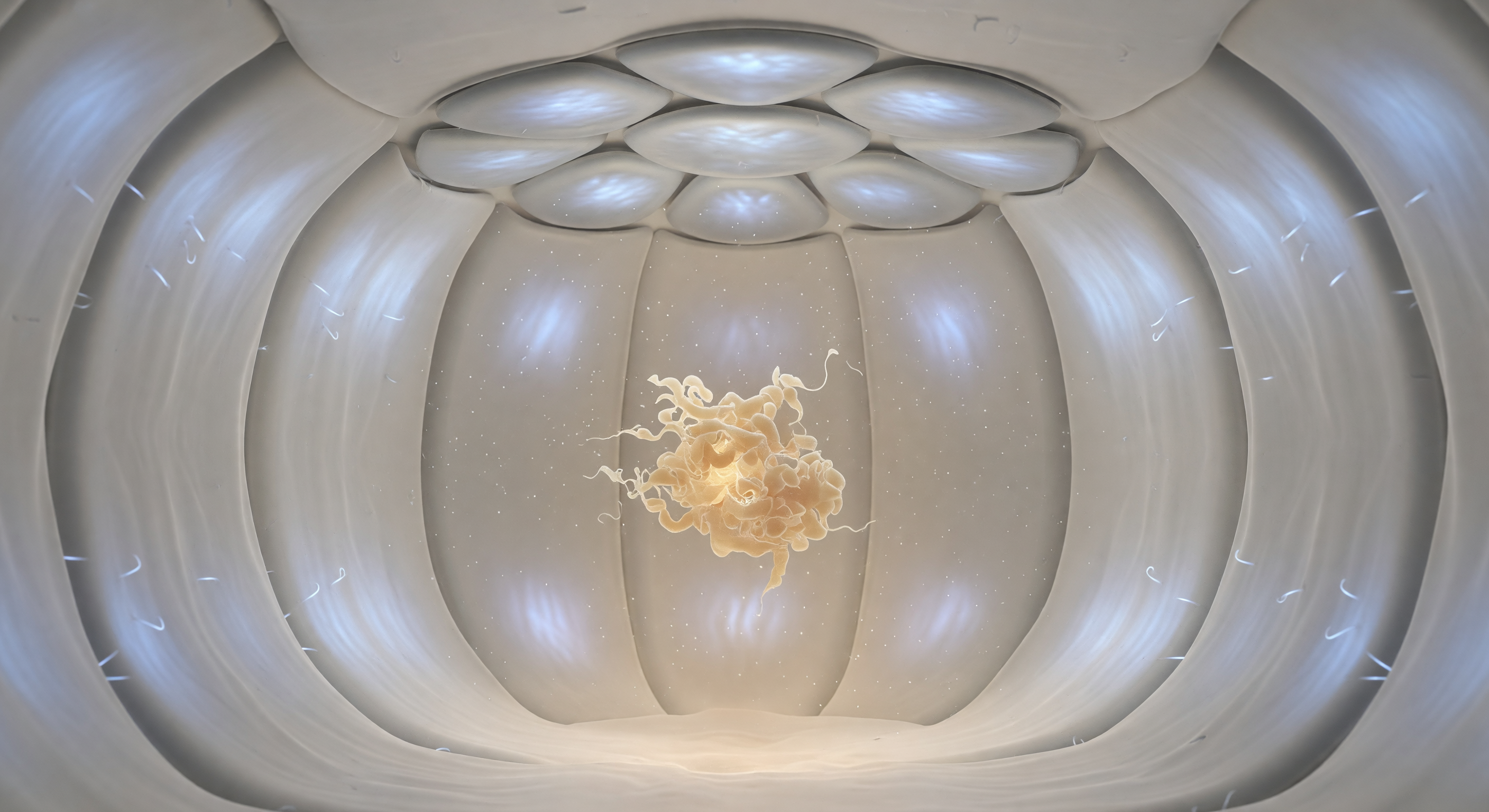
Flotas suspendido en el interior de una cámara esférica de apenas ocho nanómetros de diámetro, una bóveda molecular sellada cuyos muros curvos de GroEL se elevan a tu alrededor como el interior de una perla hueca, revestidos de residuos hidrofílicos que emiten una luminiscencia fría azul-blanca sin origen aparente, como si la materia misma respirara luz. Sobre tu cabeza, siete subunidades de GroES encajan entre sí formando una cúpula de plata mate —piedras pulidas por el río, arquitectura de precisión atómica— que sella herméticamente el espacio y convierte este recinto en una de las máquinas de plegamiento más sofisticadas que ha producido la evolución: el complejo chaperonínico GroEL-GroES, cuya función es aislar proteínas mal plegadas del caos citoplásmico y ofrecerles, a costa de hidrólisis de ATP, un entorno controlado donde los contactos hidrofóbicos aberrantes no puedan interferir con el camino hacia la conformación nativa. A tres metros de distancia en escala subjetiva —en realidad apenas un nanómetro y medio— deriva una proteína sustrato mal plegada, una masa enredada de color ámbar cálido, suave y arrugada como una cinta de caramelo colapsada sobre sí misma, cuya superficie no es un límite definido sino una frontera probabilística de densidad electrónica que se deshilacha en la niebla acuosa circundante. La quietud de este lugar es absoluta y sin embargo radicalmente dinámica: en cada instante, miles de moléculas de agua que no puedes resolver individualmente bombardean tanto las paredes como el sustrato a velocidades de centenares de metros por segundo, agitando ese ovillo luminoso en una suspensión browniana silenciosa, mientras el recinto aguarda el momento en que la proteína encontrará, en este refugio de precisión molecular, la forma correcta de existir.
Other languages
- English: Inside the Chaperonin Folding Vault
- Français: Dans la Chambre Chaperonine
- Português: No Interior da Câmara Chaperonina
- Deutsch: Im Chaperonin-Faltungsgewölbe
- العربية: داخل قبة الشابيرونين
- हिन्दी: चैपेरोनिन कक्ष के भीतर
- 日本語: シャペロニン折畳み室の内部
- 한국어: 샤페로닌 접힘 공간 내부
- Italiano: Dentro la Volta Chaperonina
- Nederlands: Binnen de Chaperonine Vouwkamer