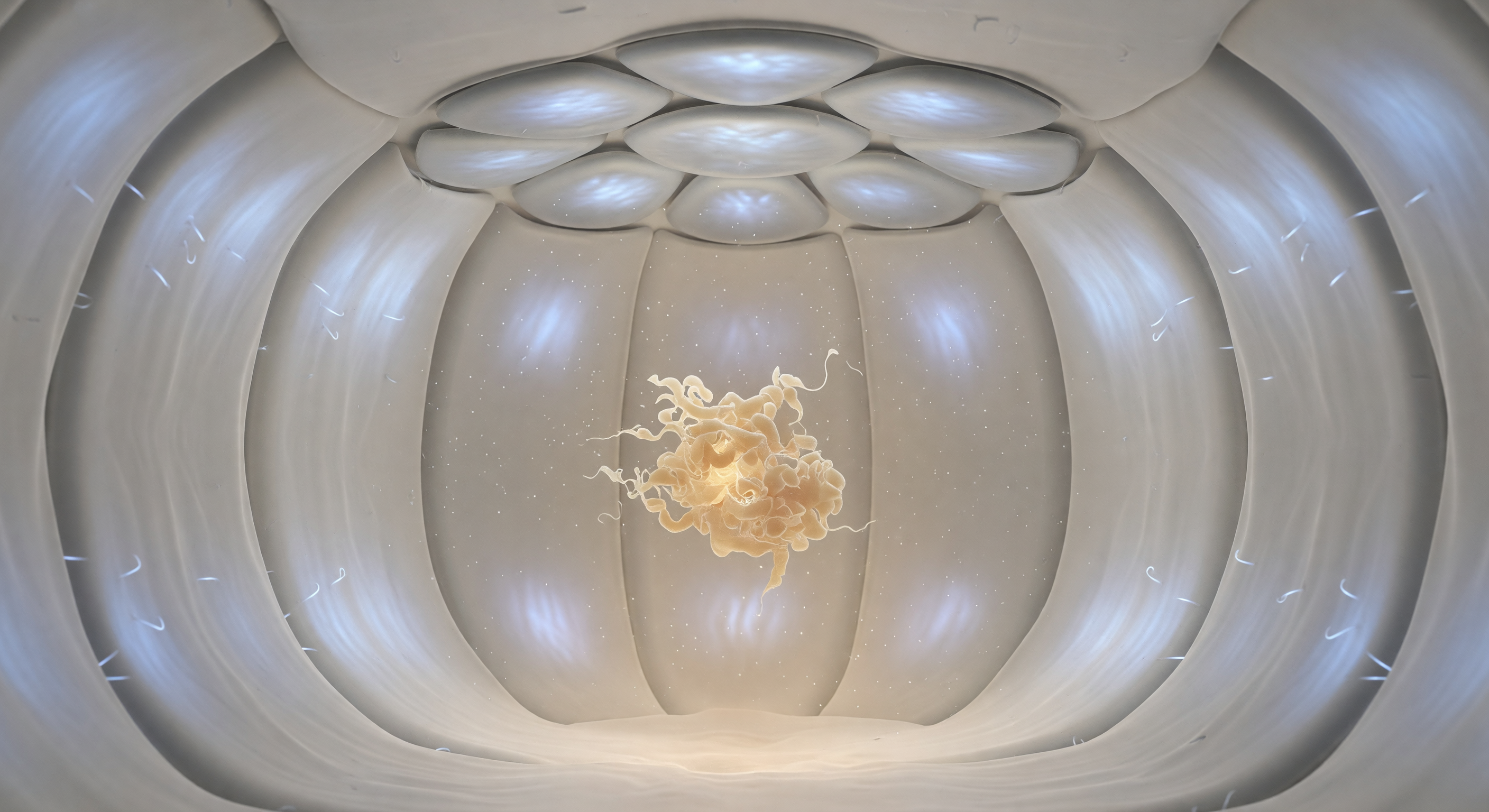
Vous flottez à l'intérieur d'une enceinte sphérique de huit nanomètres de diamètre, dont les parois incurvées de gris nacré émettent une lueur bleue-blanche uniforme — la surface intérieure du complexe chaperonine GroEL, dont les résidus hydrophiles tapissent chaque segment du tonneau cylindrique comme un revêtement de velours moléculaire. Au-dessus de vous, le couvercle formé par les sept sous-unités de GroES s'assemble en une voûte de lobes argent-étain ajustés avec une précision architecturale, scellant hermétiquement cette chambre de repliement où règne un silence thermodynamique trompeur : en réalité, des milliers de molécules d'eau bombardent chaque surface à des vitesses de plusieurs centaines de mètres par seconde, générant cette agitation brownienne perpétuelle qui maintient tout en suspension. Au centre de la chambre, à trois mètres en échelle subjective, dérive une protéine mal repliée — une masse enchevêtrée de rubans beige-ambre effondrés sur eux-mêmes, ses boucles désordonnées se dissolvant en une brume électronique probabiliste à ses marges. C'est ici, dans cet espace confiné et chimiquement reconfigurable, que la cellule consomme de l'ATP pour isoler les chaînes polypeptidiques des interactions parasites et leur offrir, dans l'équanimité de ce petit monde fermé, une seconde chance de trouver leur conformation native.
Autres langues
- English: Inside the Chaperonin Folding Vault
- Español: Dentro de la Bóveda Chaperonina
- Português: No Interior da Câmara Chaperonina
- Deutsch: Im Chaperonin-Faltungsgewölbe
- العربية: داخل قبة الشابيرونين
- हिन्दी: चैपेरोनिन कक्ष के भीतर
- 日本語: シャペロニン折畳み室の内部
- 한국어: 샤페로닌 접힘 공간 내부
- Italiano: Dentro la Volta Chaperonina
- Nederlands: Binnen de Chaperonine Vouwkamer