
Vous existez au cœur géométrique d'une protéine globulaire, comprimé dans une obscurité moléculaire quasi absolue, entouré de toutes parts par les chaînes latérales hydrophobes de leucines, de valines et de phénylalanines imbriquées à plus de soixante-quinze pour cent de densité d'empilement — un taux de remplissage comparable à celui d'un empilement de sphères cristallines, atteint ici par la seule pression de l'évolution. Les surfaces de contact entre nuages électroniques se manifestent comme des halos phosphorescents d'un ivoire cendré, séparés par l'épaisseur d'une répulsion quantique, tandis que les anneaux aromatiques des phénylalanines tranchent l'espace en disques d'obsidienne aux ombres dures et absolues, car il n'existe ici aucune lumière diffuse, seulement la lueur intime des densités électroniques au contact. Deux ou trois atomes de soufre appartenant à des méthionines dispersées dans la matrice renvoient cette luminescence résiduelle sous forme d'un éclat jaune-soufre chaud, seule couleur chaude dans un monde autrement achromatique, comme des braises entrevues à travers la pierre. À la périphérie du cœur, à une quinzaine de diamètres atomiques dans toutes les directions, un bleu-vert aqueux froid filtre entre les éléments de structure secondaire — signature lointaine du solvant et de ses dipôles d'eau en perpétuel mouvement, signal d'un monde extérieur que cette caverne protéique scelle depuis le repliement initial, maintenue dans cet équilibre tectonique par des forces de van der Waals ne dépassant pas quelques fractions de kilojoule par mole, mais collectivement assez puissantes pour que les vibrations thermiques à trente-sept degrés ne se manifestent ici que comme un lent frémissement sub-angström pulsant à travers chaque surface en contact.

Dans les profondeurs de ce corridor biochimique, le regard plonge le long d'un couloir cathédral de quelques nanomètres de diamètre, dont les parois d'ARN ribosomique — ocre, bronze brûlé, nervurées de plateformes nucléotidiques empilées comme des strates de schiste — se resserrent en une constriction si étroite que les nuages électroniques des piliers opposés se frôlent en un halo violet pâle. Depuis le foyer catalytique dix nanomètres en avant, un flux de lumière bleu-blanc trahit le travail incessant du centre peptidyl-transférase, là où chaque codon de l'ARN messager est traduit en quelques centaines de millisecondes en un maillon supplémentaire de la chaîne naissante. Cette chaîne polypeptidique — vert lime et ambre chaud, luisante comme de la cire — se déroule vers l'observateur en effleurant de ses groupements hydrophobes les parois d'ARNr, chaque contact un murmure de van der Waals aussitôt dissous par l'agitation thermique. Les molécules d'eau qui saturent cet espace ne se voient pas tant qu'elles ne se sentent : un brouillard de percussions incessantes qui fait trembler chaque surface, rappelant que les limites ici ne sont pas des murs mais des gradients probabilistes négociés entre molécule et solvant. C'est un lieu de naissance — chaud, chargé électrostatiquement, rigoureusement ordonné — où la première existence d'une protéine se déroule dans une lumière ambrée et un feu catalytique bleu.

Vous volez à l'intérieur du grand sillon de la double hélice d'ADN en conformation B, un couloir hélicoïdal de seulement 2,2 nanomètres de largeur dont les parois s'incurvent en une spirale majestueuse vers la droite, tapissées de rambardes phosphate-sucre orange translucides qui ondulent en tresse covalente rhythmique. Le sol du sillon forme une mosaïque de plateformes aromatiques empilées — ambre chaud de l'adénine, vert sauge de la thymine, sarcelle profonde de la guanine, bleu ciel de la cytosine — séparées chacune de 0,34 nanomètre, leurs nuages d'électrons π se chevauchant en une interférence violet-indigo translucide là où la densité quantique remonte entre les tiers. Au-delà des bords chargés du sillon, des cations magnésium brillent comme des étincelles blanc-bleu intenses, ceints de couches concentriques de molécules d'eau orientées, tandis que des ions sodium dérivent en halos dorés pâles dans un brouillard électrostatique dont la couche de Debye diffuse une lumière laiteuse et ondulante, semblable à une aurore lente. Le tout vibre d'un tremblement thermique continu : des sphéroïdes d'eau de 0,28 nanomètre percutent sans relâche les plateformes de bases, chaque impact un éclair blanc aussitôt englouti par la lueur aqueuse ambiante, les surfaces elles-mêmes refusant toute netteté franche, se dissolvant en une fourrure électrostatique probabiliste que l'on ressentirait comme une pression bien avant tout contact.

Au seuil de cette interface, deux falaises moléculaires se font face dans un canyon dont les parois ne sont séparées que par quelques diamètres de molécules d'eau — une gorge intime où la matière n'est pas solide mais probabiliste, des nuages de densité électronique se frôlant dans une lueur ambiante bleue-cyan qui traverse le solvant aqueux comme une lumière de fond océanique. Les six boucles CDR du fragment Fab surgissent comme les doigts d'une main colossale se refermant sur une promontoire convexe : la boucle H3, dorée comme du bronze brûlé, décrit un arc souverain au-dessus de la L3 teintée de sarcelle, leurs reliefs moléculaires révélant des volumes de chaînes latérales, des anneaux aromatiques en relief, des crevasses où se nichent les dernières molécules d'eau avant expulsion — éclairs opalescents projetés dans le solvant environnant comme des fragments de miroir brisé. Cette zone de contact de cinq sur six nanomètres est le théâtre d'une reconnaissance stéréochimique façonnée par des millions d'années de sélection immunitaire : des ponts hydrogène cyan s'allument un à un à travers l'espace résiduel en Ångströms, fils lumineux de partage électronique tissant une complémentarité de surface aussi précise qu'une empreinte continentale. On perçoit viscéralement l'échelle dans cette collision au ralenti — non pas un choc brutal, mais une apposition lente et inéluctable de deux mondes de densité électronique, liant spécificité et entropie dans le crépuscule ambré de cette étreinte moléculaire.
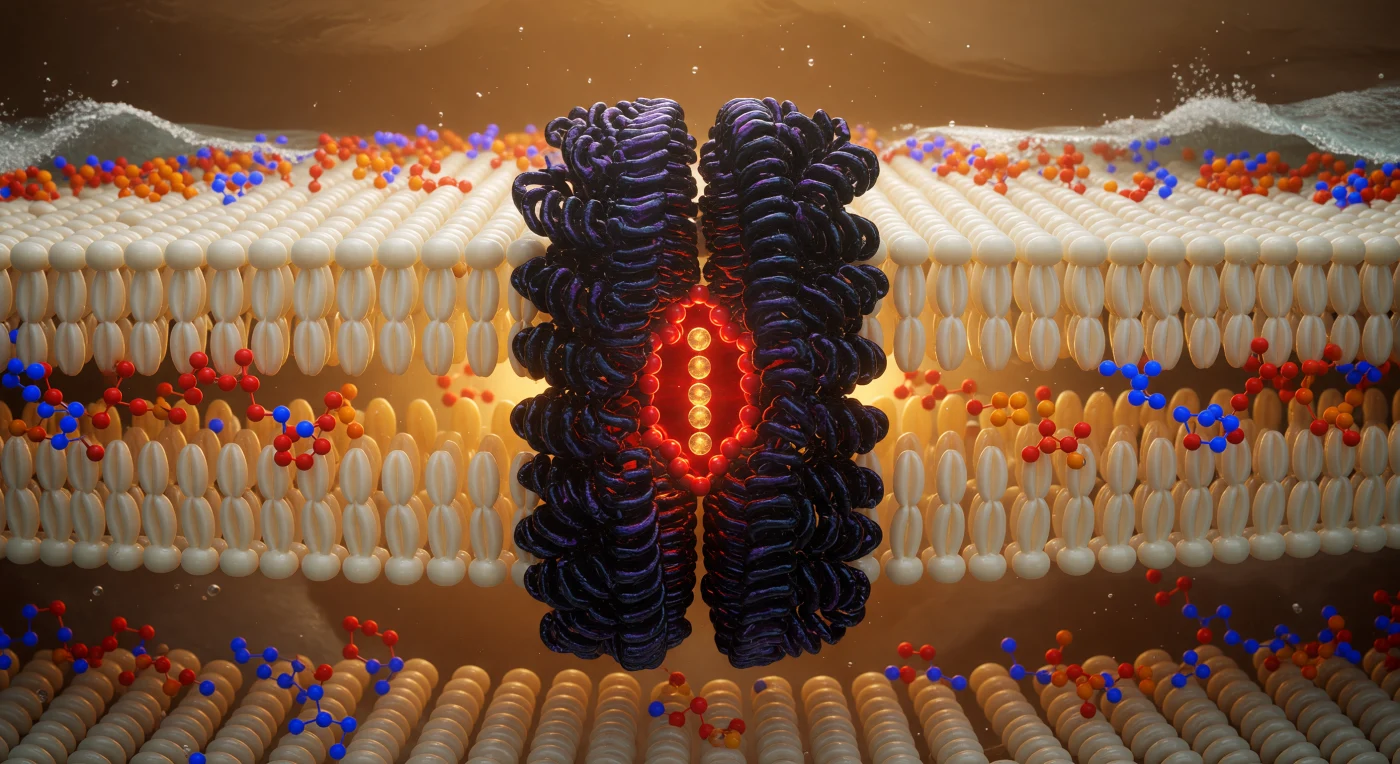
Vous flottez au cœur géométrique d'une bicouche phospholipidique, suspendu dans le plan hydrophobe à égale distance des deux feuillets, entouré d'une forêt dense de chaînes carbonées ivoire et or pâle dont les surfaces de van der Waals se pressent les unes contre les autres comme des tiges de corail poli, baignées d'un halo électrostatique diffus qui teinte l'intérieur hydrophobe d'une brume ambrée et incandescente, vibrante du mouvement thermique perpétuel. Devant vous, le canal potassique s'élève comme un monolithe de basalte violet-noir à travers le plan membranaire — une colonne à symétrie quaternaire d'environ 3,5 nm de diamètre dont les hélices transmembranaires, striées de crêtes iridescentes violet et ardoise, s'imbriquent mécaniquement avec les queues lipidiques environnantes comme de la pierre volcanique fusionnée dans une végétation dense, formant l'interface protéine-membrane décrite par les travaux cristallographiques de MacKinnon sur KcsA. Au cœur de cette colonne, le filtre de sélectivité brûle d'une luminescence rouge-orange concentrée : des atomes d'oxygène carbonyle coordonnent en file indienne quatre ions potassium dont les nuages électroniques rougeoyants dépouillent ces cations de leur hydratation avec une précision stéréochimique absolue, discriminant K⁺ de Na⁺ par un ajustement géométrique à l'angström près. Au-dessus et en dessous, les horizons des têtes polaires glycérophosphocholines pulsent de couleurs atomiques saturées — phosphores orange cadmium, azotes cobalt électrique, oxygènes esters cramoisis — tandis qu'au-delà de ces rivages chargés, l'eau extracellulaire et intracellulaire se devine comme une écume argentée turbulente, rappelant que cette membrane n'est pas une simple barrière passive mais un milieu anisotrope vivant dont l'épaisseur totale d'environ 4 nm régit la perméabilité ionique, le potentiel de repos neuronal, et la transduction du signal dans l'ensemble du vivant.

Suspendu à quelques nanomètres au-dessus de la surface, le regard balaye une plaine ondulée qui s'étend jusqu'à chaque horizon — une feuille bêta antiparallèle révélée dans son intimité atomique, ses crêtes de parchemin ambré alternant de direction avec la précision géométrique d'un dallage ancien, leurs surfaces voilées du halo translucide des nuages de densité électronique plutôt que d'une matière dure. Des oxygènes carbonyle rouge cerise sertissent chaque crête comme des grenats polis incrustés dans de l'os ancien, tandis que des pointes amide blanc nacré tapissent les vallées, pâles et légèrement lumineuses contre l'ocre chaud de l'échafaudage peptidique. Entre les brins adjacents, des ponts hydrogène cyan — filaments fantomatiques de probabilité électrostatique, distants de seulement 2,9 ångströms — lacent latéralement la plaine entière comme un haubert moléculaire, chacun portant une lueur aquamarine douce là où les nuages électroniques du donneur et de l'accepteur se recouvrent. La lumière, volumétrique et sans source directionnelle, est celle du rayonnement thermique diffus d'un milieu aqueux, une lueur blanche froide qui accroche les sommets des crêtes et laisse les vallées dans une ombre ambrée tiède, pendant qu'au loin les corrugations ordonnées se dissolvent en boucles de connexion rouges et orange — régions de turn désordonnées, figées en pleine fluctuation, leurs surfaces hérissées de chaînes latérales comme la bordure effondrée d'une falaise. Au-delà, la brume bleu-gris du solvant aqueux estompe la frontière entre la protéine structurée et le milieu bulk, faisant scintiller légèrement l'horizon comme si la limite entre ordre et chaos respirait.

Vous flottez à l'intérieur d'une enceinte sphérique de huit nanomètres de diamètre, dont les parois incurvées de gris nacré émettent une lueur bleue-blanche uniforme — la surface intérieure du complexe chaperonine GroEL, dont les résidus hydrophiles tapissent chaque segment du tonneau cylindrique comme un revêtement de velours moléculaire. Au-dessus de vous, le couvercle formé par les sept sous-unités de GroES s'assemble en une voûte de lobes argent-étain ajustés avec une précision architecturale, scellant hermétiquement cette chambre de repliement où règne un silence thermodynamique trompeur : en réalité, des milliers de molécules d'eau bombardent chaque surface à des vitesses de plusieurs centaines de mètres par seconde, générant cette agitation brownienne perpétuelle qui maintient tout en suspension. Au centre de la chambre, à trois mètres en échelle subjective, dérive une protéine mal repliée — une masse enchevêtrée de rubans beige-ambre effondrés sur eux-mêmes, ses boucles désordonnées se dissolvant en une brume électronique probabiliste à ses marges. C'est ici, dans cet espace confiné et chimiquement reconfigurable, que la cellule consomme de l'ATP pour isoler les chaînes polypeptidiques des interactions parasites et leur offrir, dans l'équanimité de ce petit monde fermé, une seconde chance de trouver leur conformation native.

Suspendu à cinq nanomètres au-dessus de la fourche de réplication, on plonge le regard dans une mécanique moléculaire d'une précision vertigineuse : l'hexamère CMG, massif anneau de quartzite gris de quinze nanomètres de diamètre, enjambe la jonction où la double hélice parentale — architecture navale profonde, colonnes phosphatées d'un bleu nuit irisé — se dénoue en deux fils sinueux, l'un d'un sarcelle phosphorescent, l'autre d'un ambre fondu qui vacille sous l'agitation brownienne des bases exposées. En avant, la ADN polymérase enserre le brin naissant comme un poing articulé de pierre ocre-grise, et à chaque incorporation de nucléotide, un bref embrasement orange-blanc éclate à son site actif — énergie du pyrophosphate libéré, aussitôt dissoute dans le halo aqueux ambiant — tandis que des ions magnésium filent en éclairs d'argent le long de canaux électrostatiques invisibles. Le milieu lui-même n'est pas du vide mais un gel tiède et luminescent, traversé de dipôles d'eau fugaces et de protéines de liaison aux brins simples dérivant telles des méduses translucides, rappelant que chaque liaison hydrogène rompue, chaque base séparée de sa paire, est une décision probabiliste plutôt qu'un acte mécanique tranché. À cette échelle, la frontière entre structure et dynamique n'existe plus : tout vibre, tout respire, et la réplication de l'ADN se révèle moins une copie qu'une perpétuelle négociation thermodynamique à la lisière du chaos.

Depuis le sol de cette forêt moléculaire, le regard remonte le long de colonnes spiralées qui s'élèvent en symétrie rythmique, chaque pilier un hélice alpha droitière dont la surface torsadée alterne entre ambre chaud et or profond, les résidus leucine hydrophobes s'enchevêtrant comme des engrenages de bronze à la jointure des coiled-coils tandis que les chaînes latérales de lysine cramoisi et d'arginine bleu électrique irradient vers l'extérieur dans le solvant aqueux. Ces structures ne sont pas des colonnes rigides mais des nuages de densité électronique en vibration thermique constante, leurs surfaces iridescentes témoignant de l'agitation picoseconde des liaisons peptidiques — chaque carbonyle du squelette un creux sombre le long du ruban hélicoïdal, chaque site N–H un nœud lumineux minuscule. L'espace entre les paires de coiled-coils est à peine assez large pour laisser passer quelques molécules d'eau, et le long des seams hydrophobes s'étend une zone d'ambre dense et sec d'où le solvant est exclu par des forces de van der Waals, créant une proximité quasi gravitationnelle entre les colonnes. Au-dessus, le ciel aqueux n'est pas bleu au sens terrestre — c'est un milieu céruléen lumineux, traversé par la micro-turbulence incessante de molécules d'eau de 0,28 nm se réorientant à une vitesse vertigineuse, leurs réseaux de liaisons hydrogène scintillant en filaments gossamer qui naissent et disparaissent en quelques picosecondes. À vingt nanomètres dans la profondeur brumeuse, les rangs successifs d'hélices se fondent en gris-bleu doux, leurs coutures leucine traçant un motif en chevrons qui s'évanouit à la limite de la visibilité moléculaire.

Vous flottez au cœur même de l'axe fibrillaire, suspendu au centre exact d'une croix formée par quatre protofilaments qui s'écartent de vous en symétrie radiale parfaite — quatre voûtes gothiques de feuillets bêta empilés à 4,7 ångströms d'intervalle, un rythme cristallin si inexorable qu'il ressemble à la pulsation d'un orgue de pierre bleue et froide. Entre ces ailes architecturales, le cœur ambre de la fermeture stérique rayonne d'une incandescence miellée : les chaînes latérales interdigitées s'y engrènent avec une précision d'horlogerie, leurs surfaces de van der Waals en contact quasi parfait, dans une sécheresse absolue d'où toute molécule d'eau a été expulsée. Ces fibrilles amyloïdes, qui émergent de l'effondrement irréversible de protéines autrefois solubles, stabilisent leur architecture grâce aux liaisons hydrogène croisées entre brins bêta parallèles ou antiparallèles — une géométrie que l'on retrouve dans les dépôts pathologiques associés à des maladies comme Alzheimer ou Parkinson. À la périphérie de chaque pétale, les résidus glutamate flambent en rouge carmin et les lysines ponctuent l'espace de touches cobalt électrique, leurs charges opposées projetées dans un halo de molécules d'eau orientées qui adoucit les contours de cette cathédrale moléculaire d'une permanence presque géologique.
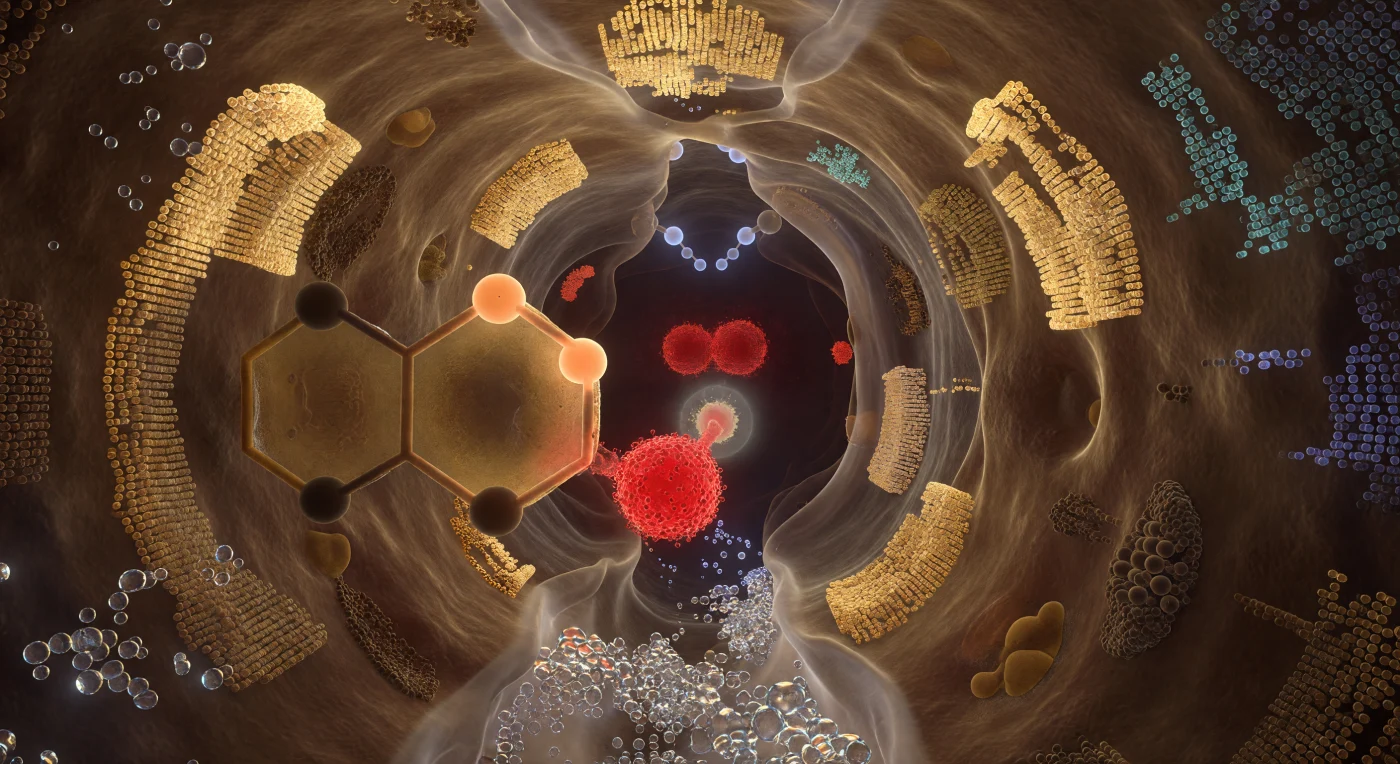
Vous vous trouvez suspendu à l'intérieur d'une poche de deux nanomètres à peine, creusée dans la masse compacte d'une sérine protéase, là où la chimie du vivant s'accomplit en une fraction de microseconde. La triade catalytique vous entoure comme trois piliers d'une crypte moléculaire : l'oxygène de la Ser195 brûle en avant-plan comme une braise rouge dont la densité électronique se tend vers la liaison scissile du substrat, séparée d'elle par un intervalle d'à peine 1,5 ångström, tandis que l'anneau imidazole de His57 se déploie sur votre gauche en un vaste panneau d'ambre translucide, le proton transféré figé à mi-chemin entre ses deux azotes dans une lueur abricot. Derrière eux, Asp102 ancre l'ensemble comme une racine dans la roche, ses deux oxygènes carboxylate pulsant d'une charge négative qui stabilise tout le relais par résonance électrostatique — c'est le mécanisme de la catalyse acido-basique générale, précis comme une mécanique d'horlogerie quantique. Au-dessus du carbone carbonyle du substrat, les deux donneurs N–H du trou oxyanionique projettent une lumière froide et blanche sur l'intermédiaire tétraédrique en formation, maintenant la charge négative transitoire qui rendrait la réaction impossible sans eux. L'ensemble de la chambre respire non pas dans le temps, mais dans la densité de probabilité électronique — chaque surface se dissout à son angström extérieur en un brouillard quantique qui rappelle que la frontière entre le solide et le spectral, ici, n'existe tout simplement pas.

Vous flottez à trois nanomètres du câble, si près que sa surface occupe toute la largeur de votre champ de vision : trois chaînes polypeptidiques — ivoire chaud, or pâle, et beige solaire — s'enroulent en une superélice droite lente, à peine 1,5 nanomètre de diamètre, tressées avec la patience d'un cordage forgé sur des temps géologiques. Les anneaux pyrrolidine rigides de la proline scandent chaque troisième position le long de chaque brin comme des jointures grises légèrement enfoncées dans le sillon de l'hélice, tandis que les groupes hydroxyle de l'hydroxyproline projettent vers l'extérieur de petits lobes ambrés chargés partiellement, chacun retenant une molécule d'eau comme une perle de rosée sur un fil d'araignée. La stabilité remarquable de ce câble ne doit rien à la chance : c'est la séquence répétée Gly–X–Y, avec la glycine minuscule nichée à l'intérieur de chaque tour, qui contraint les trois chaînes dans une étreinte de liaisons hydrogène inter-chaînes, conférant au collagène sa résistance mécanique extraordinaire — comparable, à section égale, à celle de l'acier. Autour du câble, une gaine cristalline bleu-blanc d'eau structurée en géométrie tétraédrique presque parfaite l'enveloppe comme du verre dépoli, ses dipôles ordonnés scintillant à 2,8 ångströms d'espacement, avant que cette architecture se dissolve dans le brouillard aquamarine de l'eau bulk, où des nuages de contre-ions ambrés dérivent dans la pénombre électrostatique du squelette chargé. Le câble s'éloigne devant vous sur des centaines de nanomètres, corridor lumineux qui se perd dans une brume moléculaire infinie — c'est le collagène tel qu'il existe réellement, une molécule longue de plusieurs micromètres, constituant fondamental des tendons, de la peau et des os, dont vous ne percevez ici qu'un fragment imperceptible.
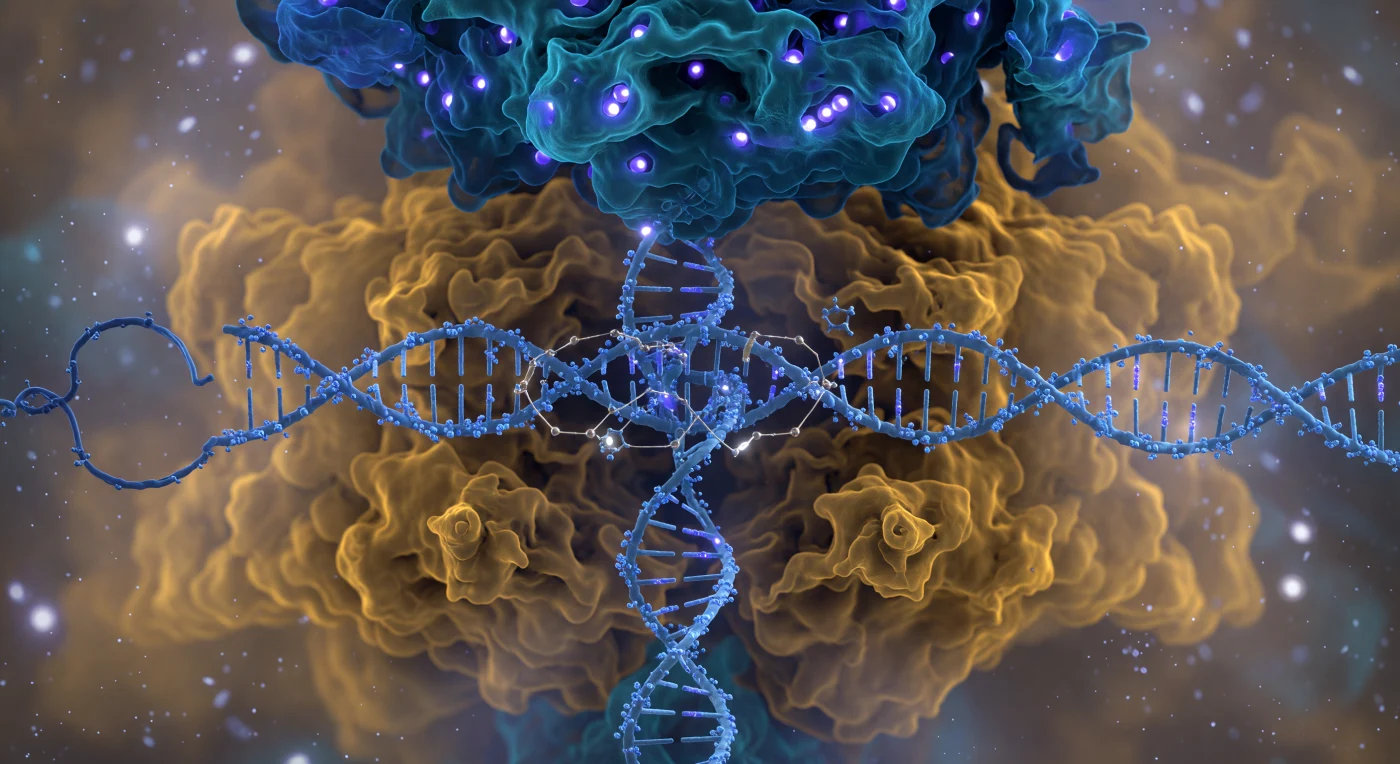
Vous flottez à quelques nanomètres seulement de la face antérieure du complexe Cas9, une macromolécule de neuf nanomètres de diamètre qui emplit votre champ de vision tout entier comme la paroi d'une cathédrale vivante — le lobe de reconnaissance cobalt et sarcelle se déployant en voûte surplombante au-dessus, tandis que le lobe nucléase ambré et ocre s'arrondit en contrebas, ses surfaces stipplées de nuages d'électrons qui ne résolvent jamais tout à fait en contours francs, la frontière entre protéine et solvant perpétuellement négociée plutôt que tracée. Entre les deux lobes, l'hélice double B-ADN traverse la structure comme un pilier de corde glacée torsadée, son squelette phosphate irradiant une luminescence violette froide tandis que des molécules d'eau tremblent en essaim autour de lui, et le sillon majeur vous fait face — un canyon ombragé dont les parois portent les signatures chimiques des bases cibles maintenues ouvertes contre leur préférence thermodynamique propre. Le guide ARN cyan électrique fend l'espace intérieur en diagonale, ses groupements 2′-OH hérissés vers l'extérieur comme de minuscules crochets, et les trois ponts de boucle-R déjà formés en avant-plan apparaissent comme des fils d'or-blanc gossamer tendus entre les surfaces complémentaires, chaque liaison hydrogène visible comme une géométrie que l'on ressent autant qu'on ne la voit. Sur le flanc droit du lobe nucléase, le domaine PAM enfonce deux chaînes latérales arginine dans le petit sillon du trinucléotide NGG — leurs groupes guanidinium, palettes aplaties cuivre-orangé, distordent localement la géométrie hélicoïdale en une étroite contraction perceptible — pendant qu'au cœur du clivage, les ions magnésium des sites actifs HNH et RuvC brûlent comme des points blancs incandescents, chacun cerclé d'une cage précise d'atomes oxygène coordinateurs en géométrie octaédrique, dans un solvant entier qui n'est pas du vide mais un océan thermique luminescent de dipôles d'eau et d'atmosphère ionique, vibrant à chaque instant sous l'agitation brownienne de l'échelle nanométrique.

Vous vous trouvez suspendu au cœur géométrique d'une protéine intrinsèquement désordonnée, immergé dans un nuage de probabilité lumineux d'environ huit nanomètres de diamètre où des dizaines de conformères de chaîne polypeptidique coexistent simultanément, chacun à peine visible, leur superposition construisant une nébuleuse bleu-blanc diffuse qui respire sans jamais se fixer. Ce n'est pas une architecture figée mais un ensemble statistique vivant : la chaîne n'adopte aucune structure unique préférentielle, son énergie libre distribuée sur un vaste paysage conformationnel que l'agitation thermique traverse en permanence à l'échelle de la nanoseconde. À votre gauche, un ruban ambré chaud se matérialise fugacement — une hélice alpha dont les liaisons hydrogène entre oxygènes carbonyles et amides NH se forment et se rompent en moins d'une microseconde — avant de se dissoudre dans le brouillard bleu-blanc de l'ensemble, pendant qu'un amas d'acides aminés aromatiques pulse d'un bref éclat jaune-or, minimum énergétique transitoire d'interactions hydrophobes qui se reformera ailleurs dans l'espace conformationnel. Partout autour de vous, des sphéroïdes d'eau de 0,28 nanomètre martelent chaque segment du squelette peptidique exposé, leur agitation thermique collective constituant le bruit de fond contre lequel toute structure naissante doit lutter pour exister, même un instant.

Depuis le sol aqueux, une tour de bronze s'élève vers un ciel bleu électrique sans horizon — l'épine dorsale ribose-phosphate de l'ARN en épingle à cheveux grimpant en spirale compacte selon sa géométrie A-form caractéristique, plus resserrée et inclinée que celle de l'ADN, ses 2'-hydroxyles cuivrés hérissés vers l'extérieur comme autant d'antennes qui trahissent l'identité chimique de la molécule. Les groupements phosphate flanquent chaque brin comme des nœuds d'obsidienne polie, chacun couronné d'un halo violet-bleu de charge négative qui structure les molécules d'eau environnantes en sphéroïdes opalescents agités de tremblements incessants, tandis que des ions sodium filent en éclats argentés et que des magnésiums dorés-verts s'ancrent plus près du squelette par des liens électrostatiques invisibles. Dans les profondeurs de la rainure mineure, les plans aromatiques des paires de bases guanine-cytosine s'empilent comme des feuilles de graphène iridescentes plum et sarcelle, leur déstabilisation électronique pi imprimant une lumière intérieure aux parois du canyon. Tout là-haut, à l'apex, la tétraloop GNRA s'épanouit en une couronne baroque de nucléotides non appariés dont les adénines s'entrecroisent en une plateforme étonnamment rigide, baignée d'un ambre chaud contre le halo bleu-blanc du solvant — une architecture d'une précision absolue, vibrante à des rythmes femtoseconde, ancienne et vivante.
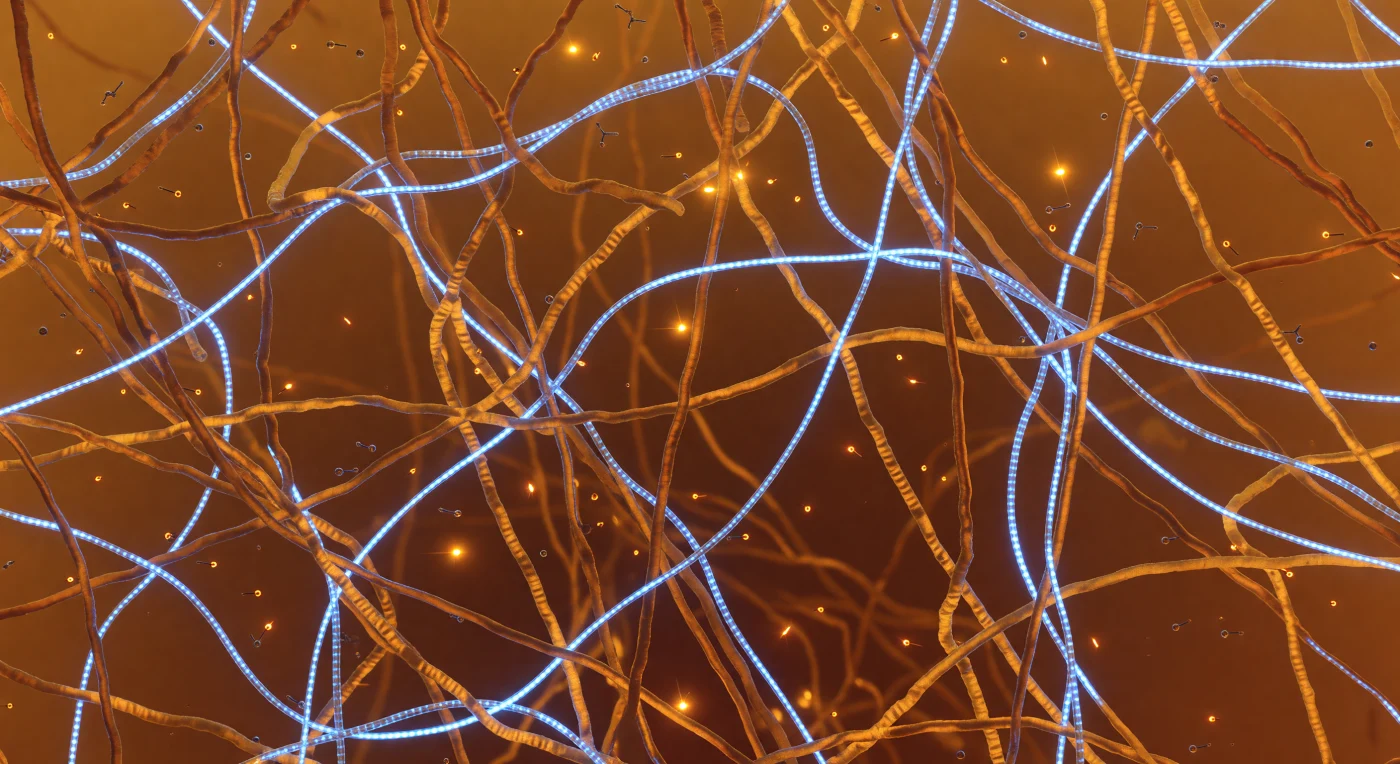
Le regard se perd dans toutes les directions à travers une jungle ambrée et suffocante de chaînes protéiques désordonnées, leurs brins de deux à trois nanomètres d'épaisseur tissant un réseau si dense que l'espace libre n'existe qu'en éclairs fugaces — de petites clairières de cinq à quinze nanomètres qui s'ouvrent et se referment avant même d'être traversées. Ces domaines de faible complexité séquencielle, dépourvus de structure fixe, maintiennent la cohésion du condensat non par des liaisons covalentes permanentes mais par une multitude de contacts transitoires : là où un résidu tyrosine presse son cycle aromatique contre le groupement guanidinium d'une arginine voisine, une étincelle ambrée plus vive s'allume une fraction de nanoseconde puis s'éteint, la thermodynamique collective de milliers de tels événements simultanés stabilisant l'ensemble comme une foule maintient sa forme sans que personne ne reste immobile. Les brins d'ARN traversent ce réseau comme des câbles à fibre optique d'un bleu-blanc froid, leur diamètre de 1,5 nanomètre et la périodicité de 0,34 nanomètre entre chaque paire de bases les rendant immédiatement distincts de la matière protéique environnante, leurs reflets teal colorant brièvement les parois ambrées les plus proches. Des molécules d'ATP dérivent sans trajectoire apparente à travers les pores du maillage, portées par l'agitation thermique d'un milieu aqueux qui n'est ni eau libre ni gel solide mais quelque chose d'intermédiaire — une phase condensée née spontanément de la séparation de phases, ce mécanisme par lequel certaines protéines et ARN s'enrichissent mutuellement dans un compartiment sans membrane pour concentrer la machinerie moléculaire là où elle est nécessaire.
















