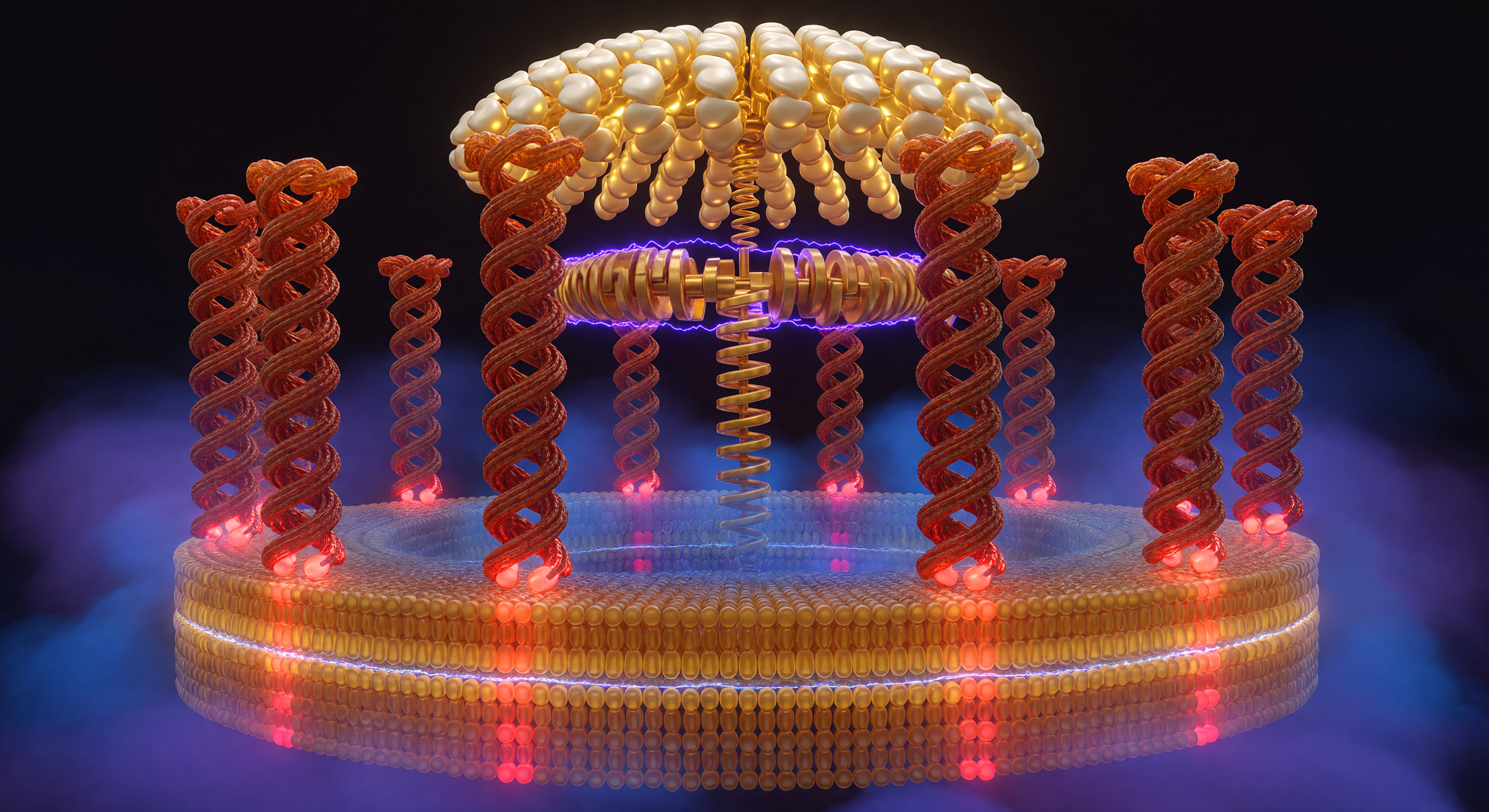
Im Inneren des c-Ring-Rotors der ATP-Synthase wölbt sich die Welt wie das Innere eines lebendigen Kolosseums: Zehn terrakottafarbene α-helikale Säulen erheben sich ringsum aus der Lipiddoppelschicht, deren äußeres Blatt in warmem Bernstein-Gold leuchtet und deren inneres Blatt in ein kühles Blau-Bernstein übergeht – eine so scharfe Grenzlinie wie eine Küstenlinie, an der Tempelstützen aus dem Wasser tauchen. An der Basis jeder Säule glüht ein einzelner Glutamatrest: die dem Protonenkanal zugewandten Reste brennen in leuchtendem Scharlachrot, elektrisch roh und deprotoniert, während jene im hydrophoben Membrankern zu einem gedämpften Ziegelrot verblassen – ein biologischer Rhythmus, wie Glut, die erlischt und wieder aufflammt. Das Spannungsgefälle der Protonenmotorischen Kraft von 150–200 Millivolt manifestiert sich nicht in Pfeilen oder Symbolen, sondern in der Qualität des Lichts selbst: Auf der einen Seite verdichtet sich ein schweres Kobaltviolett unter dem Gewicht akkumulierter Protonen, während es auf der anderen zu einem ruhigen Mitternachtsblau verblasst, als stünde die Atmosphäre kurz vor dem elektrischen Durchbruch. Darüber wölbt sich die F₁-Katalysekuppel wie ein Kathedralengewölbe aus Gold und Elfenbein, und die asymmetrische γ-Untereinheit – eine Kurbelwelle aus Protein – überträgt mit geometrischer Zwangsläufigkeit die Rotationsenergie der Protonenströmung in die chemische Bindungsenergie des ATP, eine Maschine, die seit vier Milliarden Jahren ohne Unterbrechung dreht.
Other languages
- English: ATP Synthase C-Ring Rotor Immersion
- Français: Immersion Rotor Anneau-C Synthase
- Español: Inmersión Rotor Anillo-C ATPasa
- Português: Imersão Rotor Anel-C Sintase
- العربية: غمر دوار الحلقة سي ATP
- हिन्दी: ATP सिंथेज़ सी-रिंग रोटर विसर्जन
- 日本語: ATP合成酵素Cリング回転子没入
- 한국어: ATP 합성효소 C링 로터 몰입
- Italiano: Immersione Rotore Anello-C Sintasi
- Nederlands: ATP-Synthase C-Ring Rotor Onderdompeling