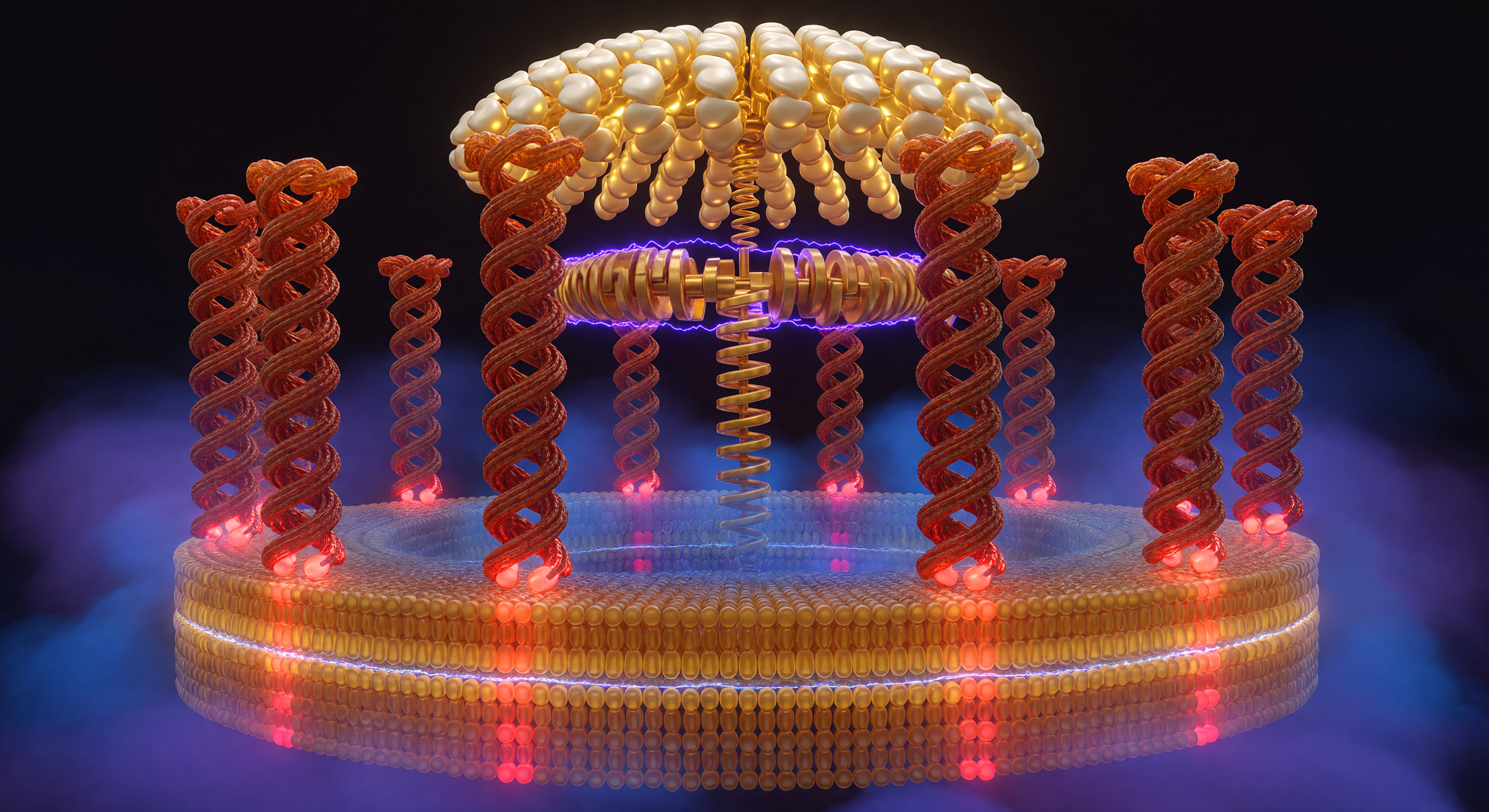
A pochi nanometri di distanza, dieci colonne elicoidali di proteina si curvano intorno all'osservatore come le pareti interne di un colosseo vivente, i loro profili terracotta e ruggine corrugati dalle spirali del backbone peptidico che costituiscono i sottodomini transmembrana della subunità c dell'ATP sintasi — una macchina molecolare che converte il flusso di protoni attraverso la membrana mitocondriale interna in legami chimici ad alta energia. Alla base di ciascuna colonna, i residui di glutammato alternano tra uno stato cremisi acceso, deprotonato e elettrostaticamente instabile nel canale protonico, e uno stato mattone spento, neutro e sepolto nel cuore idrofobico del doppio strato lipidico, un'oscillazione che scandisce la rotazione del rotore c con la cadenza di un meccanismo a scatto antico di quattro miliardi di anni. Il gradiente di forza proton-motrice di 150–200 mV non si manifesta con simboli astratti, ma nella qualità stessa della luce: cobalto e viola intensi si addensano sul versante citosolico come un'atmosfera compressa sull'orlo della scarica, mentre il versante matriciale respira un indaco più caldo e rilassato, il campo elettrostatico visibile nella densità del colore stesso. Sopra, il dominio catalitico F₁ si arcua come una volta gotica di oro pallido e avorio, i suoi sottodomini β che pulsano tra stati di legame distinti mentre l'albero a camme della subunità γ trasmette la torsione rotazionale in sintesi di ATP — un accoppiamento meccanochimico che trasforma il moto casuale di ioni in ordine molecolare impeccabile.
Other languages
- English: ATP Synthase C-Ring Rotor Immersion
- Français: Immersion Rotor Anneau-C Synthase
- Español: Inmersión Rotor Anillo-C ATPasa
- Português: Imersão Rotor Anel-C Sintase
- Deutsch: ATP-Synthase C-Ring Rotor Tauchgang
- العربية: غمر دوار الحلقة سي ATP
- हिन्दी: ATP सिंथेज़ सी-रिंग रोटर विसर्जन
- 日本語: ATP合成酵素Cリング回転子没入
- 한국어: ATP 합성효소 C링 로터 몰입
- Nederlands: ATP-Synthase C-Ring Rotor Onderdompeling