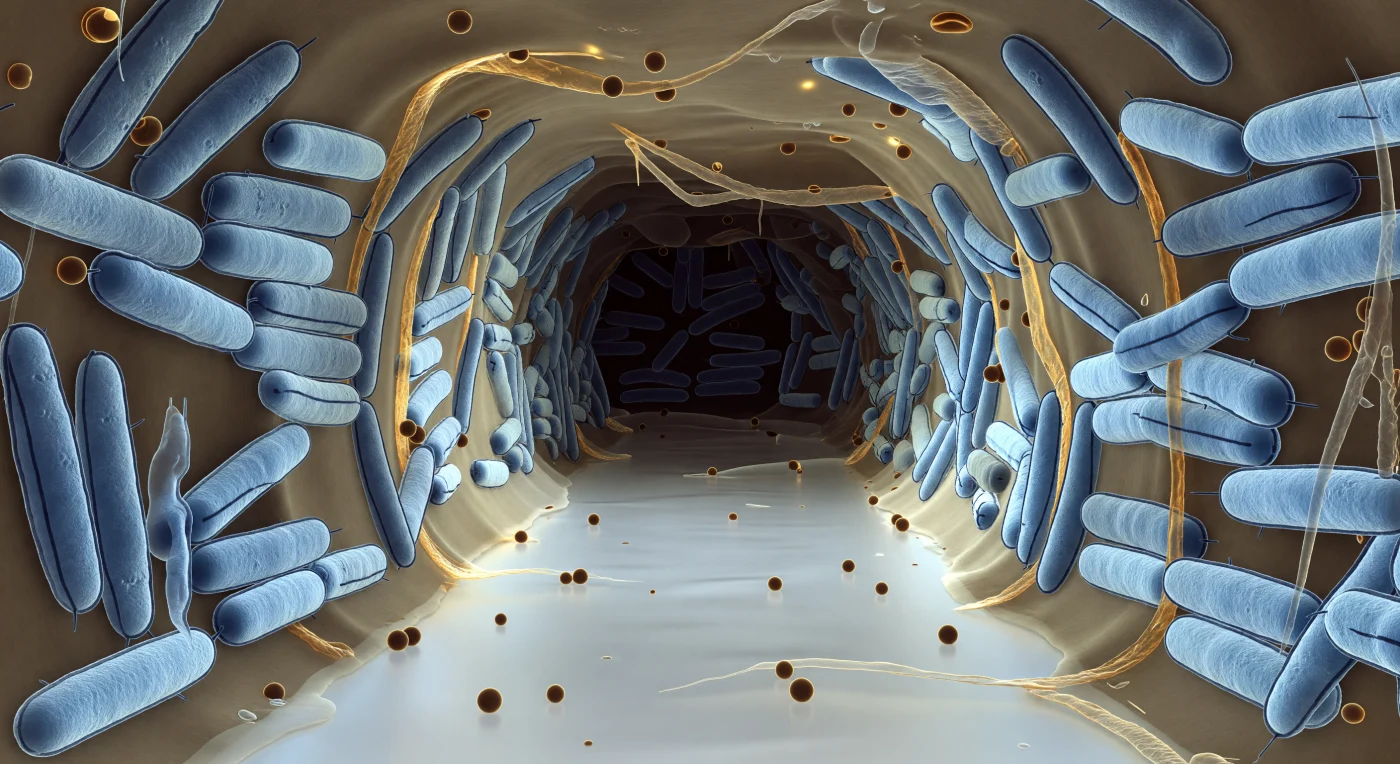
Ti trovi sospeso all'imbocco di un corridoio che taglia attraverso una colonia vivente di batteri — un vicolo di fluido quasi immobile, luminoso e leggermente refrattivo, che trasporta ossigeno disciolto e nutrienti verso l'interno come un fiume sotterraneo fermato in un singolo istante. Le pareti di questo canale sono costruite da corpi batterici di *Escherichia coli* stipati in file parallele, ciascuno un cilindro color blu ghiaccio alto cinque volte la tua statura, le cui doppie membrane esterne appaiono come due sottilissime linee scure che percorrono longitudinalmente ogni organismo — un dettaglio architettonico spettrale ripetuto centinaia di volte in profondità di campo, fino a dissolversi in una foschia azzurro-grigia dove il canale si incurva verso l'ombra totale. La matrice di esopolisaccaridi che li cementa insieme si legge come una sostanza ambrata e traslucida, a metà strada tra il miele e il vetro smerigliato, che riempie ogni interstizio e conferisce all'intera parete una flebile luminescenza calda sotto il freddo blu cellulare. Sparse sul fondo del canale e in sospensione nella colonna fluida, vescicole della membrana esterna — sfere perfette color ambra, sigillate, grandi come ciottoli alla tua scala — trasportano carichi molecolari tra gli organismi, alcune semincassate nella matrice come fossili traslucidi nell'ambra, mentre all'estremità lontana il corridoio sfuma progressivamente dal bianco argenteo verso un marrone carbone profondo, dove i gradienti di ossigeno e nutrienti declinano e la matrice si fa più densa, più opaca, e il silenzio chimico diventa assoluto.

Sospesi nell'oscurità vischiosa del liquido extracellulare, ci troviamo di fronte a una delle scene più silenziose e letali del corpo umano: decine di virioni HIV-1, ciascuno un globo traslucido di appena 120 nanometri, derivano lentamente in sospensione browniana intorno a noi, le loro superfici punteggiate da corone trimetriche di glicoproteina gp120 che brillano come oro brunito nell'uniforma luminescenza crioelettronica che non ha sorgente né direzione. Dietro di noi, la membrana plasmatica del linfocita T si erge come la parete di una trincea oceanica, ondulando in lunghe onde lente, il doppio strato lipidico che iridisce dal blu al violetto mentre i filamenti del glicocalice si proiettano verso il fluido come una foresta rada di fronde traslucide. Alcuni virioni si sono già avvicinati pericolosamente a questa foresta molecolare, i loro spike aurei che si tendono verso i recettori CD4 in una danza che non è intenzionale ma chimica — due sfere che si schiacciano leggermente contro la membrana, il loro profilo perfetto che si deforma come bolle di sapone sull'acqua. Più lontano, altri virioni si dissolvono nella foschia perlescente del fluido carico di proteine, i loro trimeri ridotti a scintille dorate sospese nel nulla, in un ambiente dove la luce è irrilevante e solo la massa e la chimica definiscono il paesaggio.

Immaginate di trovarvi sul pavimento di un canyon immaginato non di roccia, ma di membrana biologica vivente: la membrana mitocondriale interna si erge tutto intorno in pieghe enormi e convolute, una parete di bilayer lipidico color carbone intenso, macchiato di osmio e illuminato dalla calda luce artificiale della cryo-EM in falsi colori ambrati. Su ogni centimetro di quella superficie oscura proliferano migliaia di complessi dell'ATP sintasi, ciascuno simile a un fungo tozzo con la testa F1 che sporge nel matrix come una cupola arrotondata, i loro steli ancorati nella membrana come pali conficcati in una riva scura e silenziosa. Intorno a voi, il matrix mitocondriale non è aria né acqua, ma un colloide proteico densissimo — oltre 500 milligrammi per millilitro — che diffonde ogni fotone in un bagliore volumetrico color miele, dove enormi enzimi del ciclo di Krebs galleggiano come massi e i ribosomi mitocondriali vibrano di moto browniano tanto costante da sembrare immobili. In lontananza, la giunzione delle creste si restringe in un corridoio stretto e incandescente, le pareti quasi toccarsi, le teste dell'ATP sintasi così fitte da formare un soffitto quasi continuo sopra la gola luminosa: un'architettura biologica pura, respirante e viva in ogni direzione.
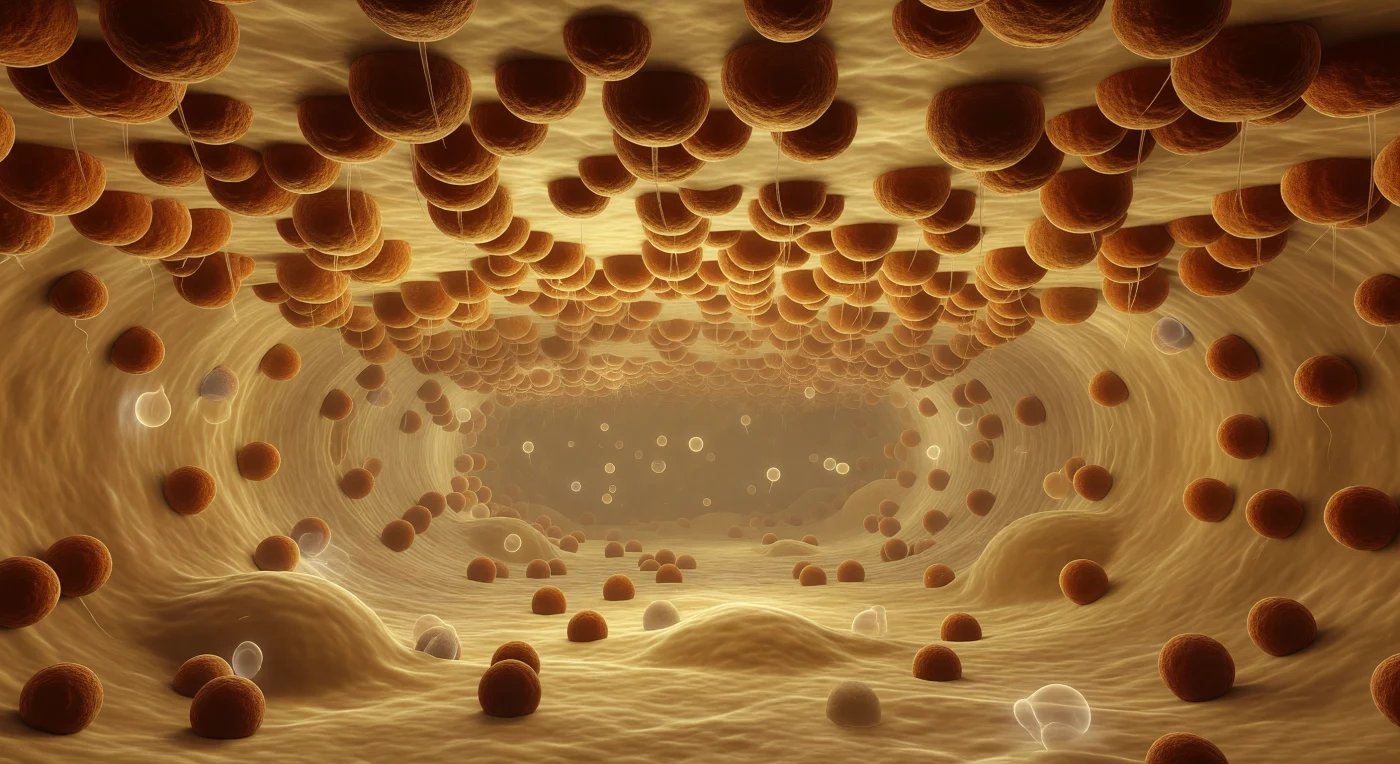
Ti trovi sospeso nel lume del reticolo endoplasmatico rugoso, immerso in una luce diffusa color miele che permea l'ambiente acquoso come una luminescenza senza sorgente, mentre proteine disciolte scivolano intorno a te come fantasmi traslucidi nella corrente. Al di sopra, un soffitto immenso e ininterrotto di membrana lipidica — caldo ocra e crema — si estende fino ad ogni orizzonte, completamente ricoperto da una moltitudine di ribosomi color ruggine, stipati come patelle su uno scafo antico, ognuno dei quali preme leggermente il doppio strato sotto il proprio peso molecolare. Da ciascuna di quelle sfere asimmetriche e granulari — grandi come architetture rispetto a te — scendono fili quasi invisibili di polipeptide nascente, guizzi iridescenti che svaniscono nella foschia dorata del corridoio prima di raggiungere il lume. Il reticolo si prolunga in prospettiva come una cattedrale, con due membrane parallele, entrambe incrostate di macchinari biologici, che convergono verso un punto di fuga perso nell'ambra morbida della distanza proteica: una fabbrica senza pausa, senza consapevolezza, che produce e traduce in ogni direzione simultaneamente.

Sospesi sull'orlo più avanzato di una cellula in migrazione, ci troviamo immersi in una giungla frattale di filamenti di actina — ciascuno appena sette nanometri di diametro, eppure qui percepiti come cavi tesi nell'oscurità, ramificati a settanta gradi precisi dai complessi Arp2/3 come corallo elettrico che cresce in assenza di luce solare. Sotto di noi, il substrato è uno specchio d'ossidiana illuminato da un'onda evanescente che penetra appena qualche centinaio di nanometri verso l'alto, rivelando le placche di adesione focale come lingotti di ambra incandescente affondati nel vetro freddo — sono i punti di ancoraggio che trasmettono la forza dell'intera rete alle proteine integrali di membrana, traducendo la polimerizzazione dell'actina in movimento diretto. Ai lati, i filopodi si proiettano nell'oscurità extracellulare come antenne di luce pura, singoli fasci paralleli di actina che sondano lo spazio inesplorato con la logica di un sistema sensoriale molecolare. L'atmosfera — se si può chiamare così la densa nebbia colloide della molecolazione di crowding — disperde la luce fredda del substrato in gradienti volumetrici che rendono l'interno della rete una foresta profonda dove ogni giunzione è identica alla precedente, dove la scala si dissolve nella ripetizione infinita di struttura che è, essa stessa, il meccanismo della vita in movimento.

Ti trovi sospeso nel nucleoplasma come in un liquido denso e viscoso, simile a miele freddo, mentre dinnanzi a te si erge una delle strutture più imponenti della cellula: il complesso del poro nucleare, un portale circolare di circa 120 nanometri che occupa interamente il tuo campo visivo, incassato nella doppia membrana nucleare color antracite come un rosone dorato e bronzeo fuso nella pietra viva. La sua simmetria otto volte radiale — ottosubcomplessi proteici disposti con precisione quasi architettonica — irradia una luce ambrata e calda, mentre dal tappo assiale centrale scendono filamenti di FG-nucleoporine come una tenda di perle traslucide, agitati da una lenta undulazione ipnotica che si interrompe ogni volta che una macromolecola in transito li attraversa, aprendo per un istante un abisso cilindrico di oscurità assoluta. Ai lati del poro, masse di eterocromatina compatta si innalzano come scogliere di mezzanotte in indaco profondo, le loro superfici granulose di nucleosomi che assorbono la luce senza rifletterla, mentre alle tue spalle la cromatina più aperta dell'eucromatina si dissolve in una foschia lavanda e lilla tenue, attraversata da droplet condensati che brillano come mercurio sospeso. Questo cancello non è soltanto un passaggio fisico: è il punto di controllo tra due mondi distinti della cellula, il filtro attraverso cui RNA messaggeri, proteine ribosomiali e segnali di regolazione negoziano ogni secondo il traffico che definisce l'identità e la sopravvivenza della cellula stessa.

Davanti a te si innalza una torre di membrana come un colonnato di giada traslucida: quindici dischi tilacoidali impilati in registro preciso, ciascuno separato dal successivo da una sottile intercapedine di lume giallo-limone che funge da giuntura luminosa tra lastre di un verde smeraldo profondo e intrinseco. Le superfici di ogni disco appaiono leggermente corrugate, quasi un lastricato irregolare, perché decine di migliaia di complessi del fotosistema II e delle antenne raccoglitrici della luce affiorano dalla membrana lipidica come teste arrotondate a pelo d'acqua, la loro densità talmente elevata da non lasciare quasi lipide libero tra l'uno e l'altro. Dal fianco della torre si protendono orizzontalmente i tilacoidi stromali, nastri smeraldo sinuosi che scivolano nel verde nebuloso dello stroma verso le grana vicine, appena percepibili come colonne luminose nella foschia molecolare — uno stroma gel-opaco intasato di complessi enzimatici di RuBisCO chiari e irregolari e punteggiato da plastoglobuli ambrati la cui superficie lipidica riscalda il verde dominante in riflessi color miele. Invisibile ma quasi percepibile, un gradiente protonico pulsa lentamente tra le membrane, più luminoso su un fianco del lume che sull'altro, traccia della forza motrice che alimenta la sintesi dell'ATP in questo paesaggio di architettura vivente costruita interamente di luce e membrana.
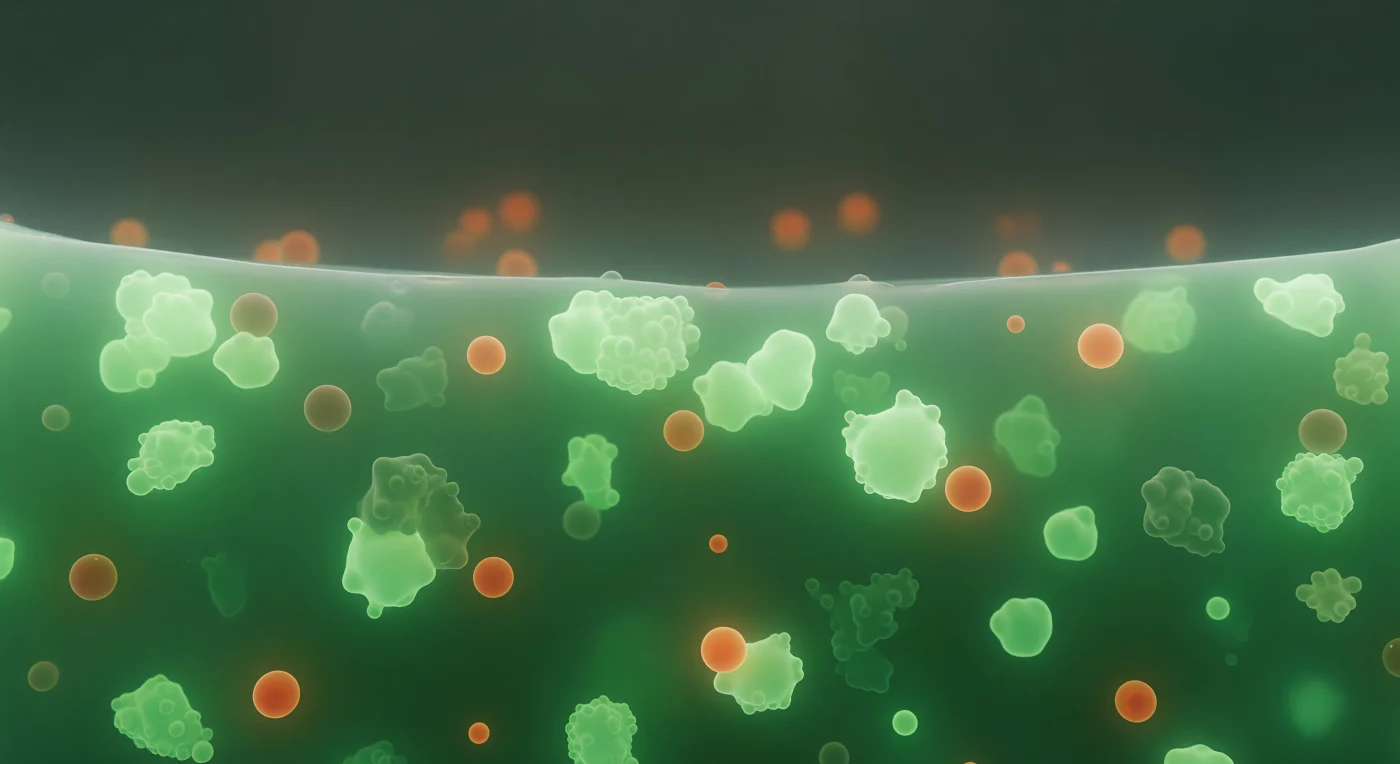
Ci si trova sospesi all'interno di un granulo da stress, una struttura di condensazione biomolecolare che si forma nelle cellule eucariotiche in risposta a situazioni di pericolo — stress ossidativo, shock termico, infezioni virali — come meccanismo di protezione e riorganizzazione dell'espressione genica. Attorno a voi, la nebbia verde smeraldo che permea ogni direzione non è luce ambientale, ma fluorescenza intrinseca della proteina G3BP1 coniugata a GFP, uno degli scaffold molecolari fondamentali che nucleano e stabilizzano questa fase condensata attraverso interazioni debolmente attrattive di tipo π-π, elettrostatico e idrofobico tra domini intrinsecamente disordinati. Il mezzo che vi circonda non è né solido né liquido nel senso convenzionale: è un fluido viscoelastico nato dalla separazione di fase liquido-liquido, un fenomeno fisico in cui specifiche proteine e RNA raggiungono localmente concentrazioni così elevate da separarsi spontaneamente dal citoplasma circostante come una goccia d'olio nell'acqua, mantenendo però la fluidità interna che consente lo scambio continuo di componenti con l'esterno. Le sfere ambra-arancio che derivano lentamente attraverso la matrice verde sono co-condensati ricchi di TIA1, una proteina con dominio prionica che tende a formare subcompartimenti distinti all'interno del granulo attraverso un'ulteriore separazione di fase interna, mentre il confine netto che si intravede lontano — quella parete verticale dove il verde luminoso precipita bruscamente nel quasi-nulla del citoplasma diluito — è la firma visibile della tensione interfacciale che definisce e mantiene l'identità fisica dell'intera struttura, un orizzonte tra due stati della materia biologica separati da pochi nanometri di transizione molecolare.

Sospeso direttamente sopra l'asse centrale del motore flagellare, lo sguardo sprofonda in una delle strutture più sofisticate che la biologia abbia mai prodotto: anelli concentrici di bronzo ossidato e acciaio scuro — gli anelli L, P e MS — si incastrano nelle membrane batteriche come sezioni di un'architettura templare vista dall'alto, ciascuno incorporato in uno strato distinto che va dal lipopolisaccaride cobalto della membrana esterna fino al piano dorato della membrana interna. Diciassette complessi statoriali MotA/MotB si dispongono radialmente attorno al rotore con una simmetria quasi perfetta, masse proteiche asimmetriche e compatte che premono contro la membrana interna come contrafforti che ancorano una turbina alla sua sede, la loro superficie opaca che cattura una luce diffusa e priva di direzione come se ogni proteina si auto-illuminasse dalla propria densità interna. Al centro, l'anello MS si estende come un pavimento scultorico di creste radiali e confini tra subunità, la sua tessitura smerlettata visibile come il segno di un meccanismo portato alla perfezione da miliardi di generazioni di selezione evolutiva. Sopra, il filamento flagellare sale a spirale nello spazio extracellulare come una fune torsadée che si dissolve in una foschia blu-grigia di molecole disciolte, collegato al rotore attraverso un gancio curvo dalla superficie ruvida come cavo intrecciato, sigillato contro la membrana esterna come un albero rotante in una guarnizione di precisione. L'intera struttura — il cui diametro nella percezione scalata evoca il pavimento di uno stadio visto dall'alto del bordo — non è mai ferma: trasmette, in ogni interfaccia proteica levigata dalla funzione, l'impressione di una macchina molecolare pronta a girare senza sosta nell'oscurità interna di un organismo vivente.

Ci si trova all'interno di una struttura vivente che respira senza saperlo: guardando verso l'alto dal pavimento epiteliale delle vie aeree, centinaia di ciglia si innalzano come colonne di ceramica bagnata, ciascuna un cilindro di deep blue-cyan largo quanto un lampione sembra a una formica, le loro superfici attraversate da sottilissime striature longitudinali — l'impronta fantasma dei nove doppietti assonemali che premono attraverso la membrana esterna come costole sotto la seta tesa. Tra i fusti più vicini, fili d'ambra dorata di muco si tendono in archi catinari lentissimi, luminosi e leggermente traslucidi come miele alla luce di una candela, assottigliandosi fino a filamenti sottilissimi nei punti di ancoraggio e ispessendosi al centro di ogni campata — un lampadario di resina organica sospeso nella navata più intima che esista. In alto, la chioma ciliare forma una volta ondulata dove un'onda metacrona è catturata in un unico istante congelato: un'intera colonnata di ciglia piegate in unison, la differenza di fase tra ogni fila che dà al soffitto l'aspetto di tegole sovrapposte colte a metà del loro scintillio, il ritmo coordinato generato dalle dineine assonali che trasformano l'idrolisi dell'ATP in movimento meccanico collettivo capace di trasportare muco a velocità di circa 5–20 µm al secondo. Il pavimento sotto i piedi si distende come una pianura di argilla geometrica, le giunzioni strette tra cellula e cellula rialzate come creste di panna secca, mentre piccoli microvilli — noduli arrotondati beige che sbiadiscono verso la crema alle loro sommità — punteggiano la superficie come ciottoli su una distesa di sabbia fluviale, tutto avvolto da una luce interna senza sorgente, blu-bianca e diffusa, che sembra emanare dalla stessa materia viva che ci circonda.
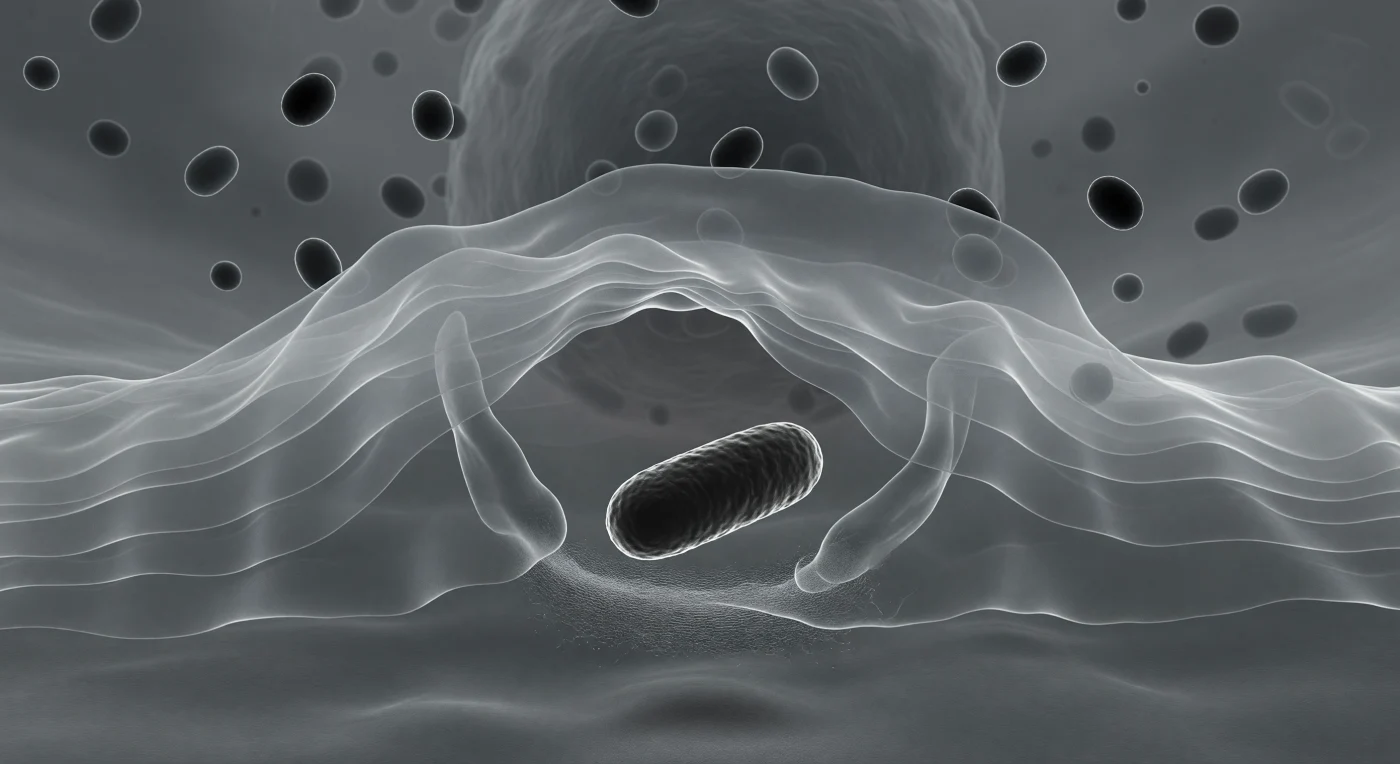
Ci si trova sospesi proprio al limite anteriore del macrofago, dentro un velo citoplasmatico traslucido che avanza lentamente come un'onda pietrificata nel suo momento di massima curvatura — il lamellipodio si allunga in lamine sovrapposte di gel grigio-argento, la sua tessitura finemente granulare tradisce la densità della rete di actina che lo sostiene, invisibile nei singoli filamenti ma percepibile come una seta tessuta appena sotto la soglia del risolvibile. Davanti, il batterio si erge come un monolite scuro, una forma bastoncellare densa e quasi nera il cui perimetro è delineato da un alone diffrattivo luminoso — le membrane pseudopodali si chiudono attorno ai suoi fianchi con la geometria lenta e inevitabile di mani che si congiungono in un gesto cerimoniale, l'inglobamento quasi compiuto. Questo processo — la fagocitosi — è uno dei meccanismi fondamentali dell'immunità innata: il macrofago riconosce il batterio tramite recettori di superficie, innesca la polimerizzazione locale dell'actina e proietta pseudopodi che avvolgeranno il patogeno in un fagosoma destinato a fondersi con i lisosomi visibili come granuli scuri nella profondità del citoplasma retrostante. Tutto si svolge su una scala di pochi micrometri e nell'arco di minuti, eppure l'atmosfera è quella di qualcosa di architettonicamente deliberato, come se la cellula operasse con una pazienza vastissima e silenziosa.

Ti trovi sospeso al centro di un immenso bacino ambrato: la concavità centrale di un eritrocita umano si distende in ogni direzione come il pavimento di un cratere da impatto su un mondo ocra e tiepido, la membrana plasmatica che si allontana come una pianura di oro traslucido, tesa tra il caramello e il miele al sole, percorsa da dolci ondulazioni che il fascio obliquo di luce secondaria trasforma in creste brillanti e ombre taglienti come metallo inciso. Appena sotto quella superficie luminosa, un reticolo di filamenti di spectrina si imprime in rilievo come una rete di linee geodetiche scolpite nel vetro ambrato — l'impalcatura elastica che mantiene la cellula deformabile abbastanza da attraversare capillari più stretti del suo stesso diametro, respirando con una tensione quasi impercettibile. A distanza media, le cellule vicine si sono impilate in rouleaux, torri biconcave dai fianchi lisci che si ergono come colonne di arenaria nel plasma color paglia, mentre piastrine spinose — irregolari, stellate, irte di proiezioni di superficie — captano la luce obliqua come punti speculari dispersi nel mezzo sieroso. L'intera scena ha la qualità di un paesaggio planetario intimo e vastissimo insieme, dove ogni materiale biologico — membrana, citoscheletro, plasma — si rivela come qualcosa tra seta bagnata, resina lucidata e metallo vivo.
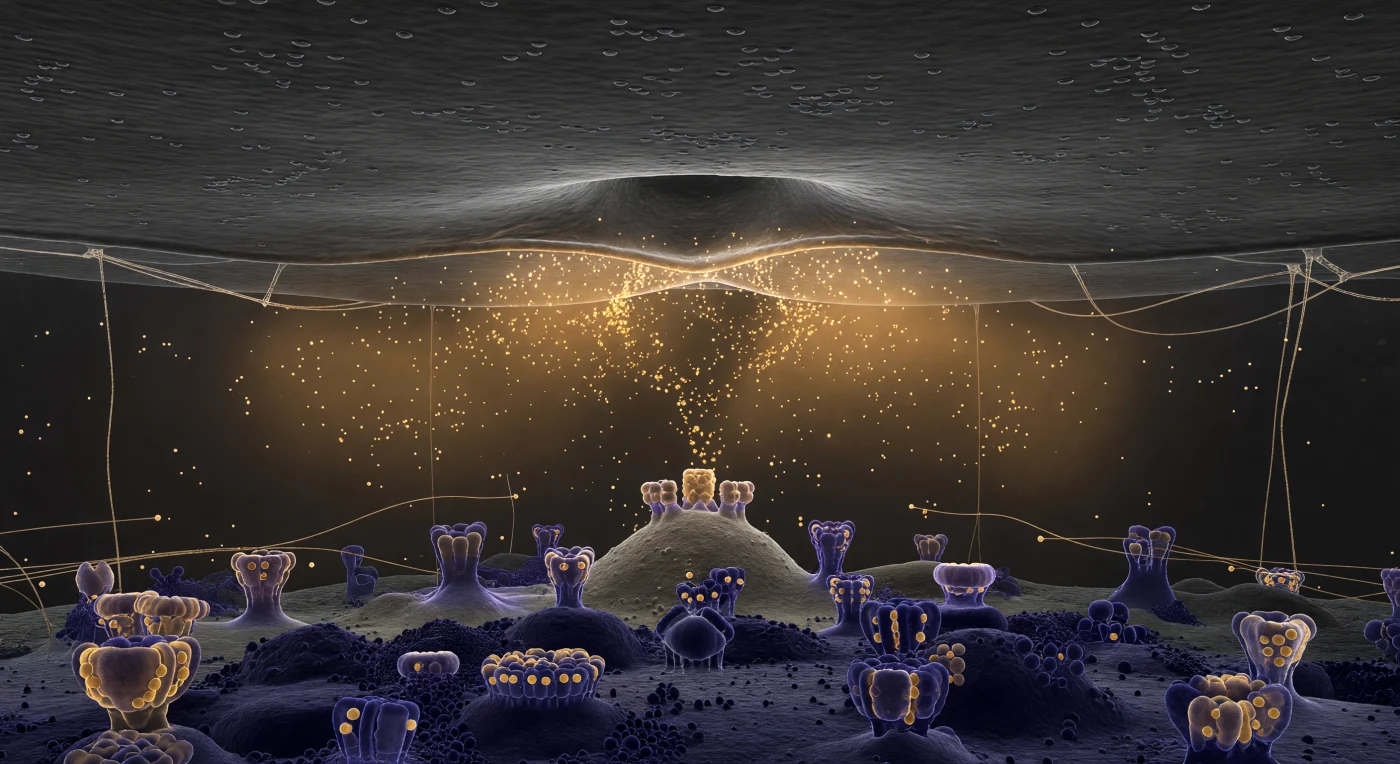
Ti trovi sospeso nell'interstizio più stretto dell'intero sistema nervoso: la fessura sinaptica, un corridoio di soli 25 nanometri in cui il soffitto e il pavimento sono presenti simultaneamente, separati da uno spazio che a questa scala percettiva non supera l'apertura delle tue braccia. Sopra di te, la membrana presinaptica si distende come una pianura di carbone scuro leggermente ondulata, e al suo centro una vescicola ha appena consumato la propria fusione: le due membrane si sono compenetrate in una forma a omega perfetta, i foglietti lipidici in collasso mentre un'aureola glistening segna il punto in cui due bilayer sono diventati un'unica lamina continua. Da quell'apertura si diffonde una luminescenza ambrata — non raggi, ma un'esalazione volumetrica di migliaia di molecole di neurotrasmettitore che si espandono lateralmente come una marea calda, più densa presso il poro di fusione e sempre più trasparente verso i margini, con filamenti proteici extracellulari tesi tra soffitto e pavimento come cavi traslucidi che captano il bagliore dorato in sottili linee di fuoco. Sotto, la densità postsinaptica si rivela come un paesaggio architettonico fondamentalmente diverso: un tappeto compatto di viola scuro, ricco di scaffolding elettrondenso da cui emergono verso l'alto i complessi recettoriali AMPA e NMDA come formazioni lapidee antiche, le cui superfici superiori restituiscono la luce ambra dei neurotrasmettitori in riflessi viola-dorati, l'unico evento cromatico caldo in un mondo altrimenti monocromatico e compresso.
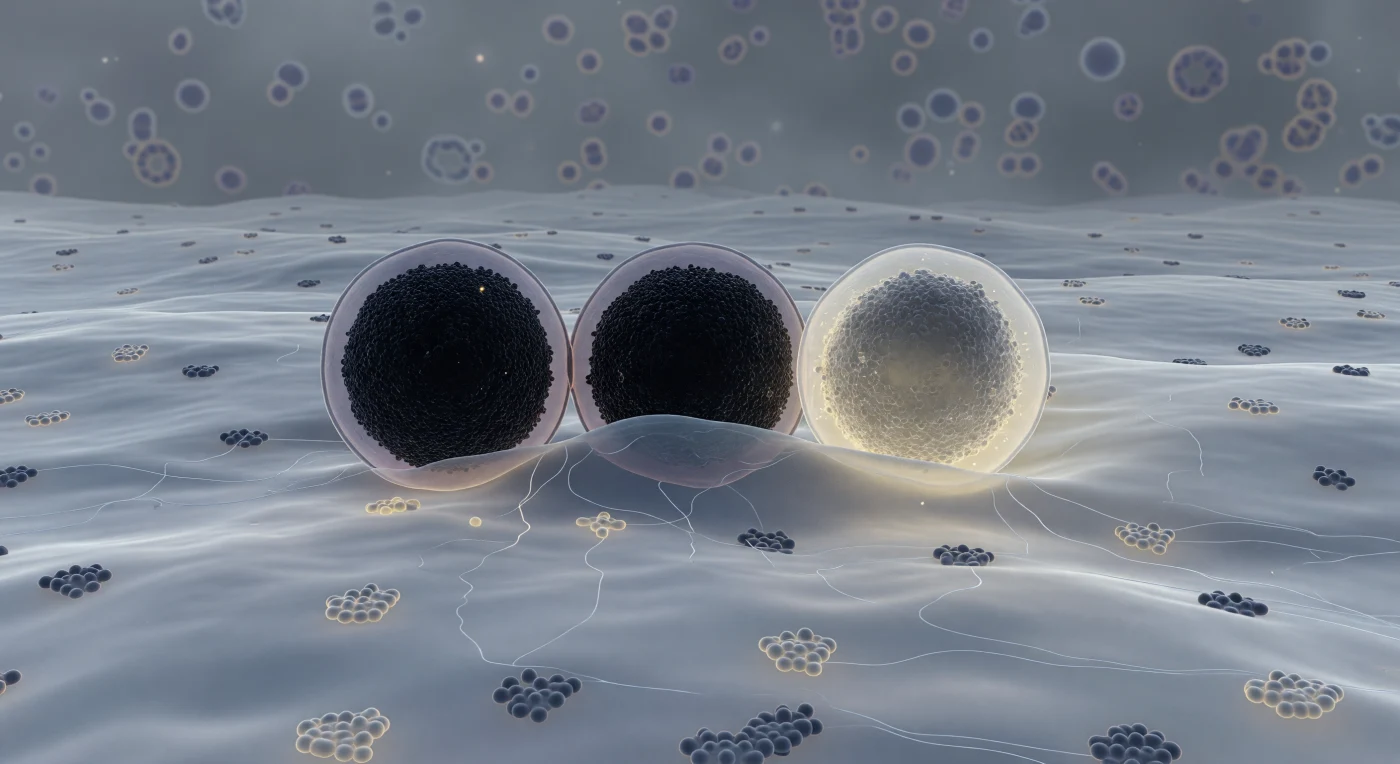
Ci si trova all'interno di una cellula beta pancreatica, scivolando rasente alla faccia citoplasmatica della membrana plasmatica come se si galleggiasse appena sopra un'immensa pianura ondulante di lipidi blu-grigi, percorsa da silhouette scure di complessi proteici e chiazzata da domini ricchi di colesterolo che brillano di un tenue riflesso iridescente. Tre granuli secretori di insulina dominano il campo visivo come edifici sospesi: il primo è ancorato con precisione alla membrana, il suo nucleo cristallino di esameri zinco-insulina quasi opaco circondato da un sottile alone lavanda; il secondo ha già iniziato a cedere, la membrana plasmatica che si piega verso l'interno in una dolce depressione dove i due doppi strati cominciano a fondersi in un collare di grigio indistinto; il terzo, a destra, è già oltre il punto di non ritorno — il suo contenuto denso si dissolve in una foschia calda color avorio che sfuma nello spazio extracellulare ambrato come inchiostro in acqua. Tra i granuli, sottili filamenti di cortex actinico formano una trama rada e spettrale, mentre il citoplasma profondo recede in una nebbia macromolecolare brulicante di ribosomi e membrane lontane, tutto catturato in un istante immobile che ha la qualità luminosa e implacabile di una micrografia a trasmissione elettronica trasformata in realtà dimensionale.

Ci si trova sospesi nell'istante esatto in cui la cellula incontra il mondo esterno: la punta di ogni microvillo ci affiora intorno come la cima di una foresta di pilastri pallidissimi, ciascuno non più largo di cento nanometri, stipati con la regolarità geometrica di un alveare cristallizzato in materia vivente. Ogni fusto è irrobustito al suo interno da un fascio di filamenti di actina — proteine che si polimerizzano e si accorciano continuamente, mantenendo la rigidità di queste proiezioni che moltiplicano per decine di volte la superficie assorbente dell'enterocita. Dal margine superiore di ogni colonna si alza il glicocalice: una peluria di filamenti polisaccaridici lunghi pochi nanometri, abbastanza densa da formare un feltro continuo che filtra, rallenta e concentra le molecole del chimo prima che raggiungano le proteine di trasporto di membrana sepolte al di sotto. Guardando tra i fusti verso il basso, la luce obliqua si perde in ombra densa come il fondo di un canyon, mentre in superficie il calore ambrato dell'illuminazione rivela ogni impercettibile irregolarità — un fusto leggermente inclinato, un ciuffo di glicocalice più fitto — testimonianza silenziosa del fatto che questa architettura apparentemente minerale è tessuto vivente, in perenne e quieto movimento.

Sospesi al centro geometrico di una cellula in divisione, si è avvolti da una cattedrale di luce biologica: dai due poli centrosomiali lontani, sopra e sotto, si diramano decine di cavi di microtubuli fluorescenti — cilindri luminosi di tubulina polimerizzata, colorati con il verde elettrico intenso del coniugato Alexa 488 — che si incrociano intorno alla posizione del osservatore formando un reticolo tridimensionale in tensione. Le fibre cinetocore, più spesse e abbaglianti, tirano con forza le masse cromosomiche indaco-viola verso i rispettivi poli, rivelando la meccanica molecolare dell'anafase: la segregazione dei cromatidi fratelli guidata dai motori proteici e dalla depolimerizzazione dei microtubuli ai cinetocori. Esattamente all'altezza dello sguardo, il corpo mediano taglia il campo visivo come una barra di fuoco bianco-verde, zona di sovrapposizione antiparallela così densamente impaccata da surclassare per luminosità ogni altra struttura. Oltre il fuso, il buio assoluto del citoplasma — non vuoto ma colmo di macromolecole che disperdono dolcemente il bagliore verde ai margini dei microtubuli in aureole di nebbia lattiginosa — ricorda che questa geometria di cavi luminosi è, in ogni suo dettaglio, materia proteica viva e dinamica, una macchina dell'eredità in piena azione.

Ti trovi sospeso nel mezzo argenteo pallido del plasma sanguigno, mentre davanti a te si erge un'immensa parete biologica che occupa l'intera metà inferiore del campo visivo: il glicocalice, una foresta fitta e traslucida di catene di proteoglicani e glicoproteine alte tra mezzo e due micrometri, i cui filamenti di solfato di eparan si arcuano e biforcano come rami di betulla invernale, scintillando di luce fredda e diffusa nella precisa palette cromatica del colorante rutenio rosso in false-color TEM, tra il blu-argento e l'indaco. La membrana plasmatica sottostante è appena percepibile — una linea di carbone scuro intravista in frammenti lontani, come il fondo di un oceano in tempesta visto attraverso la volta di una foresta sommersa — celata da una lacca sempre più impenetrabile di polimeri biologici il cui intreccio si fa più fitto e oscuro man mano che lo sguardo sprofonda verso il basso. Sopra di te, la tua ombra — il grande disco convesso del globulo rosso in avvicinamento — si proietta sul baldacchino del glicocalice come un'eclissi morbida e silenziosa, trasformando i filamenti gelidi in blu indaco e quasi-nero, mentre i margini illuminati della foresta continuano a risplendere con quella qualità acquosa e carica ionicamente che è meno luce e più campo elettrostatico. Ogni superficie è bagnata, semi-trasparente e molecolarmente granulare: i gruppi solfato si presentano come minuscoli nodi irrisolti lungo ciascun filamento, e il plasma tutt'intorno porta una qualità quasi particolata ai margini della visione, rendendo l'orizzonte lattiginoso e indistinto, così che il mondo si restringe su se stesso e ciò che esiste è soltanto questo — la foresta ramificata e debolmente luminosa che sale lentamente verso di te, la sua struttura a reticolo che inizia già a stringersi attorno al bordo anteriore della tua vasta superficie curva nel momento inevitabile del contatto.
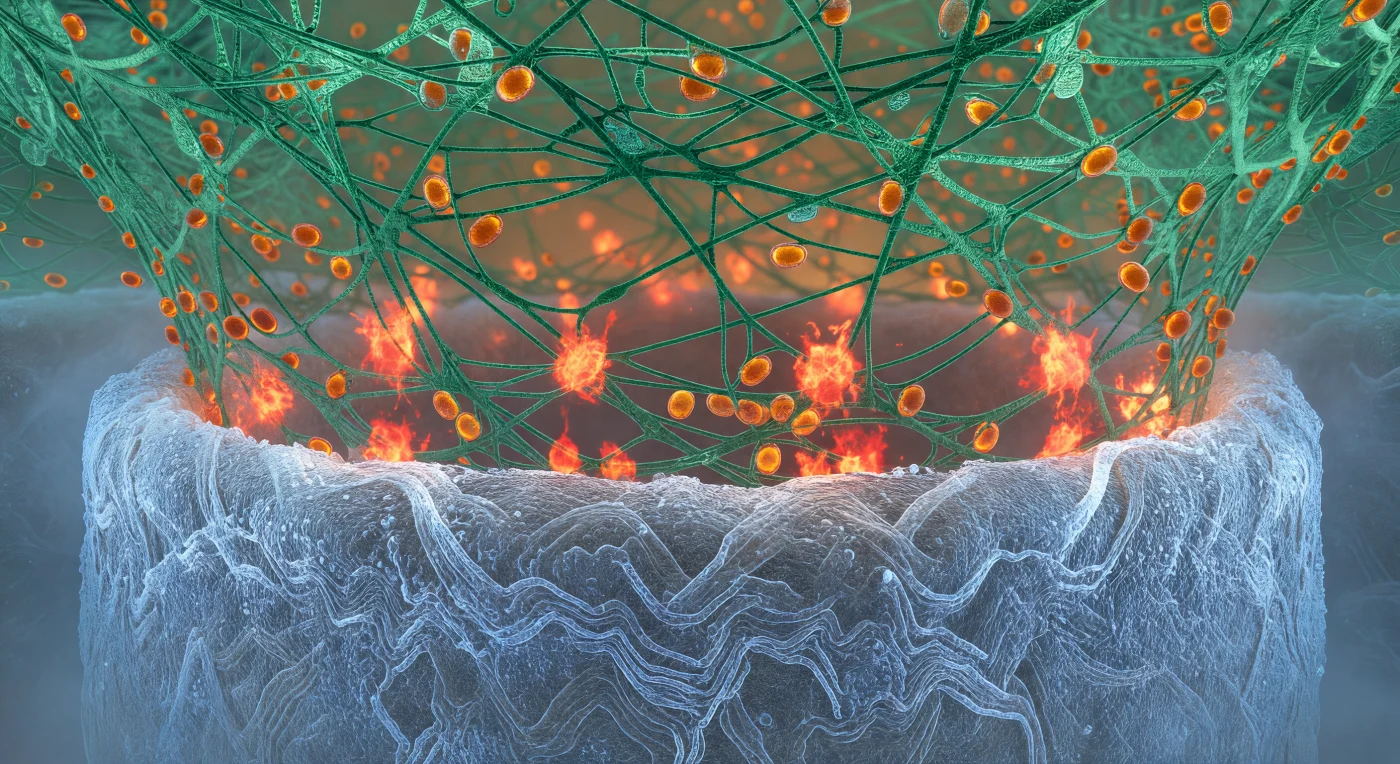
Ti trovi schiacciato tra due architetture biologiche di scala monumentale, testimone di una guerra chimica combattuta a colpi di molecole. Sotto di te, la parete del filamento fungino si estende come lo scafo di una nave colossale — una superficie densa di fibre di chitina intrecciate che brilla di una luminescenza bianco-azzurra spettrale, rigida e antica come basalto, le cui curvature si perdono in una foschia blu ai lati, troppo vaste per essere contenute nel campo visivo. Dall'alto e da ogni lato, la culla di actina del neutrofilo cala intorno a te come un'impalcatura di cavi viridiani in tensione: filamenti di F-actina ramificati e densamente reticolati stringono la ifa con la precisione organizzata di un meccanismo di cattura, i fili più vicini taglienti e lucenti di una luce resinosa, quelli più profondi dissolti in una nebbia giada. Alla zona di contatto tra le due strutture, violente scariche rossearancio eruttano in impulsi irregolari — ciascuna un nodo concentrato di specie reattive dell'ossigeno che deflagra come un lampo fotografico al rallentatore, illuminando dal basso le fibre di actina con bagliori di rame, trasformando l'interfaccia in un fronte di combustione lenta e smoldering. Attraverso il reticolo verde, granuli azzurofili color ambra derivano in processione silenziosa lungo i cavi di actina verso il fronte di reazione, ognuno una riserva sigillata di enzimi letali che si avvicina alla propria detonazione.
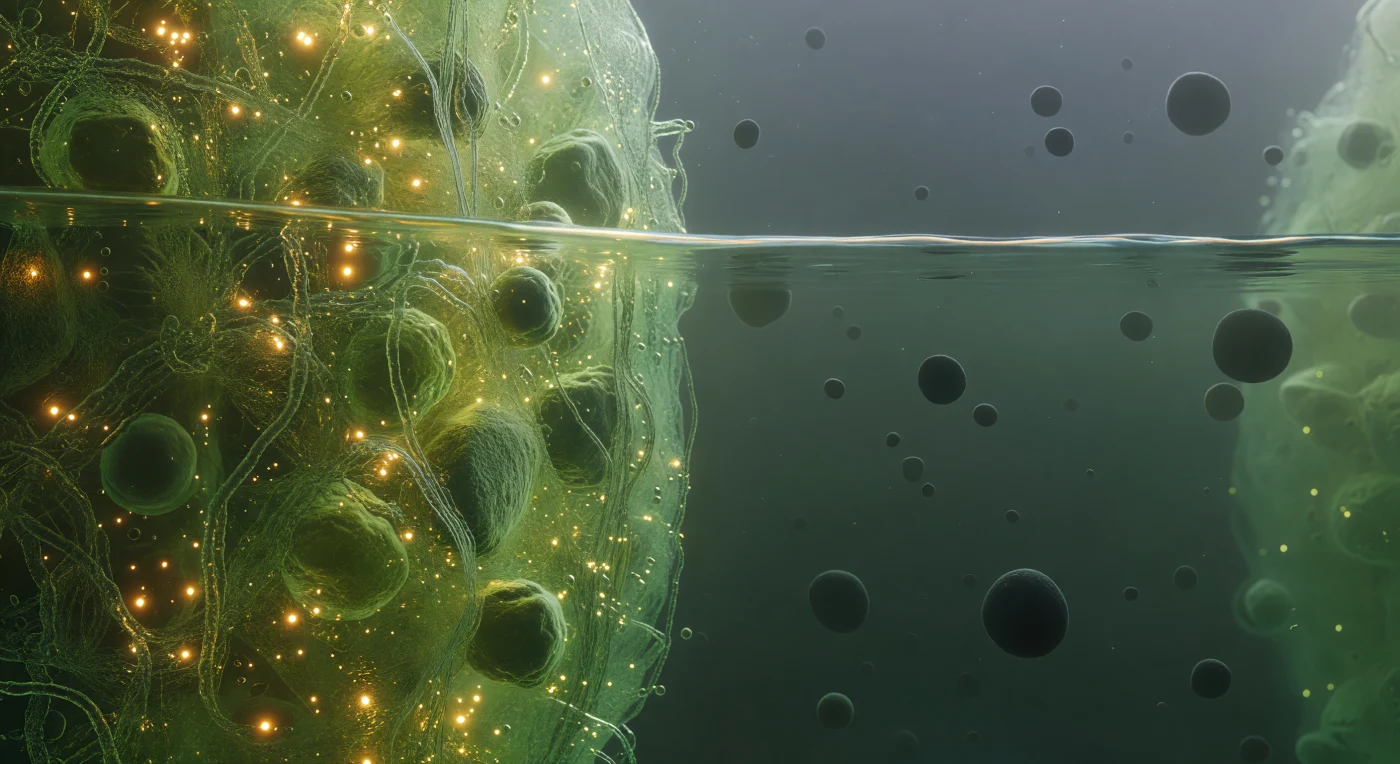
Ti trovi esattamente al confine tra due mondi, la tua posizione divisa con precisione netta tra l'interno di un granulo da stress e il citoplasma circostante: alla tua sinistra, la fase condensata si dispiega come un mare denso e luminoso di verde-oro, un mezzo così saturo di catene di mRNA aggrovigliate e proteine disordinate che la luce sembra rallentare e accumularsi nella rete molecolare, pulsando debolmente con il tremore browniano di diecimila macromolecole premute l'una contro l'altra. Direttamente davanti a te, la discontinuità termodinamica della separazione di fase liquido-liquido si manifesta come un'interfaccia tremante e precisa — non un gradiente ma una vera superficie di tensione, paragonabile al confine tra olio e acqua, illuminata dall'interno della condensata in modo da proiettare una sottile linea caustica iridescente che oscilla a scala nanometrica. Alla tua destra il mondo si apre in una foschia verde-azzurra diffusa, il citoplasma diluito, dove singoli ribosomi derivano come sfere opache e scure, ciascuno immenso rispetto alla foschia di fondo, separati da distanze che sembrano praterie aperte dopo la claustrofobia dell'interno condensato. Questo confine che calpesti — il solo vero bordo in un paesaggio altrimenti fluido e probabilistico — è la struttura più nitida che esista in questo universo molecolare vivente.

Ci si trova sospesi nell'interstizio acquoso tra due pareti epiteliali colossali, orientati lungo l'interfaccia cella-cellula dove la geometria dell'incontro tra le due membrane rivela la sua architettura in tutta la sua complessità stratificata: una cintura cremisi di proteine della giunzione occludente — claudine, occludina, ZO-1 — forma un sigillo continuo e incandescente che cinge l'intera periferia cellulare come una sutura di metallo fuso, separando ermeticamente il lume tubulare soprastante, un vuoto oscuro e cavernoso, dallo spazio basolaterale sottostante. Immediatamente al di sotto, una seconda banda di giunzioni aderenti emanates una luce verde smeraldo più morbida e traslucida, dove i domini extracellulari delle E-caderine si intrecciano attraverso il clivaggio intercellulare con la precisione molecolare di dita che si stringono, mantenendo la coesione meccanica del tessuto mentre le due membrane laterali, pressate in apposizione a meno di venti nanometri di distanza, scorrono verso il basso come tende di grafite iridescente disseminate di proteine. Più in profondità nei corpi cellulari, enormi nuclei ovoidali irradiano una luminescenza indaco attraverso la loro busta nucleare porosa, come vetrate illuminate dall'interno di una cattedrale gotica, trasformando l'intera scena in una geometria liturgica dove le giunzioni sono il piombo che tiene uniti i pannelli di vetro colorato. Questa architettura non è semplice adesione: è un dispositivo fisiologico di precisione che governa il trasporto selettivo di ioni e soluti attraverso l'epitelio renale, una frontiera molecolare da cui dipende l'omeostasi dell'intero organismo.




















