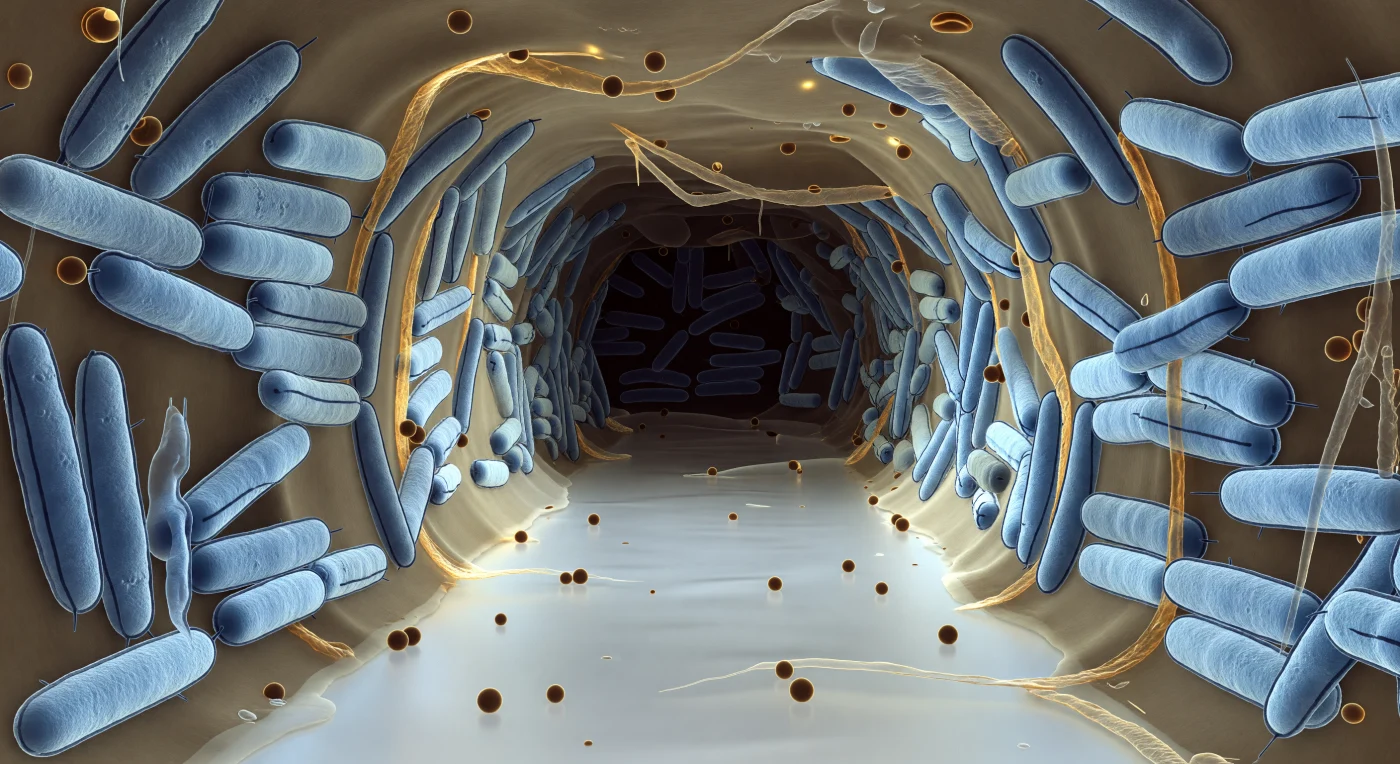
Au fond de ce couloir livide, les parois s'élèvent de chaque côté comme des immeubles taillés dans la glace — des bâtonnets d'*Escherichia coli* serrés flanc contre flanc, teintés d'un bleu arctique, chacun ceint de deux lignes sombres et parallèles qui trahissent la double membrane caractéristique des bactéries à Gram négatif, ce rempart moléculaire de sept à dix nanomètres d'épaisseur répété à l'infini jusqu'au flou bleu-gris de la profondeur de champ. Entre eux, la matrice d'exopolysaccharides — cette substance ambrée quelque part entre le miel et le verre dépoli — soude l'édifice entier, constituant l'échafaudage collectif du biofilm, une architecture vivante où des millions de cellules partagent ressources, signaux chimiques et protection contre les antibiotiques. Dans le vide lumineux du canal, des vésicules de membrane externe dérivent comme des perles de résine translucide, chacune un ballot clos transportant enzymes, fragments d'ADN et molécules de signalisation d'une cellule à l'autre à travers ce réseau hydraulique primitif. Le corridor lui-même est une infrastructure de survie : creusé collectivement dans la masse du biofilm, il achemine l'oxygène dissous et les nutriments vers les couches intérieures selon un gradient qui s'éteint progressivement, le blanc argenté de l'entrée se muant en brun sombre là où la densité de la matrice étrangle enfin toute diffusion moléculaire. L'ensemble exhale la quiétude trompeuse d'une coupe cryo-FIB-SEM figée en un instant — mais chaque membrane vibre, chaque ribosome traduit, et ce labyrinthe chimiquement actif prospère dans une indifférence absolue à l'œil qui le traverse.

Vous flottez dans le liquide extracellulaire, suspendu face à la paroi de la membrane plasmique d'un lymphocyte T qui se déploie dans toutes les directions comme la falaise abyssale d'une fosse océanique, son feuillet lipidique irisé de bleus et de violets froids, hérissé de récepteurs CD4 et de filaments glycocalyciaux translucides se balançant dans la densité visqueuse du milieu. Autour de vous dérivent des dizaines de virions du VIH-1, chacun une sphère de cent vingt nanomètres à peine, son intérieur gris-bleu fumeux laissant deviner la silhouette conique de la capside, sa surface parsemée de couronnes trimériques gp120-gp41 dorées comme des lanternes éteintes sur une bouée nocturne. Ce mouvement n'est pas de la nage : c'est l'agitation brownienne pure, la chaleur du milieu elle-même qui secoue, pousse et déplace chaque particule sans intention ni direction, la physique statistique se substituant à toute volonté. Les virions les plus proches de la membrane s'y enfoncent déjà dans la forêt glycocalyciale, leurs spics dorés progressant vers les sites d'ancrage comme si la chimie seule décidait de ce qui doit inévitablement se produire, les enveloppes les plus proches s'aplatissant légèrement contre la vaste paroi cellulaire. La lumière ici n'a ni source ni ombre, seulement cette luminescence diffuse bleu-gris de cryo-microscopie qui dilue toute perspective et transforme les virions lointains en étincelles chaudes se dissolvant dans la brume protéique du milieu extracellulaire.

Vous vous trouvez au fond d'un canyon dont les parois ne sont pas de la roche mais de la membrane — la membrane interne mitochondriale s'élevant en plis convolutés sur des centaines de longueurs de corps, sa surface d'un brun charbonneux profond marquée par la coloration à l'osmium, hérissée de milliers de complexes ATP synthase dont les têtes F1 arrondies s'inclinent vers vous comme autant de champignons ancrés dans une falaise vivante. La matrice dans laquelle vous baignez n'est ni air ni eau : c'est un collier dense et ambré, un colloïde protéique concentré à plus de 500 milligrammes par millilitre, qui diffuse chaque photon en une lueur volumétrique dorée et presse contre vous des enzymes du cycle de Krebs — des blocs globulaires aux surfaces feuilletées de brins bêta et d'hélices alpha que vous pourriez presque effleurer du doigt. Des ribosomes mitochondriaux flottent à proximité comme des monolithes asymétriques traversés d'un tremblement brownien si constant qu'il se confond avec l'immobilité, tandis que des boucles d'ADN mitochondrial décrivent des arcs superenroulés dans la brume, leur squelette nucléotidique teinté d'un bleu-blanc pâle par la fausse couleur cryo-EM. Au loin, la jonction des crêtes se resserre en un corridor étroit et incandescent entre deux parois membranaires qui se rapprochent presque jusqu'au contact, les têtes F1 y formant un plafond cobblestone baigné d'or chaud, au-delà duquel s'ouvre une nouvelle chambre dont la paroi se perd dans la profondeur atmosphérique ambrée — une architecture biologique pure, respirante, vivante et géologique dans chaque direction.
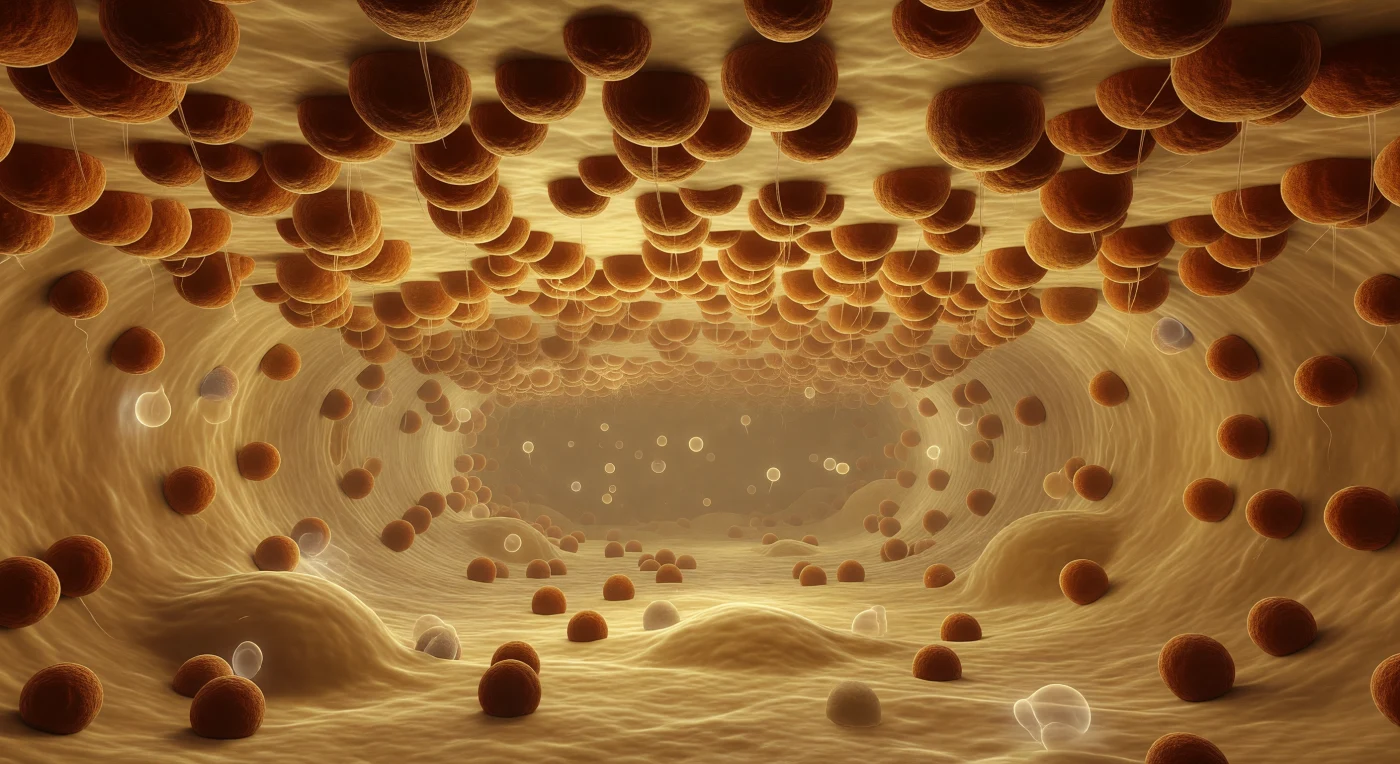
Vous dérivez en suspension dans la lumière du réticulum endoplasmique rugueux, enveloppé d'une clarté diffuse couleur miel dilué qui émane du milieu aqueux lui-même, dense de protéines fantomatiques dérivant lentement autour de vous comme des présences translucides. Au-dessus, s'étendant jusqu'à chaque horizon sans la moindre interruption, un plafond de bicouche lipidique — crème et ocre chaud, légèrement ondulé — disparaît entièrement sous une croûte serrée de ribosomes : des sphères massives couleur rouille et ombre brûlée, chacune d'environ vingt-cinq nanomètres, assemblées avec la densité ininterrompue de bernacles soudés à une coque, leurs sous-unités asymétriques imprimant de légères déformations dans la membrane comme des empreintes dans de la cire tiède. De chaque ribosome descend un fil presque invisible de polypeptide naissant qui capture par instants la lumière intérieure en un reflet irisé avant de se dissoudre dans la brume dorée du corridor — car le réticulum se révèle ici comme une nef de cathédrale, le plafond encroûté de machines traductionnelles se répercutant en perspective jusqu'à un point de fuite noyé dans une pénombre ambrée, la membrane inférieure tout aussi couverte de ribosomes lui faisant face à distance serrée. Ce que vous percevez n'est pas un décor mais un procédé industriel ininterrompu : la cellule fabrique ses protéines destinées à la sécrétion et aux membranes en continu, sans pause, sans conscience, dans chaque direction à la fois, et l'encombrement macromoléculaire total de cet espace — trop dense pour être traversé librement — vous rappelle que vous êtes moins un observateur qu'une particule supplémentaire perdue dans la machinerie.

Depuis la frontière absolue de la cellule, la vue plonge vers l'intérieur d'un labyrinthe de filaments d'actine de 7 nanomètres de diamètre, organisés en un réseau fractal de branchements à soixante-dix degrés émergeant des complexes Arp2/3 — ces nœuds denses qui orchestrent la polymérisation dirigée permettant à la cellule de migrer, de sentir, d'envahir. Le substrat obsidien en dessous est illuminé par une onde évanescente à pénétration sub-longueur d'onde, révélant uniquement les structures qui affleurent la surface : les plaques d'adhésion focale brûlent d'un ambre chaud, zones d'ancrage mécanique où les intégrines transmembranaires transmettent les forces entre l'actine intracellulaire et la matrice extracellulaire, convertissant la tension mécanique en signaux biochimiques. Sur les flancs, des filopodes s'élancent dans le vide extracellulaire comme des antennes solitaires, chaque faisceau d'actine parallèle sondant l'espace chimique environnant à la recherche de gradients de guidage — chémokines, rigidité du substrat, topographie moléculaire. La brume bleu-gris qui emplit l'espace interfilamentaire n'est pas un artefact mais une réalité physique : l'encombrement macromoléculaire, à des concentrations de trois cents à quatre cents milligrammes par millilitre, transforme le cytoplasme en un milieu viscoélastique où la diffusion elle-même obéit à d'autres lois, et où chaque filament vibre sous l'agitation thermique permanente d'un monde où le bruit brownien gouverne tout.

Vous dérivez dans le nucléoplasme dense comme dans un milieu visqueux chargé d'une phosphorescence froide et diffuse, et devant vous, le complexe du pore nucléaire s'impose comme un portail monumental d'environ 120 nanomètres de diamètre — une rosette dorée à symétrie octuple, incrustée dans la double enveloppe nucléaire sombre comme un médaillon de bronze oxydé serti dans du charbon. Ses huit sous-complexes protéiques rayonnent avec une précision architecturale organique, leurs arcs cuivrés convergeant vers un axe central d'où pendent les filaments de nucléoporines FG tels un rideau de perles ivoire translucides, ondulant lentement et s'écartant parfois au passage d'une molécule cargo en transit. De part et d'autre du pore, les masses d'hétérochromatine s'élèvent en falaises irrégulières d'indigo profond — chromatine compactée, chargée de nucléosomes, absorbant toute lumière ambiante — tandis que derrière vous, l'euchromatine plus lâche se déploie en un voile lavande pâle, parsemé de condensats sphéroïdes aux surfaces luisantes issus de séparation de phase liquide-liquide. Ce complexe n'est pas une simple ouverture mais un filtre moléculaire hautement sélectif, orchestrant le trafic bidirectionnel de milliers de molécules par seconde entre deux compartiments aux identités biochimiques radicalement distinctes.

Devant vous s'élève une tour de quinze disques membranaires empilés avec une précision absolue — le granum —, chacun émettant un vert émeraude profond et intrinsèque, non pas coloré mais vivant, issu des milliers de complexes protéiques du photosystème II et des antennes collectrices de lumière noyés dans la bicouche lipidique. Entre chaque membrane, un mince espace luminal d'un jaune citron pâle sépare les disques comme des joints lumineux dans une maçonnerie translucide, où les protons migrent en gradients invisibles mais presque perceptibles dans la légère asymétrie de la lumière. La surface de chaque disque se résout, à cette proximité, en une mosaïque de têtes protéiques légèrement saillantes, si densément tassées qu'elles laissent à peine entrevoir la membrane lipidique nue en dessous. Des lamelles stromales s'étendent horizontalement comme des rubans d'émeraude, reliant cette tour aux colonnes voisines estompées dans le brouillard macromoléculaire du stroma, tandis que des plastoglobules — sphères ambrées et luisantes, riches en lipides — dérivent parmi les masses pâles et irrégulières des complexes RuBisCO qui encombrent chaque ligne de vue. L'ensemble baigne dans une lumière omnidirectionnelle sans source, filtrée par les couches de chlorophylle qui enveloppent cet espace intérieur d'une forêt de vert superposé, à la fois absorbant et rayonnant.
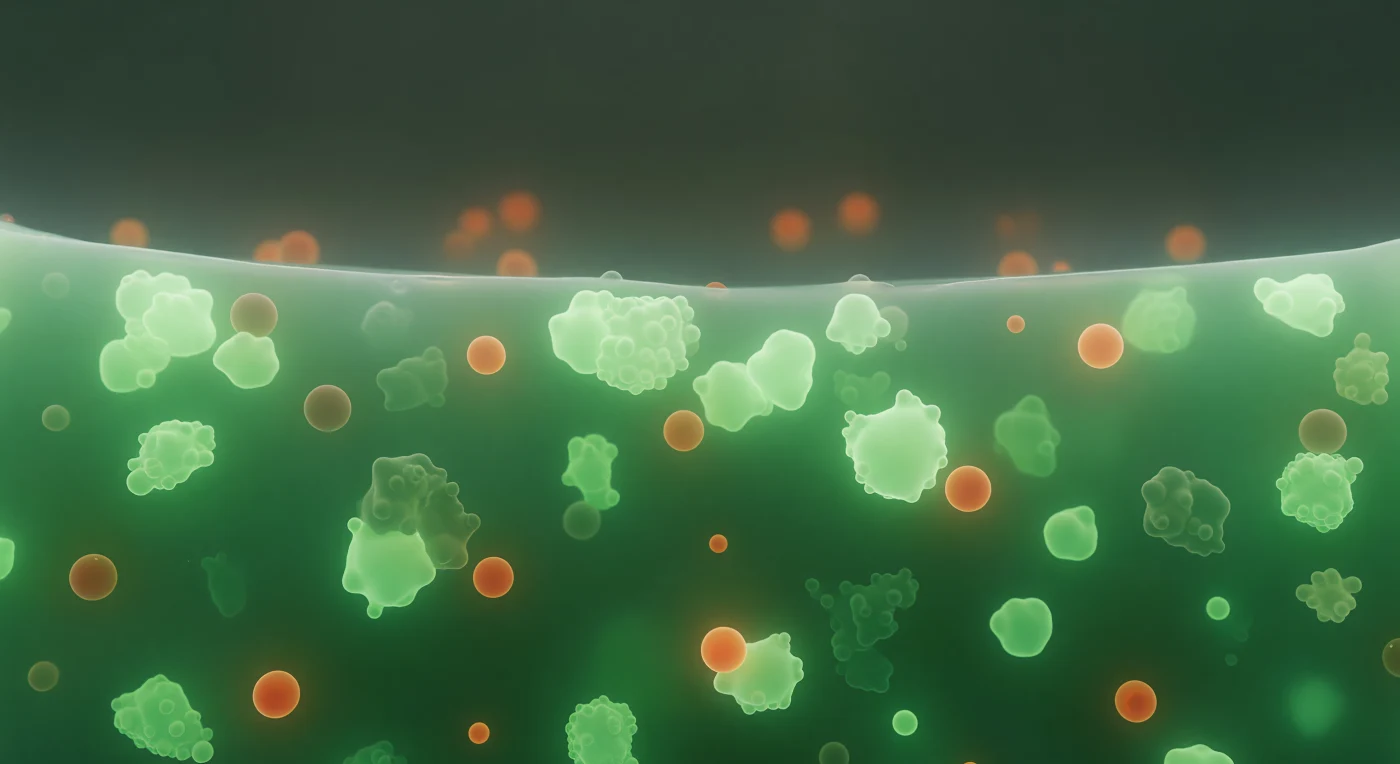
Vous flottez au cœur d'un granule de stress, suspendu dans un milieu viscoélastique qui n'est ni liquide ni solide, mais quelque chose d'intermédiaire — une brume émeraude dense et doucement bioluminescente émanant de la matrice moléculaire elle-même, portée par les protéines G3BP1 fluorescentes qui saturent cet espace de leur lueur froide et diffuse. Des nœuds plus brillants émergent par endroits dans le haze vert, là où des complexes ARNm-protéines se sont condensés en amas plus denses, leurs contours fondus dans la matière environnante par l'agitation thermique permanente qui ne laisse aucune frontière nette exister. Des sphères ambre-orangées dérivent lentement parmi eux — des co-condensats enrichis en TIA1, dont la chaleur rougeoyante tranche la lumière froide comme des braises dans du brouillard, témoins d'une séparation de phases liquide-liquide où deux compositions moléculaires distinctes coexistent sans se mélanger. À la périphérie, visible comme un horizon absolu, la limite du granule se dresse en une muraille abrupte où la densité verte s'effondre en un seul précipice pour laisser place au cytoplasme dilué, presque obscur — une frontière maintenue non par une membrane mais par les seules forces d'interface thermodynamique qui gouvernent l'organisation de la matière vivante à cette échelle.

Suspendu au-dessus de l'axe central du moteur flagellaire, le regard plonge vers le bas à travers les membranes concentriques d'une bactérie comme dans la coupe transversale d'une cathédrale mécanique vue depuis sa voûte — les anneaux L, P et MS se déploient en halos emboîtés de bronze oxydé et d'acier sombre, chacun serti dans sa couche membranaire respective avec la précision d'une pièce d'horlogerie évoluée sur des milliards d'années. Dix-sept complexes statoriques MotA/MotB ceinturent le rotor en symétrie radiale quasi parfaite, masses asymétriques et trapues pressées contre la membrane interne comme des contreforts monolithiques autour d'une turbine, leurs interfaces moléculaires captant la lumière ambiante en reflets d'étain mat. La filament flagellaire s'élève en spirale hors du champ, vrillé comme un câble vivant dans le milieu extracellulaire légèrement trouble, tandis que la région du crochet assure la jonction entre rotor et filament avec la rigueur d'un joint mécanique étanche. Ce que l'on contemple n'est pas une structure figée : chaque interface protéique porte l'empreinte d'une fonction ininterrompue, polie par le mouvement, l'ensemble témoignant d'une architecture parfaitement accordée pour tourner sans relâche dans l'obscurité de l'organisme vivant.

Au pied de cette forêt de cils, le regard monte le long de centaines de colonnes cylindriques bleu-cyan qui s'élèvent vers une canopée distante, leurs surfaces portant le reflet légèrement humide d'une céramique vernissée, tandis que la plaine épithéliale ocre s'étend en dessous comme un lit de rivière asséché, ses jonctions serrées formant des crêtes de crème pâle aux géométries précises. Chacun de ces cils — un axonème de 200 nanomètres de diamètre armé de neuf doublets de microtubules et d'un axe central, le tout baigné de dynéines moléculaires consommant de l'ATP — participe à une onde métachrone, ce ballet coordonné où chaque rangée se penche légèrement en décalage par rapport à la suivante, créant une impression de vent minéral figé dans la pierre traversant la voûte de cils. Entre les tiges les plus proches, des filaments d'or ambré — le mucus viscoélastique piégeant pathogènes et particules — tendent leurs arches caténaires translucides à la façon d'un lustre de résine organique, s'amincissant en fils capillaires là où la tension de surface les ancre contre chaque colonne. La lumière ici n'a pas de source identifiable : elle émane du cytoplasme sous-jacent et des shafts eux-mêmes, baignant les corridors étroits d'une ombre indigo profonde tandis que les travées plus larges s'illuminent d'un blanc-bleu froid — un organe qui respire sans jamais en avoir conscience, et dont chaque battement déplace un monde entier.
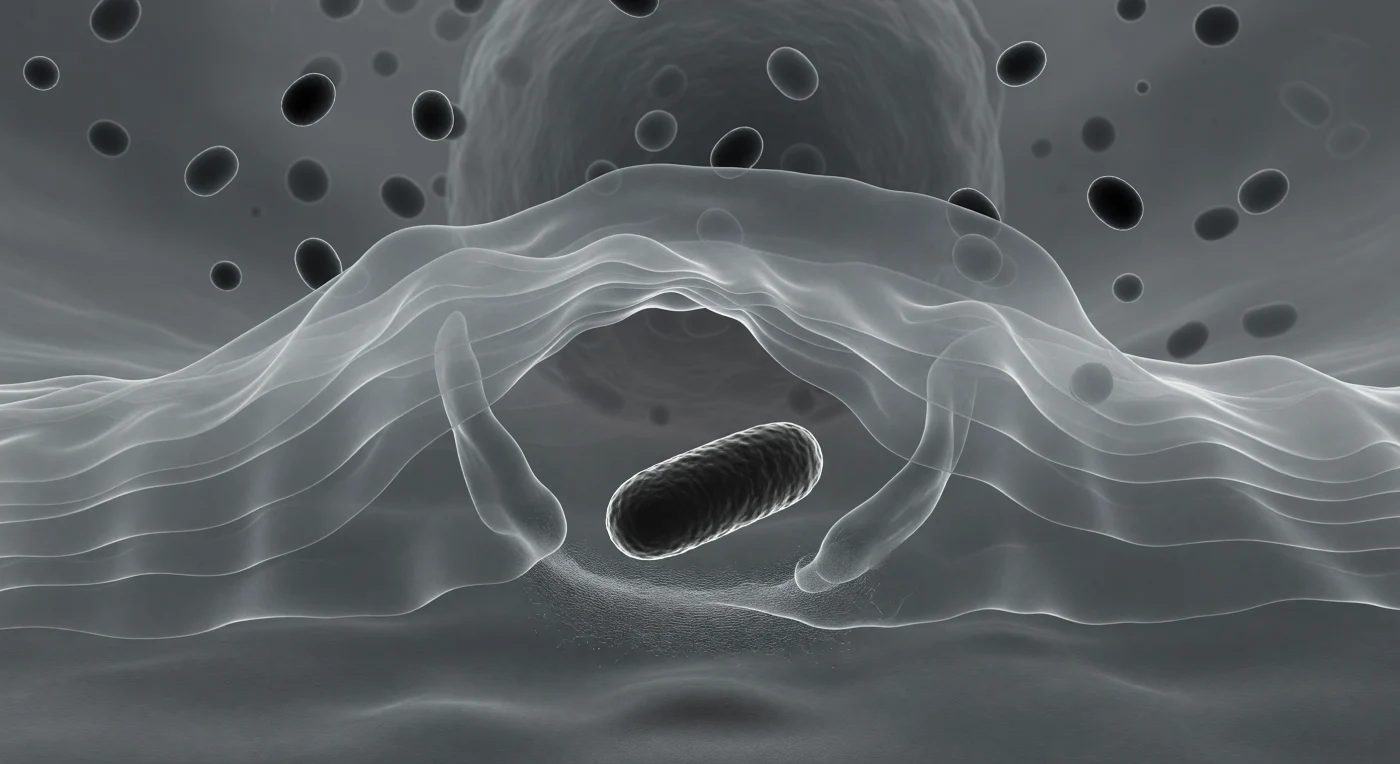
Vous vous trouvez à l'extrême pointe d'un pseudopode de macrophage en plein acte d'engloutissement, porté par le voile cytoplasmique translucide qui s'incurve en avant comme une vague figée dans son élan — à quelques micromètres à peine, une bactérie en forme de bâtonnet se dresse telle un monolithe sombre, déjà encerclée par les deux bras membranaires qui se referment sur elle avec la lenteur inexorable d'une étreinte. Le matériau qui vous entoure est le lamellipode, une structure enrichie en filaments d'actine polymérisée dont le réseau serré confère à ce voile sa rigidité étrange, ni liquide ni solide, oscillant entre le gel et la membrane vivante sous la tension d'une dynamique de treadmilling incessante. Derrière vous, dans l'épaisseur croissante du cytoplasme, les granules lysosomiaux attendent — des compartiments acides chargés d'hydrolases capables de digérer la paroi bactérienne dès que la membrane phagosomale se sera refermée, fusionnant avec eux pour former le phagolysosome. Tout ici est rendu en nuances de gris DIC, chaque structure révélée non par la couleur mais par son indice de réfraction, chaque bord dessiné d'un halo lumineux qui trahit la densité optique de la matière vivante traversée par la lumière transmise.

Vous vous trouvez suspendu au creux le plus profond d'un érythrocyte humain, au nadir d'un bassin membranaire qui s'étend à la manière d'un immense cratère d'impact aux teintes ambrées, sa surface dorée et translucide révélant en filigrane le réseau hexagonal des filaments de spectrine — l'armature cytosquelettique invisible à l'échelle ordinaire, ici perceptible comme une dentelle géodésique gravée sous du verre caramélisé. La lumière oblique du faisceau d'électrons secondaires frappe la membrane avec une précision chirurgicale, sans diffusion ni haze, dessinant des ombres nettes dans la dépression centrale et faisant briller chaque crête de la bicouche lipidique comme du bronze poli — un matériau biologique qui se tient quelque part entre le métal vivant et la soie humide. À mi-distance, les érythrocytes voisins se sont empilés en rouleaux, ces colonnes de disques biconcaves pressés face à face qui évoquent des falaises de grès surgissant d'un plasma couleur de paille, tandis que des plaquettes hérissées — irrégulières, étoilées, couvertes de fines projections membranaires — dérivent dans le sérum interstitiel, suspendues sans se déposer dans un milieu dont la viscosité non-newtonienne à cette échelle dépasse toute intuition humaine. Ce monde est entièrement fait de surfaces biologiques et de fluide, intime et planétaire à la fois, un paysage où chaque polymère, chaque courbure de membrane et chaque agrégat de glycoprotéines devient un relief géographique à part entière.
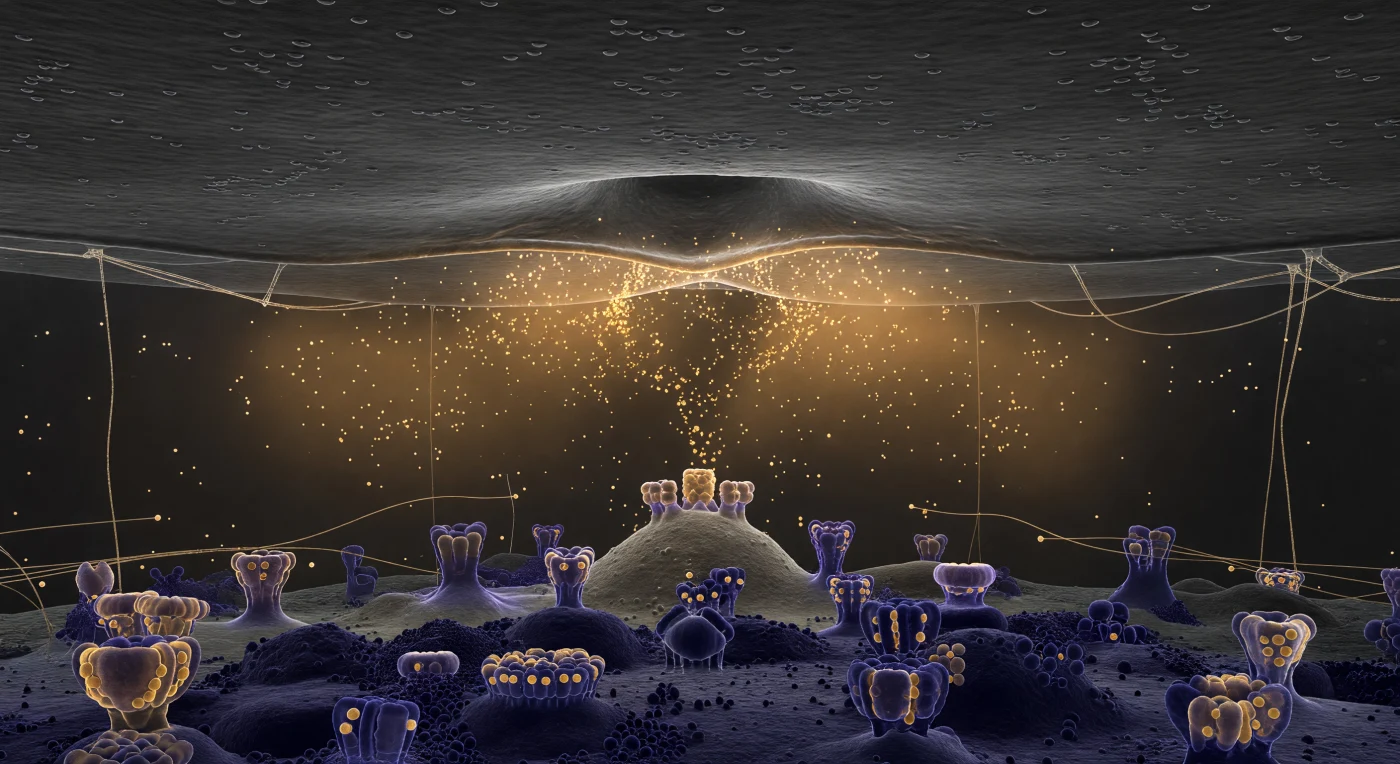
Vous flottez suspendu dans la fente synaptique, corridor si étroit que son plafond et son plancher s'offrent simultanément à votre regard, séparés d'une distance à peine plus grande que l'envergure de vos bras tendus — vingt-cinq nanomètres de vide aqueux qui constituent l'un des espaces les plus critiques du système nerveux. Au-dessus, la membrane présynaptique s'étend comme une plaine de charbon sombre et ondulante, et en son centre une vésicule synaptique achève sa fusion en un omega parfait, déversant dans le couloir une marée ambrée de neurotransmetteurs — glutamate ou acétylcholine — qui se diffusent latéralement en nuages dorés, guidés par le seul gradient de concentration selon les lois de la diffusion brownienne. De fines cordes translucides de protéines d'adhésion synaptique et de filaments matriciels extracellulaires traversent l'espace de plafond à plancher, captant la lumière dorée en minces lignes de reflet, rappelant que cette fente n'est pas un vide inerte mais un milieu structuré et réfractif. En bas, la densité postsynaptique se dresse comme un paysage architectural de violet sombre et compact, hérissé de récepteurs AMPA et NMDA qui émergent tels des formations rocheuses anciennes, leurs faces supérieures renvoyant le halo ambré des molécules qui arrivent et déclenchent, en quelques millisecondes, la conversion d'un signal chimique en courant ionique.
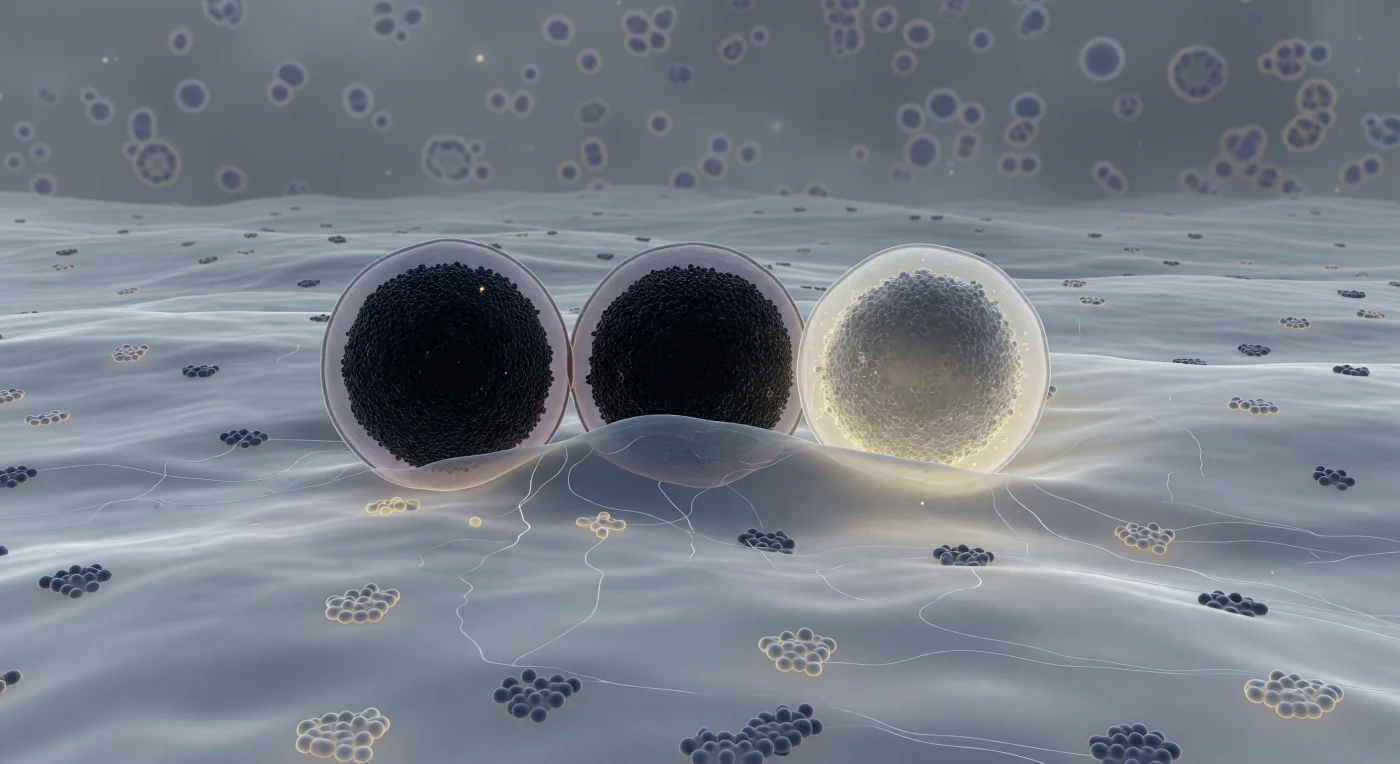
Vous vous trouvez suspendu contre la face cytoplasmique de la membrane plasmique d'une cellule bêta pancréatique, immergé dans un univers aux tonalités de graphite et d'ambre pâle que seule la microscopie électronique à transmission sait révéler : un vaste plan ondulant de bicouche lipidique s'étire jusqu'à chaque horizon, semé de complexes protéiques enchâssés comme des monuments dans une plaine vivante, ses domaines riches en cholestérol luisant par endroits d'un éclat légèrement plus ordonné. Trois granules sécrétoires d'insuline s'imposent dans le champ visuel comme des bâtiments sphériques — le premier arrimé à la membrane en un contact intime et hermétique, son cœur cristallin de zinc-insuline si dense qu'il absorbe presque toute lumière ; le deuxième engagé dans une hémi-fusion où les deux bicouches commencent à s'interpénétrer, la membrane se creusant en un doux sillon d'identité lipidique indécise ; le troisième déjà passé de l'autre côté, son noyau opaque se dissolvant en un halo chaud d'ivoire jaunâtre qui se disperse dans l'espace extracellulaire lumineux. Entre ces colosses, un réseau lâche de filaments d'actine corticale court comme du givre sur verre, tandis que le cytoplasme profond recule en une obscurité structurée, saturée de ribosomes et de membranes d'organites estompées comme un fond marin vu d'en bas. Tout est suspendu dans un instant figé, mais la membrane à demi-fusionnée et le cœur en cours de dissolution semblent retenir leur souffle — pris en plein milieu d'un acte thermodynamiquement irréversible par lequel des millions de molécules d'insuline s'apprêtent à rejoindre la circulation sanguine.

Vous planez au ras des sommets de la bordure en brosse, suspendu à la hauteur exacte des extrémités des microvillosités qui tapissent l'entérocyte en dessous — un champ infini de cylindres de cent nanomètres de diamètre, serrés comme les cellules d'un basalte biologique, leurs parois légèrement striées par les faisceaux d'actine qui les arment intérieurement. Une lumière oblique ambrée rake la surface depuis la droite, sculpte des ombres en croissant sur le flanc de chaque fût et transforme la plaine tout entière en un bas-relief d'une régularité presque minérale, les gorges étroites entre les villosités noyées dans une obscurité aqueuse dense en protéines. De chaque sommet monte le glycocalyx, cette forêt de filaments polysaccharidiques de quelques nanomètres d'épaisseur à peine qui fusionne, de touffe en touffe, en un pelage continu d'ivoire vieux et de brume bleutée — filtre moléculaire vivant où enzymes membranaires et nutriments partiellement digérés se croisent dans une agitation brownienne incessante. Regarder vers le bas entre les fûts, c'est plonger du regard dans un canyon dont le fond ochre — le cytoplasme de la cellule — disparaît dans l'obscurité comme un plancher abyssal, rappelant que cette architecture d'une précision quasi cristalline est avant tout vivante, capturée dans l'instant d'une vie ininterrompue.

Vous flottez au cœur géométrique d'une cellule en division, suspendu à l'équateur exact où deux masses chromosomiques indigo-violet s'éloignent lentement vers leurs pôles respectifs, tirées par des câbles de tubuline d'un vert électrique intense — les fibres kinétochoriques, épaisses comme des cordages sous tension maximale, leurs surfaces légèrement striées révélant la densité de marquage de chaque sous-unité protéique. Depuis deux foyers centrosomaux lumineux, éblouissants comme des étoiles froides perdues dans l'obscurité cytoplasmique, des dizaines de microtubules rayonnent en tous sens et se croisent à votre niveau en un treillis tridimensionnel de lumière verte phosphorescente, les fibres interpolaires glissant les unes contre les autres en chevrons serrés qui forment autour de vous des parois de jade fluorescent. Directement à votre hauteur, le corps intermédiaire barre le champ visuel comme une ligne de feu blanc-vert d'une densité aveuglante — une zone de chevauchement antiparallèle où les microtubules se compriment en un faisceau si compact qu'il surpasse en éclat tout le reste de la scène, entouré d'un halo diffus de brume fluorescente. Au-delà de ce réseau lumineux, le cytoplasme s'étend en un noir absolu, non pas vide mais saturé de macromolécules invisibles dont la présence se trahit dans la façon dont la lumière verte se disperse doucement aux bords des fibres, diffusée en auréoles laiteuses par l'encombrement moléculaire avant de se fondre dans l'obscurité. Ce fuseau mitotique est une machine d'hérédité à l'œuvre — un édifice de polymères protéiques dynamiques dont chaque câble, chaque tension, chaque déplacement orchestre la transmission fidèle du génome en deux cellules filles identiques.

Vous dérivez dans le milieu argenté pâle du plasma sanguin, suspendu face à une paroi biologique immense qui occupe toute la moitié inférieure de votre champ de vision : la membrane endothéliale elle-même n'est qu'une ligne de charbon sombre à peine entrevue en profondeur, noyée sous la forêt dense du glycocalyx, une épaisseur de polymères biologiques de un à deux micromètres qui s'élève vers vous comme une canopée de cathédrale. Les brins d'héparane sulfate s'arquent et se ramifient en filaments bleu-argent translucides — comparables à des branches de bouleaux hivernaux vus à l'extrême grossissement — reliés latéralement par des ponts gossamer qui donnent à l'ensemble la qualité d'un brouillard lumineux rendu solide, oscillant avec lenteur sous la pression viscoélastique du plasma environnant. Cette structure n'est pas un simple revêtement passif : elle régule l'échange de signaux mécaniques et chimiques entre le sang circulant et la cellule endothéliale sous-jacente, filtre le passage des molécules, et protège la membrane contre les contraintes de cisaillement du flux sanguin. Votre propre ombre — le grand dôme biconcave de votre érythrocyte en approche — se projette sur la canopée comme une éclipse diffuse, virant les filaments de bleu glacé à l'indigo puis au noir de charbon, tandis que les marges illuminées brillent de cette lueur aqueuse et froide propre à la fausse couleur cryo-TEM au rouge de ruthénium, comme si la lumière elle-même portait une charge ionique.
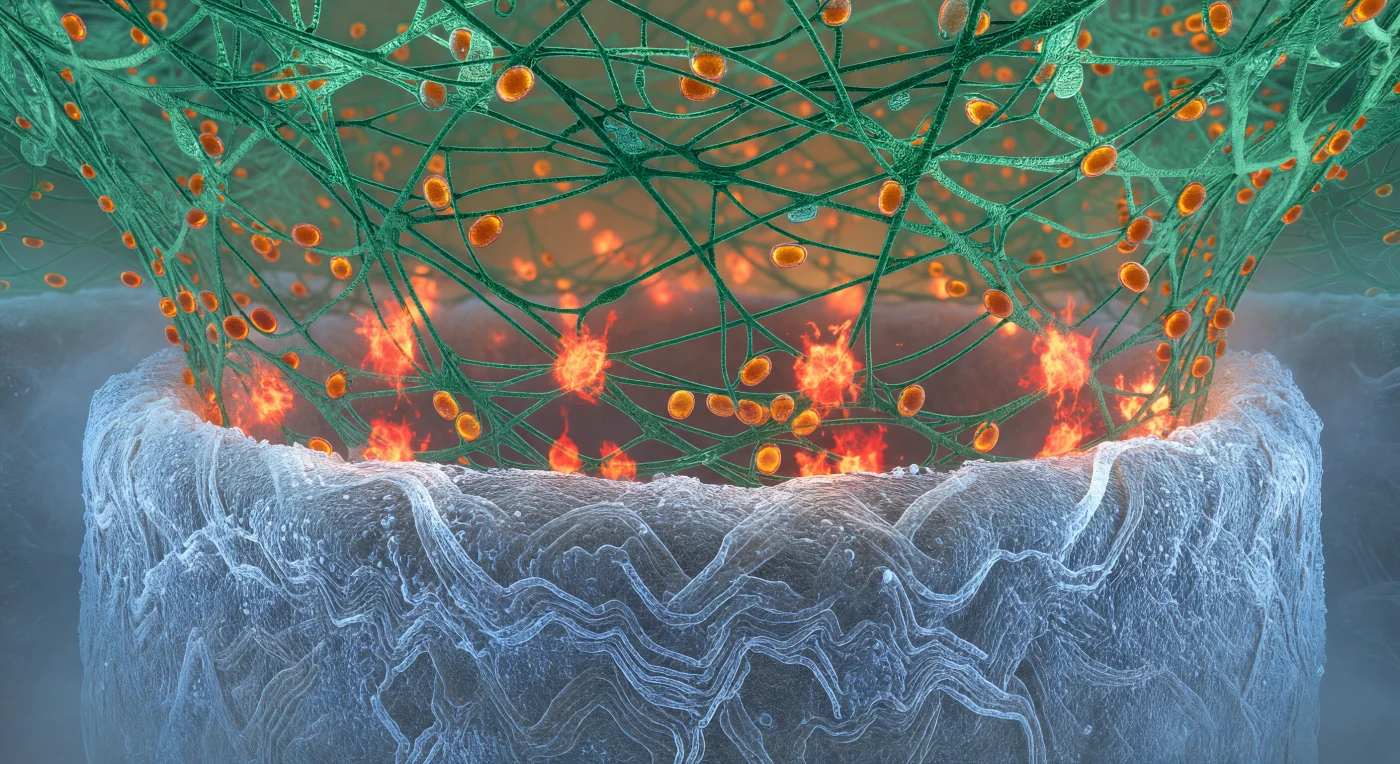
Vous vous trouvez écrasé entre deux architectures biologiques d'une brutalité architecturale absolue : sous vos pieds, la paroi de l'hyphe fongique déploie sa surface de chitine comme la coque d'un vaisseau colossal, chaque brin polysaccharidique rendu incandescent par le calcofluor en une lumière froide et spectrale bleu-blanc, la courbure cylindrique s'étendant au-delà de tout horizon résolvable, aussi massive et ancienne qu'une falaise de basalte. Au-dessus et de tous côtés, le berceau d'actine du neutrophile descend en un filet de filaments d'actine-F ramifiés, chaque brin émeraude tendu comme un câble de pont sous charge, organisé en coupe pour étreindre l'hyphe avec la précision mécanique d'un outil vivant. À la zone de contact que vous habitez, des éruptions rouge-orange d'espèces réactives de l'oxygène jaillissent en impulsions irrégulières — chaque détonation chimique est une knot de violence rédox brève, un front de combustion biologique qui illumine par en dessous le maillage d'actine en cuivre ardent, témoignant de la machinerie oxydative déployée par le neutrophile pour démanteler la paroi chitineuse par oxydation enzymatique directe. Dans ce réseau vert, les granules azurophiles dérivent vers l'avant comme des réservoirs d'ambre chargés d'enzymes lytiques, se rapprochant inexorablement de l'interface où la chimie est devenue une arme.
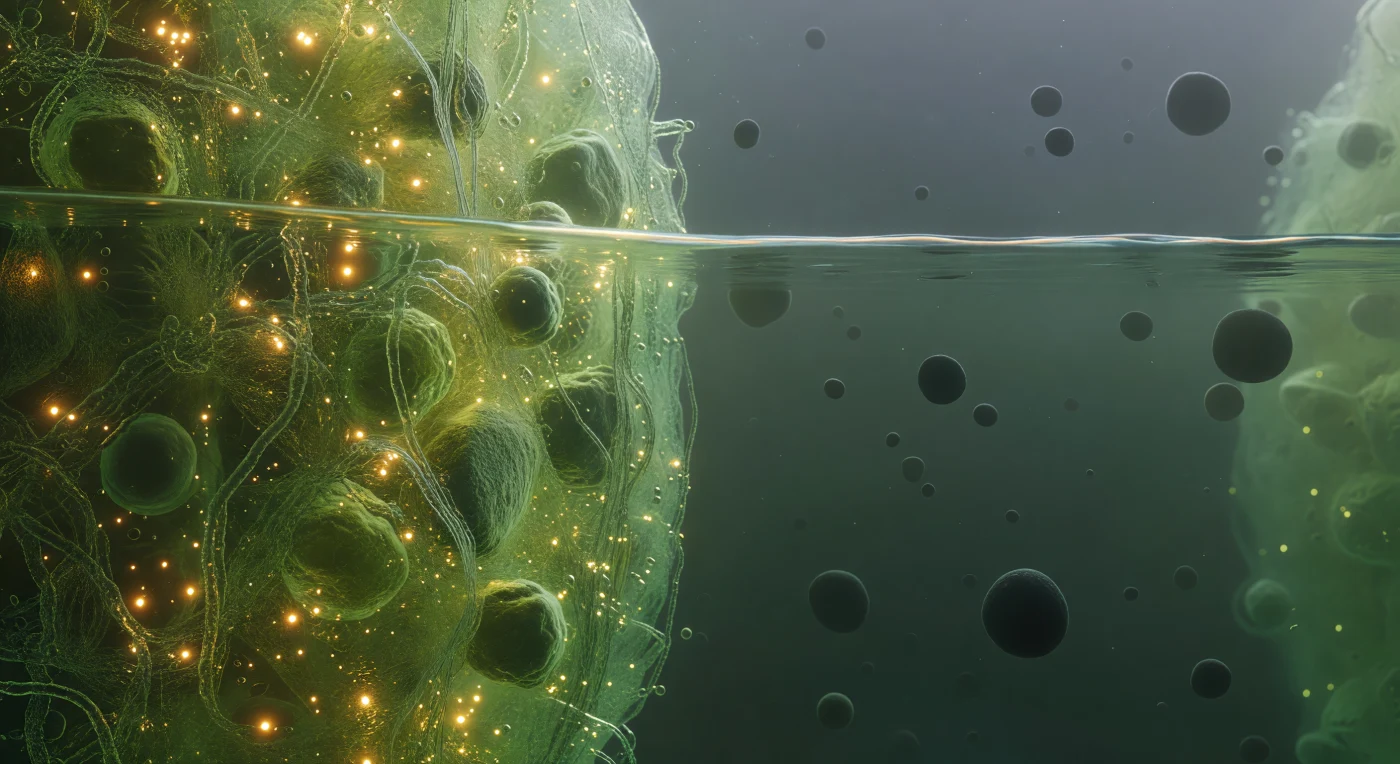
Vous flottez exactement à la frontière entre deux états de la matière vivante, le corps coupé en deux par une interface thermodynamique d'une netteté presque impossible dans ce monde ordinairement flou : à gauche, la phase condensée du granule de stress brûle comme de l'ambre en fusion, un milieu dense et lumineux où des chaînes d'ARNm entrelacées et des protéines à régions intrinsèquement désordonnées s'enchevêtrent en un réseau si concentré que la lumière confocale y ralentit visuellement, se diffusant en stries dorées et verdâtres qui pulsent doucement sous l'agitation brownienne de milliers de macromolécules comprimées les unes contre les autres. Ce phénomène de séparation de phase liquide-liquide — analogue à l'immiscibilité entre huile et eau, mais orchestré ici par des interactions transitoires entre protéines à faible complexité de séquence et ARN — maintient les deux phases distinctes par une tension de surface nanométrique, et l'interface elle-même tremble devant vous comme une surface de verre dépoli vue par la tranche, parcourue de fluctuations capillaires qui produisent un fin liseré irisé, discontinuité vraie plutôt que gradient. À droite, le cytoplasme dilué s'ouvre comme un océan brumeux et presque vide où des complexes ribosomiques isolés dérivent en sphères sombres et mats à travers une brume bleu-vert diffuse, chacun séparé de ses voisins par des distances qui semblent démesurées après la claustrophobie saturée du condensat — et cette frontière que vous chevauchez demeure la seule ligne franche dans un univers par ailleurs liquide, probabiliste et sans bords.

Vous vous trouvez suspendu dans l'infime corridor aqueux entre deux parois cellulaires colossales, à l'endroit précis où deux cellules épithéliales du tubule rénal scellent leur frontière commune — une jonction si étroite que l'espace entre les membranes se mesure en dizaines de nanomètres à peine, un couloir humide baigné d'ions et de sucres glycocalyxiens d'une teinte dorée fantomatique. Juste au-dessus de vous, la lumière tubulaire s'ouvre comme le gouffre d'une fosse océanique, noire et caverneuse, sa paroi délimitée par une ceinture cramoisie et continue de protéines ZO-1 et de claudines — une bande de jonction serrée qui ceint le périmètre entier de la cellule comme un métal en fusion soudé dans le tissu vivant, parfaitement horizontale, parfaitement ininterrompue, pulsant d'une lumière interne rouge-cinabre. Juste en dessous, un second anneau émeraude de jonctions adhérentes à E-cadhérine lui fait écho en jade bioluminescent, ses ectodomaines moléculaires s'entremêlant comme des doigts noués à travers la fente intercellulaire, tandis que plus bas les membranes latérales des deux cellules forment deux rideaux parallèles graphite, séparés de moins de vingt nanomètres, qui s'écartent progressivement vers les espaces basolatéraux ambrés. Au fond, les noyaux apparaissent comme d'immenses ovoïdes cobalt, leur chromatine irradiant une luminescence indigo diffuse à travers l'enveloppe nucléaire — l'ensemble composant, depuis l'intérieur même du réseau de jonctions, la géométrie d'un vitrail de cathédrale vu depuis le cœur du plomb, les protéines jonctionnelles formant le réseau brillant et les corps cellulaires les panneaux de verre coloré rayonnant dans l'obscurité.




















