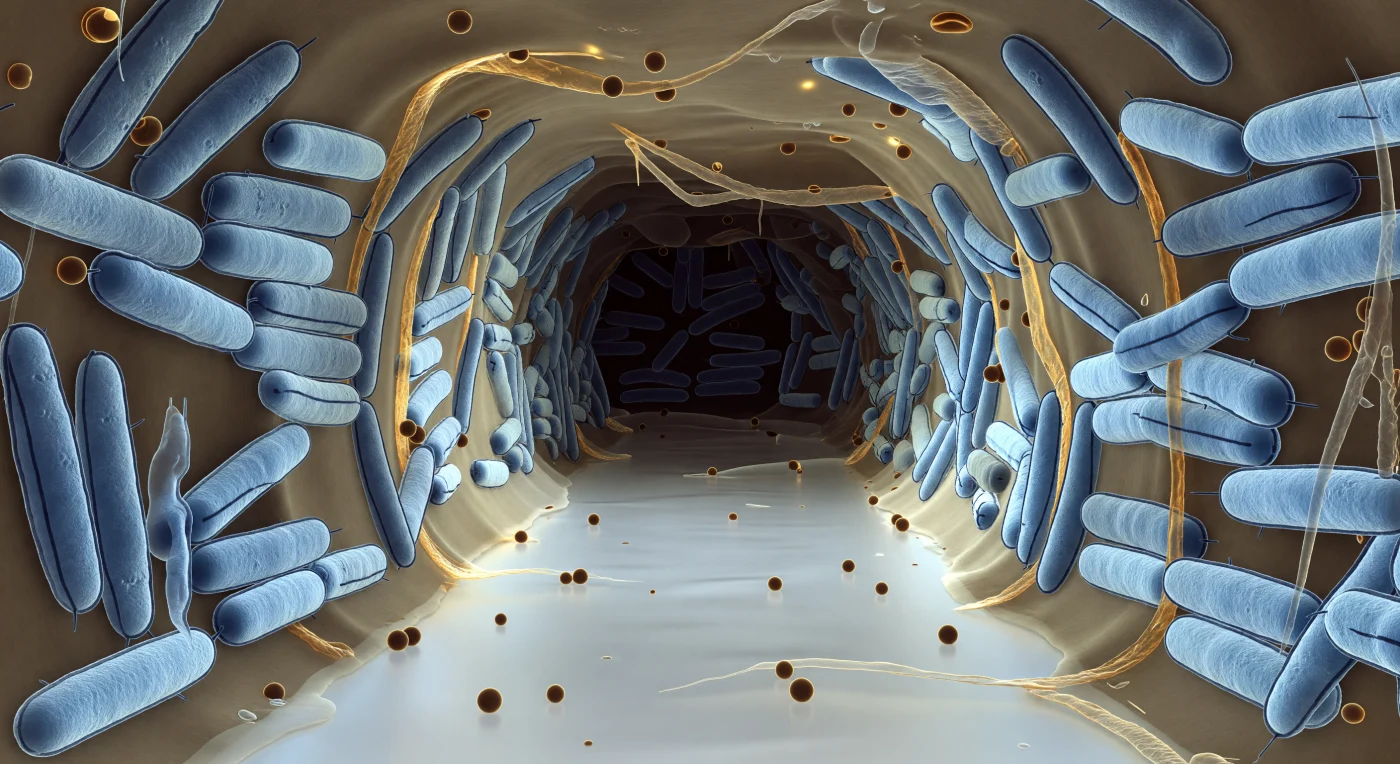
Te encuentras suspendido en la boca de un canal de agua que atraviesa un biofilm de *E. coli* vivo, un corredor pálido y luminoso flanqueado por filas compactas de bastones bacterianos teñidos de azul glacial, cada uno de una altura cinco veces mayor que la tuya, sus dobles membranas externas visibles como dos líneas oscuras y paralelas que se repiten cientos de veces hasta desvanecerse en una neblina azul grisácea donde el canal se estrecha y se pierde en la sombra. La matriz de exopolisacáridos que une a los organismos entre sí aparece como una sustancia traslúcida color ámbar dorado, entre miel y vidrio esmerilado, que atrapa la poca luz difusa que filtra por el biofilm y confiere a las paredes una tenue luminiscencia cálida bajo el frío azul de las células. Dispersas por el suelo del canal y suspendidas en la columna de fluido casi inmóvil, vesículas de membrana externa flotan como cuentas de ámbar perfecto, cada una una burbuja sellada de membrana que transporta carga molecular entre organismos, algunas semihundidas en el borde del EPS como fósiles traslúcidos atrapados en resina. La luz carece de fuente definida: es ambiental, fría y se consume progresivamente hacia el fondo del corredor, donde los gradientes de oxígeno y nutrientes caen y la matriz se vuelve más densa y opaca, recordando que este pasillo no es una imagen sino un espacio químicamente activo e indiferente a cualquier presencia. Filamentos de pili apenas perceptibles se extienden desde algunas células hacia el espacio del canal como hilos tentaculares, y la superficie de los organismos más cercanos muestra en bajorrelieve la textura de complejos proteicos que revelan, sin palabras, la escala inabarcable de lo que te rodea.

Te encuentras suspendido en el fluido extracelular a escasos nanómetros de la membrana de un linfocito T, y lo que te rodea no es vacío sino una espesura translúcida y temblorosa de proteínas disueltas que filtra la luz fría y omnidireccional como el agua bajo el hielo polar. Decenas de viriones del VIH-1 derivan a tu alrededor en suspensión browniana, cada uno una esfera de entre cien y ciento veinte nanómetros de diámetro velada en azul grisáceo, con su núcleo capsídico apenas insinuado como una sombra cónica en su interior y su superficie sembrada de trímeros gp120-gp41 que brillan en un oro cálido, pequeñas coronas glucoproteicas que representan la maquinaria molecular con la que el virus reconoce y asalta la célula huésped. Detrás de ti, la membrana plasmática del linfocito se alza y ondula como el flanco de una fosa abisal, interrumpida por los voluminosos complejos proteicos anclados en ella —receptores CD4, canales transmembrana, filamentos del glucocáliz que se proyectan hacia afuera como una arboleda translúcida—, y dos o tres viriones ya presionan contra esa frontera con una suavidad que parece gravitacional, sus espículas doradas buscando los sitios de anclaje en lo que la bioquímica describe como el primer paso irreversible de la infección. El ambiente entero vibra en la escala de la agitación térmica: aquí no hay sombras direccionales ni fotones relevantes, solo masa, química y la implacable democracia del movimiento browniano definiendo cada encuentro.

Te encuentras en el fondo de un cañón colosal cuyas paredes no son roca sino membrana: la membrana mitocondrial interna se eleva en pliegues profundamente convolucionados, teñida de un marrón carbón saturado por el ósmio y salpicada de miles de complejos ATP sintasa cuyos cabezales F₁ sobresalen como hongos microscópicos anclados en el lípido, cada uno girando imperceptiblemente mientras conjura moléculas de ATP de un gradiente de protones invisible. La matriz en la que estás sumergido no es aire ni agua, sino una neblina ámbar densa y coloidal —cargada de enzimas del ciclo de Krebs, ribosomas mitocondriales que vibran con el temblor browniano constante y lazos de ADN mitocondrial en arcos superenrollados— todo ello comprimido a más de quinientos miligramos de proteína por mililitro, de modo que cada fotón se dispersa en un resplandor volumétrico color miel que da al conjunto la profundidad atmosférica de una garganta geológica. Más adelante, la unión de la cresta se estrecha hasta convertirse en un corredor de ranura apretada, iluminado desde dentro por ese mismo oro cálido concentrado casi hasta la incandescencia allí donde las dos paredes membranosas casi se tocan, sus cabezales de ATP sintasa tan densamente agrupados que forman un techo adoquinado sobre la garganta pulsante. Más allá de la junción, otra cámara se abre hacia una oscuridad que se siente geológica en su escala, otro acantilado de bicapa lípidica erguiéndose en la profundidad ámbar: un mundo de arquitectura biológica pura, que respira, atestado y vivo en cada dirección.
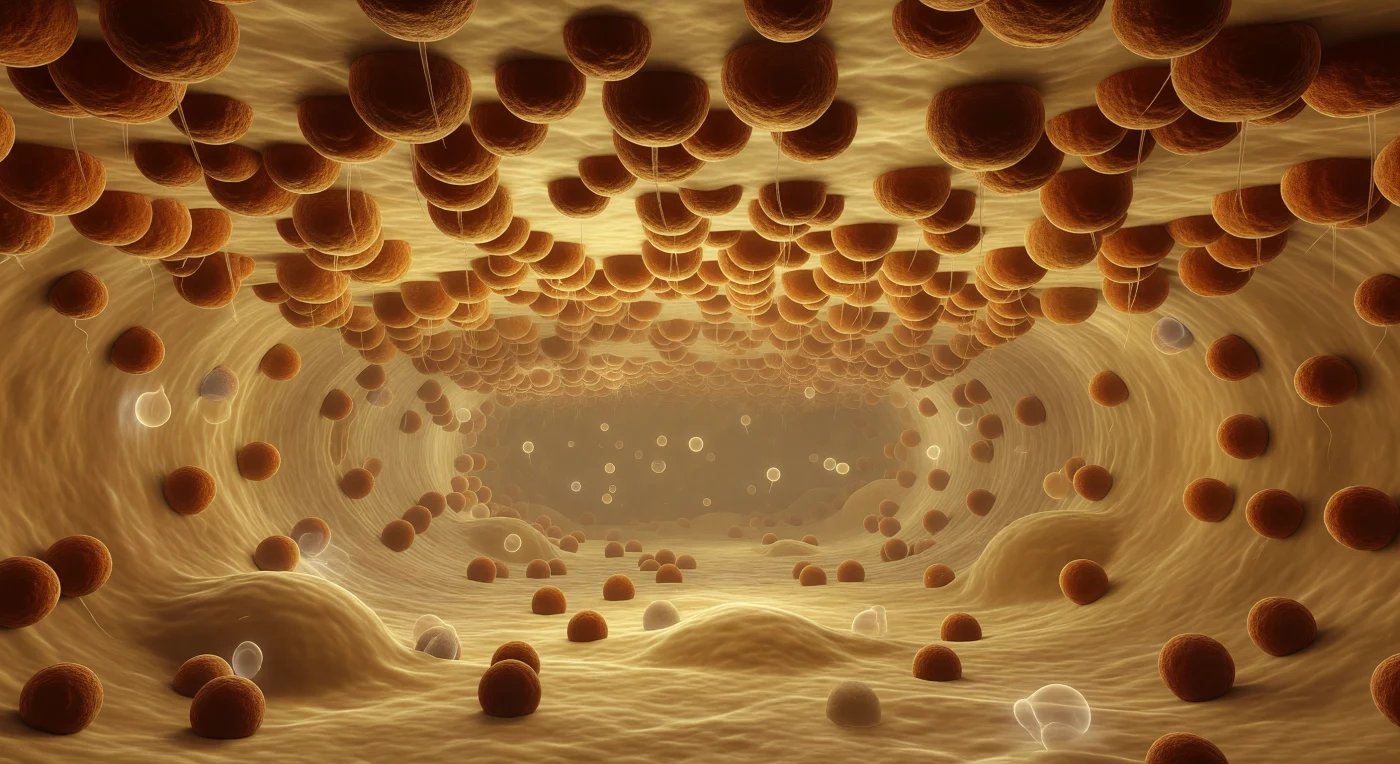
Te encuentras suspendido en el interior del lumen del retículo endoplásmico rugoso, envuelto en una luminosidad suave y uniforme color miel diluida que emana del propio medio acuoso, denso de proteínas disueltas que derivan a tu alrededor como fantasmas translúcidos. Sobre ti se extiende hasta cada horizonte un techo continuo e interrumpido de membrana lipídica —una llanura ondulante de tonos crema y ocre— completamente recubierta por una canopea apretada de ribosomas: esferas de arcilla oxida y umber, cada una de unos 25 nanómetros de diámetro, empaquetadas hombro con hombro como lapas sobre el casco de un barco, sin dejar visible ni un fragmento desnudo de bicapa. Desde la base de cada ribosoma descienden hacia ti filamentos casi invisibles de polipéptido naciente —hilos de pescador que capturan el resplandor interior en destellos iridiscentes antes de disolverse en la neblina dorada del corredor— mientras el lumen se aleja en perspectiva entre dos membranas igualmente pobladas, convergiendo hacia un punto de fuga perdido en una bruma ambarína de proteínas. La escala no se percibe por comparación sino por repetición e inevitabilidad: esta maquinaria industrial biológica no tiene pausa ni conciencia de sí misma, fabricando proteínas en todas direcciones a la vez, una manufactura sin arquitecto que ocurre en el interior de cada célula viva en este preciso momento.

Estás suspendido en el frente de combate de una célula viva, en el filo más adelantado de su lamelipodio, mirando hacia adentro a través de una selva de filamentos de actina de siete nanómetros de diámetro que se ramifican en ángulos de setenta grados desde densos nodos de complejo Arp2/3, extendiéndose hacia el interior en una arquitectura fractal de verde-azul eléctrico y jade frío, tan intrincada y repetida que el ojo pierde toda referencia de límite o de borde. Bajo tus pies, un plano de sustrato casi negro refleja una luz evanescente de onda fría —la iluminación TIRF que solo penetra unos pocos cientos de nanómetros hacia arriba— y en esa penumbra rasante brillan las placas de adhesión focal como lingotes de ámbar y oro fundido incrustados en vidrio oscuro, anclas bioquímicas donde integrinas y proteínas de andamiaje transmiten la tensión mecánica entre el citoesqueleto y la matriz extracelular. A cada lado, espigas filopodiales emergen solitarias más allá del dosel ramificado, filamentos de actina paralelos envueltos en fascina que proyectan sus puntas hacia el vacío extracelular como antenas luminosas probando territorio desconocido. La red entera está en movimiento perpetuo: la polimerización de actina en los extremos barba empuja el borde hacia adelante a razón de micrómetros por minuto, mientras las miosinas y las proteínas de corte como cofilina desensamblan los filamentos más viejos en la retaguardia, convirtiendo este bosque de fuego verde frío en una máquina molecular de locomoción dirigida.

Te aproximas lentamente hacia la entrada del complejo del poro nuclear, una roseta dorada de simetría octogonal perfecta que se alza ante ti como un portal monumental de 120 nanómetros incrustado en la doble membrana del envoltorio nuclear, cuyas capas de color carbón oscuro se extienden hacia los lados como bóvedas de piedra impregnadas de una tenue bioluminiscencia ámbar. A ambos lados del poro, masas de heterocromatina compactada se elevan en azules profundos e índigos —densos, rugosos, absorbentes de luz— como acantilados costeros que enmarcan la única abertura en una muralla biológica casi impenetrable. El transporte nucleocitoplasmático ocurre precisamente aquí: unas 1000 moléculas por segundo atraviesan cada poro, mediadas por la danza hipnótica de los filamentos FG-nucleoporinas que cuelgan del tapón central como una cortina de cuentas translúcidas, seleccionando con precisión química qué puede pasar y qué no en función del tamaño molecular y las señales de localización nuclear. Detrás de ti, la eucromatina más laxa se dispersa en una neblina lila y violeta pálido, y pequeñas gotas de condensado flotan como esferas de mercurio suspendidas en el nucleoplasma gelatinoso, recordándote que el interior del núcleo no es un compartimento uniforme sino un paisaje bioquímico dinámico, organizado en dominios funcionales sin membranas que lo delimiten.

Ante ti se eleva una torre monumental de membranas apiladas con precisión geométrica, quince discos translúcidos de un verde jade intenso separados por delgadas rendijas de color amarillo limón pálido, como si un artesano antiguo hubiera construido una columna de luz y lípidos cuya lógica interna es la de atrapar fotones. Cada membrana tilacoide está densamente poblada por los complejos del fotosistema II y los complejos antena cosechadores de luz, proteínas-pigmento cuya clorofila absorbe quanta luminosos y los convierte en electrones excitados, iniciando así la primera etapa de la fotosíntesis oxigénica que oxigenó la atmósfera terrestre hace más de dos mil millones de años. Desde el grana se extienden horizontalmente las lamelas del estroma, cintas esmeraldas sinuosas que conectan esta torre con grana vecinos apenas visibles como columnas luminosas en la distancia, mientras que el estroma circundante —denso, gelatinoso, opalescente— está atiborrado de complejos de RuBisCO que aparecen como bloques irregulares de color pálido, y de plastoglóbulos ambarinos que flotan como pequeñas esferas de miel atrapando y calentando la luz difusa. La escala es aplastante en su intimidad: la superficie corrugada de cada membrana revela, a distancia cercana, un mosaico compacto de cabezas proteicas que casi no dejan lípido desnudo visible, y entre los discos se percibe el gradiente de protones migrando lentamente de un lado al otro del lumen, esa fuerza motriz que impulsa la ATP sintasa y convierte el flujo iónico en la moneda energética de toda la célula.
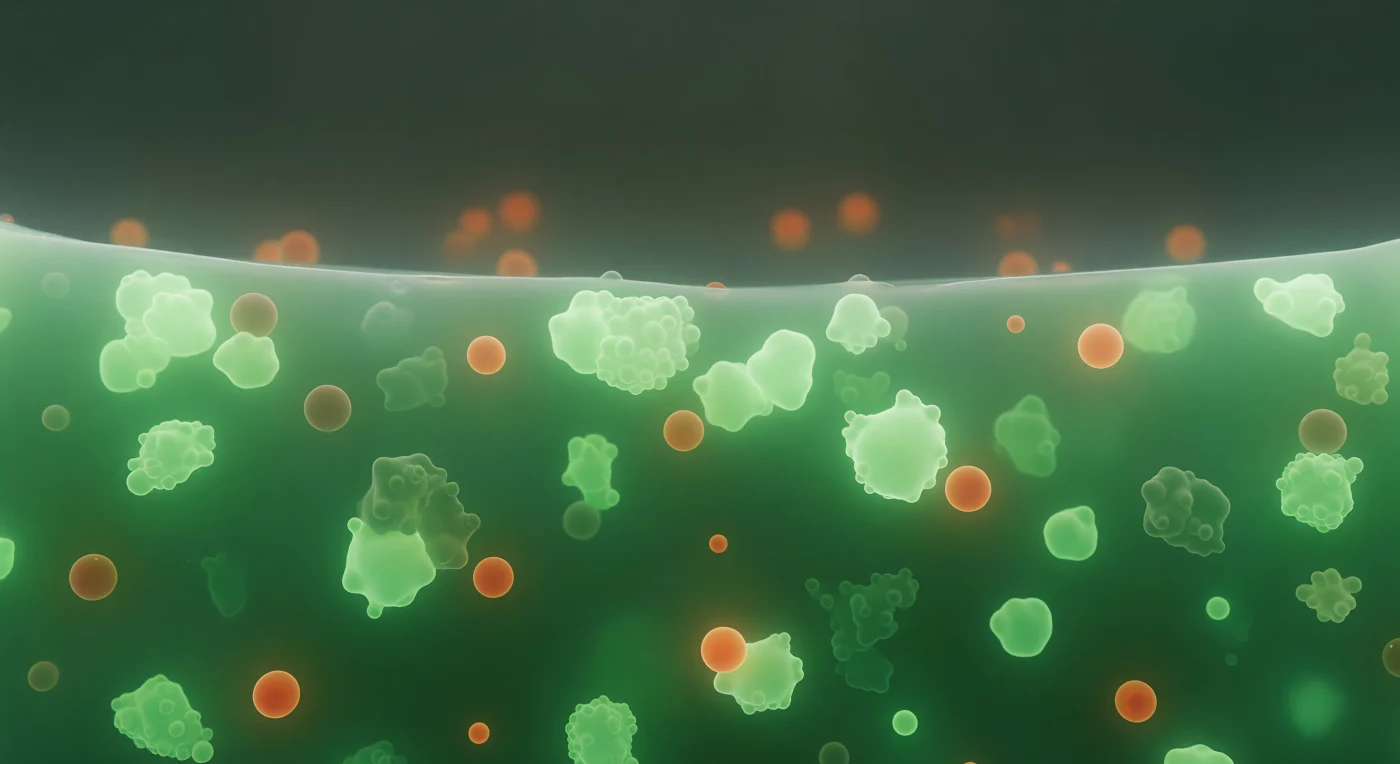
Te encuentras suspendido en el interior de un gránulo de estrés, una de las estructuras más enigmáticas que la célula construye cuando el mundo exterior se vuelve hostil: un condensado de separación de fases líquido-líquido, una gota viscoelástica que se organiza espontáneamente a partir del caos molecular cuando la traducción proteica colapsa bajo el calor, la hipoxia o el daño oxidativo. A tu alrededor, la matriz verde esmeralda —cargada de G3BP1 y cientos de proteínas de unión a ARN— no es un sólido ni un líquido convencional, sino algo intermedio: un gel suave y respirante que obedece tanto a la física de los fluidos como a la de los materiales elásticos, capaz de fluir lentamente y de resistir deformaciones breves al mismo tiempo. Los nódulos más brillantes que emergen de esa neblina luminosa son acumulaciones densas de ARNm poliadenilados y sus proteínas asociadas, mensajes genéticos secuestrados temporalmente fuera de los ribosomas, en espera de que la crisis pase y la traducción pueda reanudarse; las esferas ámbar-naranja que flotan entre ellos son co-condensados ricos en TIA1, una proteína de agregación que nuclea el ensamblaje de estos gránulos y que forma su propia fase inmiscible dentro de la fase ya separada, líquido dentro de líquido en una jerarquía de organización sin membranas. Y allí, en el horizonte verde, la pared abrupta del condensado —donde la densidad molecular cae en picado hacia el citoplasma diluido exterior— es la firma física más pura de la separación de fases: no una membrana construida, sino una frontera termodinámica emergente, mantenida por el equilibrio de fuerzas moleculares que define dónde termina un mundo y comienza otro.

Suspendido sobre el eje central del motor flagelar bacteriano, el observador mira hacia abajo a través de las membranas concéntricas como si contemplara la sección transversal de un templo sumergido: el anillo L resplandece con un bronce frío en la membrana externa de cobalto oscuro, el anillo P reposa sobre la capa de peptidoglicano con un cálido fulgor ámbar, y el complejo MS llena el plano de la membrana interna con una arquitectura circular de oro oxidado y acero sombrío, sus bordes esculpidos en una textura escalonada de subunidades proteicas. Diecisiete complejos estatoriales MotA/MotB, cada uno una masa asimétrica de color peltre, rodean el rotor en simetría radial casi perfecta, presionando contra la membrana interna como contrafuertes colossales que anclan una turbina a su carcasa. Este motor molecular, de apenas 45 nanómetros de diámetro, convierte el gradiente de protones transmembrana en torque mecánico rotatorio puro, girando a entre 100 y 1.000 Hz en condiciones fisiológicas sin consumir ATP directamente. Por encima, el filamento flagelar asciende en espiral hacia el espacio extracelular, un cable helicoidal de subunidades de flagelina perdiéndose en una neblina azul-grisácea de moléculas disueltas; la región del gancho curvo conecta rotor con filamento como un sello mecánico alrededor de un eje en rotación perpetua. La totalidad de la escena irradia la estética de una máquina perfectamente refinada por miles de millones de años de selección: cada interfaz molecular pulida por la función, cada componente ensamblado con una precisión que ninguna ingeniería humana ha logrado replicar a esta escala.

El suelo bajo tus pies es una llanura de arcilla cálida, sus fronteras intercelulares marcadas como crestas pálidas y geométricas de uniones estrechas apretadas entre sí, y desde aquí se alzan hacia arriba, en todas las direcciones, centenares de columnas cilíndricas de un azul-cian profundo que se pierden en una bóveda lejana y tenue. Cada uno de estos cilios mide apenas doscientos nanómetros de diámetro —su eje interno de nueve pares de microtúbulos más dos centrales presiona suavemente contra la membrana exterior como costillas bajo seda húmeda— y su función colectiva es propulsar el moco de las vías respiratorias hacia la faringe, atrapando patógenos y partículas en ese lento río ámbar que ahora cuelga entre las puntas como hilos de miel iluminados por dentro. Lo que se ve en la bóveda no es quietud sino movimiento congelado: la ola metacrónica, ese acuerdo coordinado entre cientos de células vecinas, ha inclinado una columnata entera entre diez y quince grados mientras la siguiente ya recupera la vertical, y el techo de puntas superpuestas ondula como tejas escalonadas atrapadas a mitad de su brillo. Todo el espacio entre las columnas está saturado por el medio extracelular hidratado, y su dispersión refractiva convierte los cilios más lejanos en varillas luminosas y difusas, recordándote que estás dentro de una estructura que respira sin saberlo.
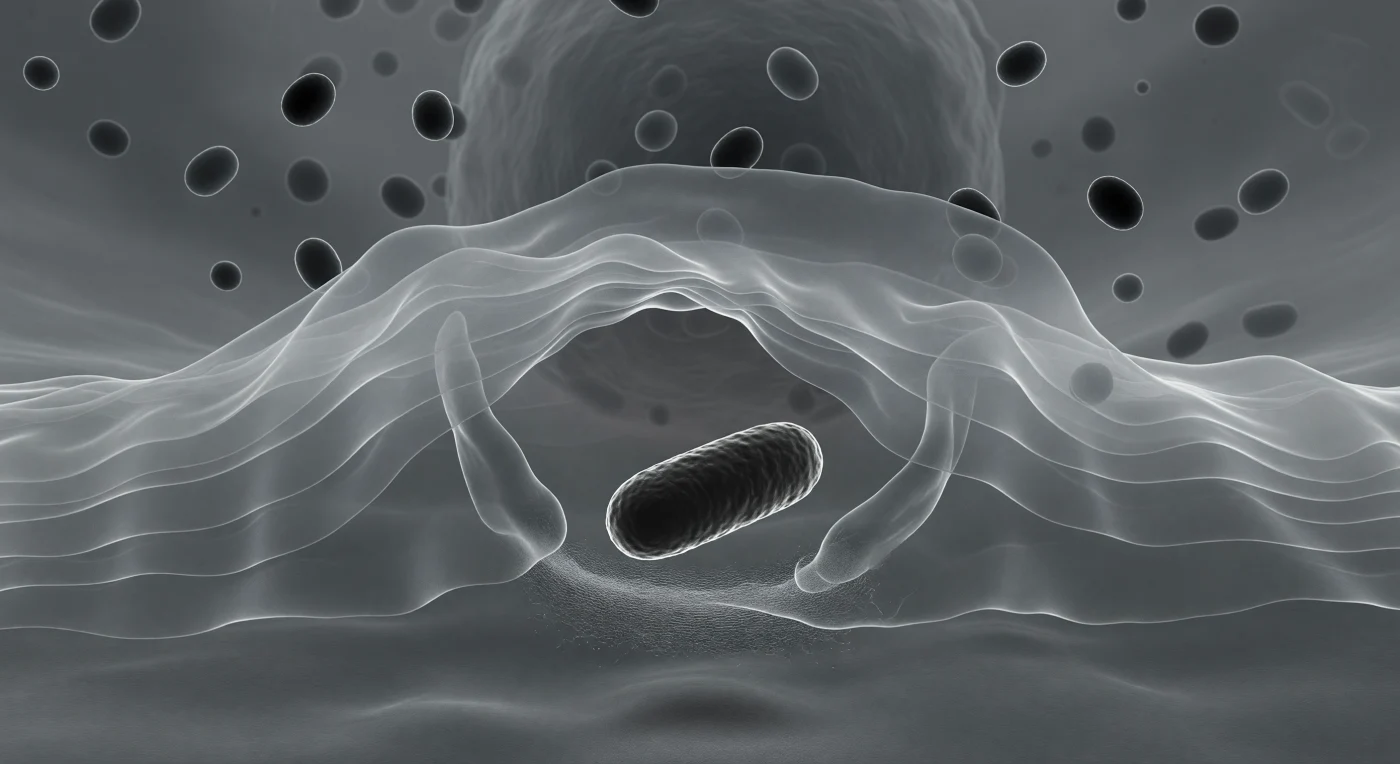
Te encuentras justo en el filo de la ingesta, suspendido detrás del borde más avanzado de un velo citoplasmático translúcido que se curva hacia adelante como una ola congelada a mitad de su quiebre, compuesto por una red densa de filamentos de actina que se polimerizan en tiempo real para empujar la membrana hacia su presa. Directamente frente a ti, una bacteria con forma de bastón domina el campo visual como un monolito de carbón, su silueta recortada por un halo de difracción luminoso mientras los pseudópodos del macrófago la envuelven desde ambos flancos en un abrazo arquitectónico e inevitable, las membranas casi tocándose en el polo distal de la célula bacteriana. Este proceso, conocido como fagocitosis, es uno de los mecanismos centrales de la inmunidad innata: receptores de superficie del macrófago han reconocido patrones moleculares en la pared celular bacteriana, desencadenando una cascada de señalización que reorganiza el citoesqueleto de actina en segundos y convierte a la célula inmunitaria en una arquitectura de captura. Detrás de ti, en el interior más profundo del macrófago, gránulos lisosomales flotan como piedras densas en suspensión, cargados de enzimas hidrolíticas que aguardan para fusionarse con la vacuola fagocítica y disolver todo lo que la vaina translúcida está a punto de sellar dentro de sí.

Te encuentras suspendido en el centro de una cuenca de oro cálido que se extiende hacia todos los lados como el cráter de un mundo íntimo y orgánico: es la concavidad central de un eritrocito humano, un disco bicóncavo de apenas ocho micrómetros de diámetro que a esta escala percibida se despliega como una llanura continental de membrana plasmática traslúcida, ámbar y tensa, bajo cuyos pocos nanómetros de espesor se adivina el entramado espectrínico hexagonal presionando desde abajo como filigrana grabada en cristal de miel. La iluminación oblicua de electrones secundarios cae desde la izquierda sin dispersión atmosférica alguna, esculpiendo cada ondulación de la membrana en relieves de bronce biológico y hundiendo la depresión central en sombras de ámbar oscuro con la precisión de metal cortado. A media distancia, los eritrocitos vecinos se han apilado en columnas de rouleaux —torres lisas de discos bicóncavos cara a cara, su corrugación rítmica alzándose sobre un fondo pajizo y translúcido que es el plasma, un suero amarillo-dorado cuya viscosidad se intuye en la forma en que las plaquetas espinosas quedan suspendidas entre las columnas celulares, sus proyecciones superficiales captando la luz como puntos especulares brillantes. Todo aquí, desde la red geodésica bajo tus pies hasta las columnas celulares que se pierden en la distancia luminosa, es superficie biológica y fluido: un universo donde la escala íntima y la planetaria coexisten en perfecta nitidez.
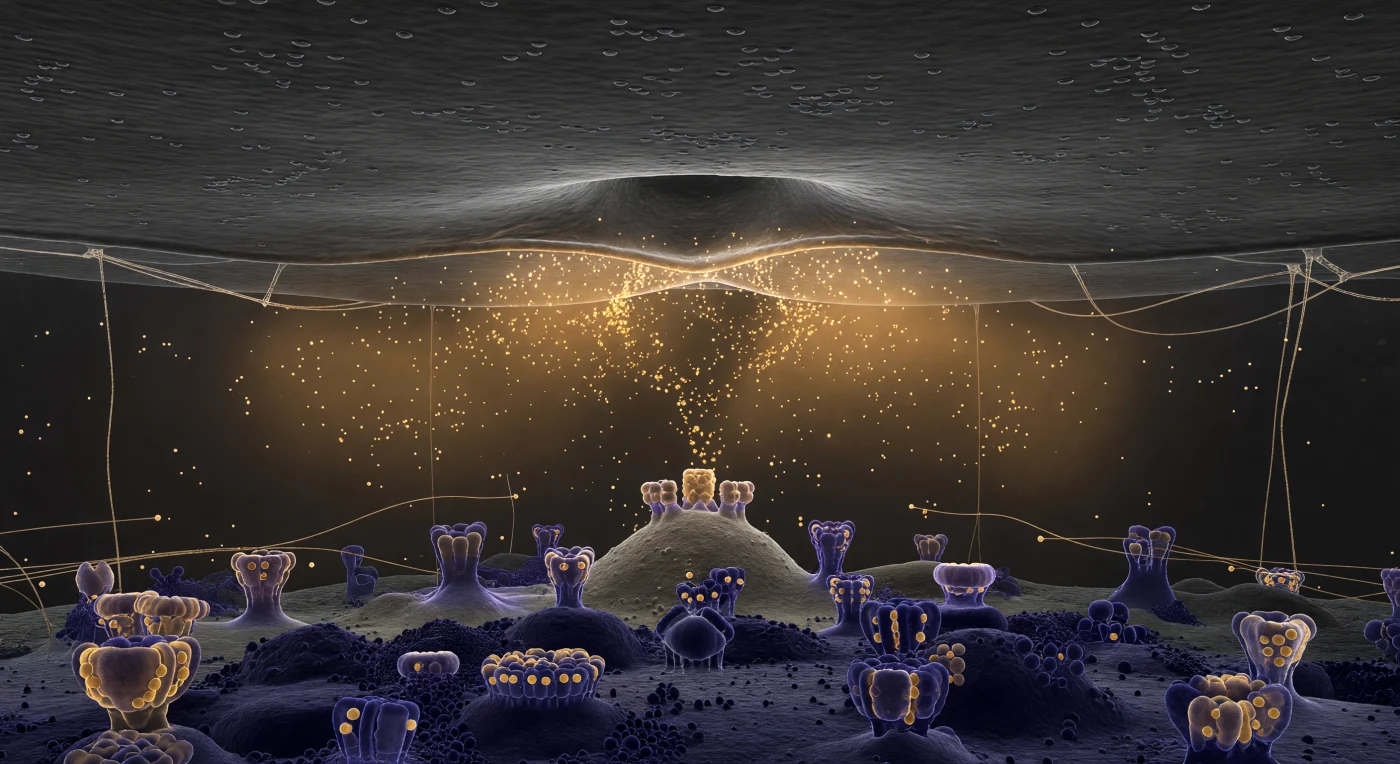
Te encuentras suspendido en uno de los corredores más angostos del sistema nervioso: la hendidura sináptica, un pasaje acuoso de apenas 25 nanómetros donde el techo y el suelo se perciben simultáneamente, separados por una distancia que no supera la envergadura de tus brazos extendidos. Directamente sobre tu cabeza, una vesícula sináptica ha alcanzado el punto de no retorno: su membrana se ha fusionado con la membrana presináptica formando una perfecta omega de lípidos en colapso, y desde esa apertura fluye hacia el espacio una marea difusa de moléculas de neurotransmisor, un halo ámbar-dorado que se expande lateralmente como una exhalación cálida en la oscuridad grisácea del corredor. El medio que te rodea no está vacío: filamentos de proteínas de adhesión y matriz extracelular atraviesan el espacio de techo a suelo como cables translúcidos que atrapan el resplandor ámbar en finos destellos dorados, mientras la solución acuosa en sí posee una densidad y viscosidad que a esta escala resultan casi gelatinosas. Bajo tus pies, la densidad postsináptica se extiende como un paisaje arquitectónico de alfombra púrpura oscura, sus receptores AMPA y NMDA emergiendo como formaciones pétreas antiguas cuyos vértices capturan el fulgor ámbar de los neurotransmisores que descienden hacia sus sitios de unión, y en ese encuentro químico —moléculas liberadas buscando receptores a milésimas de segundo de distancia— se enciende la señal eléctrica que sostiene el pensamiento.
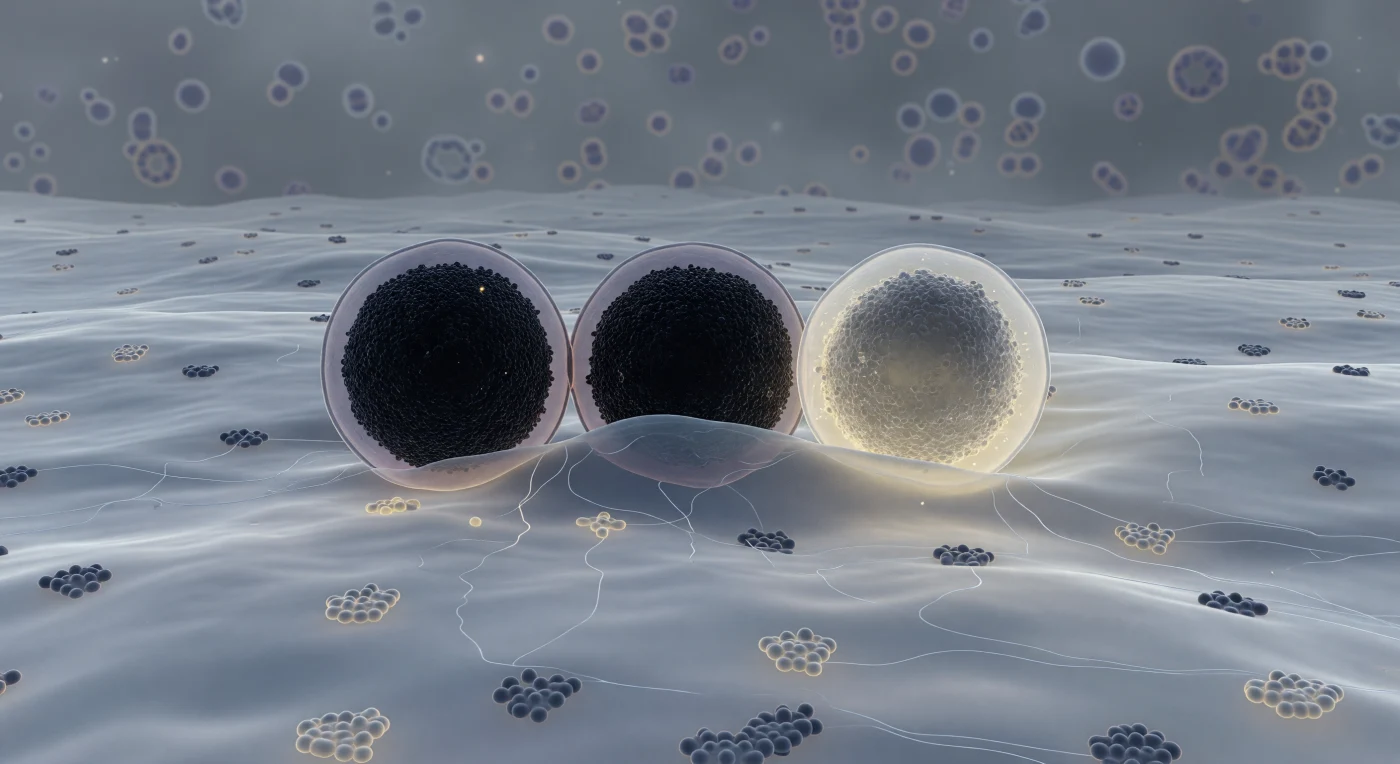
Desde el interior citoplasmático de una célula beta pancreática, la membrana plasmática se extiende como una inmensa llanura ondulante de bicapa lipídica azul-grisácea, salpicada de dominios raft más claros y ordenados donde el colesterol se concentra, y perforada por los perfiles oscuros de complejos proteicos transmembrana. Tres gránulos secretores de insulina dominan el espacio intermedio como edificios esféricos en distintos estadios de exocitosis: el primero permanece anclado con precisión milimétrica contra la membrana, su núcleo cristalino de hexámeros zinc-insulina casi opaco rodeado de un halo lavanda; el segundo ha iniciado la hemifusión, deformando la membrana en una depresión suave donde las dos bicapas comienzan a interpenetrarse en una zona de identidad lipídica disuelta; el tercero ha completado la transición, su núcleo denso deshaciéndose en una neblina cálida de marfil y ámbar que se dispersa hacia el espacio extracelular luminoso. Este proceso —la exocitosis regulada— es el mecanismo por el cual los gránulos de núcleo denso fusionan su membrana con la membrana plasmática y vierten su contenido al exterior en cuestión de milisegundos, disparado por el aumento de calcio intracelular que sigue a la elevación de glucosa en sangre. Entre los gránulos, filamentos de actina cortical forman una malla fantasmal de líneas finas, mientras el citoplasma circundante se pierde en una penumbra densa y particulada de ribosomas y organelas distantes, todo suspendido en un instante que parece al tiempo estático e irrevocable.

Te encuentras suspendido en el preciso umbral del borde en cepillo intestinal, a la altura exacta de los extremos de los microvilli, contemplando hacia abajo una llanura geométricamente perfecta de cilindros de cien nanómetros de diámetro que se extiende hasta un horizonte biológico difuso en todas las direcciones. Cada uno de estos miles de estructuras está anclado internamente por un haz de filamentos de actina, que confieren rigidez mecánica a estas proyecciones de la membrana plasmática y maximizan de forma extraordinaria la superficie de absorción del enterocito —hasta veinticinco veces la de una célula lisa equivalente—, permitiendo que el intestino delgado capture glucosa, aminoácidos y lípidos con una eficiencia que ninguna arquitectura plana podría igualar. Sobre la cima de cada villus asciende el glucocáliz: una nube de filamentos de polisacáridos y glicoproteínas de apenas unos nanómetros de grosor que se funde con la de sus vecinos para formar un tapiz continuo de marfil antiguo, ligeramente fosforescente en la luz oblicua, donde enzimas digestivas como la lactasa y la sacarasa-isomaltasa están ancladas y trabajan en el umbral mismo entre la célula y el lumen, atrapando sustratos que derivan en lenta suspensión browniana a través de ese medio acuoso, proteico y ligeramente viscoso. Los canales entre los cilindros se hunden hacia una oscuridad de ámbar y tabaco que sugiere la profundidad de un cañón, y en ese instante congelado una leve irregularidad —un villus inclinado dos grados, una nube de glucocáliz asimétricamente engrosada— recuerda que esta arquitectura casi mineral es, en realidad, tejido vivo atrapado en un único fragmento de su incesante vida biológica.

Te encuentras suspendido en el ecuador exacto de una célula en división, y el espacio que te rodea es una catedral de luz viviente: desde dos polos distantes arriba y abajo, cables luminosos de microtúbulos emergen en abanico como columnas de jade eléctrico, cada uno un cilindro de tubulina polimerizada que cruza el campo visual en diagonal, formando una celosía de tensión tridimensional que te enmarca por completo. Las fibras del cinetocoro —más gruesas, más tensas, brillando con una intensidad que supera a las demás— desaparecen en masas cromosómicas de violeta índigo que se alejan poleward, arrastradas por la maquinaria de segregación más precisa que haya evolucionado en la biología eucariota: un proceso en el que errores de un solo cromosoma pueden resultar en aneuploidía y colapso celular. Directamente a tu altura, el cuerpo medio corta el espacio como una barra de fuego blanco-verde, zona de solapamiento antiparalelo tan densamente empaquetada con proteínas motoras y MAP cinasas que su luminosidad aplasta todo lo demás en la escena. El fondo más allá del huso es una oscuridad absoluta, no el vacío del espacio sino la penumbra del citoplasma —abarrotado de macromoléculas a concentraciones de 300–400 mg/mL— que dispersa el resplandor de cada fibra en aureolas de niebla verde lechosa que se disuelven lentamente en la nada. No existe orientación salvo la simetría bilateral perfecta de esta máquina de herencia, y la geometría luminosa de sus cables converge en perspectiva de túnel hacia dos soles centrosomales que titilan como estrellas vistas a través de una atmósfera biológica.

Te encuentras suspendido en el plasma sanguíneo, un medio plateado y ligeramente opalescente, a la deriva hacia una pared biológica que ocupa todo el horizonte inferior de tu visión: el glucocáliz de la célula endotelial, un bosque denso y translúcido de cadenas de proteoglicanos y glicoproteínas que se alza entre medio micrómetro y dos micrómetros desde la membrana subyacente, apenas entrevista como una línea carbón oscura al fondo. Cada filamento de heparán sulfato se ramifica como ramas de abedul en pleno invierno a escala molecular, su superficie revestida de grupos sulfato y agua de hidratación que les confieren un frío destello azul-plata bajo una iluminación difusa de tinción con rojo de rutenio, mientras puentes laterales gossamer interconectan los núcleos proteoglicánicos en una lacería luminosa de múltiples profundidades. El glucocáliz no es una estructura estática: ondula con la lentitud viscoelástica del plasma, y su densidad se vuelve progresivamente impenetrable hacia la membrana basal, actuando como una barrera físico-química que regula la adhesión leucocitaria, el transporte de solutos y la mecanotransducción hidrodinámica en los capilares. Tu propia sombra —la cúpula convexa del eritrocito que se aproxima, con su característica silueta bicóncava— cae sobre el dosel de filamentos como un eclipse suave, tiñendo los filamentos azul hielo de índigo y casi negro, mientras los márgenes iluminados de este bosque biológico resplandecen con la precisión fría de la criomicroscopía electrónica, y el entramado entero se cierra lentamente a tu alrededor.
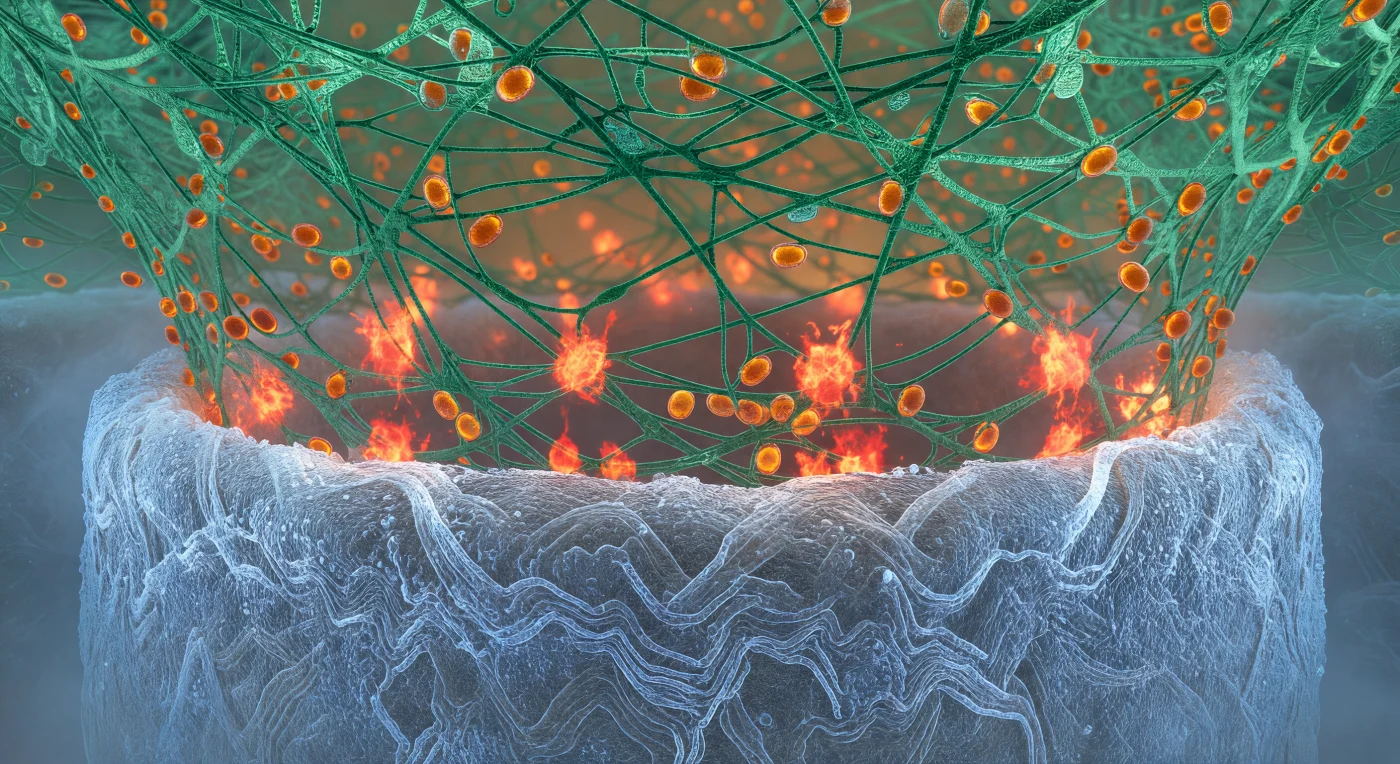
Te encuentras aplastado entre dos arquitecturas biológicas de proporciones colosales, atrapado en el frente de batalla donde la química se convierte en violencia molecular. Bajo tus pies, la pared de la hifa de *Candida* se arquea como el casco de un buque inmenso, su superficie de quitina —una malla de polisacáridos entrelazados con la densidad de basalto antiguo— irradia una luminiscencia azul-blanca espectral provocada por la tinción de calcoflúor, cada hebra brillando con la frialdad incandescente de escarcha bajo presión geológica. Desde arriba desciende la cuna de actina del neutrófilo: una red viridiana de filamentos ramificados de F-actina, tan densa y tensada como cables de andamiaje, que agarra la hifa con la ferocidad organizada de una trampa biológica —esta reorganización del citoesqueleto define la zona de exclusión fagocítica que el neutrófilo construye para confinar y destruir filamentos demasiado grandes para ser engullidos—. En la interfaz entre ambas estructuras, donde tú habitas, estallan detonaciones rojas y anaranjadas de especies reactivas de oxígeno generadas por la NADPH oxidasa: cada destello es un nudo de química redox que ilumina desde abajo la malla esmeralda con cobre de fragua, un frente de combustión vivo que calcina la pared fúngica polisacárido a polisacárido. Por encima, los gránulos azurofílicos —ovoides ámbar cargados de mieloperoxidasa y defensinas— se deslizan con propósito a lo largo de los cables de actina hacia el frente ardiente, reservorios sellados de destrucción enzimática acercándose a su punto de liberación.
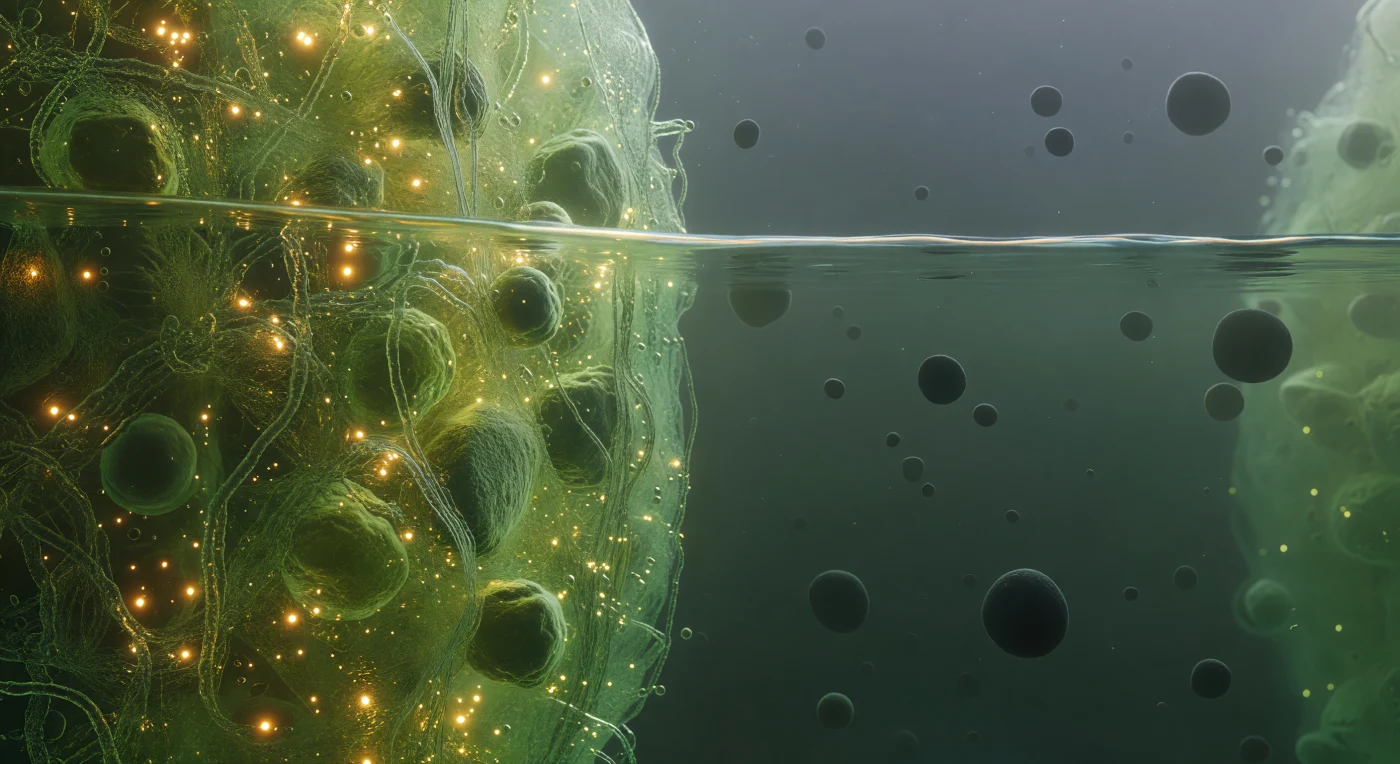
Te encuentras suspendido exactamente en el umbral entre dos mundos líquidos: a tu izquierda, el interior del gránulo de estrés se despliega como un medio denso y luminoso de oro verdoso, una malla viva de cadenas de ARNm entrelazadas y proteínas intrínsecamente desordenadas tan concentradas que la luz parece ralentizarse y acumularse en ámbar bioluminiscente, con ribosomas semisepultados en la interfaz como piedras oscuras incrustadas en un arrecife resplandeciente. Directamente ante ti, la frontera de fase se manifiesta no como un gradiente sino como una discontinuidad termodinámica verdadera, el resultado de la separación de fases líquido-líquido que mantiene dos fases biológicas inmiscibles separadas mediante tensión superficial, temblando con fluctuaciones capilares nanométricas que producen un leve destello iridiscente, un menisco atrapado en oscilación perpetua. A tu derecha, el mundo se abre hacia una bruma verdosa tenue y vasta —el citoplasma diluido— donde complejos de ribosomas individuales derivan como esferas oscuras y opacas separadas por distancias que parecen praderas abiertas tras la claustrofóbica densidad del condensado. Este tipo de organelas sin membrana, los condensados biomoleculares, emergen espontáneamente cuando proteínas con regiones de baja complejidad secuencial superan umbrales de concentración críticos, segregando ARNm y factores de traducción fuera del equilibrio durante el estrés celular. La frontera que atraviesas a la mitad de tu cuerpo es el único borde verdadero en este paisaje fluido y probabilístico, el filo más nítido de un universo gobernado por el ruido térmico y el movimiento browniano incesante.

Te encontrás suspendido en el corredor húmedo entre dos células epiteliales del túbulo renal, apenas un destello de espacio intersticial separándote de cada membrana, y lo que domina el horizonte es una banda carmesí continua —las proteínas ZO-1 y claudinas del complejo de unión estrecha— que sella con precisión absoluta el perímetro de ambas células, impidiendo que cualquier soluto cruce libremente entre la luz tubular y el espacio basolateral. Justo por debajo, una segunda orla de esmeralda fría marca las uniones adherentes de E-cadherina, cuyos ectodominos se entrelazan a través del espacio intercelular como dedos trabados, anclando mecánicamente la monocapa y transmitiendo señales que sostienen la polaridad apico-basal del epitelio. Las membranas laterales de ambas células descienden desde ese ecuador fluorescente como dos cortinas de grafito en aposición casi perfecta —separadas por apenas 10–20 nanómetros—, sus bicapas lípidicas sembradas de proteínas integrales que centellean como incrustaciones minerales en la penumbra. Más abajo, los núcleos de cada célula emiten su resplandor añil de cromatina marcada con DAPI, enormes óvalos cobalto que recuerdan que toda esta arquitectura molecular existe para proteger, con geometría de ventana de catedral, el transporte selectivo que mantiene la homeostasis del filtrado glomerular.




















