Confianza científica: Alto
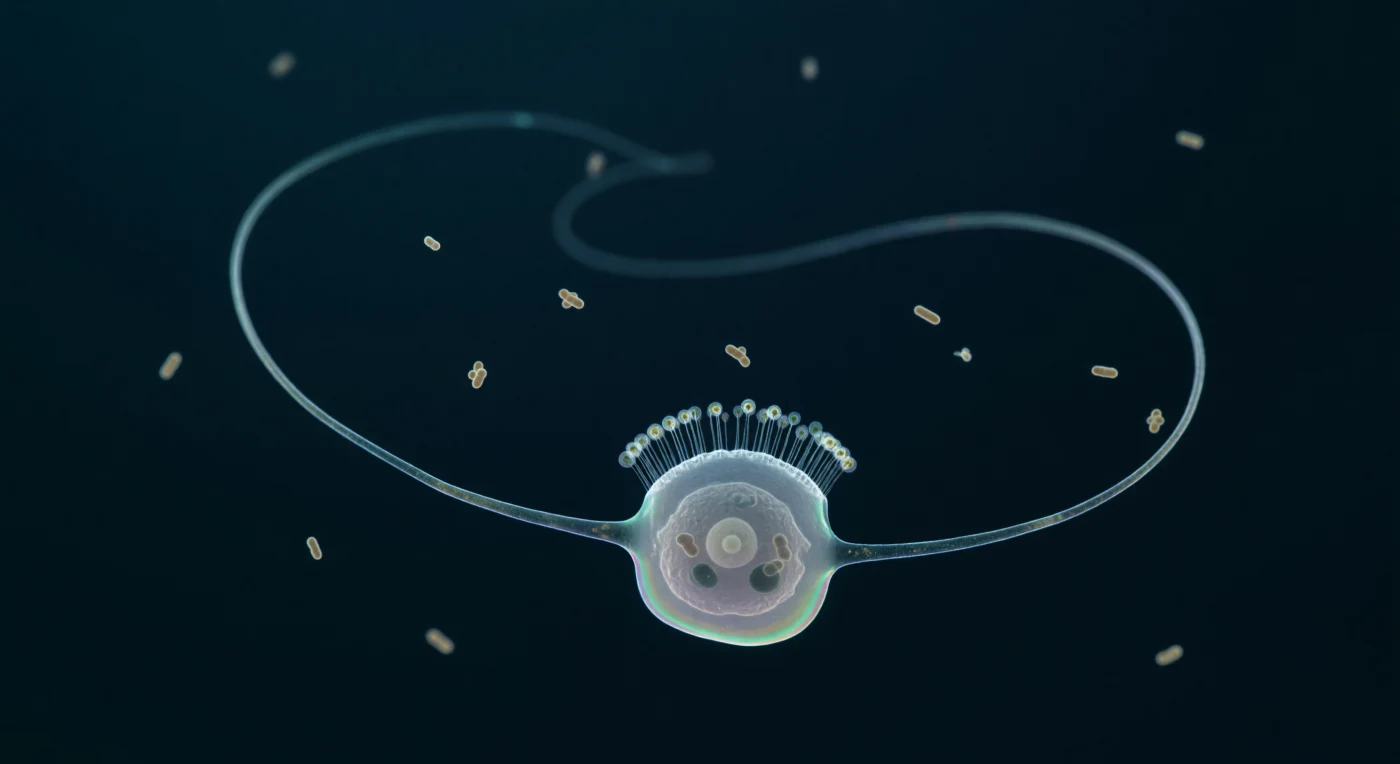
Suspendido en la oscuridad pelágica absoluta, te encuentras cara a cara con uno de los organismos más antiguos y decisivos de la historia evolutiva animal: un coanoflagelado solitario cuyo flagelo —un látigo helicoidal de veinte micrómetros— acaba de barrer el medio viscoso con la precisión de una ola sinusoidal congelada en el tiempo, dejando tras de sí una huella fantasmal de plata pálida que registra el instante exacto en que la física del mundo microscópico transformó el movimiento en alimentación. A esta escala, el agua no es líquida en ningún sentido intuitivo: es un medio dominado por la resistencia viscosa y el ruido térmico browniano, donde la gravedad carece de significado y un simple gradiente de presión generado por ese único axonema —nueve dobletes de microtúbulos moviéndose gracias a la dineína— es suficiente para arrastrar bacterias hacia el collar de treinta y cinco microvilli que rodea su base, una jaula casi invisible cuyos filamentos de actina filtran la materia orgànica disuelta como una red molecular. El cuerpo celular, una gota casi incolora de siete micrómetros atravesada por un núcleo vesicular que ocupa un tercio de su interior y por dos vacuolas alimentarias que aún conservan la silueta comprimida de bacterias en digestión, representa algo más que un organismo unicelular: es el pariente vivo más próximo a los animales, y su collar —estructuralmente idéntico a los coanocitos que tapizan las cámaras internas de las esponjas— es la prueba morfológica de que la multicelularidad animal surgió, hace más de seiscientos millones de años, de células que ya sabían atrapar, engullir y digerir. A tu alrededor, una docena de bacterias en forma de bastón tiemblan en la oscuridad teal como luciérnagas ámbar atrapadas en glicerina fría, ajenas a que la geometría luminosa que domina este mundo —un flagelo arqueado sobre el vacío como el trazo de un calígrafo— es el origen de toda la complejidad animal que alguna vez existirá.

Suspendido en el agua abierta de un estuario, el observador contempla una de las estructuras más antiguas y significativas de la historia de la vida animal: una colonia roseta de *Salpingoeca rosetta* compuesta por treinta y dos células, que flota ante él como una luna de luz fría, sus treinta y dos flagelos extendidos en una corona vibrante que recuerda a un erizo de mar congelado en el instante de su máxima tensión. Cada célula —un ovoidе plateado de apenas tres a cinco micrómetros— apunta radialmente hacia el exterior, sus microvellosidades del collar formando un encaje fantasmal alrededor de la base flagelар, mientras sus polos basales convergen hacia un núcleo de matriz extracelular de tono ámbar tenue, el único calor cromático en una escena por lo demás fría y casi acromática. En la posición de las dos en punto, una célula en plena división muestra su cuerpo ligeramente estrangulado en forma de cacahuete, con dos densidades nucleares grises desplazadas en el interior del citoplasma que se alarga —un instante de la mitosis que tardará entre una y cuatro horas en completarse. El agua que rodea la colonia no es transparente en ningún sentido humano: es un medio de azul-negro profundo y ligeramente opalescente, lleno de cópulos de nieve marina —agregados de detritos orgánicos y mucílago— que derivan en el campo medio y confieren profundidad espacial a este mundo viscoso donde la gravedad es irrelevante y la tensión superficial lo gobierna todo. Esta colonia representa uno de los nexos evolutivos más debatidos y fascinantes de la biología: el umbral entre la unicelularidad y la multicelularidad animal, un organismo que vive hoy prácticamente idéntico a los ancestros que, hace más de seiscientos millones de años, pudieron dar origen a los primeros animales.
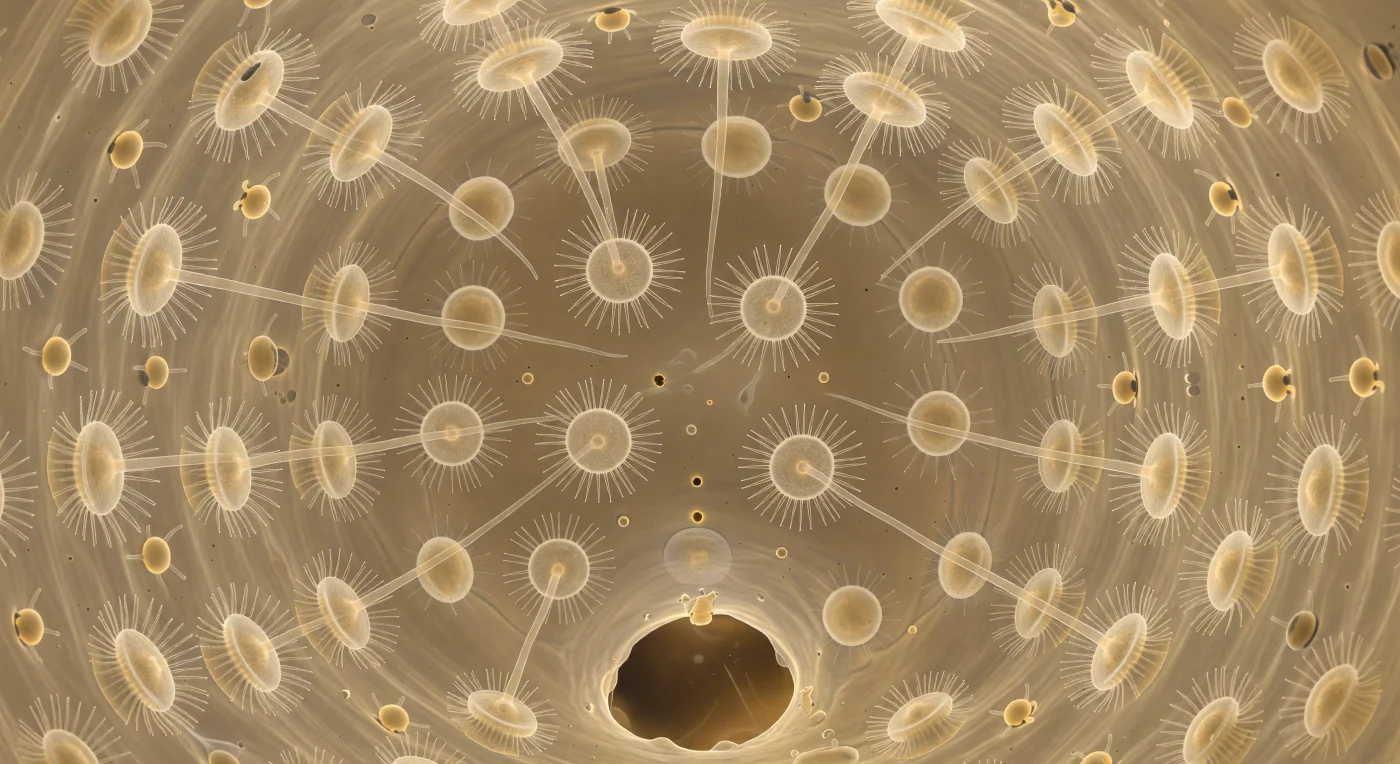
Suspendido en el centro exacto de esta esfera de cuarenta micrómetros, el observador se encuentra rodeado por veinticinco coanocitos dispuestos en una cobertura continua e ininterrumpida, cada uno coronado por un collar de microvellosidades cristalinas y un flagelo único que apunta hacia el interior de la cámara como la vara de un director de orquesta invisible. Los flagelos no laten al unísono sino en fases escalonadas, y esa coordinación imperfecta pero precisa genera una corriente laminar continua que desplaza el agua desde la pared hacia el poro apopilo abierto al frente, un arco de citoplasma rasgado que anuncia la salida hacia los canales internos de la esponja. Dos pequeños poros prosopilares, apenas dos o tres micrómetros de diámetro, perforan la pared ambarína de la cámara como ventanas hacia el océano, dejando pasar hilos casi imperceptibles de agua cargada de bacterias y materia orgánica disuelta que los collares capturarán mediante filtración pasiva. Más allá de la capa celular, el mesoilo se extiende como un encaje traslúcido de fibras de colágeno en tonos dorados, habitado por arqueocitos ameboides que avanzan con sus pseudópodos extendidos, recogiendo y redistribuyendo los nutrientes ya capturados. Todo el conjunto —collar, flagelo, cámara, andamiaje y célula errante— constituye una de las arquitecturas de filtración más eficientes que la evolución ha producido, y su parecido estructural con los coanoflagelados de vida libre sugiere que en este espacio íntimo y luminoso late el ancestro común de todos los animales.
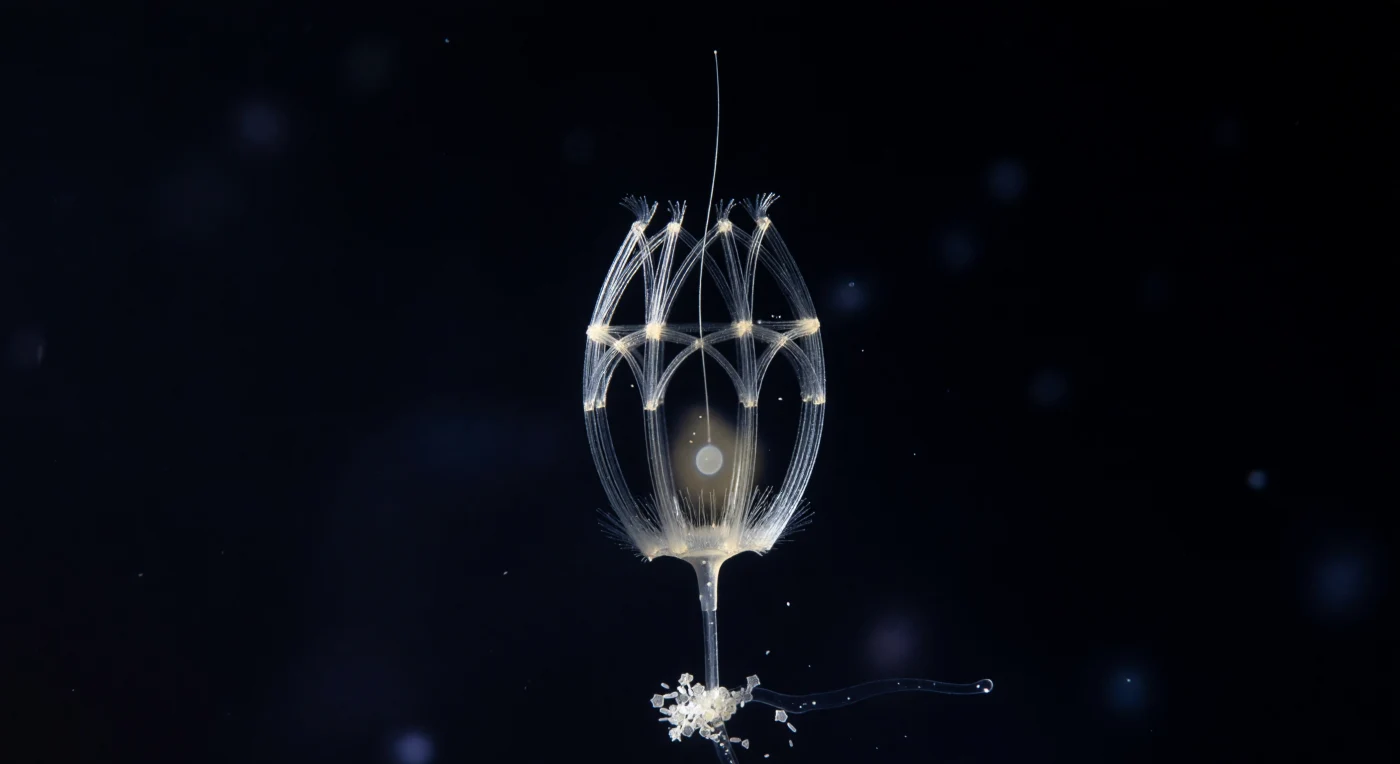
En la oscuridad absoluta de la columna mesopelágica, ante ti se eleva una jaula de barras de sílice entretejidas en dos sistemas de costillas —longitudinales y transversales— que se iluminan con la frialdad de un metal fundido al recibir la luz lateral, transformando cada varilla en un filamento de vidrio incandescente que contrasta con el negro circundante como una catedral gótica suspendida en el vacío. Esta estructura, la lórica de una única célula de *Diaphanoeca grandis*, es fabricada por el organismo a partir de sílice disuelto en el agua marina y ensamblada en dos haces de tiras costales que se entrecruzan con una precisión geométrica surgida de la biología y no del diseño consciente, permitiendo que el agua fluya libremente hacia el interior mientras la célula que la habita genera con su flagelo una corriente helicoidal para capturar bacterias. En el interior de esa arquitectura tan frágil como persistente, la célula viva no es más que una neblina ámbar casi invisible, un núcleo apenas intuido y una corona de microvilli ciliares que disuelven sus contornos antes de alcanzar la resolución, mientras el flagelo asciende por el polo anterior abierto y se pierde en la negrura como un hilo de seda tendido hacia lo desconocido. El tallo rígido que ancla la lórica desciende hasta un agregado de nieve marina donde frústulos de diatomeas y bastones bacterianos —cada uno una décima parte del grosor de la varilla de sílice más delgada— reflejan la luz como diminutos espejos geométricos, recordando que incluso en la oscuridad más profunda, la materia orgánica cae sin cesar y alimenta vidas de una delicadeza casi inverosímil. Los coanoflagelados como éste son los parientes unicelulares más próximos a todos los animales, y el collar de microvilli que los define reaparece, conservado a lo largo de seiscientos millones de años de evolución, en los coanocitos que tapizan las cámaras filtrantes de las esponjas, convirtiendo este organismo solitario en un testigo vivo del instante en que la vida multicelular estaba aún por inventarse.

Suspendido en la oscuridad absoluta del fondo oceánico, el observador se encuentra cara a cara con la pared de un cilindro de vidrio vivo: la malla hexagonal de Euplectella aspergillum se eleva como la nave de una catedral gótica tejida en sílice, cada espícula fusionada en su intersección con las demás para formar un armazón sincicial de precisión casi desconcertante. La sílice actúa como fibra óptica verdadera, canalizando la bioluminiscencia azul-verde del agua circundante a lo largo de toda la longitud de cada varilla, de modo que la estructura entera se convierte en una geometría autoluminosa suspendida en el vacío, sus ventanas cuadradas enmarcando el átrio interior como vitrales de una iglesia sumergida. En las secciones fracturadas de los nodos más próximos se distinguen anillos de laminación concéntrica, capas de sílice depositadas en torno a una plantilla orgánica que el animal fue construyendo durante décadas a razón de milímetros por año, el material semi-transparente y ligeramente ámbar en el núcleo más denso antes de transitar a un blanco glacial en la vaina exterior. Dentro del átrio, dos camarones comensales aparecen como siluetas ámbar-rosadas retroiluminadas por el resplandor interior, sus formas segmentadas y antenas plumosas convertidas en figuras de vitral viviente, sellados para siempre dentro de su catedral de vidrio desde que, siendo larvas, encontraron refugio entre sus paredes y ya no pudieron salir. La columna de agua que pesa sobre toda la escena se percibe únicamente en el silencio total y en la perfecta quietud de esas dos criaturas que se desplazan en arcos lentos, como si el tiempo mismo hubiera espesado junto con la presión.
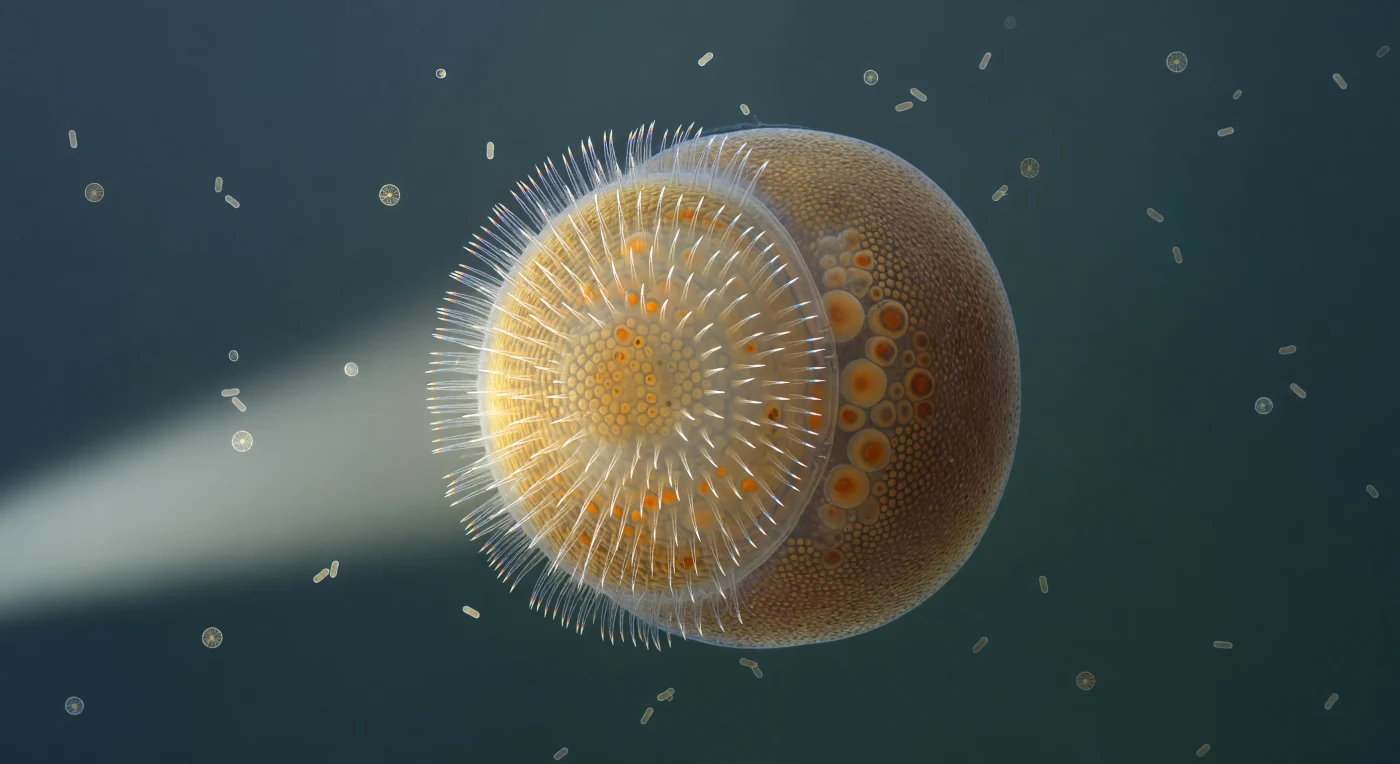
Suspendido en la columna de agua sobre un arrecife rocoso, el visitante se encuentra frente a frente con una larva amphiblástula de esponja calcárea: un óvalo translúcido de unos cuatrocientos micrómetros de diámetro que rota lentamente sobre sí mismo, iluminado desde un lateral por un haz frío de luz blanca que lo divide en creciente radiante y sombra profunda con la precisión de un instrumento óptico. El hemisferio anterior, densamente poblado de cilios que laten en ondas metacrónicas coordinadas a decenas de ciclos por segundo, genera un halo espectral en el borde ecuatorial donde la luz se difracta en arcos de violeta, cian y oro pálido, recordando que incluso esta diminuta franja de membrana viva es capaz de descomponer la luz como un prisma cristalino. El hemisferio posterior, más grande y silencioso, revela a través de su pared traslúcida las masas redondeadas de arqueocitos cargados de lípidos, inclusiones ámbar oscuro que dispersan la luz transmitida como pequeñas linternas apagadas tras un cristal esmerilado, almacenando la energía necesaria para la metamorfosis que transformará esta larva natatoria en un animal sésil filtrador. Esta forma larvaria constituye uno de los momentos más antiguos y conservados de la biología animal: una estructura bifuncional que separa la motilidad ciliar de la reserva vitelina, un diseño que los poríferos llevan perfeccionando desde hace más de seiscientos millones de años. Dispersos en el agua azul-verdosa que rodea la larva, diatomeas con sus frústulas grabadas y bacterias en deriva browniana recuerdan que este organismo navega un ecosistema microbiano denso del que extraerá todo lo necesario para sobrevivir.

Te encuentras suspendido en agua marina tibia y cargada de sal, flotando en el borde mismo del ósculum de una enorme esponja barril tropical, mirando hacia el interior de una chimenea circular de unos cuatro centímetros de diámetro que desciende en terracota quemada y naranja profundo, sus paredes corrugadas y porosas recordando a una piedra arenisca impregnada de óxido de hierro, mientras que abajo los canales exhalantes ramificados se pierden en sombras ámbar. Desde esta abertura asciende sin pausa una corriente exhalante de agua filtrada: la esponja bombea aproximadamente 20.000 veces su volumen corporal al día, trabajo realizado por miles de coanocitos internos que baten sus flagelos a 30–60 Hz en cámaras esféricas de apenas 25–50 micrómetros de diámetro, generando un flujo laminar coordinado que se convierte, a esta escala, en el chorro tembloroso y cargado de partículas que ahora asciende hacia ti, dispersando detritus orgánico, nubes pálidas de bacterias y fragmentos silíceos en lentas espirales iluminadas por la luz turquesa que ondula desde la superficie. La pared exterior de la esponja se extiende en todas direcciones desde el borde del ósculum, salpicada de ostios oscuros y colonizada por algas coralinas lavanda y encajes blancos de briozoos, mientras que en el fondo cálido y desenfocado ramas de coral y peces arrecifales de cobalto y amarillo derivan sin prisa, recordando que toda esta arquitectura filtrante y viva pulsa sin cesar desde hace más de 600 millones de años, en el umbral mismo donde el origen de los animales sigue haciéndose visible.
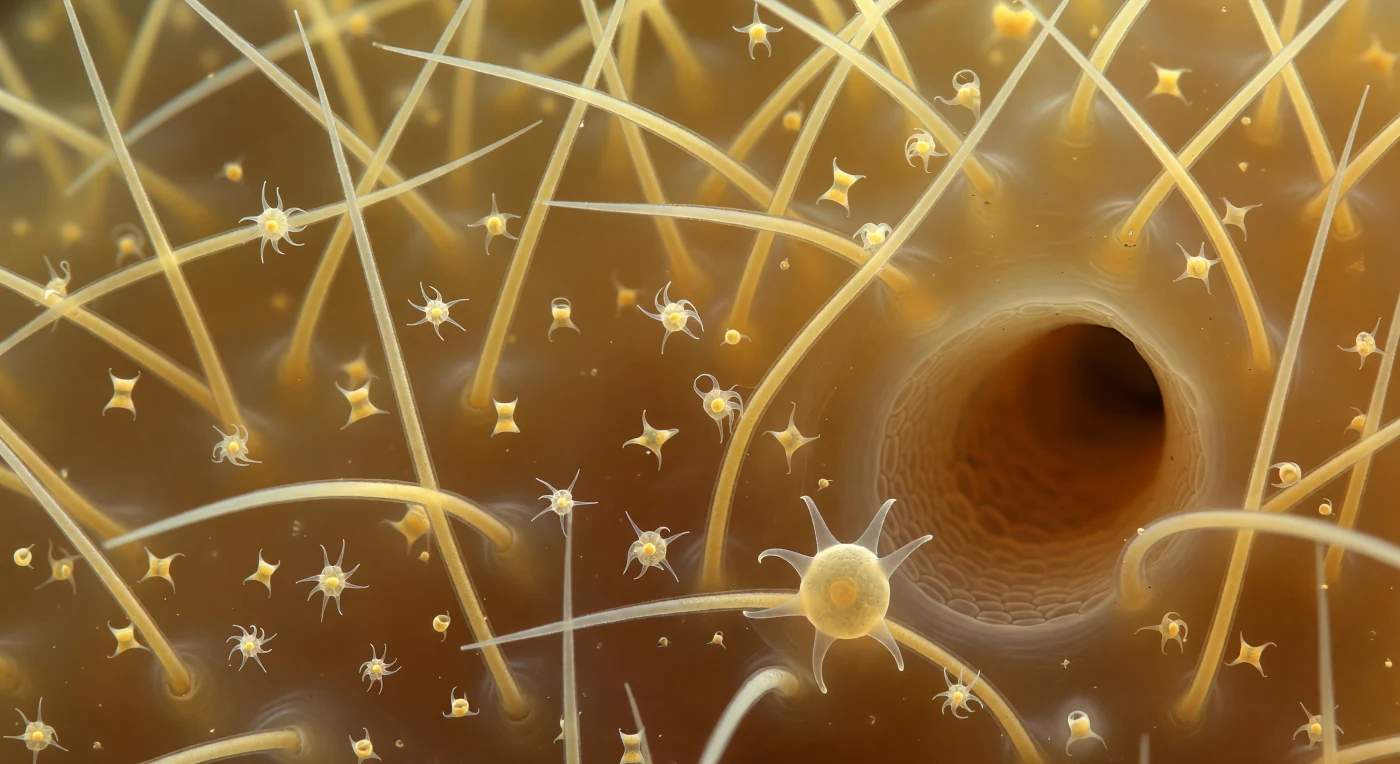
Adrift en el interior ámbar de la mesohila de una esponja demosponja, te encuentras suspendido entre una catedral de agujas de sílice —las megaescleras oxeas— que se elevan en todas direcciones con sus doscientas micras de longitud, captando la luz en reflejos especulares brillantes que recorren toda su longitud curva y translúcida color crema. El gel que las rodea, coloreado como miel retroiluminada, no es un vacío pasivo sino una matriz coloidal viva: en él derivan microscleras en forma de sigma y quelas espirales que giran lentamente por el movimiento browniano, cada una una diminuta escultura de vidrio que captura y devuelve la luz ámbar como un joyel en suspensión. Las fibras de espongina conectan las bases de las espículas como cables de oro orgánico, formando el andamiaje tensil que unifica toda la arquitectura porosa, mientras un túnel de canal oscuro se abre en diagonal a través del campo medio, sus paredes de pinacodermo apenas visibles como una tesela poligonal en el borde de esa caverna de sombra cobriza por donde circula el agua filtrada. Sobre una de las espículas del primer plano, un arqueocito solitario despliega sus pseudópodos en láminas traslúcidas, su núcleo denso visible como una esfera ámbar en el centro del citoplasma, manteniendo con tacto lento y químico la empresa constructiva del animal más antiguo de la historia de la vida pluricelular.
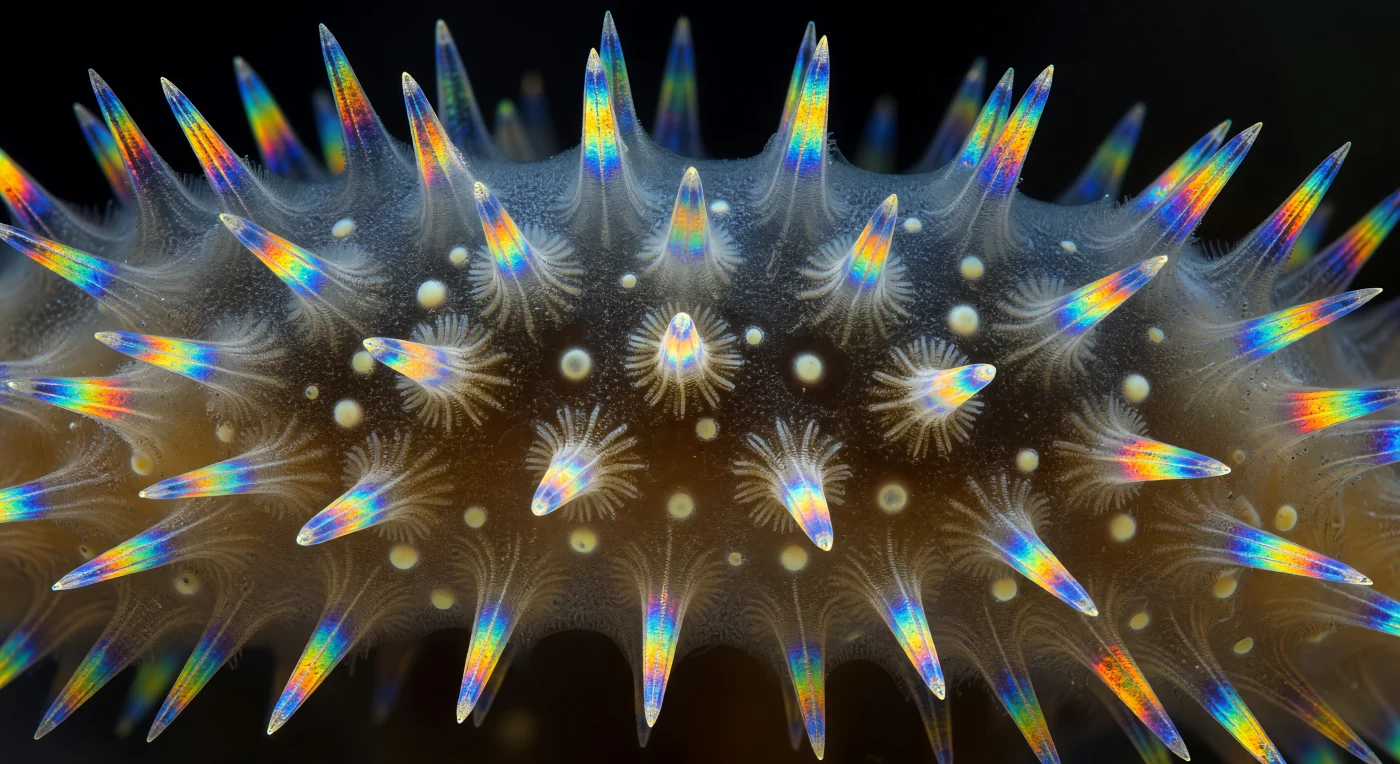
En el interior de la pared de un Sycon ciliatum seccionado transversalmente, el mundo visible es una arquitectura de luz y mineral vivo: canales radiales se abren como naves de una catedral gótica, separados por tabiques de mesohilo ambarino denso y fibroso, mientras espículas de calcita triactina y tetractina estallan en el campo visual con una brillantez alucinante bajo luz polarizada, ardiendo en azul cobalto eléctrico, amarillo azufre, naranja fundido y verde esmeralda contra un fondo de negro absoluto. Cada espícula es un cristal óptico activo: la birrefringencia de la calcita descompone la luz polarizada en retardos de fase que el analizador traduce en colores espectrales puros, con gradientes cromáticos nítidos a lo largo de sus rayos y puntos de luz blanco-dorada donde las puntas se proyectan perpendicularmente hacia el observador como agujas en un alfiletero. Donde varias espículas se cruzan, sus patrones de interferencia se superponen en aureolas iridiscentes que derivan del ámbar al violeta y al azul verdoso, el equivalente óptico de una vidriera iluminada por luz invernal. El mesohilo entre los canales no es vacío sino una matriz extracelular granulosa y viva, habitada por arqueocitos cuyos núcleos flotan como linternas pálidas en la penumbra, mientras los lúmenes de los canales se abren como corredores vastos en relación con las secciones transversales de las espículas, generando una sensación vertiginosa de espacio interior dentro de un organismo que no supera el tamaño de una uña. La escena entera es geometría biológica congelada en fuego espectral: parte mineral, parte tejido vivo, parte pura óptica.

En las profundidades heladas del Pacífico nororiental, a doscientos metros bajo la superficie, las torres del arrecife de esponjas de vidrio *Aphrocallistes vastus* se alzan desde el sedimento calcáreo como agujas de una catedral sumergida, sus esqueletos de espículas de sílice fundidas tejidas en una malla hexagonal de precisión geométrica extraordinaria. El haz del ROV golpea la columna más cercana desde abajo, y la sílice conduce la luz a lo largo de cada estribo vítreo como si fueran cables de fibra óptica, encendiendo la torre desde su interior con una luminiscencia cálida de marfil y ámbar que convierte cada cámara vacía en una vidriera de alabastro retroiluminada. El sedimento a los pies de la torre destella con miles de fragmentos de espículas rotas que devuelven la luz como agujas de vidrio microscópico, mientras estrellas frágiles enrollan sus brazos bicromos a través de los hexágonos de la celosía y un pez de roca permanece inmóvil en la oscuridad entre columnas, su ojo atrapando el haz como un único punto de luz viva. Más allá del borde del haz, un rastro de puntos azul-verdosos bioluminiscentes cruza el campo de visión y se extingue en tres segundos, recordando que este bosque de torres de vidrio —extendiéndose en la oscuridad cientos de metros en todas las direcciones— bombea colectivamente volúmenes de agua equivalentes a miles de veces su propio cuerpo cada día, filtrando el océano con una paciencia de escala geológica.

Suspendido en la capa límite bentónica, tu campo visual entero queda consumido por un terreno que a esta escala se lee como una vasta meseta alienígena: la alga coralina costrosa se extiende como una tundra magenta-carmesí fracturada, sus placas calcáreas poligonales bordeadas por crestas tectónicas teñidas de lavanda pálida y rosa, salpicadas por frústulas de diatomea que se alzan como monumentos de sílice vitrificada, hexagonales y radialmente simétricas, algunas intactas y centelleantes como ventanas de catedral atrapando la luz azul-verdosa que desciende desde la columna de agua, otras rotas en esquirlas que capturan el haz oblicuamente. Entre ellas, el biofilm bacteriano se despliega como una matriz de ámbar translúcido, un laberinto de filamentos de exopolisacárido que se acumula en las depresiones del sustrato, iridiscente con la física coloidal de la materia orgánica disuelta. En el centro de la escena, la larva de esponja calcaréa —un disco crema-ámbar de apenas trescientas micras— se encuentra atrapada en el instante más radical de su metamorfosis: la inversión morfogenética que transforma un organismo natante y ciliado en un organismo sésil filtrante, su hemisferio apical invaginándose hacia adentro mientras los futuros pinacocitos del margen externo se aplanan ya en teselados de pavimento y se propagan lateralmente sobre la superficie del alga en ondas concéntricas, como un frente de cristalización lento, sus bordes más delgados translúcidos al contraluz como una membrana de vitral ámbar que concentra toda la luz del océano frío.
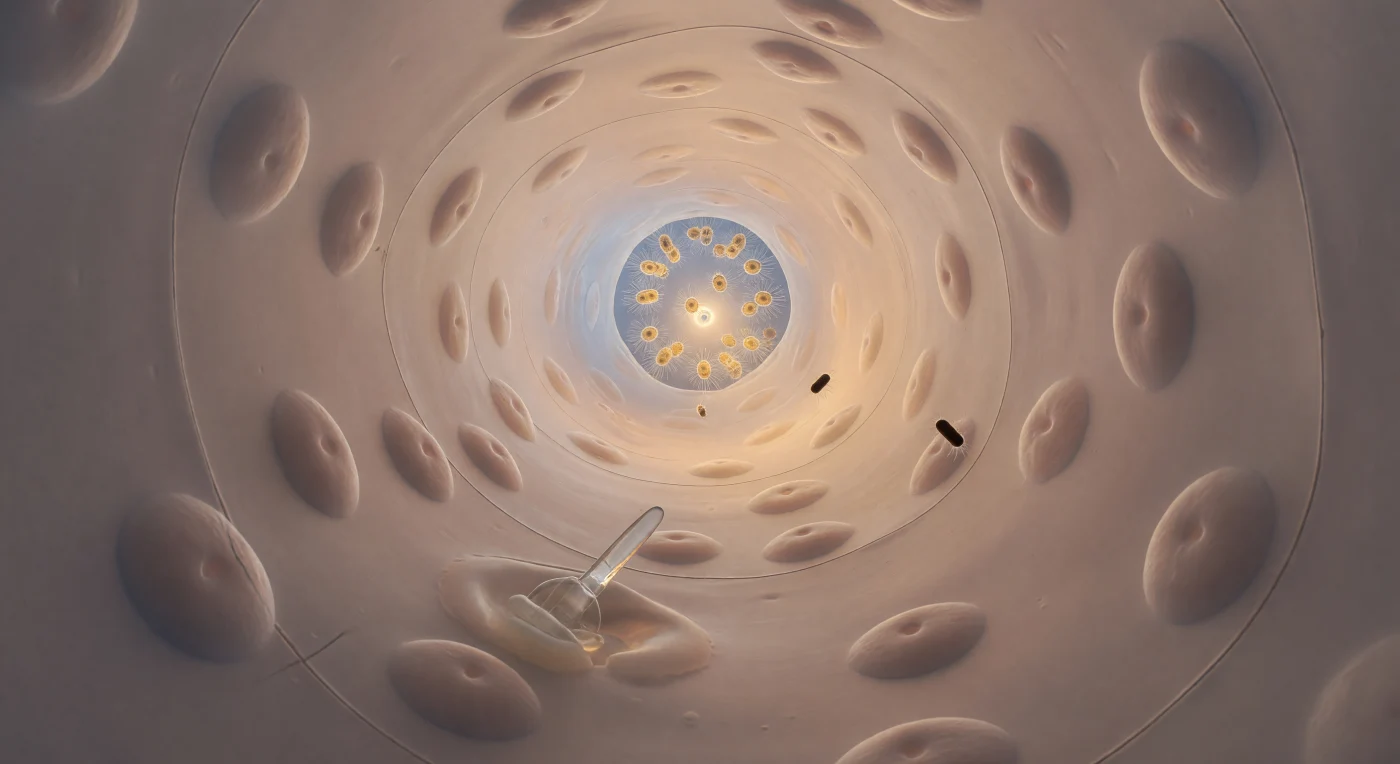
Dentro del cuerpo de una esponja, el observador se encuentra suspendido en la entrada de un canal inhalante, un túnel cilíndrico de apenas setenta micrómetros de diámetro cuyas paredes vivas se curvan suavemente hacia adelante hasta desaparecer en un punto luminoso de ámbar cálido: la prosopila, un poro de cinco micrómetros que da acceso a la cámara de coanocitos palpitante en su interior. Las paredes del canal están tapizadas por endopinacocitos aplanados como láminas de seda húmeda, sus membranas casi especulares salvo por los suaves abultamientos de los núcleos que emergen como colinas de cristal bajo la superficie translúcida de marfil y melocotón; en la pared inferior, una espícula de carbonato cálcico atraviesa el tejido a bajo ángulo y capta la luz transmitida proyectando un destello prismático sobre las células vecinas, mientras un arqueocito ameboide se deforma lentamente a su alrededor, empujando su citoplasma entre las uniones celulares como cera tibia. La corriente que conduce al observador hacia adelante no fluye en ningún sentido ordinario: el régimen de Stokes convierte el agua en un medio casi viscoso, silencioso y laminar, y las bacterias con forma de bastón que derivan a su lado giran con imperceptible suavidad sin que ninguna turbulencia las perturbe. Detrás, la boca del canal enmarca un resplandor azul blanco de océano abierto, recordando que este pasaje es un nodo de una arquitectura de filtración que lleva seiscientos millones de años conduciendo el mar a través de la carne viva, una bacteria a la vez.
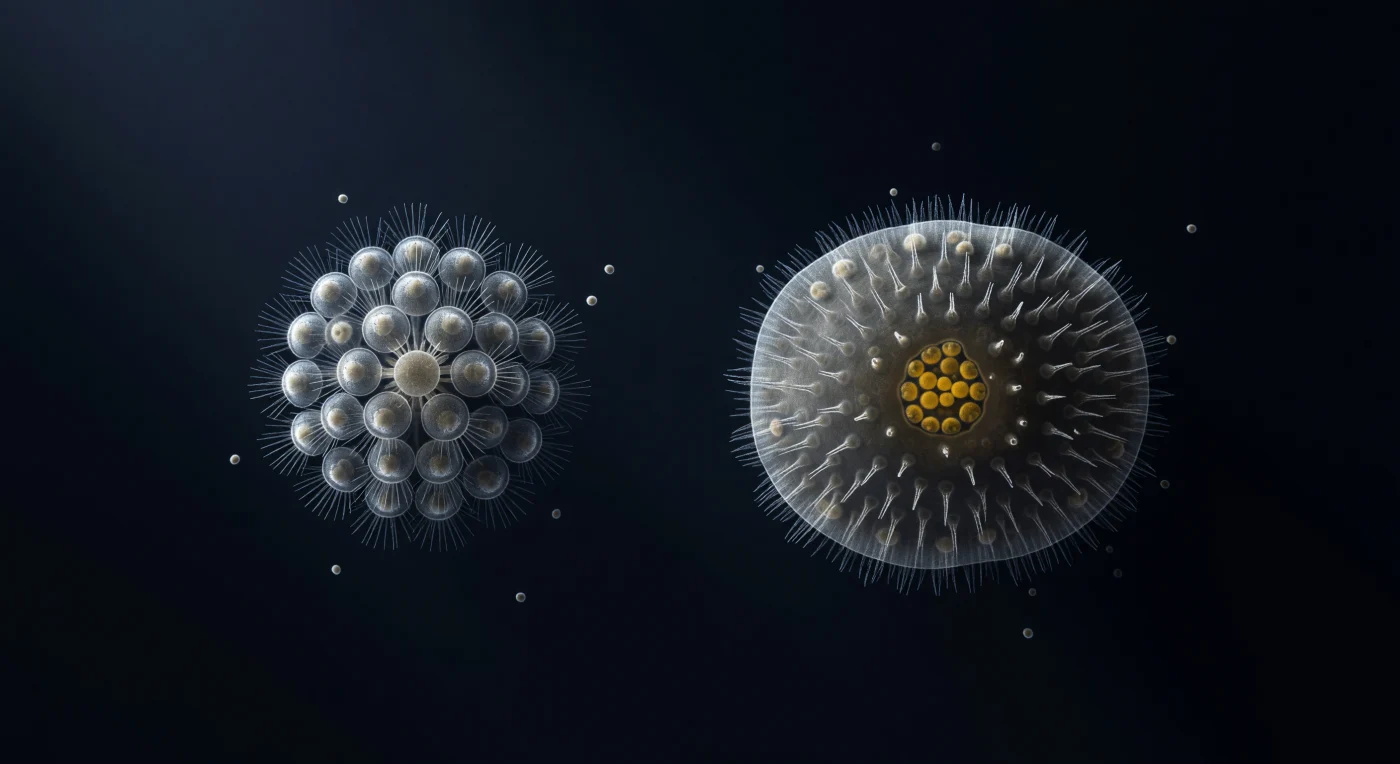
En este campo de visión iluminado por contraste de interferencia diferencial, dos organismos flotan separados por cien micras de océano silencioso: a la izquierda, una colonia en roseta de *Salpingoeca rosetta* de treinta y dos células se sostiene como una esfera de vidrio viviente, sus unidades collar-flagelo apuntando hacia afuera en una arquitectura casi cristalina, cada collar una jaula cilíndrica de microvellosidades de actina captando la luz oblicua como agujas de plata; a la derecha, una larva parenchymela de esponja calcárea domina el campo con su masa interior densa y semiopaca, su capa superficial de células ciliadas revelada por el relieve dramático del DIC como un manto de filamentos plateados aplastados contra la membrana, y en su polo posterior, las células vitelinas cargadas de lípidos arden en el único tono cálido de toda la escena, un ámbar dorado que arde como brasas en una habitación de hielo. La luz rasante proveniente del ángulo superior izquierdo esculpe cada membrana en bajo relieve de alto contraste, convirtiendo el agua misma en un medio de presencia viscosa faintly perceptible, un océano comprimido en doscientas micras. Lo que hace de esta imagen algo más que una simple composición de microscopía es lo que ocurre en el interior de esa larva: hacia su hemisferio anterior, donde la luz penetra con mayor profundidad a través de un citoplasma más delgado, ciertas células internas ya traicionan la sombra de una morfología collar, condensaciones apicales minúsculas que apuntan hacia un plan corporal que la evolución lleva ensayando desde hace setecientos millones de años, mientras el vacío acuoso entre los dos organismos —aparentemente vacío salvo por unas pocas siluetas bacterianas a la deriva— carga en su transparencia toda la distancia entre la vida colonial y la multicelularidad animal verdadera.

Suspended dentro de la pared cortada de la gémmula, contemplas un universo de contención perfecta: una fortaleza laminada de tres capas que te rodea como los muros de una catedral seccionada, donde la membrana exterior —ambarino translúcido, ligeramente iridiscente— cede paso a una empalizada de espículas anfidisco de sílice cristalina, cada una un diminuto mancuerno cuyos discos rotulares se ensamblan como postes helados que lanzan destellos prismáticos en blanco glacial, azul fantasma y rosa pálido, todo embebido en cemento de espongina color crema. Más adentro, una capa lisa de espongina color miel curva hacia la cavidad interior donde los arqueocitos, apretados hombro con hombro en esferas de diez a veinte micrómetros, arden como faroles de azafrán, naranja tangerina y amarillo cadmio, cargados de vesículas lipídicas que concentran las reservas energéticas necesarias para sobrevivir el invierno en animación suspendida. A la derecha, el tubo del micrópilo perfora la armadura —un pasaje tapado por una columna de células pálidas apretadas como corchos— cuya apertura circular se asoma hacia un exterior de agua fría color oliva oscuro, haciendo que el resplandor ámbar del interior resulte aún más intenso y vital. Esta estructura, la gémmula de Spongilla lacustris, representa uno de los dispositivos de resistencia más sofisticados de los invertebrados de agua dulce: una cápsula de supervivencia con paredes reforzadas por espículas biosilíceas organizadas por señalización genética homóloga a la de los tejidos animales más complejos, testimonio del linaje evolutivo que une a las esponjas con los ancestros de todos los animales.

En el envés oscuro y empapado de un tronco sumergido, una esponja de agua dulce se despliega como una alfombra viva de terciopelo verde eléctrico, encendida desde dentro por los cloroplastos de las miles de algas simbióticas que habitan sus tejidos y que atrapan cada destello de luz que se filtra desde la superficie ondulante del arroyo. La textura de esta costra viva es una contradicción sensorial: suave a la vista pero erizada de agujas de sílice, las espículas de la armadura interna del animal, cuyos extremos capturan la luz como cristales de escarcha y proyectan un halo plateado sobre toda la superficie. Sobresaliendo de ese tapiz verde como adoquines enterrados, las gémulas —esferas color caoba de medio milímetro, selladas herméticamente y ornamentadas con arquitecturas radiales de espículas— esperan inmóviles, cápsulas de supervivencia llenas de células madre capaces de reconstruir un organismo completo cuando el frío o la sequía destruyan al organismo que las produce. Por la superficie se deslizan ostrácodos cuyas valvas bivalvas relumbran como perlas rodando por seda, y planarias translúcidas cuyo vientre deja ver el verde de la esponja a través de su propio cuerpo; sobre todo ellos, la columna de agua del arroyo se alza como una catedral de claridad verde y fría, sus haces de luz desplazándose en lentas oleadas sobre este organismo cuyo diseño fundamental —bombear, filtrar, albergar— no ha cambiado en seiscientos millones de años.

La piel de esta esponja demospongia tropical se extiende bajo la mirada como un pavimento vivo de teselas poligonales de color naranja terracota ardiente, cada borde celular levantado en una cresta fina que captura la luz difusa del arrecife y dibuja sombras suaves en las ranuras que separan los exopinacocitos, confiriendo al conjunto la apariencia de cerámica lacada calentada desde dentro por la concentración de pigmentos carotenoides. Salpicando esta llanura de quince a treinta micrómetros por azulejo, los ostios se abren como calderas volcánicas de distintas magnitudes: algunos completamente dilatados muestran la oscuridad absoluta del sistema de canales inhalantes que desciende hacia el interior del animal, mientras que otros están casi cerrados, reducidos a una hendidura pálida por la contracción del porocito bajo la presión del gradiente de filtración. Sobre la superficie, una biopelícula de pocas micras de espesor —bacterias en bastón, colonias de cocos y cianobacterias filamentosas entretejidas en hebras de mucopolisacáridos que iridiscen con la luz del arrecife— recubre las teselas como una escarcha translúcida que registra en tres dimensiones la intensa negociación metabólica entre el huésped y sus comensales microbianos. Un poliqueto emerge de uno de los ostios mayores arqueando su cuerpo pálido y segmentado sobre el umbral del canal, sus palpos ciliados barriendo la capa límite en abanicos lentos de luz dorada, mientras en el extremo opuesto del campo visual un copépodo aterriza fugaz, su caparazón vítreo refractando el azul ambiental como una lente antes de ser desviado por el gradiente de presión invisible que emana de un ósculum próximo.
















