Confiance scientifique: Élevé
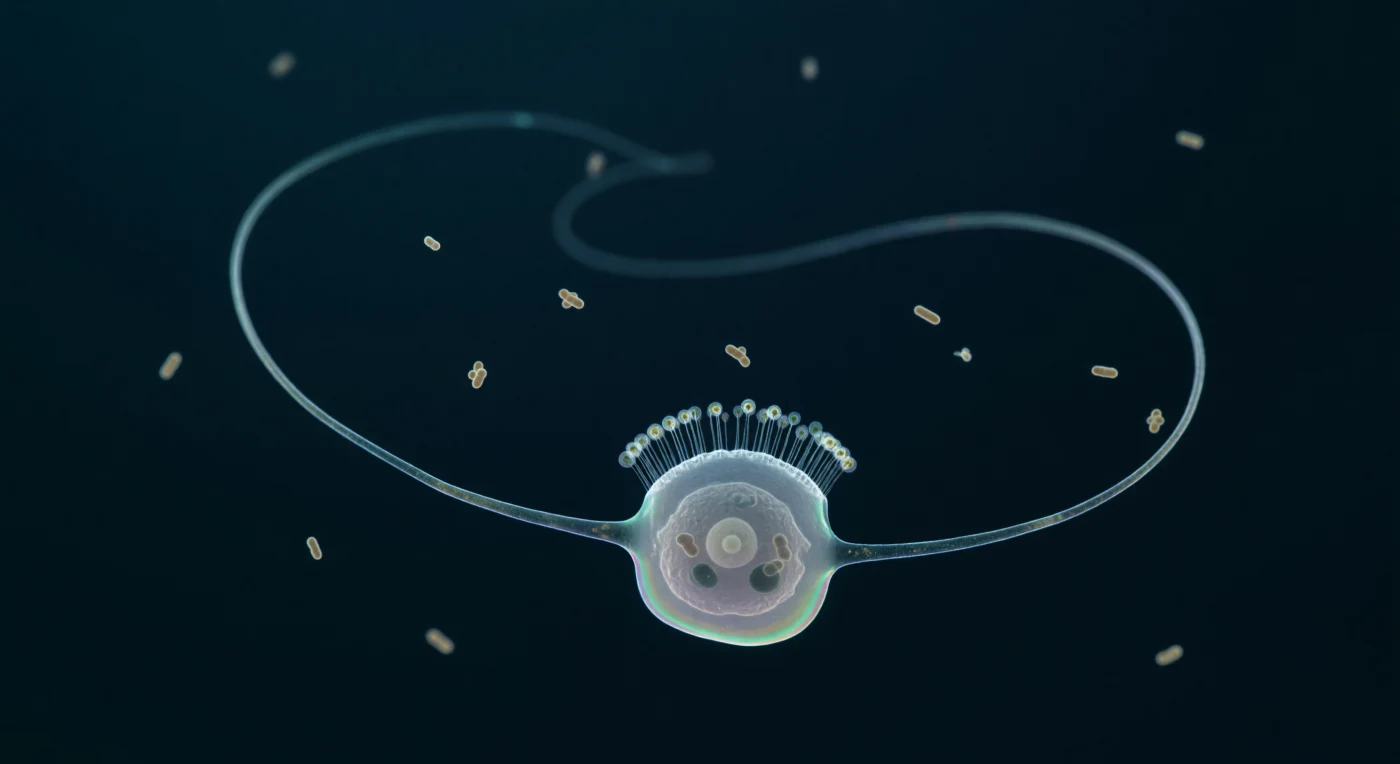
Vous êtes suspendu dans un vide pélagique d'un bleu-noir absolu, un milieu qui n'est ni eau ni air mais quelque chose de troisième — visqueux, résistant, saturé du tremblement thermique invisible des molécules qui vous pressent de toutes parts avec la douceur froide de la glycérine. La présence qui domine votre monde est le flagelle : un fouet sinueux de vingt microns, enroulé en S hélicoïdal à travers presque tout votre champ visuel, son axe pas plus épais qu'un fil de soie d'araignée mais rendu lumineux par la lueur bleue-verte qui filtre de quelque part au-dessus, et derrière lui, fantômée dans le milieu sombre comme une mémoire structurale, une traîne argentée témoigne de la vague sinusoïdale qui vient de traverser sa longueur une fraction de seconde plus tôt. Le corps cellulaire lui-même — une gouttelette presque incolore de sept microns à peine — révèle à travers sa membrane translucide un noyau pâle comme une lune brumeuse, flanqué de deux vacuoles alimentaires opaques dont chacune emprisonne encore la silhouette comprimée d'une bactérie à demi digérée, tandis que la collerette de trente-cinq microvillosités encercle la base du flagelle comme une cage quasi invisible, fracturant la lumière descendante en couronnes d'interférences irisées d'or froid et d'aquamarine. À l'arrière-plan, une douzaine de bactéries en bâtonnet dérivent dans le champ profond, tremblant sur place sous l'agitation brownienne, se dissolvant en bokeh dans le gradient de bleu profond qui, à dix microns de votre visage dans chaque direction, se referme en noir absolu.

À quelques dizaines de micromètres de distance, une sphère d'une quarantaine de micromètres de diamètre occupe tout votre champ de vision comme une lune-lustre en lente rotation : la colonie en rosette de *Salpingoeca rosetta*, trente-deux cellules disposées en géométrie radiale parfaite, chacune pointant vers l'extérieur avec son flagelle déployé en couronne électrisée qui donne à l'ensemble la silhouette d'un oursin microscopique suspendu dans les eaux estuariennes. Chaque corps cellulaire — un ovoïde translucide de trois à cinq micromètres — est rendu dans la palette argentée et quasi-achromatique de la microscopie en contraste interférentiel différentiel, avec l'ombre plus dense du noyau visible en son intérieur, tandis qu'à deux heures une cellule en cours de division affiche son corps légèrement étranglé en forme d'arachide, ses deux noyaux-filles décalés dans le cytoplasme qui s'allonge. Les pôles basaux de toutes les cellules convergent vers un cœur d'extracellulaire matrice d'un ambre chaud et légèrement translucide — seule note de couleur chaude dans cet univers de tons froids —, reliés par des ponts cytoplasmiques si ténus qu'ils n'apparaissent que comme des filaments à peine plus brillants que le milieu environnant. Cette architecture coloniale, à la frontière exacte entre unicellularité et multicellularité, incarne l'un des plus anciens carrefours évolutifs connus : le groupe frère des animaux, dont les choanocytes des éponges modernes conservent le même plan d'organisation, la même couronne de microvillosités filtrantes autour d'un flagelle battant à trente à soixante hertz, pompant l'eau océanique depuis des centaines de millions d'années.
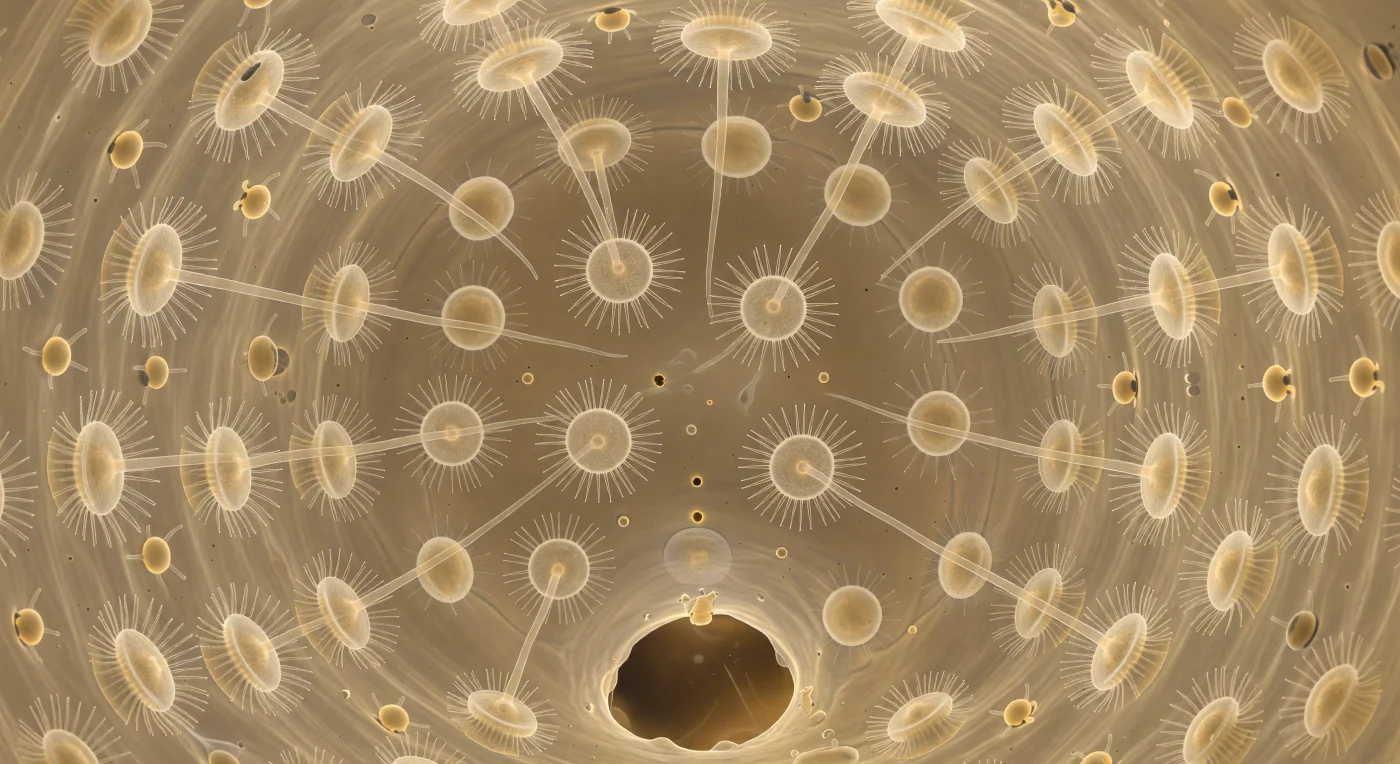
Suspendu au centre exact de cette sphère vivante d'une quarantaine de micromètres de diamètre, le regard embrasse en un seul coup d'œil la totalité d'une chambre choanocytaire de l'éponge — une pièce close dont chaque paroi est tapissée sans interruption de cellules choanocytes debout, chacune couronnée d'un collet de microvillosités cristallines d'où émerge un flagelle unique qui bat en rythme décalé avec ses voisins, insufflant à l'ensemble une ondulation continue et organique semblable à un champ d'anémones bercées par un courant imperceptible. Deux pores prosopyles, sombres et circulaires, percent la paroi ambrée à deux-o'clock et huit-o'clock, livrant passage à de fins filets d'eau chargés de bactéries fantômes, tandis que devant soi s'ouvre en grand l'apopyle, l'arche de sortie dont le bord cytoplasmatique effiloché donne sur le réseau canalaire au-delà. La lumière qui enveloppe cet espace n'a pas de source directe : elle est biologique, filtrée à travers plusieurs micromètres de membrane et de matrice extracellulaire avant d'arriver ici comme une lueur ambre sans ombre ni direction, traversée de reflets prismatiques que découpent les flagelles en mouvement. Dans la couche de mésohyle visible derrière la paroi cellulaire, un treillis de fibres collagéniques dorées retient des archéocytes amiboïdes qui dérivent avec la lenteur du verre en fusion, portant en eux la mémoire évolutive du pont entre la cellule solitaire et le premier animal multicellulaire.
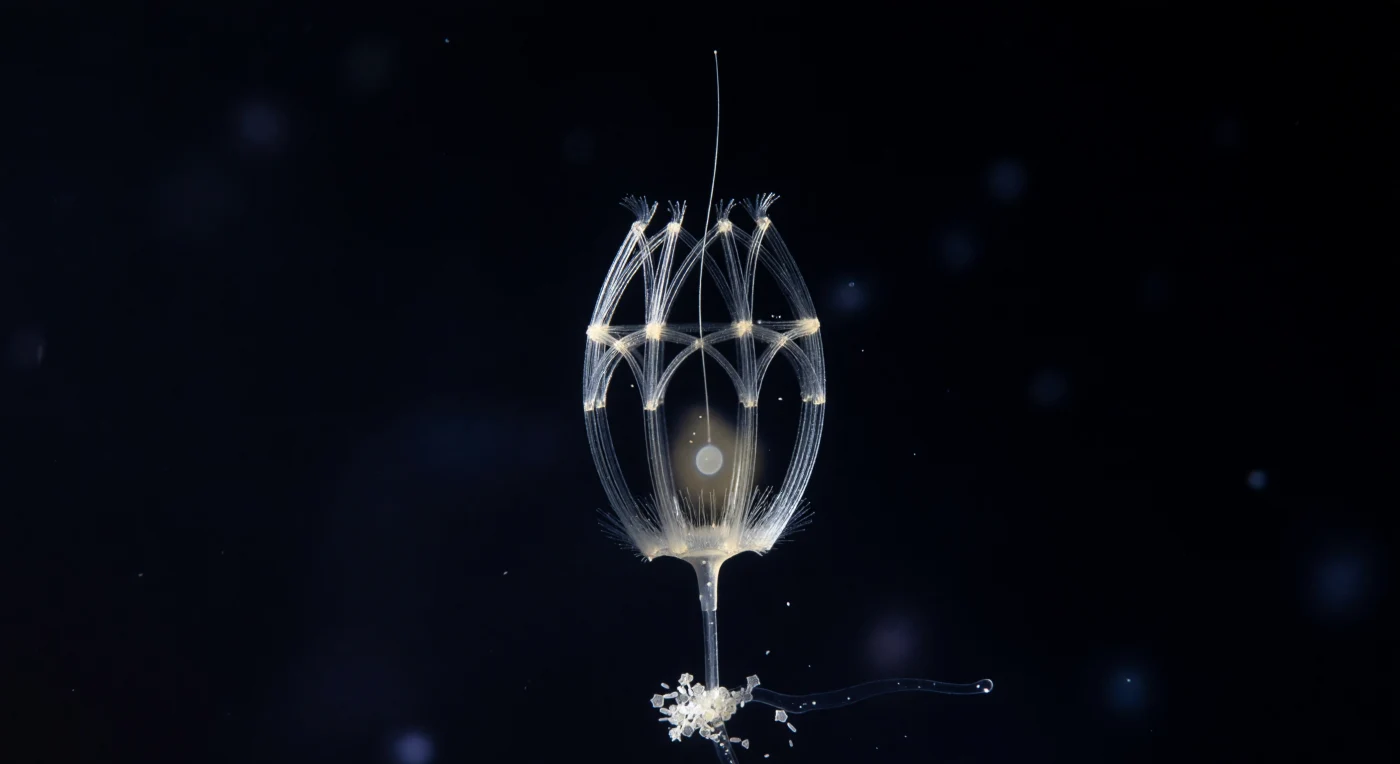
Dans les abysses mésopelagiques, là où nulle lumière naturelle ne pénètre, une structure d'une précision architecturale stupéfiante occupe le centre du champ de vision : la lorica de *Diaphanoeca grandis*, cage gothique de vingt microns assemblée à partir de bâtonnets de silice organisés en deux systèmes entrecroisés — nervures longitudinales s'élevant de la base au sommet comme les ogives d'une voûte cathédrale, cerclées à intervalles réguliers par des anneaux transversaux — et que la lumière latérale froide fait brûler en fils d'argent contre le noir absolu, révélant par contraste extrême la profondeur et le volume de cette géométrie trop précise pour sembler accidentelle. À l'intérieur du treillis lumineux, la cellule vivante n'est qu'une rumeur : une brume cytoplasmique ambrée à peine perceptible, d'où s'élève le flagelle unique qui passe par le pôle antérieur ouvert et se prolonge dans les ténèbres comme une ligne translucide effilée jusqu'au néant, rappelant que cette architecture de verre gelé est avant tout un organisme en train de filtrer l'eau de mer. La lorica repose sur un pédoncule ancré à un fragment de neige marine dont les frustules de diatomées captent la lumière rasante comme de minuscules miroirs hexagonaux, et dont les bâtonnets bactériens disséminés constituent autant de rappels de l'échelle — chacun dix fois plus petit que le rod de silice le plus fin de la cage. Cette cellule solitaire appartient aux choanoflagellatés, protistes à collerette dont l'organisation intime — flagelle unique entouré de microvillosités filtrantes — est aujourd'hui reconnue comme le miroir évolutif des choanocytes qui tapissent les chambres filtrantes des éponges, faisant de cette minuscule lanterne siliceuse un jalon vivant à la frontière même de l'origine des animaux.

Au cœur des abysses, une structure se dresse dans l'obscurité absolue comme une cathédrale de lumière froide : le squelette d'*Euplectella aspergillum*, éponge hexactinellide dont la paroi cylindrique tisse un damier parfait de spicules de silice fusionnés en un réseau syncytial d'une précision déconcertante, si régulière qu'elle semble davantage conçue par un ingénieur que façonnée par le vivant. Chaque spicule conduit la faible luminescence bleue-verte de l'eau environnante comme une véritable fibre optique, irradiant depuis son cœur même une lueur fantomatique qui se propage sur toute sa longueur et projette à l'intérieur de l'atrium central des grilles d'ombres géométriques en perpétuelle imbrication. Sur les sections fracturées visibles aux nœuds les plus proches, des anneaux de lamination concentriques témoignent de la croissance lente de cette silice biogène, matière semi-transparente dont l'ambre du cœur se fond en un blanc glaciaire vers la gaine externe, l'ensemble déposé autour d'un gabarit organique depuis longtemps disparu. À l'intérieur de cette lanterne de verre, deux crevettes commensales apparaissent en silhouettes ambrées et rosées, leurs antennes translucides découpées par la lueur intérieure — prisonnières volontaires d'une chambre close depuis leur métamorphose, dépendantes à jamais du flux d'eau filtrée que leur hôte de verre ne cesse, en silence, de faire passer à travers lui.
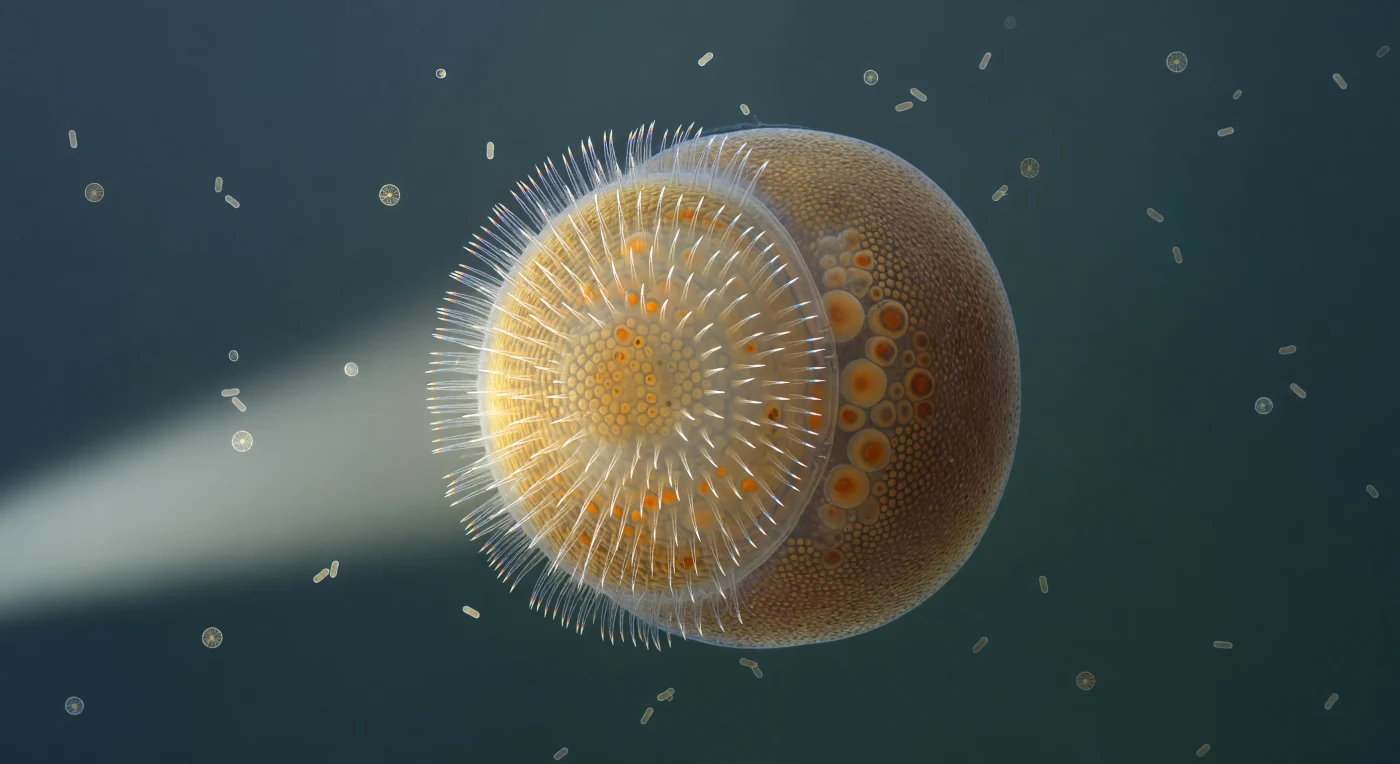
Dans l'eau ouverte au-dessus d'un récif rocheux, une larve amphiblastule d'éponge calcaire d'environ 400 microns occupe le champ visuel comme un monde à part entière — un ovale translucide tranché en deux hémisphères radicalement distincts, l'un doré et vibrant, l'autre sombre et laiteux, tous deux révélant leur géométrie interne comme une lanterne à paroi fine. L'hémisphère antérieur est entièrement tapissé de cellules ciliées dont les cils battent en ondes métachronales coordonnées, créant une frange scintillante qui diffracte la lumière latérale en un mince halo spectral — violet, cyan, or pâle — pulsant et se reformant sans cesse à la périphérie de la larve. L'hémisphère postérieur, plus grand et plus calme, est occupé par des archéocytes gorgés de réserves lipidiques, leurs inclusions ambré-brun visibles par transparence comme des sphères pressées les unes contre les autres dans une architecture dense et serrée, pendant que l'ensemble dérive dans une colonne d'eau bleu-vert peuplée de diatomées et de bactéries indifférentes. Cette larve libre-nageuse représente une phase éphémère et critique du cycle de vie des éponges : avant de se poser sur un substrat et de se métamorphoser en jeune spongiaire sessile, elle explore activement son environnement, propulsée par ses cils et guidée par des gradients chimiques et lumineux, portant en elle les instructions cellulaires complètes pour édifier l'un des plus anciens plans d'organisation animaux connus.

Au bord de l'osculum de cette éponge tonneau, le regard plonge dans une cheminée circulaire d'environ quatre centimètres de diamètre dont les parois intérieures, couleur terre cuite et orange brûlé, descendent en pente abrupte vers des canaux exhalants ramifiés se perdant dans l'ombre ambrée — à cette distance, la structure évoque la bouche d'un volcan vivant plutôt qu'un filtre biologique. L'éponge pompe en permanence des volumes d'eau équivalant à vingt mille fois sa propre masse corporelle chaque jour, un exploit accompli par des milliers de chambres à choanocytes tapissées de cellules à collerette microscopiques dont les flagelles battent en chœur à une trentaine de cycles par seconde, poussant chaque particule de nourriture vers les microvillosités qui la capturent. Le courant d'expulsion qui monte depuis l'osculum se trahit dans la colonne d'eau par un frémissement de mirage thermique, des stries de détritus organiques translucides — sphères ambrées, nuages bactériens, fragments siliceux — emportés en spirale dans la lumière turquoise qui filtre depuis la surface et diffracte sur chaque crête des parois de tissu vivant. Ces choanocytes, architectes discrets de toute cette machinerie hydraulique, sont les homologues évolutifs directs des choanoflagellés unicellulaires libres qui colonisent la même eau de récif, un lien cellulaire qui relie l'origine de la multicellularité animale à ce jet continu et silencieux. La surface externe de l'éponge s'étale autour du bord de l'osculum comme un plateau de grès imprégné d'oxyde de fer, troué de puits d'ostia sombres et colonisé par des algues coralliennes lavande et des dentelles de bryozoaires crème, pendant que des poissons flous de cobalt et de jaune dérivent dans les coraux en arrière-plan, indifférents à l'architecture respirante qu'ils longent.
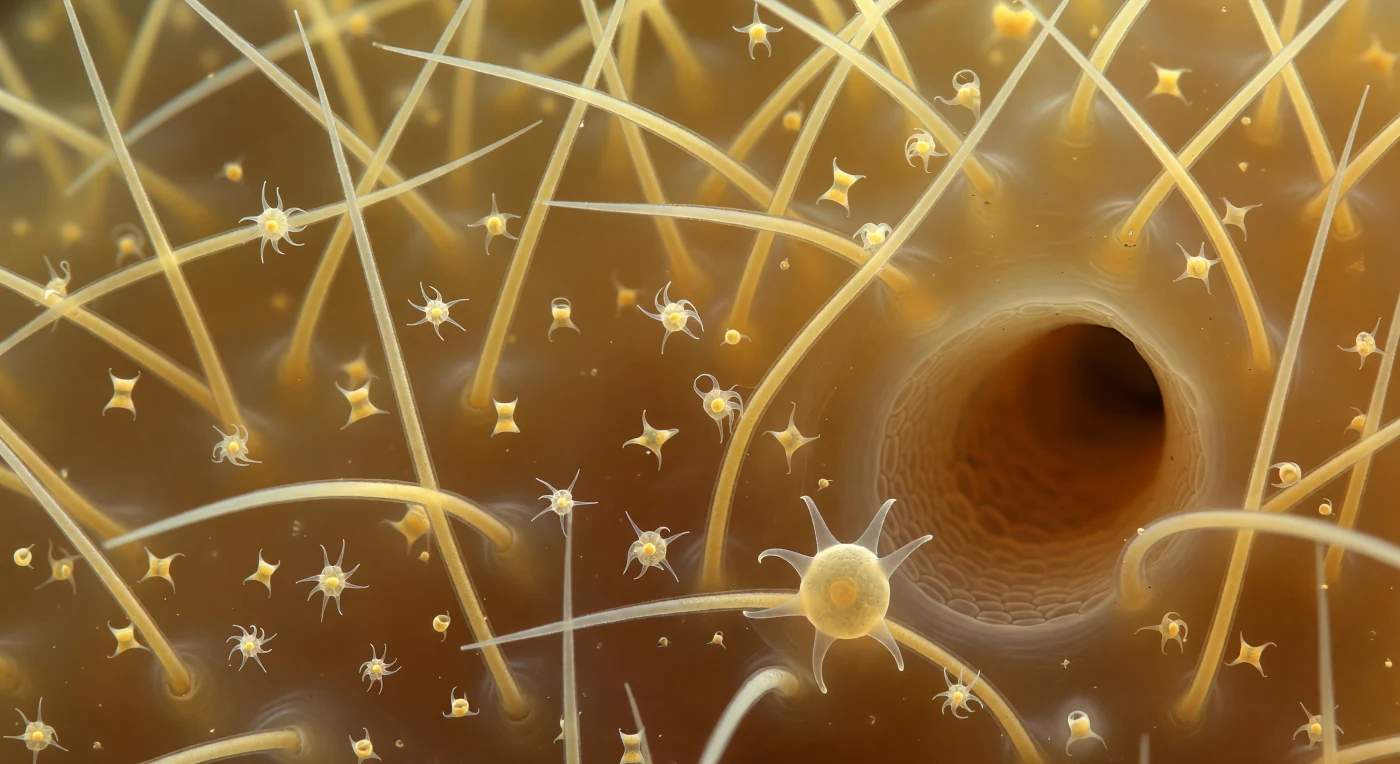
Au sein du mésohyle d'une démosponge vivante, le regard plonge dans une forêt de mégasclères en oxéa — de fines aiguilles de silice biogénique, longues de deux cents microns, dont les pointes effilées captent la lumière ambiante et la restituent en éclats spéculaires blancs qui courent le long de leurs flancs translucides couleur ivoire crème. L'espace entre ces piliers de verre est occupé par le mésohyle lui-même, une matrice gélatineuse teintée d'ambre, milieu vivant traversé d'une turbidité dorée dans lequel dérivent, au gré du mouvement brownien, des microsclères en sigma et des chélae spiralées — sculptures miniatures en verre dont la géométrie interne reste visible par transparence — tandis que des fibres de spongine courent en câbles dorés et mats entre les bases des spicules, formant l'armature tensile de toute cette architecture. Un tunnel canalaire sombre coupe en diagonale le plan intermédiaire, son lumière en ombre cuivrée rappelant que cet organisme est une machine à filtrer l'eau : à chaque instant, le courant invisible y charrie nutriments et particules organiques à travers un réseau de canaux dont la conception hydraulique n'a pas d'équivalent dans le monde minéral. Sur l'un des spicules au premier plan, un archéocyte étend ses pseudopodes en larges voiles translucides contre la surface de verre, son noyau visible comme une sphère dense au cœur d'un cytoplasme ambré — une seule cellule animale assurant, par contact chimique et mobilité lente, l'entretien de tout cet édifice vivant.
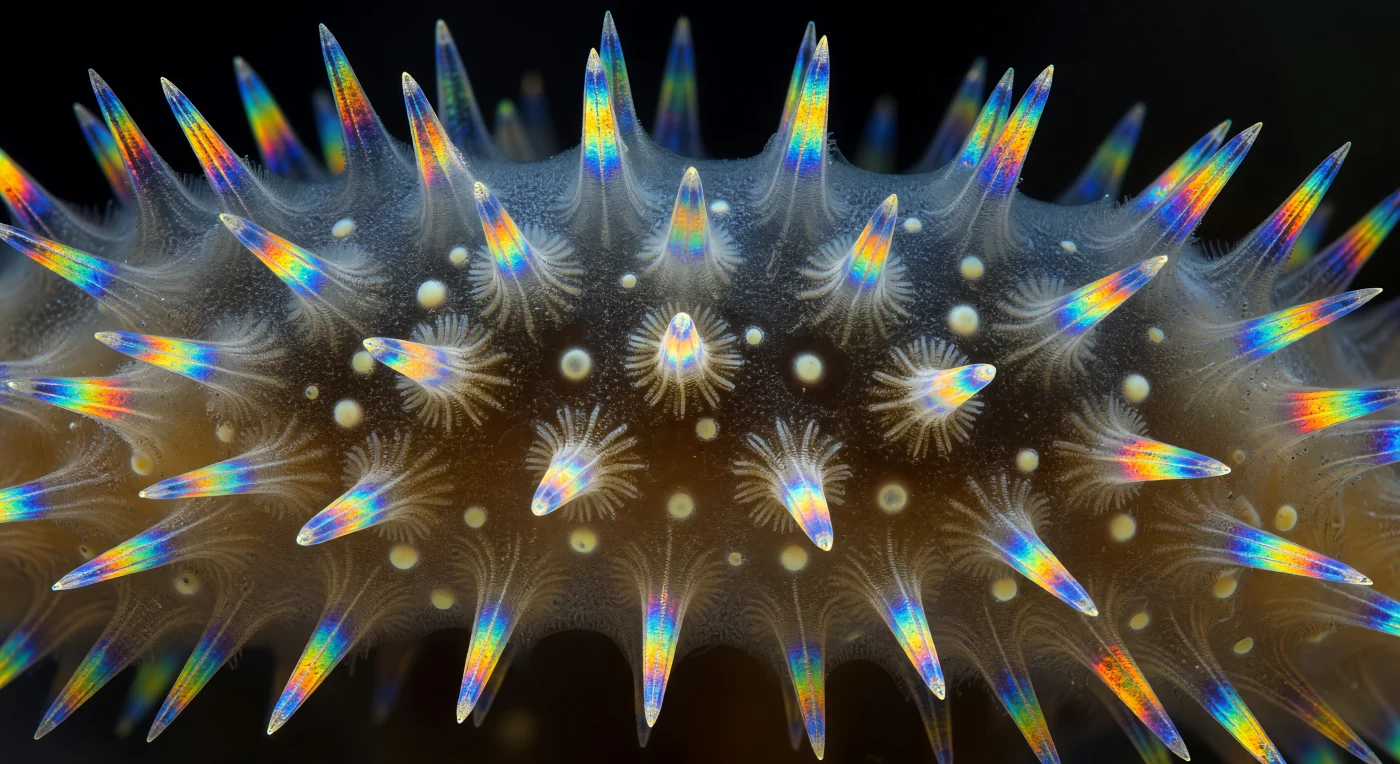
Suspendu à l'intérieur de la paroi sectionnée d'un *Sycon ciliatum*, le regard embrasse une architecture radiale hypnotique : de longs canaux cylindriques se succèdent comme les nefs d'une cathédrale vivante, séparés par des cloisons de mésohyle ambre-gris dense, chargé de matrice extracellulaire fibreuse et d'archéocytes aux noyaux pâles flottant dans la pénombre. Ce qui s'impose avec une force hallucinatoire, ce sont les spicules de calcite — triactines et tetractines — qui jaillissent du tissu en flammes biréfringentes : bleu cobalt électrique, jaune soufre, orange fondu, vert émeraude froid, chacun allumé de l'intérieur par l'effet optique de la lumière polarisée sur le réseau cristallin, tandis que leur troisième rayon pointe droit vers l'observateur comme une aiguille tendue depuis l'abîme. Là où les spicules se croisent, leurs figures d'interférence s'accumulent en auréoles irisées — ambre glissant vers le violet, puis vers le bleu-vert — équivalent optique d'un vitrail illuminé par un soleil d'hiver. Cette géométrie n'est pas un ornement : les spicules constituent le squelette minéral porteur de l'éponge, orientés selon des règles précises de croissance cristalline contrôlée par les sclérocytes, tandis que les canaux radiaux qu'ils encadrent acheminent chaque jour un volume d'eau équivalent à vingt mille fois le volume de l'animal, filtré par les collerettes des choanocytes dont les cils invisibles battent sans relâche dans l'obscurité ambrée.

Dans la nuit absolue à deux cents mètres de profondeur, le faisceau du ROV frappe par en dessous la colonne d'*Aphrocallistes vastus* et quelque chose d'impossible se produit : le squelette de silice s'allume de l'intérieur, conduisant la lumière le long de chaque strut vitreux comme une fibre optique, de sorte que la tour entière — quarante centimètres de diamètre, plus d'un mètre de hauteur — brûle d'une luminescence crème et ambrée, ses chambres hexagonales nichées en ombres concentriques dans les parois translucides comme les fenêtres à résille d'une cathédrale engloutie. Cette architecture n'est pas construite mais sécrétée : chaque strut est une spicule de silice amorphe fusionnée à ses voisines en nœuds d'ancrage précis, l'ensemble formant un treillis tridimensionnel d'une rigueur géométrique que seule la biominéralisation peut produire, solide comme du quartz et pourtant ouvert, poreux, vivant dans ses espaces vides. Le sédiment calcaire autour de la base scintille d'éclats de spicules brisées — un tapis de milliers d'aiguilles de verre microscopiques renvoyant le faisceau en givre froid — pendant qu'une étoile de mer ophiure drape ses bras rayés sur la lattice de silice et qu'un poisson-roche cuivré suspend son immobilité dans le couloir d'obscurité entre deux tours, son œil unique capturant la lumière comme un point vif. À la périphérie du faisceau, là où la lumière meurt dans le bleu-noir, une traînée bioluminescente vert-bleu dérive pendant trois secondes puis disparaît, laissant derrière elle le souvenir d'un organisme invisible dans un silence si profond qu'il a sa propre texture, pendant que la récif de verre s'étend dans l'obscurité dans toutes les directions, colonne après colonne, sur des centaines de mètres de patience géologique.

Vous flottez dans la couche limite benthique, à quelques centimètres au-dessus d'une paroi rocheuse sous-marine, et votre champ de vision tout entier est occupé par une larve de spongiaire calcaire de quelque trois cents microns de diamètre, suspendue en pleine métamorphose sur un substrat d'algues corallines encroûtantes d'un rose-magenta intense. La larve — un disque crème-ambré — subit une inversion morphogénétique : son hémisphère cilié s'invagine vers l'intérieur selon un axe apical, tandis que ses futurs pinacocytes périphériques s'aplatissent déjà en pavés irréguliers qui progressent vers l'extérieur depuis le point d'ancrage central, comme un front de cristallisation au ralenti. Le substrat sur lequel elle repose est lui-même un monde à part entière : les plaques calcifiées des algues corallines forment un plateau magenta fracturé hérissé de frustules de diatomées en silice — monuments géométriques translucides, hexagonaux et radiairement symétriques — tandis qu'un biofilm bactérien s'étend entre eux en une matrice d'exopolysaccharides ambrée et iridescente, révélant sa texture tridimensionnelle sous la lumière bleue-verte qui déferle depuis la colonne d'eau au-dessus. Ce moment de fixation larvaire marque une transition évolutive fondamentale : l'animal choisit son habitat définitif en réponse à des signaux chimiques du biofilm microbien, et engage un programme développemental qui, en quelques heures, transformera une larve nageuse libre en un organisme sessile filtrant dont l'architecture de choanocytes rappelle, à l'échelle cellulaire, la parenté profonde entre les spongiaires et l'ancêtre commun de tous les animaux.
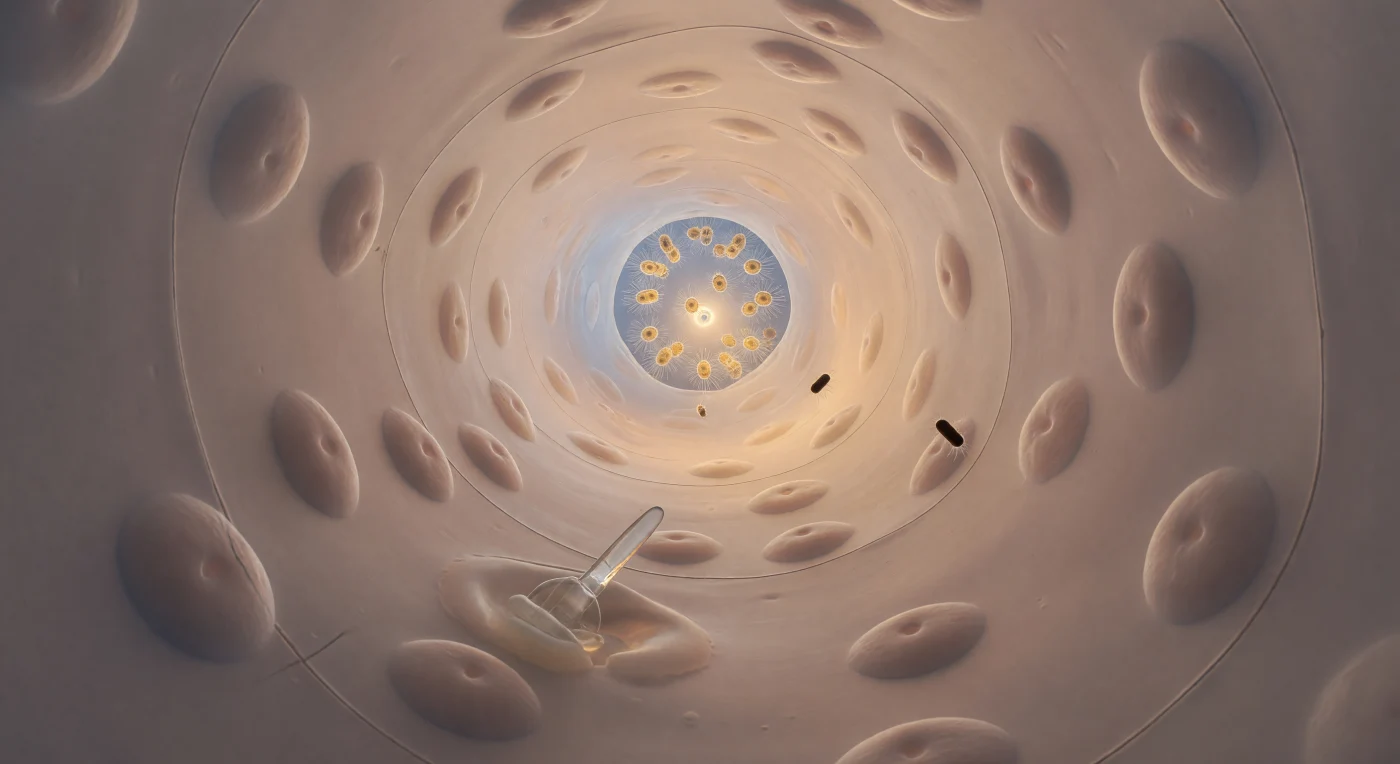
Vous êtes suspendu à l'entrée d'un tunnel vivant de soixante-dix micromètres de diamètre, regardant s'incurver devant vous un couloir cylindrique dont les parois sont tapissées d'endopinacocytes aplatis comme de la soie mouillée, leurs noyaux formant de douces protubérances dans la chair translucide couleur ivoire et pêche, et dont les sutures intercellulaires se devinent à peine comme de fines coutures sombres. Au loin, à travers l'épaisseur dorée de l'eau — une suspension d'organiques dissous qui donne au fluide la chaleur optique d'une lumière de bougie filtrée dans du thé faible — le prosopyle terminal, cinq micromètres à peine, brille comme un œil de cuivre incandescent, laissant irradier l'ambre vivant de la chambre choanocytaire où des dizaines de flagelles battent à quarante cycles par seconde. L'eau ici n'est pas un fluide au sens familier : soumise au régime de Stokes, elle progresse avec une douceur visqueuse et sans turbulence, portant paresseusement deux bactéries en forme de cigare qui dérivent le long de la paroi comme des fragments d'acajou poli, tandis qu'un archéocyte amoeboïde se déforme lentement autour de la base d'un spicule de calcite enchâssé dans la paroi, sa cytoplasme se pliant comme de la cire tiède entre deux jonctions cellulaires. Derrière vous, la lumière froide et blanche de l'océan inonde l'ostium d'entrée, silhouettant la bouche circulaire du canal et rappelant que ce réseau de passages — perfectionné depuis six cents millions d'années — filtre l'océan un micro-organisme à la fois, dans une patience architecturale que nul ingénieur n'a jamais égalée.
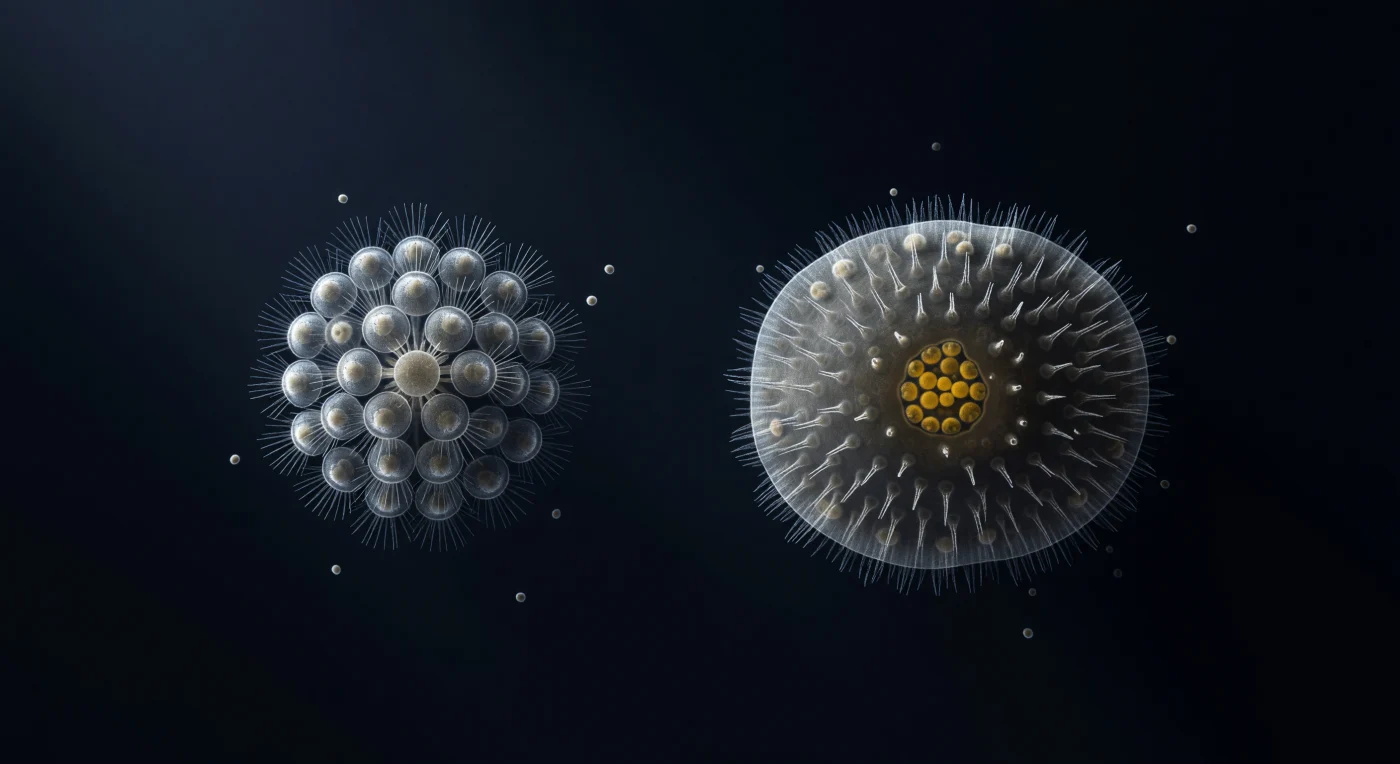
Dans ce champ unique éclairé en contraste interférentiel différentiel, deux formes de vie se font face à travers cent microns d'eau marine silencieuse, séparées par ce qui est en réalité l'un des intervalles évolutifs les plus vertigineux de l'histoire du vivant. À gauche, la colonie rosette de *Salpingoeca rosetta* — trente-deux cellules assemblées en sphère de cinquante microns — exhibe chacune de ses unités collier-flagelle tournées vers l'extérieur, architecture d'une précision quasi cristalline dont les microvillosités captent la lumière rasante en fines aiguilles d'argent : c'est la même machinerie filtrante que l'on retrouvera, sept cents millions d'années plus tard, dans les choanocytes des éponges, preuve moléculaire d'une filiation directe entre ces unicellulaires coloniaux et l'ensemble du règne animal. À droite, la larve parenchymella d'une éponge calcinéenne — cent cinquante microns de cellules ciliées encerclant une masse intérieure dense — porte déjà, dissimulés dans son hémisphère antérieur, quelques cellules dont la morphologie annonce le col caractéristique des choanocytes, comme si l'évolution répétait à voix basse le plan d'un corps qu'elle est encore en train d'inventer. Seules les cellules postérieures gorgées de vitellus brillent d'un ambre chaud au cœur de cette scène autrement monochrome, réserves lipidiques destinées à alimenter la métamorphose imminente d'une larve qui n'a pas encore choisi son substrat. L'espace d'eau apparemment vide entre les deux organismes n'est pas un vide : c'est la distance la plus chargée de sens qui soit, le lieu invisible où la multicellularité animale a émergé une seule fois, irréversiblement, depuis un ancêtre que ces deux formes nous permettent encore, aujourd'hui, d'entrevoir.

À l'échelle d'une bactérie, vous flottez suspendu à l'intérieur même de la paroi bisectée d'une gemmule de Spongilla, contemplant une coupe transversale qui s'étend devant vous comme la nef d'une cathédrale fendue par un cataclysme géologique — une structure de survie façonnée par l'évolution pour traverser les hivers les plus rigoureux. La paroi qui occupe le tiers gauche de votre champ de vision est une forteresse en trois couches : une membrane externe ambrée et légèrement irisée, puis une palissade d'amphidisques de silice cristalline dressés dans un ciment de spongine crème, leurs extrémités en rondelles s'emboîtant comme les pieux d'une clôture microscopique et projetant de fugaces éclats prismatiques — blanc glacé, bleu fantôme, rose pâle — partout où la lumière se réfracte dans leurs tiges vitreuses. Derrière cette armure s'ouvre la cavité intérieure, monde saturé d'ambre et d'or où les archéocytes serrés les uns contre les autres luisent comme des lanternes, leurs cytoplasmes gorgés de vésicules lipidiques jaune safran et orange mandarine — réserves énergétiques soigneusement accumulées pour la future réactivation printanière. Sur la droite, le tube micropylaire perce l'armure en section transversale, son chenal obturé par une colonne de cellules pâles pressées les unes contre les autres comme des bouchons, unique point de communication potentielle entre cet univers intérieur incandescent et le monde extérieur froid, indistinct, d'un gris olive lugubre — contraste visuel et thermodynamique qui confère à cette section la densité dramatique d'une géode brisée en plein cœur de l'hiver.

Vous vous trouvez à quelques centimètres au-dessus d'un bois immergé et gorgé d'eau, face à une croûte vivante de *Spongilla lacustris* qui s'étend comme une toundra alien d'un vert électrique, illuminée par les colonnes de lumière qui traversent la surface mouvante du ruisseau — là où ces rayons frappent directement, le vert s'embrase en une lueur presque phosphorescente, alimentée par les algues symbiotiques logées dans les tissus vivants de l'éponge, organismes qui pompent et filtrent l'eau selon un plan architectural vieux de six cents millions d'années. La texture de la croûte est celle d'un velours hérissé d'aiguilles de verre : le squelette de spicules en silice dépasse à chaque millimètre de surface, chaque pointe captant la lumière à son extrémité comme un cristal de givre, créant un halo diffus de micro-éclats argentés sur l'ensemble de la croûte. Enchâssées dans ce tissu vert, de sombres sphères acajou — les gemmules, chacune d'environ un demi-millimètre de diamètre — affleurent comme des pavés enfouis, leurs surfaces ornées d'une architecture radiale de spicules disposés en fleur blindée, capsules de survie hermétiquement closes contre l'hiver et la sécheresse, patientes et inertes parmi les cellules vivantes qui pompent sans relâche autour d'elles. De minuscules ostracodes glissent sur la surface, leurs carapaces bivalves captant la lumière comme des perles nacrées roulant sur du velours, tandis que des planaires translucides décrivent de lents arcs, leurs corps si fins que le vert du tissu spongieux transparaît à travers leur face ventrale, unissant prédateur et proie dans la même palette de lumière aquatique.

Vous flottez à un souffle au-dessus de la peau d'une éponge démosponge tropicale vivante, et ce qui s'étend sous vous ressemble à une plaine de lave refroidie photographiée depuis quelques centimètres : un pavage irrégulier de cellules polygonales — les exopinacocytes — saturées d'un orange brûlé intense, chacune bordée d'une crête microscopique qui capte la lumière diffuse du récif et dessine des ombres fines dans les sillons intercellulaires, donnant à toute la surface l'apparence d'une céramique lacquée et chaude. Parsemés sur ce terrain à intervalles irréguliers, les ostia s'ouvrent comme des caldeiras miniatures — certains béants, leur porocyte rétracté laissant entrevoir un noir absolu qui plonge dans le réseau de canaux inhalants, d'autres resserrés jusqu'à n'être plus qu'une fente pâle, témoignant de la capacité de l'éponge à réguler activement son débit de filtration, jusqu'à vingt mille fois son volume corporel par jour. Entre ces puits d'aspiration, un biofilm tridimensionnel — bactéries en bâtonnet, amas coccoïdes, filaments de cyanobactéries tissés dans une pellicule de mucopolysaccharides — recouvre les tuiles d'une fourrure givrée et irisée, négociant à l'échelle du micron un territoire chimique partagé avec leur hôte. Un petit ver polychète émerge de l'un des ostia les plus larges, ses palpes antérieurs balayant lentement la couche limite en frémissant d'or, tandis qu'un copépode, carapace transparente scintillant comme une lentille de verre bleuté, effleure la surface un instant avant d'être dévié par le gradient de pression imperceptible qu'exhale un osculum voisin — révélant, dans ce détail fugace, la physique des fluides à bas nombre de Reynolds qui gouverne toute vie à cette échelle.
















