Affidabilità scientifica: Alto
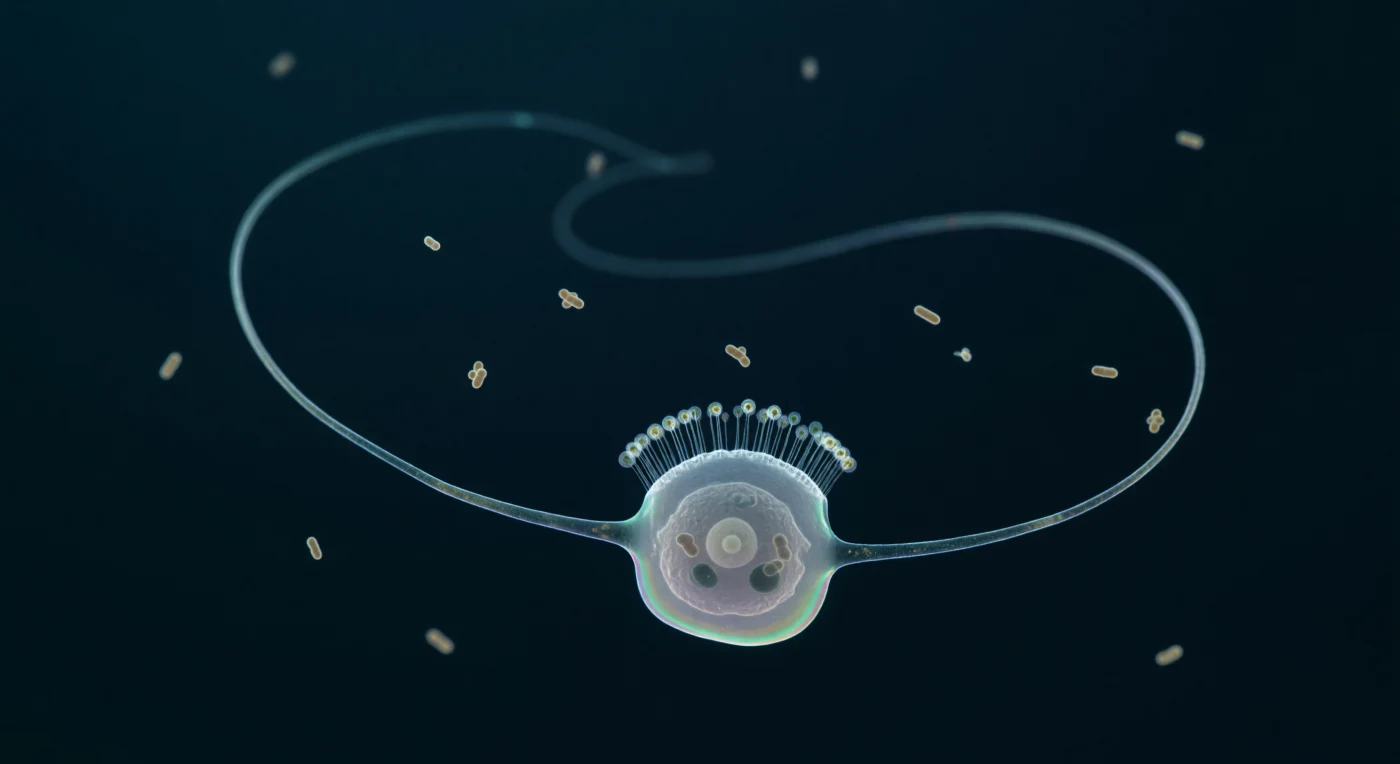
Ci si trova sospesi in un vuoto pelagico di un blu-nero assoluto, immersi in un mezzo che alla scala di pochi micron si comporta meno come acqua che come una terza sostanza — viscoso, denso di rumore termico invisibile, attraversato da una luce blu-verde diffusa e fredda che filtra da un altrove lontanissimo. La presenza dominante è il flagello di un singolo coanoflagellate: un frustino sinuoso lungo una ventina di micron che descrive un'ampia curva elicoidale a esse lungo quasi tutto il campo visivo, il suo fusto sottilissimo rivestito di un glicocalice che diffrange la luce in un'iridescenza oleosa, mentre dietro di esso persiste uno spettro traslucido — la traccia cinematica di un'ondata sinusoidale passata una frazione di secondo fa, argento pallido sul fondo cobalto. Il corpo cellulare, una goccia quasi incolore di sette micron, è visibile solo come differenza di indice di rifrazione: la sua membrana plasma rifrange la luce teal in aloni iridescenti di lavanda, oro e verde fantasma, e al suo interno un nucleo vesicolare occupa come una luna opaca un terzo del citoplasma, affiancato da due vacuoli alimentari scuri in cui si intuisce ancora la sagoma compressa di un batterio in digestione. Nell'intorno, una dozzina di batteri a forma di bastoncino deriva nel mezzo a varie profondità, tremolanti per l'agitazione browniana termica, alcuni nitidi nella luce ambrata rifratta, altri dissolti in un bokeh tenue fino a scomparire nel gradiente di nero assoluto che interrompe la profondità di campo a poche lunghezze cellulari di distanza in ogni direzione.

Sospesi nell'acqua scura come un batterio gigante, ti trovi di fronte a una struttura che riempie l'intero campo visivo: una colonia rosetta di *Salpingoeca rosetta*, trentadue cellule disposte in geometria radiale perfetta, ciascuna che punta verso l'esterno con il proprio flagello esteso in una corona tremolante, conferendo all'insieme la sagoma irta di un riccio di mare congelato nel mezzo di un respiro. Ogni cellula è un ovoide traslucido di pochi micrometri, resa nella scala di grigi fredda della microscopia DIC con luci compresse sulla membrana plasmatica e l'ombra densa del nucleo visibile nell'interno, mentre ai poli basali sottilissimi ponti citoplasmatici convergono su un nucleo di matrice extracellulare ambrata — l'unico calore cromatico in una scena altrimenti quasi monocromatica. Al quadrante delle due, una cellula è a metà divisione, il corpo leggermente strozzato in forma di arachide con le due densità nucleari già spostate nell'allungarsi del citoplasma, testimonianza silenziosa di come questa colonia costruisca se stessa per gemmazione coordinata. L'acqua intorno non è trasparente nel senso umano: è un mezzo opalescente di blu-nero profondo, percorso da un tremito continuo di moto browniano e punteggiato da fiocchi di neve marina — aggregati di detriti organici e polisaccaridi — che derivano nel campo medio e lontano, stabilendo la profondità spaziale e ricordando che questa colonia fluttua libera in un oceano di particolato vivo. Questa geometria — cellule flagellate in corona radiale legate da ponti citoplasmatici — non è solo una forma coloniale: è la stessa architettura che, centinaia di milioni di anni fa, avrebbe potuto dare origine alle prime camere coanocitarie delle spugne, il primo passo nella storia della multicellularità animale.
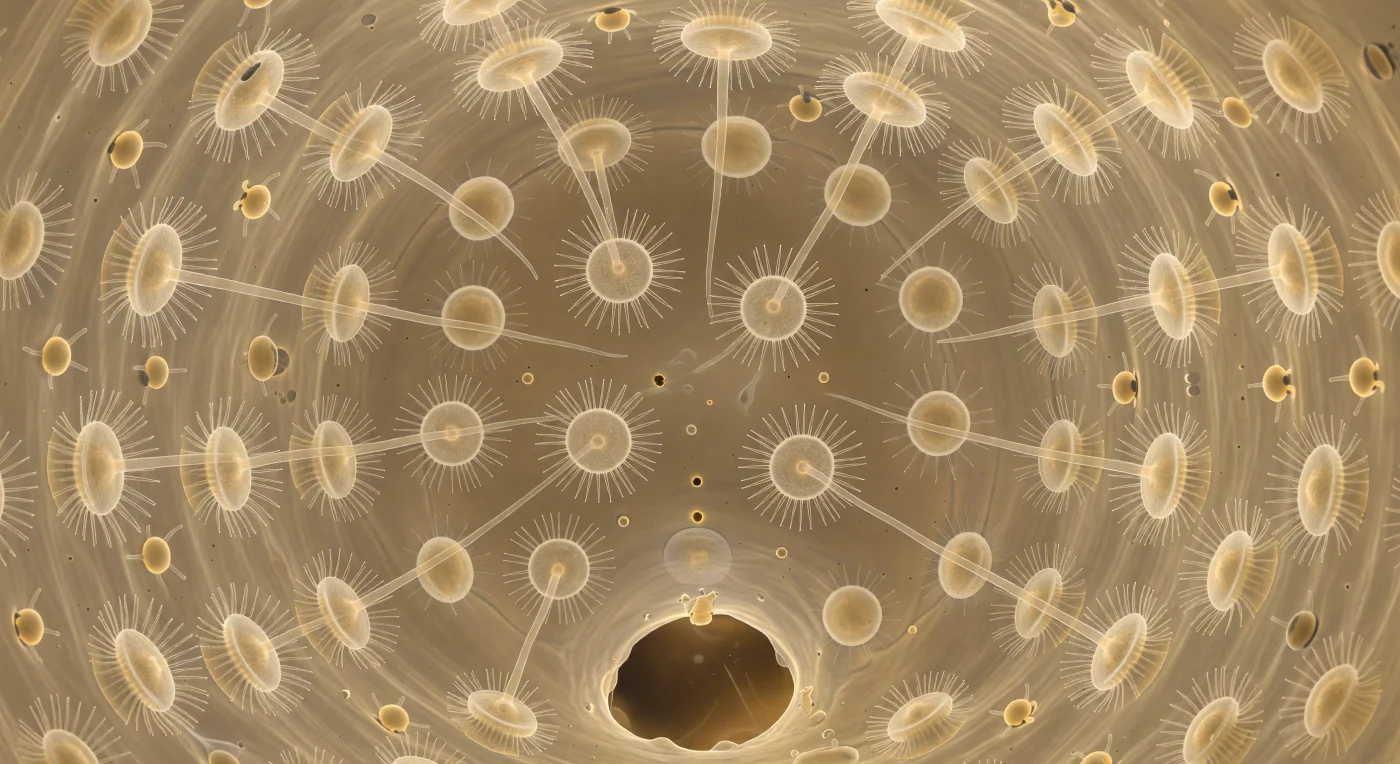
Ci si trova sospesi al centro esatto di una camera sferica di appena quaranta micrometri di diametro, avvolti da una cupola vivente le cui pareti sono interamente rivestite da choanociti — cellule a forma di campana, ciascuna coronata da un collare di microvilli cristallini e da un singolo flagello che batte verso l'interno in fase sfasata rispetto ai vicini, generando un'onda collettiva e continua che trasforma l'intera superficie della camera in qualcosa di simile a un campo di anemoni in una corrente gentile. La luce che pervade questo spazio non proviene da alcuna sorgente diretta: è luce oceanica filtrata attraverso diversi micrometri di membrana cellulare e matrice extracellulare, che arriva come un bagliore ambrato, morbido e privo di ombre, mentre attraverso i due pori prosopilariali — piccoli fori scuri posizionati ai lati della parete — entrano sottili filamenti di corrente carichi di batteri e materia organica discioluta. Il moto flagellare coordinato dei venticinque choanociti spinge con efficienza quasi perfetta il fluido verso il grande poro apopilare aperto davanti a noi, una soglia citoplasmatica che dà accesso ai canali efferenti della spugna, rendendo questo microscopico vano non un semplice contenitore ma il cuore pulsante di una delle più antiche e sofisticate architetture di filtrazione biologica mai evolute. Oltre lo strato cellulare, il mesoilo si stende come un reticolo ambrato di fibre collagene-simili attraversato da archaeociti ameboidi che scivolano con la lentezza del vetro fuso, testimoni silenziosi di un sistema che pompa ogni giorno un volume d'acqua pari a ventimila volte il corpo dell'intera spugna.
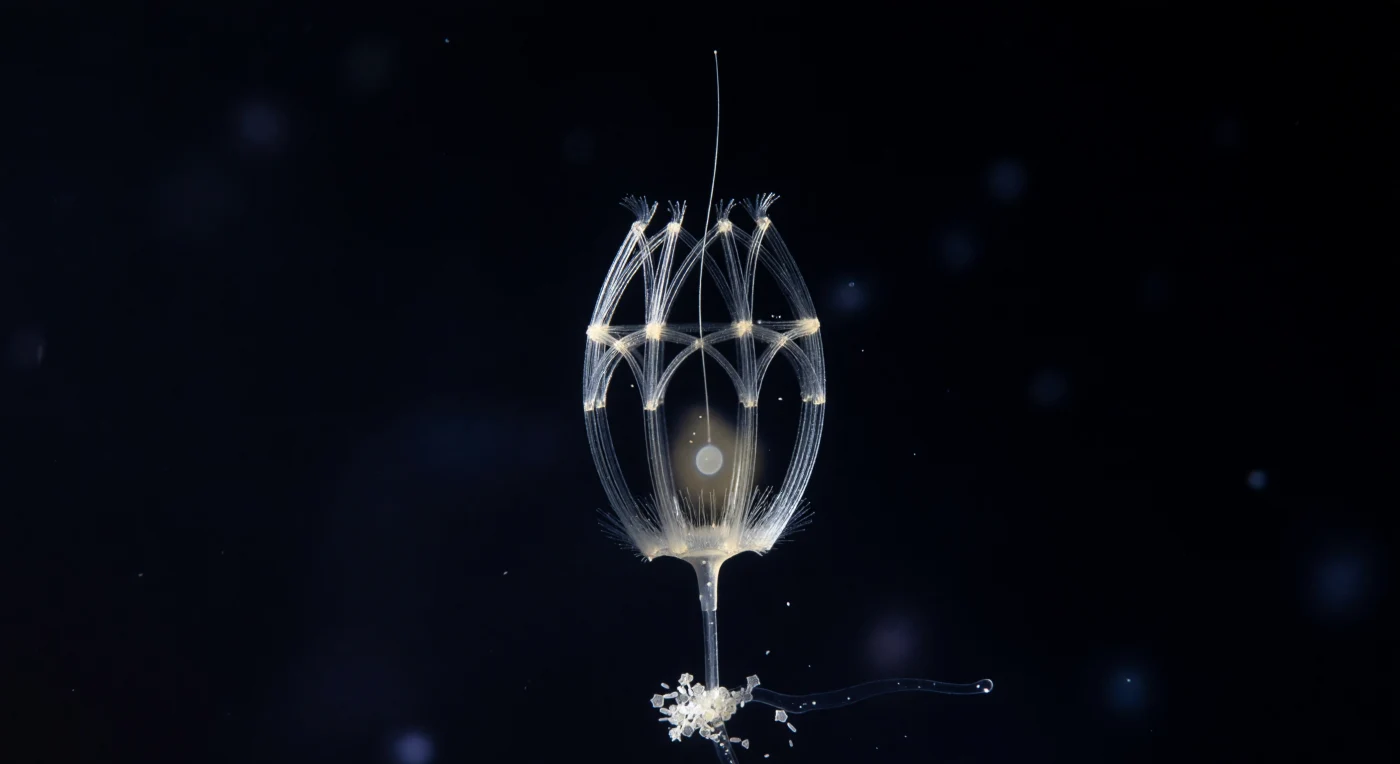
Nel buio assoluto della colonna mesopelagica, sospesi in un'oscurità che sembra avere peso e consistenza propri, si erge una struttura di geometria quasi impossibile: una gabbia di bastoncini silicei intrecciati in due sistemi distinti — costole longitudinali che si arcuano dalla base all'apice come nervature di una volta gotica, e cerchi trasversali che le stringono a intervalli regolari — illuminata da un'unica sorgente laterale che fa divampare ogni singola verga in un filamento bianco-argento contro il nero assoluto, trasformando la lorica di *Diaphanoeca grandis* in una lanterna di vetro ghiacciato sospesa nel vuoto. All'interno della gabbia, appena percepibile come un alito di ambra diluita, vive la cellula: il citoplasma si intuisce più che vedersi, il flagello sale dall'interno verso il polo anteriore aperto e poi scompare nel buio come un filo di seta che cerca qualcosa di invisibile, mentre le microvilli del collare formano una corona luminescente attorno alla sua base che si dissolve prima di risolversi del tutto. Questa struttura, assemblata senza enzimi litici né strumenti — per pura autoassemblaggio biochimico — è composta da strisce costali di silice organica che questo choanoflagellate secerne e dispone con una precisione architettonica che sfida la scala alla quale opera, poche decine di micron in un oceano di chilometri. In basso, il peduncolo ancorano la lorica a un fiocco di neve marina — frustule di diatomee i cui pannelli esagonali riflettono la luce laterale come specchi in miniatura, bastoncelli batterici dispersi tra loro come segni di punteggiatura addormentati — ricordando che questo organismo unicellulare, la cui morfologia è quasi identica ai coanociti che rivestono le camere interne delle spugne, si trova al confine evolutivo tra la solitudine della cellula e l'invenzione dell'animale.

Sospesi appena fuori dalla parete cilindrica di uno scheletro di *Euplectella aspergillum*, ci troviamo di fronte a una struttura che sembra uscita dall'immaginazione di un architetto gotico: una torre reticolare di spicole silicea a sei raggi, fuse in ogni intersezione in un unico sincizio rigido, che si erge nel buio assoluto degli abissi come la navata di una cattedrale costruita in vetro filato. Ogni spicola conduce la luce blu-verde dell'acqua circostante lungo tutta la propria lunghezza, comportandosi come una vera fibra ottica biologica, così che l'intera griglia appare autoilluminata, sospesa nel nulla, ogni apertura quadrata incorniciando una finestra traslucida sull'atrio centrale cavo. Guardando attraverso le pareti dello scheletro, l'interno si rivela una lanterna di straordinaria delicatezza: griglie d'ombra si moltiplicano verso l'interno mentre ogni strato rifrange la geometria luminescente, e sulle sezioni fratturate delle spicole più vicine si distinguono anelli di laminazione concentrici nella silice, crescita registrata come negli strati di un albero di vetro. In fondo all'atrio, due gamberetti commensali appaiono come sagome ambrate e rosate controluce, le loro forme segmentate e le antenne piumate rese semitrasparenti dal bagliore interno: creature viventi sigillate per sempre nella loro cattedrale di luce e silicio, compagne di una simbiosi antica quanto la comparsa dei primi animali multicellulari sul pianeta.
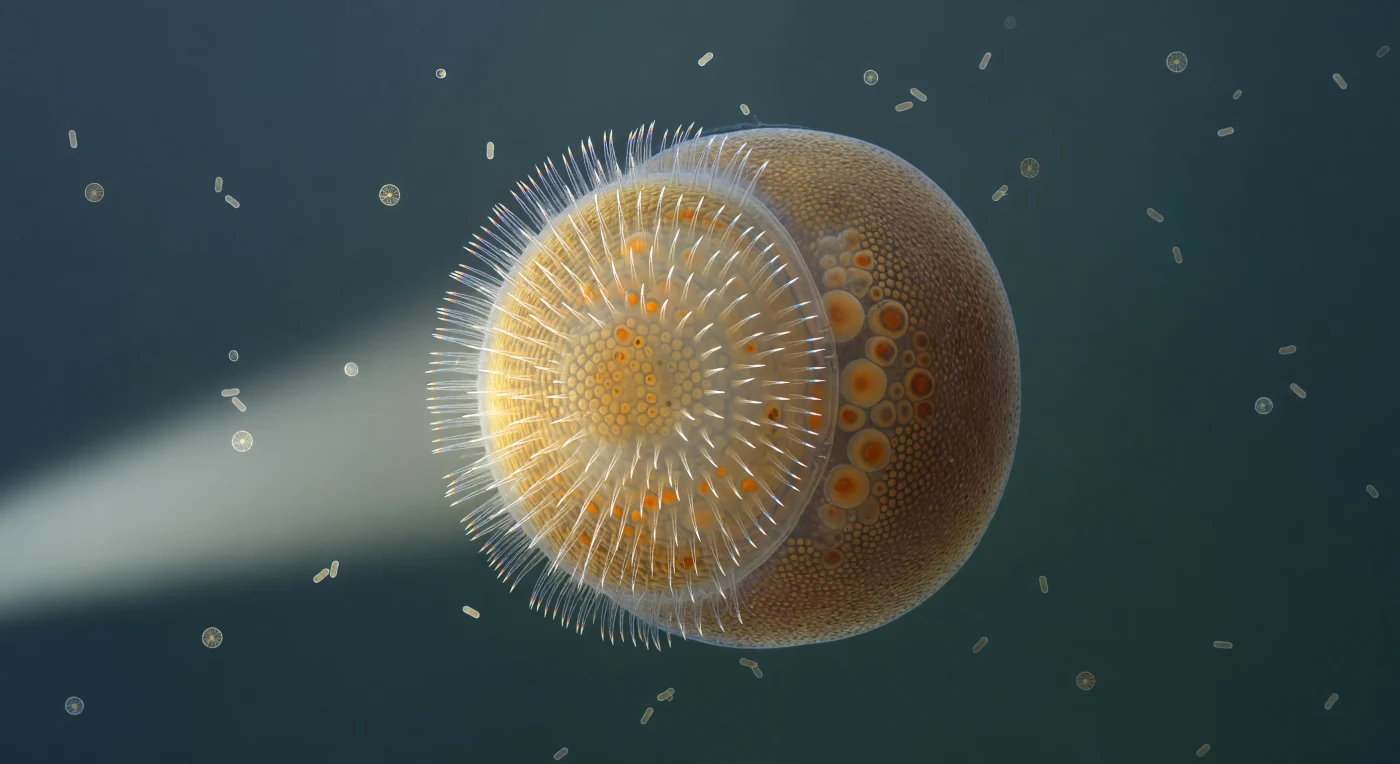
Nell'acqua sopra la scogliera, sospesa come un granello di polvere luminosa, fluttua una forma ovale che sembra contenere in sé un intero universo biologico: la larva amphiblastula di una spugna calcarea, circa quattrocentomicron di diametro, divisa nettamente in due emisferi di natura opposta. L'emisfero anteriore, dorato e vibrante, è rivestito di ciglia che battono in onde metacronali sincronizzate, diffrattando la luce laterale in un'aureola prismatica di violetto, ciano e oro pallido che si rinnova continuamente come un arcobaleno instabile; queste ciglia, trasparenti come aghi di vetro, sono la macchina propulsiva della larva, orchestrate con una precisione che preannuncia la complessità del sistema nervoso animale ancora di là da venire. L'emisfero posteriore è un paese più silenzioso e scuro, denso di archeociti carichi di riserve lipidiche ambrate visibili attraverso la parete traslucida come lanterne dietro vetro smerigliato, cellule destinate a costruire l'intera architettura filtrante della futura spugna adulta. Attorno alla larva, in un'acqua blu-verde che sembra un gel appena luminoso, diatomee dalle frustrule incise come medaglioni e batteri a bastoncino percorrono traiettorie browniane lente e indifferenti, testimoni muti di un momento evolutivo straordinario: il confine biologico tra la singola cellula e la prima vera animalità multicellulare.

Sospeso nell'acqua tiepida e salata di una scogliera tropicale, ti trovi esattamente sul bordo dell'osculo di una grande spugna a barile, affacciato su un camino circolare di circa quattro centimetri che si apre come la bocca di un cratere vulcanico in miniatura: le pareti interne scendono ripide in una tonalità di terracotta bruciata, dense di corrugazioni finissime e camere coanocitarie che filtrano incessantemente l'acqua circostante. Dal profondo della struttura sale un getto continuo di acqua esalata, reso visibile da un tremolìo da miraggio termico e da striature di particelle organiche in sospensione — detriti ambrati, nuvole batteriche evanescenti, frammenti silicei che catturano e diffondono la luce caustica turchese proveniente dalla superficie — testimoni silenziosi di un processo di pompaggio che, in una singola giornata, può far transitare attraverso il corpo della spugna un volume d'acqua pari a ventimila volte la propria massa. La superficie esterna si estende in ogni direzione come un paesaggio di pietra viva: pozzi scuri di ostia perforano la carne arancione in griglie irregolari, alghe coralline color lavanda si appiattiscono in strati calcarei, e merletti di briozoi bianchi si ramificano in filigrane frattali sui bordi stabili del tessuto. Sullo sfondo, coralli staghorn sfocati brillano nella luce diffusa e pesci dai colori vivaci attraversano l'acqua carica di significato biologico, ricordando che questa architettura filtrante — erede diretta di un piano corporeo rimasto quasi invariato per oltre seicento milioni di anni — non è un fossile, ma un organismo che respira e pulsa a ogni secondo.
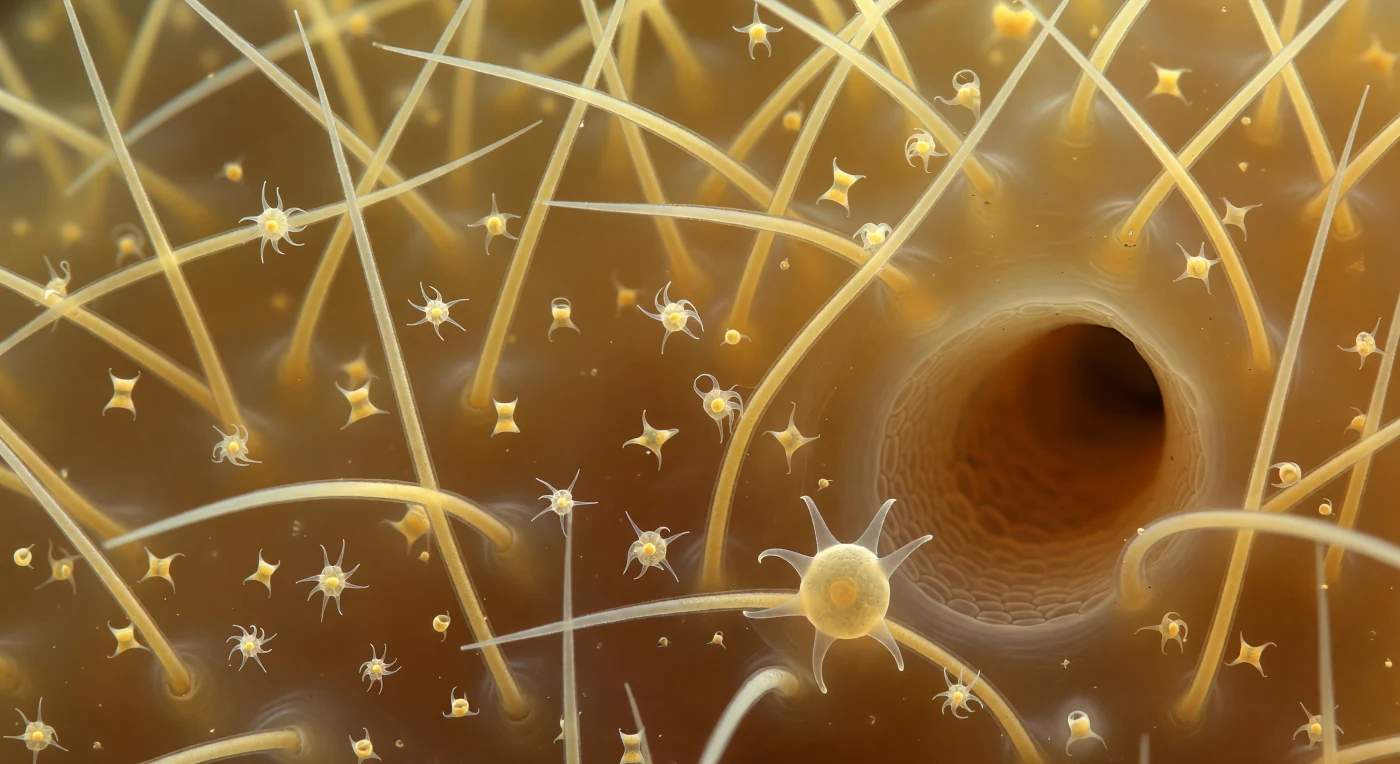
Nel cuore di una spugna demospongia, il mondo si rivela come una foresta di aghi di vetro: i megascleri ossea, lunghi quanto un acaro, si innalzano in ogni direzione con le loro punte affilate che spezzano la luce diffusa in lampi bianchi lungo le superfici curvate, immersi in un gel mesohylare color ambra che li avvolge come resina fossile ancora liquida. Questo materiale gelatinoso — una matrice extracellulare ricca di collagene e proteoglicani — non è vuoto inerte, ma un mezzo vivente in cui galleggiano microscleri a forma di sigma e chele spiralate, sculture in miniatura di silice amorfa che ruotano nel moto browniano della soluzione colloidale. Le fibre di spongina collegano le basi dei megascleri come cavi organici color miele, formando il telaio tensile dell'intera architettura filtrante, mentre un tunnel scuro del sistema canalare taglia la scena in diagonale — una delle vie attraverso cui la spugna pompa volumi d'acqua pari a ventimila volte il proprio corpo ogni giorno. Su uno degli aghi in primo piano, un archaeocita estende i suoi pseudopodi come lamine di sapone iridescenti, guidando con mani chimiche lente e deliberate la deposizione di silice che edifica, spicola dopo spicola, questo cosmo trasparente.
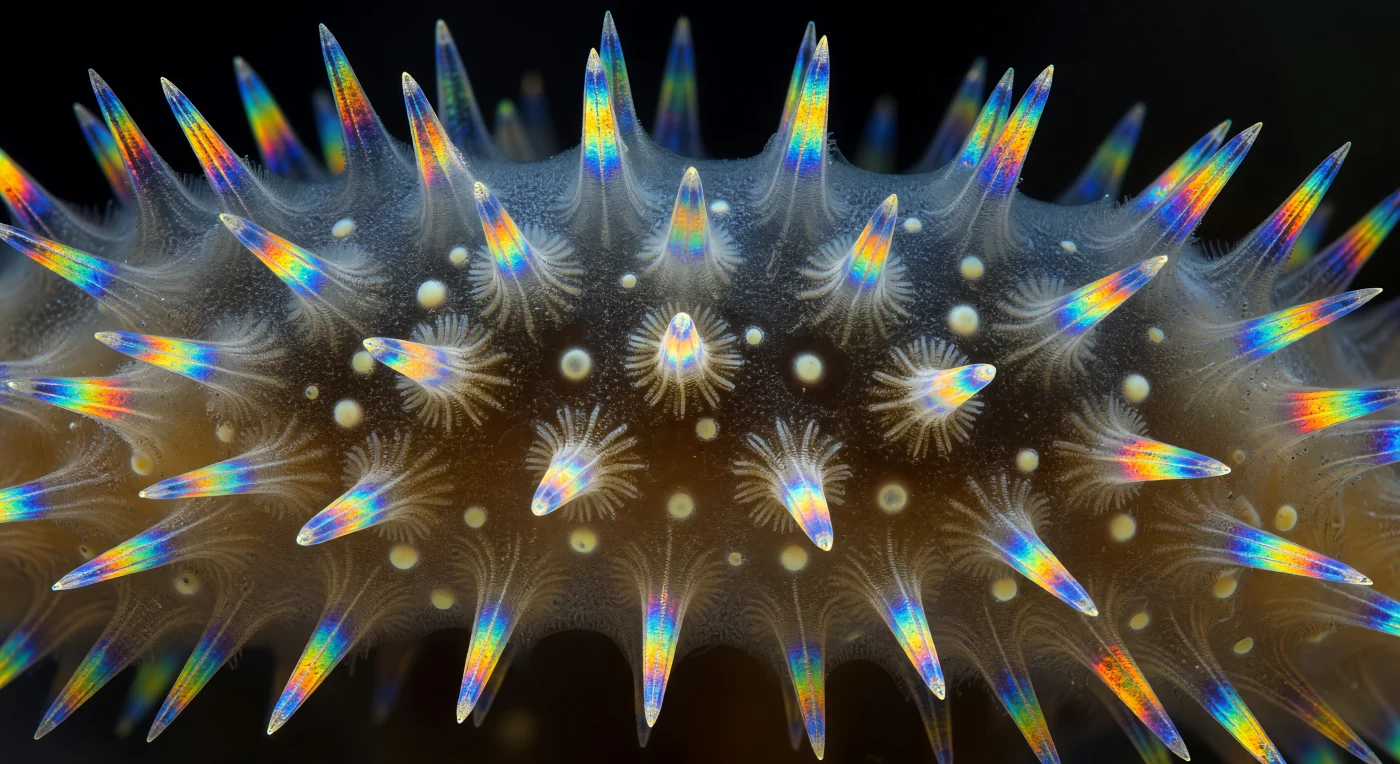
Sospesi all'interno della parete sezionata di un *Sycon ciliatum*, ci si trova immersi in un'architettura impossibile: una cattedrale minerale e vivente in cui i canali radiali si aprono come navate gotiche rivestite di coanociti, separati da costolature di mesoilo ambrato percorse da una fitta trama di matrice extracellulare. Le spicole di calcite — triactini e tetractini — esplodono nel campo visivo con un fulgore allucinatorio sotto luce polarizzata: blu cobalto elettrico, giallo zolfo, arancio fuso, verde smeraldo freddo, ciascuna cristallizzata in un'identità cromatica propria contro il nero assoluto del fondo, i loro reticoli cristallini che trasformano la luce in interferenze spettrali, aureole iridescenti che si sovrappongono là dove le spicole si incrociano. Due raggi di ogni triactina giacciono nel piano della parete, mentre il terzo si proietta perpendicolarmente verso l'osservatore come un ago puntato dall'interno, la sua punta colta in un punto speculare di luce bianco-oro. La scena si articola in piani di profondità sovrapposti — spicole a fuoco tagliente in primo piano, pareti canalari che si dissolvono in un'ambra traslucida a distanza, e poi il nero totale dove la luce polarizzata non penetra più — restituendo la vertigine di uno spazio interiore vastissimo racchiuso in un organismo delle dimensioni di un'unghia.

Nell'oscurità assoluta del fondale del Pacifico nordorientale, le torri di *Aphrocallistes vastus* si ergono come guglie di una cattedrale sommersa, i loro scheletri di spicole silicee fuse in un reticolo esagonale tridimensionale che il fascio del ROV trasforma dall'interno in una luminescenza ambrata e lattea, conducendo la luce lungo ogni travatura vitrea come un cavo in fibra ottica. Questi esachinellidi — spugne di vetro — costruiscono il proprio impalcato pompando acqua attraverso camere tappezzate di coanociti, cellule flagellate la cui architettura a collare di microvilli è omologa alle cellule fondatrici della multicellularità animale stessa, filtrando tonnellate d'acqua nel corso di decenni di crescita millimetrica per anno. Il sedimento calcareo ai piedi delle torri brilla come un campo di aghi di quarzo — detriti di spicole accumulate da colonie cresciute e crollate in secoli di silenzio glaciale — mentre stelle serpentine intrecciano le loro braccia attraverso le maglie del lattice come se la geometria della spugna fosse stata progettata anche per loro. Al margine del fascio luminoso, una scia bioluminescente azzurra-verde attraversa il buio per tre secondi e scompare, ricordando che questa quiete apparente è abitata da organismi che comunicano con la luce in un mondo dove il sole non è mai arrivato. L'intera scena — la foresta di colonne translucide che si estende nell'oscurità per centinaia di metri, la neve marina che scende verticale e imperturbabile — trasmette la pazienza geologica di una struttura vivente costruita un fotogramma alla volta nell'acqua più fredda e più buia dell'oceano.

Sospesi a pochi centimetri sopra la roccia, l'intero campo visivo è occupato da un paesaggio che a questa scala non ha nulla di subacqueo: una vasta pianura magenta e cremisi di alga corallinacea incrostante, la cui superficie calcificata si frange in placche poligonali irregolari con bordi sollevati come creste tettoniche, punteggiata da monumenti vitrei di frustuli di diatomee — architetture esagonali di silice che catturano la luce blu-verde diffusa proveniente dall'alto come finestre di una cattedrale sommersa. Fra queste strutture, un biofilm batterico si stende come una prateria di ambra traslucida, i suoi filamenti di esopolisaccaridi che si avvolgono e si raccolgono nelle depressioni, l'intera superficie che scintilla di un'iridescenza colloidale viva e tridimensionale. Al centro di questa scena, una larva di spugna calcarea di circa trecento micron si trova a metà metamorfosi: il suo emisfero ciliato si sta visibilmente invaginando verso l'interno in un movimento di inversione morfogenetica, mentre il margine del disco si appiattisce in cellule-pavimento — i futuri pinacociti — che irradiano verso l'esterno dal punto di attacco in onde concentriche silenziose. La luce radente rivela ogni dettaglio topografico del substrato, e il bordo periferico della larva, sottile come un'unica cellula, risplende di un ambra traslucida come una membrana di vetro colorato, fragile annuncio di tutto ciò che la vita multicellulare diventerà.
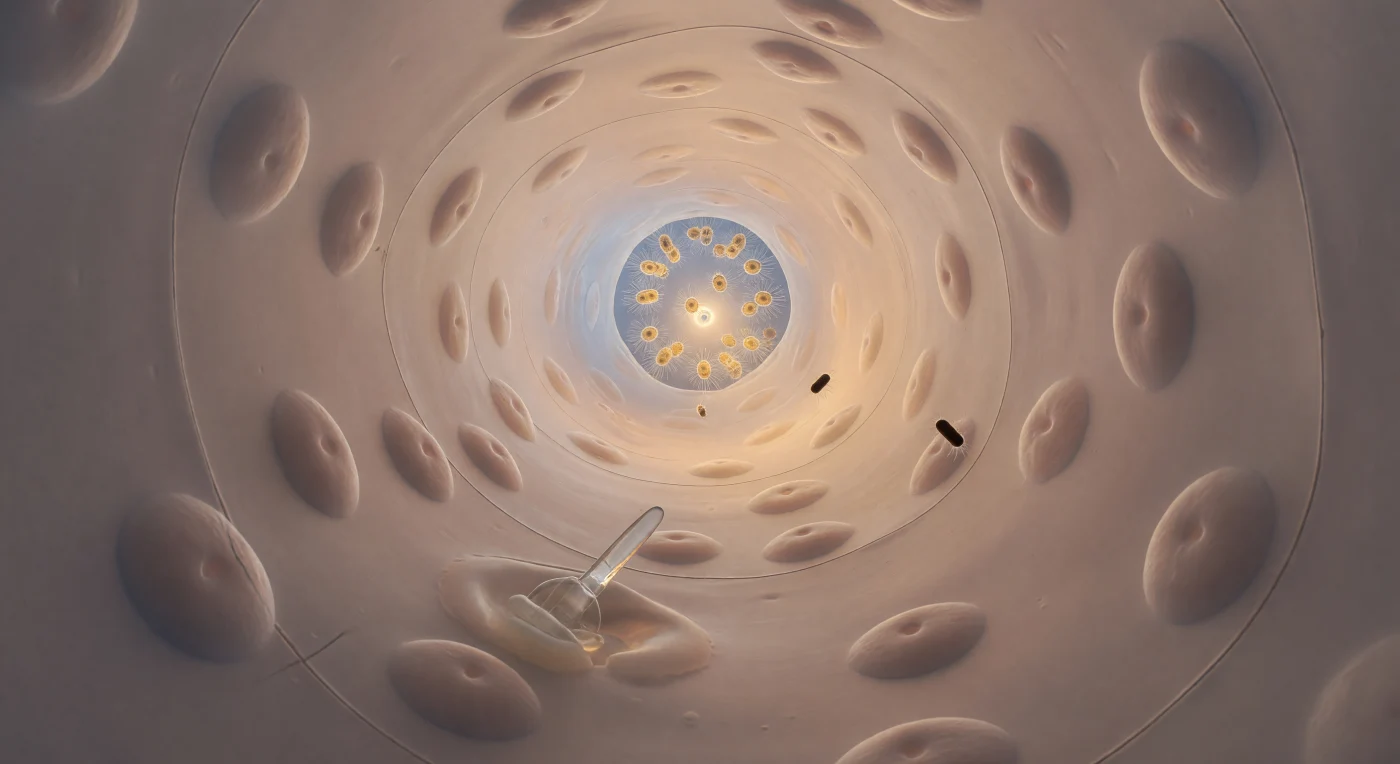
Dentro al canale inalante della spugna, ci si trova sospesi all'imbocco di un tunnel cilindrico dai contorni morbidi, le pareti rivestite da endopinacociti appiattiti come lamine di seta umida, i loro nuclei che emergono in dolci rigonfiamenti traslucidi a intervalli irregolari lungo la superficie color avorio e pesca. La corrente d'acqua si muove in regime di Stokes, laminare e silenziosa, portando avanti batteri a forma di bastoncello che derivano senza turbolenza mentre un archeoocita ameboide si contorce lentamente attorno alla base di uno spicolo calcareo incastonato nella parete, deformando il proprio citoplasma come cera tiepida per stringersi tra le giunzioni cellulari. A soli settanta micron di diametro, questo corridoio è un'infrastruttura di filtrazione che evolve da seicento milioni di anni, e ogni dettaglio delle sue superfici — le suture quasi immateriali tra le cellule, il riflesso prismatico dello spicolo, il peso viscoso del fluido stesso — appartiene a una dimensione in cui la gravità non conta nulla e la tensione superficiale governa ogni cosa. In fondo alla curva, la prosopilo brilla come un portale ambrato di appena cinque micron, oltre il quale si intravede il pulsare delle camere dei coanociti, decine di flagelli che battono in ritmo coordinato, filtrando pazientemente l'oceano un batterio alla volta.
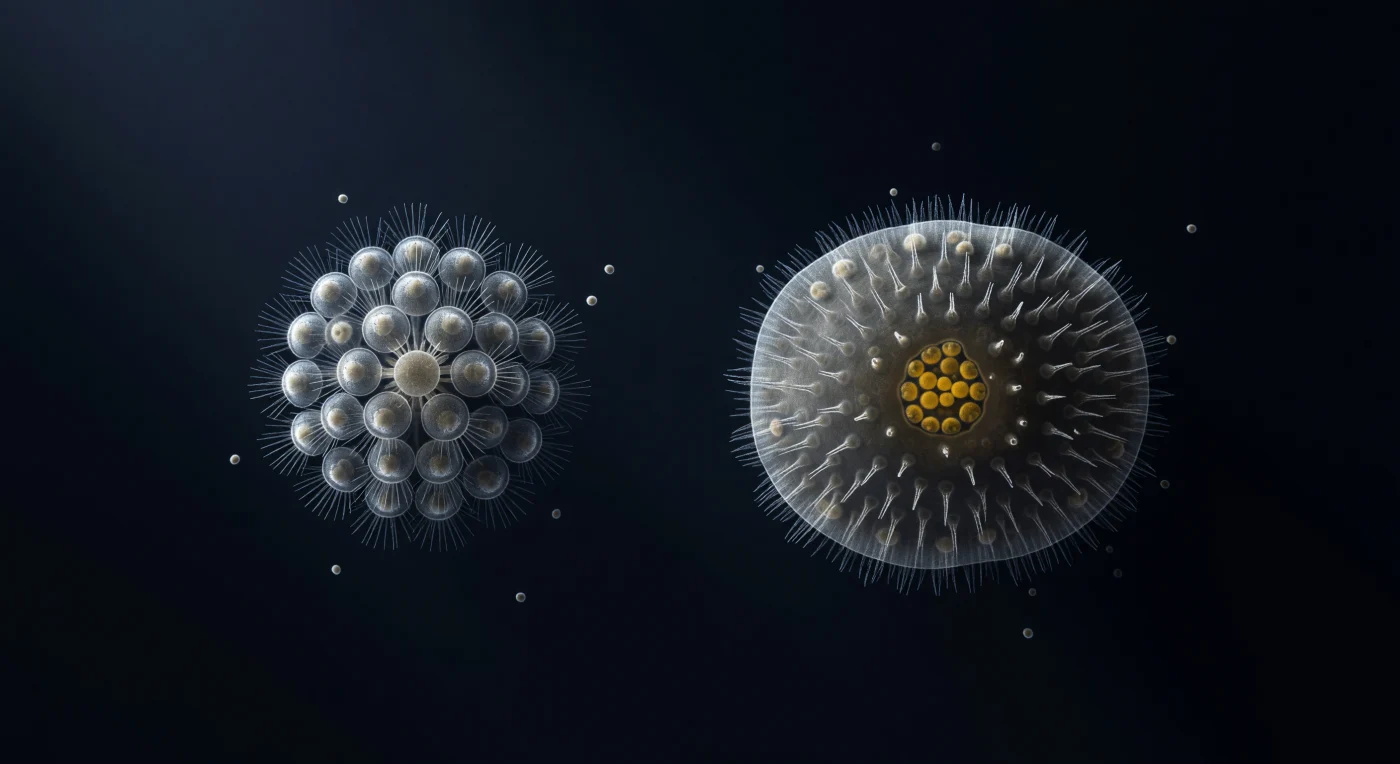
Nel campo visivo illuminato dalla luce DIC, l'oscurità ha la consistenza e il peso dell'oceano profondo — un vuoto blu-nero così denso da sembrare pressurizzato, attraversato da una sola sorgente luminosa obliqua proveniente dall'alto a sinistra che trasforma ogni membrana cellulare in rilievo argentato, ogni ombra in un abisso. A sinistra, la colonia a rosetta di *Salpingoeca rosetta* — trentadue cellule disposte con una precisione quasi cristallina, i collari di microvilli eretti come aghi d'argento intorno ai flagelli, le cellule legate tra loro da ponti intercellulari che sono forse il primo abbozzo di un corpo animale — fluttua nella sua simmetria fredda e acromatica, separata da un centinaio di micron di acqua apparentemente vuota da qualcosa di radicalmente diverso: la larva parenchimella di uno spugna calcarea, corpo ovale semiopaco la cui superficie è interamente rivestita di cellule ciliate e il cui nucleo interno cela, verso il polo posteriore, una costellazione di cellule ricche di vitello che ardono nel solo calore cromatico dell'intera scena — un ambra denso e bruciante come braci in una stanza di ghiaccio. Quella centuria di micron d'acqua tra i due organismi è visivamente quasi vuota, abitata solo da pochi profili batterici che derivano senza direzione apparente, eppure è carica di un peso invisibile: settecento milioni di anni di distanza evolutiva, la frontiera silenziosa tra ciò che è ancora una colonia unicellulare e ciò che è già, irrevocabilmente, un animale.

Sospesi nell'istante come un batterio alla deriva, ci troviamo appena all'interno della parete sezionata di una gemmula di *Spongilla*, guardando verso un interno luminoso che si apre davanti a noi come la navata di una cattedrale spaccata da un cataclisma geologico. La parete alla nostra sinistra si rivela come un'autentica fortezza laminata: una membrana esterna traslucida color ambra, poi una palizzata di spicole anfidisco in cemento di spongina color crema — ciascuna un manubrio di silice cristallina con estremità a disco che s'incastrano come una recinzione microscopica, rifrango la luce in guizzi prismatici bianco-glaciale e azzurro fantasma — e infine uno strato interno liscio, quasi laccato, che delimita la cavità interna. Dentro quel confine il mondo si fa caldo e saturo: gli archeociti sono stipati l'uno accanto all'altro, cellule gonfie da dieci a venti micron di diametro, il loro citoplasma così carico di gocciole lipidiche da brillare come lanterne in tonalità zafferano intenso, arancione tangerino, giallo cadmio, ogni cellula simile a un baccello d'olio in procinto di scoppiare. Sulla destra, il tubo del micropilo perfora l'armatura come un oblò: attualmente ostruito da una colonna compatta di cellule più pallide che si premono l'una contro l'altra come tappi in una bottiglia, con la sua apertura circolare che si affaccia sull'oscurità esterna olivastra e fredda, rendendo l'incandescenza ambrata dell'interno ancora più autosufficiente e viva. L'intera scena — chimica, strutturale, sospesa nell'animazione della diapausa invernale — è una dimostrazione di come la vita possa sigillare sé stessa contro il tempo, comprimendo mesi di metabolismo in una sfera di silice e spongina larga meno di mezzo millimetro.

Ci si trova sospesi a pochi centimetri dal legno sommerso, completamente avvolti da un mondo di verde acquatico e di buio organico: la spugna d'acqua dolce *Spongilla lacustris* si estende davanti a noi come una crosta vivente, di un verde erba elettrico che si accende dove i raggi di luce filtrano tremolando dalla superficie del ruscello, e sfuma verso il crema pallido nelle zone d'ombra più profonda. Il colore non è della spugna in sé, ma dei suoi simbionti fotosintetici — alghe verdi unicellulari intrappolate all'interno dei tessuti dell'animale, che catturano ogni fotone disponibile e lo convertono in energia, trasformando l'organismo in una lamina biologica capace di sfruttare la luce come un vegetale pur rimanendo un animale filtrante. La superficie brulica di dettagli alla scala dei millimetri: le spicole di silice — minuscoli aghi secreti cellula per cellula — emergono dal tessuto come una brina di cristallo, diffondendo la luce in un alone argenteo su ogni centimetro della crosta, mentre sfere color mogano di mezzo millimetro affiorano come ciottoli sepolti — i gemmuli, capsule di sopravvivenza sigillate, impassibili tra le cellule vive e pulsanti che li circondano. Ostracodi dalle valve lucenti come perle e platelminti translucidi scivolano lenti sulla superficie, i loro corpi abbastanza trasparenti da rivelare il verde del tessuto sottostante, mentre sopra di noi la colonna d'acqua del ruscello si apre come una cattedrale di chiarezza fresca, i raggi di luce volumetrici che spazzano la crosta in onde lente — un organismo rimasto invariato nel suo piano fondamentale da seicento milioni di anni, ancora intento a pompare e filtrare sul suo substrato di legno morto.

Nell'abitare questa pianura arancione e viva ci si trova sospesi a distanza di un battito di ciglio sopra la pelle esterna di una spugna tropicale, un paesaggio che si distende in ogni direzione come una distesa di terracotta incandescente vista da un drone radente, la cui geometria imperfetta di cellule poligonali — l'esopinacoderma — è interrotta a intervalli irregolari da oscuri pozzi circolari, gli osti, alcuni spalancati come calderoni vulcanici che inghiottono acqua di mare verso i canali inalanti interni, altri contratti in sottili fessure dal porocita che ne regola il diametro in risposta a stimoli chimici e meccanici. La superficie tra un ostio e l'altro non è mai inerte: un biofilm tridimensionale di batteri bastoncellari, aggregati coccoidi e filamenti di cianobatteri intreccia una pellicola microbica di pochi micron nello strato di muco che riveste le cellule pinacodermiche, cedendo nutrimento alla spugna stessa mentre negozia la propria sopravvivenza su un substrato che filtra ogni giorno un volume d'acqua ventimila volte superiore al proprio corpo. In primo piano un piccolo polichete emerge da uno degli osti più larghi, i palpi anteriori cigliati che ondeggiano nel sottile strato limite come antenne in cerca di particelle organiche, mentre nell'angolo superiore destro un copepode dal carapace trasparente tocca brevemente la superficie prima che il gradiente di pressione generato dal vicino osculo ne devii la traiettoria, ricordando che anche a questa scala minuta la meccanica dei fluidi governa ogni contatto tra forme di vita.
















