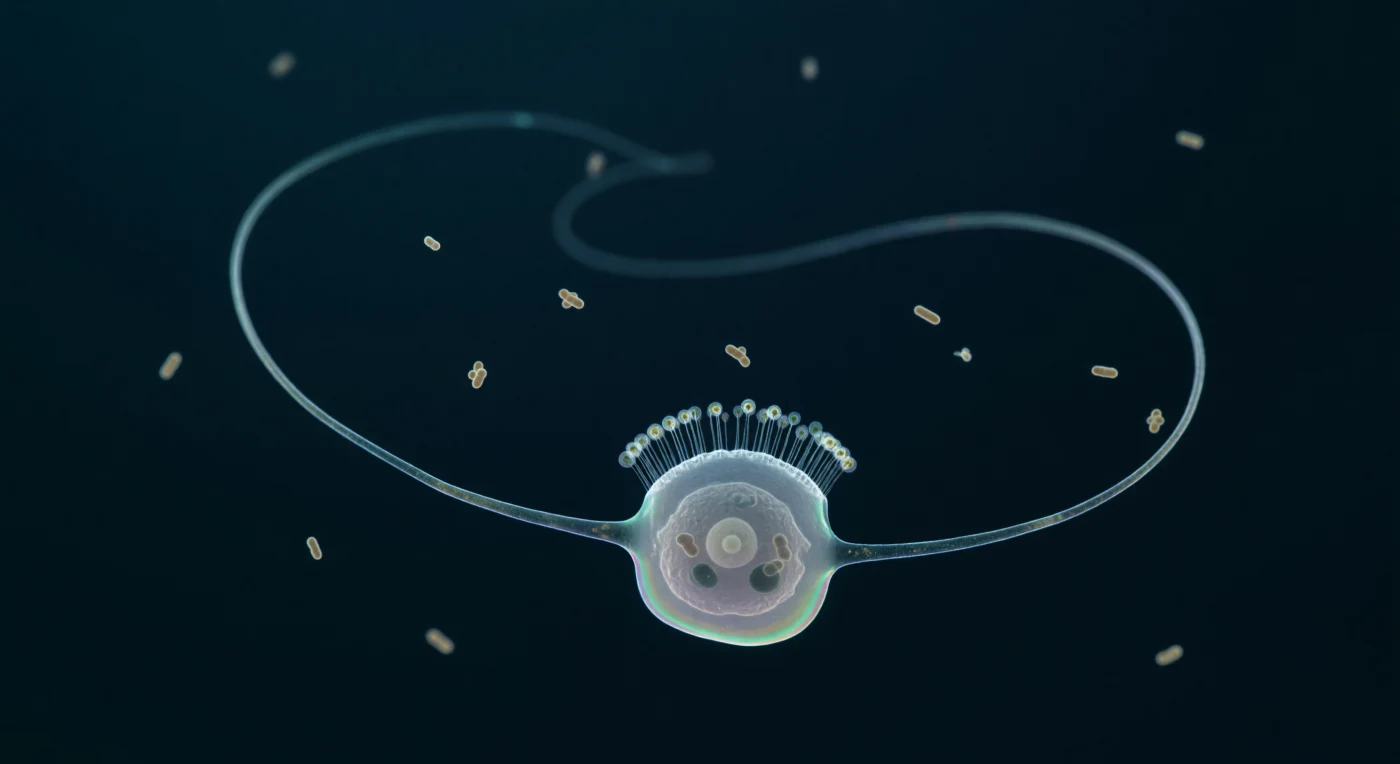
In diesem Augenblick bist du vollständig von einem dunkelblauen Nichts umhüllt, das sich weniger wie Wasser als wie eine dritte Form von Materie anfühlt — ein zähflüssiges Medium, in dem thermisches Rauschen die einzige Bewegung ist und Schwerkraft keine Rolle spielt. Vor dir beherrscht eine einzige Choanoflagelatenzelle das Bild: ihr Geißel, zwanzig Mikrometer lang und kaum dicker als ein Spinnenfaden, schwingt in einer eingefrorenen helikalen S-Kurve über dein gesamtes Sichtfeld, während ein silbrig-transparenter Nachklang im dunklen Medium den vorherigen Herzschlag des Flagellums nachzeichnet — das Ergebnis einer sinusförmigen Welle, die diese Zelle mit dreißig bis sechzig Schlägen pro Sekunde antreibt und dabei einen Mikrowirbel erzeugt, der Bakterien wie in einem molekularen Netz durch den Kragen aus fünfunddreißig Mikrovilli zieht. Der Kragen selbst ist kaum als feste Struktur wahrnehmbar — jeder Mikrovillus liegt unterhalb der Wellenlänge des sichtbaren Lichts und manifestiert sich nur als irisierender Interferenzschimmer, eine schwebende Krone aus Gold und kaltem Aquamarin über dem Zellkörper, dessen durchsichtiges Zytoplasma einen blass leuchtenden Zellkern und zwei dunkle Nahrungsvakuolen birgt, in denen die Silhouette halbverdauter Bakterien noch zu erahnen ist. Im Hintergrund treiben ein Dutzend Stäbchenbakterien im Brownischen Zittern des Mediums — manche scharf konturiert, andere bereits zu blassen Schimmern in der blauen Tiefe verschwommen, denn jenseits weniger Zellbreiten verschluckt die absolute Dunkelheit jeden Horizont.

In der opaleszierenden Tiefe eines Ästuars schwebt vor dir eine Struktur, die das gesamte Sichtfeld ausfüllt wie ein langsam rotierender Kronleuchter aus lebendem Silber: eine 32-zellige Rosetten-Kolonie von *Salpingoeca rosetta*, deren Zellen in perfekter radialer Geometrie nach außen weisen und mit ihren ausgestreckten Geißeln eine elektrisierende Korona bilden – ein mikroskopischer Seeigel, eingefroren im Moment seiner maximalen Ausdehnung. Jede Zelle ist ein prall gefülltes, leicht transluzentes Ovoid, dessen Plasmamembran kalte DIC-Glanzlichter trägt, während im Inneren der dunkle Ellipsoid des Zellkerns kaum erkennbar schimmert; an der Zwei-Uhr-Position verrät eine leicht eingezogene, erdnussförmige Zelle, dass die Kolonie gerade im Begriff ist, sich durch Teilung zu erweitern. Die basalen Pole aller Zellen laufen auf einen gemeinsamen Kern zu, verbunden durch zytoplasmatische Brückenfäden, die als kaum sichtbare, geringfügig hellere Speichen zu einer warm bernsteinfarbenen extrazellulären Matrix führen – der einzige warme Farbton in einer sonst kühlen, nahezu monochromen Szene. Diese Kolonie ist kein bloßes Einzelwesen, sondern ein lebendes Argument über den Ursprung der Vielzelligkeit: Die koordinierte Geometrie, die geteilte Matrix und die interzellulären Brücken spiegeln exakt jene Bauprinzipien wider, die Hunderte Millionen Jahre später die Choanozytenkammern der Schwämme organisieren werden. Um die Kolonie herum treiben locker strukturierte Marine-Snow-Flocken durch das blauschwarz schimmernde Wasser – Aggregate aus Polysaccharid-Fäden und eingebetteten Bakterienrods –, die dem Ganzen räumliche Tiefe verleihen und die Kolonie als frei schwebendes Objekt in einer belebten, partikelreichen Welt verorten.
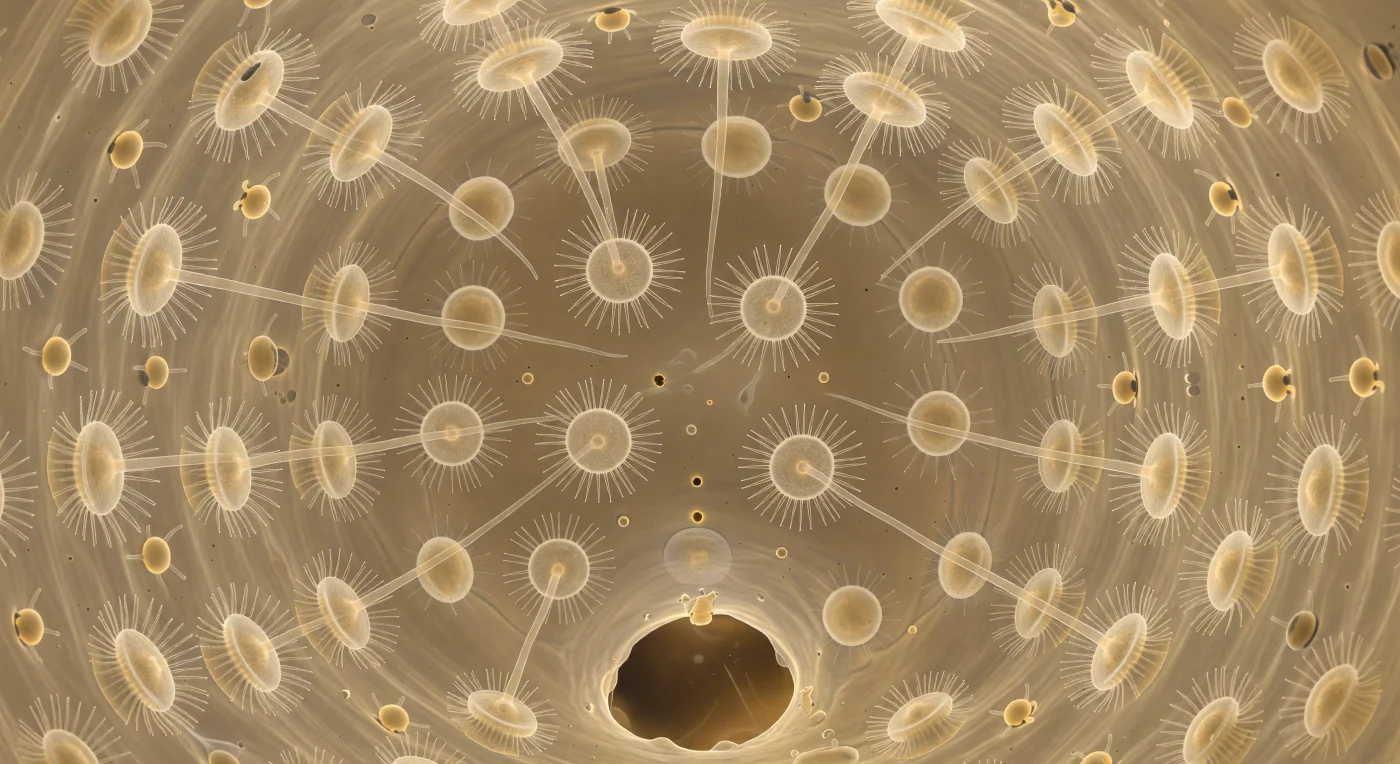
Innerhalb dieser winzigen Kugel aus lebendigem Gewebe schwebt man im Zentrum einer Choanozyten-Kammer — einem vollständig ausgekleideten Hohlraum von etwa vierzig Mikrometern Durchmesser, dessen gesamte Wandfläche von fünfundzwanzig dicht stehenden Choanozyten bedeckt ist, jede Zelle mit einem transparenten Kragen aus haarfeinen Mikrovilli und einer einzelnen, peitschenden Geißel versehen, die sich im versetzten Takt der Nachbarzellen bewegt und dabei ein weiches, wellenartiges Schimmern in der bernsteinfarbenen Kammer erzeugt. Dieses abgestimmte Geißelschlagen ist keine bloße Bewegung, sondern eine biologische Pumpe: Durch die zwei kleinen Prosopyl-Poren in der Kammerwand strömt partikelbeladenes Meerwasser ein, wird an den Mikrovilluskragen jeder Zelle vorbeigeleitet und dabei gefiltert, Bakterien und organische Moleküle im Submikrometerbereich aus der Flüssigkeit herausgefangen und phagozytiert. Jenseits der Zellschicht ist das Mesohyl sichtbar — das gallertartige Bindegewebe des Schwamms, durchzogen von kollagenartigen Fasern und langsam kriechenden Archaeozyten, die mit ausgestreckten Pseudopodien Nährstoffe zwischen den Kammern transportieren. Direkt voraus öffnet sich das Apopyl wie ein dunkles Tor, durch das das gefilterte Wasser weiterfließt — ein winziger Schritt in einem System, das täglich das zwanzigtausendfache seines eigenen Körpervolumens durchpumpt und damit zu den effizientesten biologischen Filteranlagen der Erde gehört.
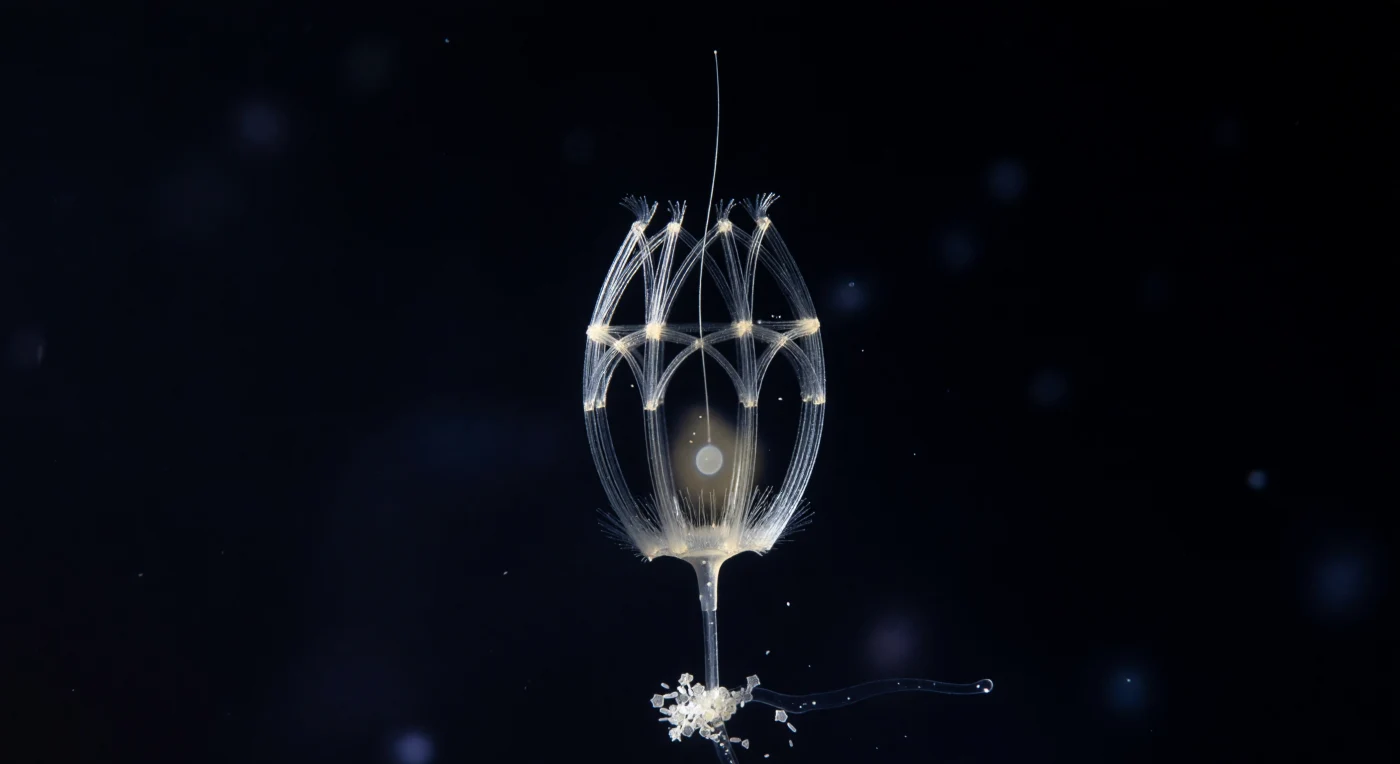
In der Tiefe des mesopelagischen Ozeans schwebt vor dem Betrachter ein Gebilde von unwirklicher Zartheit: ein geometrisches Käfigwerk aus Siliziumdioxid-Stäbchen, kaum zwanzig Mikrometer im Durchmesser, das im schrägen Seitenlicht zu weißsilbrigem Glühen aufflackert – die Lorica von *Diaphanoeca grandis*, einer Kragengeißeltierchen-Art, deren kostalem Gerüst aus längs verlaufenden Rippen und quer gespannten Reifen eine Präzision innewohnt, die eher an gotische Kathedralarchitektur als an biologische Selbstorganisation erinnert. Die Siliziumstäbchen sind keine bloße Hülle, sondern ein aktiv sekretiertes Außenskelett, das dem Organismus Auftrieb und Strömungsschutz bietet, während es gleichzeitig den Wasserfluss durch seine offenen Maschen kanalisiert und so die Nahrungsaufnahme begünstigt. Im Inneren des Käfigs ist das lebende Tier kaum mehr als eine bernsteinfarbene Ahnung – eine blasse Zytoplasmatrübung, aus der das Flagellum durch den offenen Vorderpol nach oben in die Dunkelheit fädelt, wo es als ein einziger, kaum fassbarer Silberfaden verschwindet. Am Fuß des Stiels, mit dem die Lorica an einem Partikel marinen Schnees verankert ist, schimmern die geometrischen Siliziumplatten von Diatomeen-Frusteln wie winzige, zerbrochene Spiegel und erinnern daran, dass dieser Organismus – evolutionär gesehen an der Schwelle zur Vielzelligkeit – dieselbe chemische Sprache des Meeressiliziums spricht wie die Welt, in der er treibt.

Vor dir erhebt sich die zylindrische Wand von *Euplectella aspergillum* in der absoluten Schwärze der Tiefsee wie das Mittelschiff einer gotischen Kathedrale aus gefrorenem Licht – ein schachbrettartiges Gitter aus sechsstrahligen Kieselsäure-Spicula, die an jedem Kreuzungspunkt zu einem einzigen starren Synzytium verschmolzen sind, die Geometrie so präzise und regelmäßig, dass sie eher konstruiert als gewachsen wirkt. Jede Spicula glüht über ihre gesamte Länge in einem kalten Blaugrün, weil das Siliziumdioxid wie eine echte Lichtleitfaser wirkt und das schwache Biolumineszenzlicht des umgebenden Wassers in sich aufnimmt und kanalisiert, sodass das Leuchten aus dem Innern des Stabes selbst zu emanieren scheint. Blickt man durch die Gitterwand in den hohlen Atrium-Innenraum, multiplizieren sich komplexe Schattenraster nach innen, und an gebrochenen Spiculaquerschnitten sind konzentrische Laminationsringe im Silizium sichtbar – Wachstumsschichten wie die eines gläsernen Baumes, halb durchscheinend und bernsteinfarben im dichten Kern, bevor sie in ein reines, glaziales Weiß übergehen. Tief im Innern des Atriums erscheinen zwei kommensale Garnelen als warm bernsteinrosa Silhouetten, von dem sanften Leuchten hinter ihnen durchdrungen, ihre segmentierten Körper und fedrigen Antennen wie lebendige Buntglasfiguren, die für immer in ihrer gläsernen Kathedrale eingeschlossen sind, während das Wasser ringsum – mit dem Gewicht der gesamten Wassersäule darüber – in vollkommener Stille und Dunkelheit jenseits des Leuchthalos verharrt.
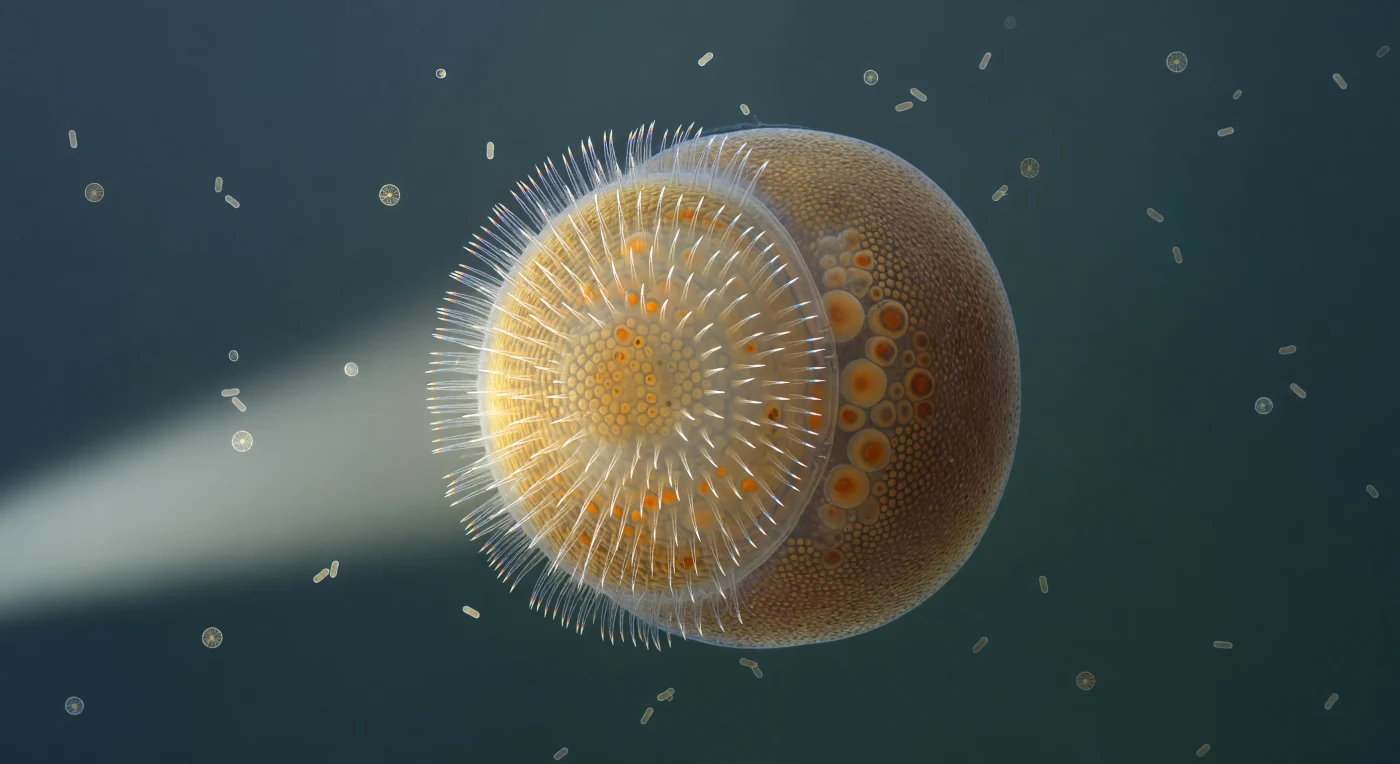
Vor dir schwebt ein ovaler Mikrokosmos von etwa 400 Mikrometern Durchmesser — kaum größer als ein feines Sandkorn, und doch in sich vollständig und von erschreckender Schönheit: die Amphiblastula-Larve einer Kalksschwamms, ein Entwicklungsstadium, das seit Hunderten von Millionen Jahren durch die Weltmeere treibt. Die dem Licht zugewandte vordere Hemisphäre brennt in warmem Gold-Bernstein, ihr gesamter Rand in einen vibrierenden Fransenkranz aus metachronal schlagenden Wimpern aufgelöst, deren koordinierte Wellenbewegung das Seitenlicht in eine flüchtige Spektralkorona bricht — Violett, Cyan und blassgold zucken und verlöschen in einem fort entlang der Äquatoriallinie. Diese Kinozilien, jede ein gläserner Faden von wenigen Mikrometern Länge, erzeugen kollektiv jenen Antrieb, der die Larve durch eine Wassersäule befördert, die sich aus ihrer Perspektive wie ein zähes, von Brownscher Molekularbewegung durchwirktes Gel anfühlt. Die hintere Hemisphäre zieht sich ins Ockerfarbene und Dunkelbraune zurück: Durch die hauchdünne, transluzente Wandung zeichnen sich die dicht gepackten Archäozyten als weiche Schattenformen ab, ihre lipidreichen Dottereinschlüsse wie bernsteinbraune Laternen hinter mattem Glas. Wenn die Larve den richtigen Substratreiz empfängt, wird sie sich festsetzen, ihre Cilien verlieren und sich in die ersten Zellschichten eines neuen Schwammindividuums umorganisieren — ein Übergang, der die Grenze zwischen freischwimmendem Tier und sessiler Filtermaschine markiert.

Du schwebst direkt über dem Rand des Osculums eines gewaltigen Fasserschwamms, und was sich vor dir öffnet, wirkt wie der Schlund eines lebenden Vulkans – ein kreisrundes Kaminloch, dessen terrakottafarbene Innenwände sich in dunkel verzweigte Exhalantkanäle hinab verlieren, während ein kontinuierlicher Ausstromstrahl gefiltertes Meerwasser nach oben treibt und die Wassersäule mit einem flimmernden, schlierenartigen Wärmespiegeleffekt erfüllt. Dieser Schwamm ist kein passives Riffgebilde: Er pumpt täglich das Zwanzigtausendfache seines eigenen Körpervolumens durch ein internes Labyrinth aus Kammern und Kanälen, angetrieben von Tausenden mikroskopischer Choanozyten, deren synchron schlagende Geißeln im Verborgenen eine laminare Strömung erzeugen, die Bakterien, gelöste organische Substanzen und Partikel aus dem vorbeiziehenden Wasser herausfiltert. Die im Aufstrom schwebenden Partikel – transluzente Detritusflocken, blasse Bakterienwolken, einzelne Kieselsäuresplitter – fangen das türkisblaue Kaustikmuster des Oberflächenlichts ein und treiben träge in die offene Wassersäule, während die raue Außenwand des Schwamms von eingewachsenen Bryozoen und korallinischen Algen besiedelt wird und weich defokussierte Rifffische im warmen Hintergrund die Lebendigkeit dieser uralten, atemgleichen Architektur bezeugen. Schwämme gehören zu den frühesten mehrzelligen Tieren der Erdgeschichte, und ihre Verwandtschaft mit den koloniebildenden Choanoflagellaten – einzelligen Organismen mit nahezu identischem Kragenzelltyp – macht diesen Ort zum molekularen Schwellenwert zwischen Einzeller und Tierkörper.
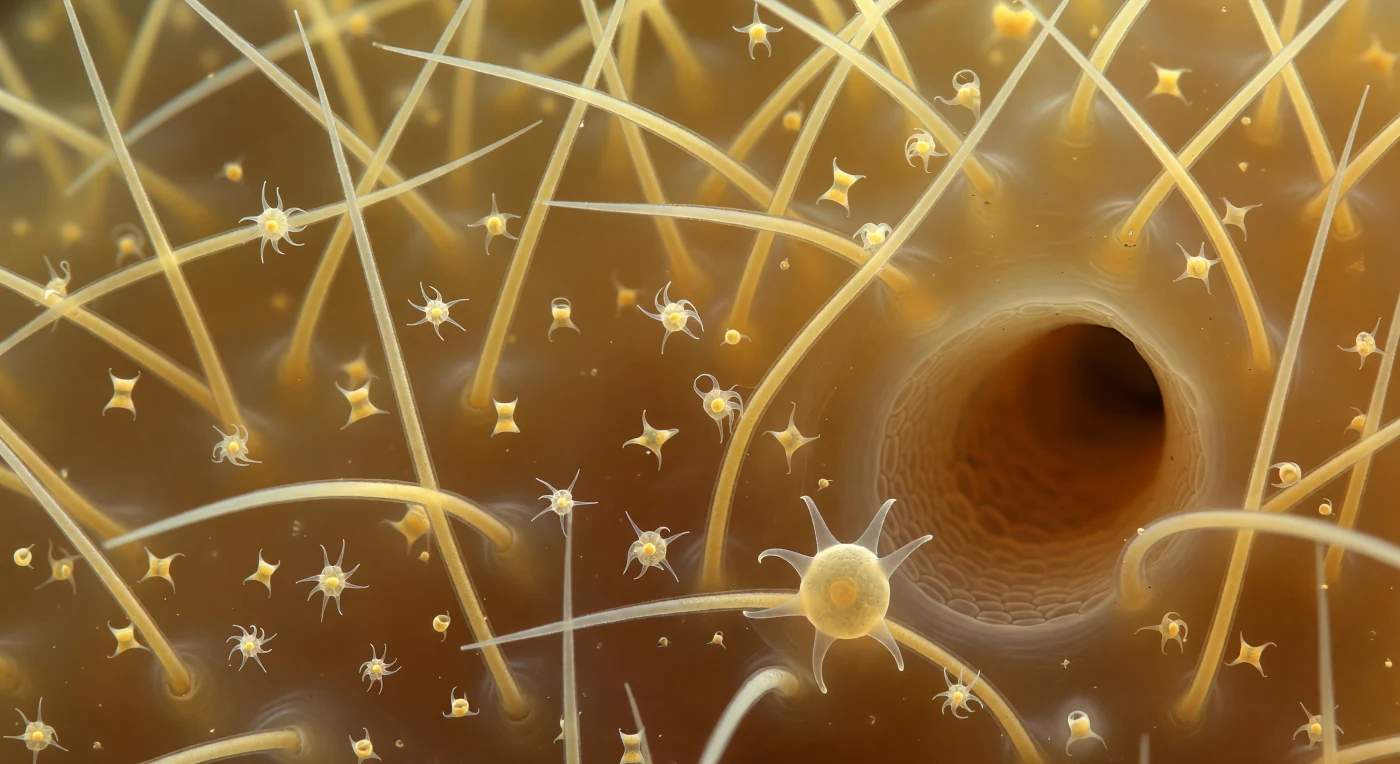
Im Inneren eines lebenden Demoschwamms treibst du durch ein Universum aus Bernstein und Glas: Oxea-Megaskleren aus biogenem Siliziumdioxid erheben sich wie die Rippen einer gefrorenen Kathedrale um dich herum, je zwei Millimeter lang und an beiden Enden zu haarscharfen Spitzen ausgezogen, ihre halb durchsichtigen Schäfte von einem inneren Leuchten durchdrungen, als würde Mittagslicht durch flüssigen Bernstein gefiltert. Das kolloidale Mesohyl füllt den Raum zwischen ihnen als eine lebendige, honigwarme Gelmatrix, in der Sigma-Mikroskleren und spiralförmige Chelae langsam im Brown'schen Taumeln rotieren – winzige Glasskulpturen, deren Krümmungen Lichtsilber zurückwerfen. Spongin-Fasern ziehen sich als goldfarbene organische Kabel von Spicula-Basis zu Spicula-Basis und bilden zusammen mit den Nadeln ein einziges tensiles Gerüst, das das gesamte Filtergewebe des Schwamms in Form hält. Wenige Körperlängen entfernt öffnet sich ein dunkler Kanalgang als kupferbraune Röhre aus flachen Pinakozyten – eine Wasserstraße, durch die täglich das Zwanzigtausendfache des Körpervolumens strömt. An einem der Vordergrundspicula krallen sich die breitausladenden Pseudopodien eines einzelnen Archäozyten in die glatte Siliziumoberfläche, sein cytoplasmatischer Leib ein durchscheinender goldener Blasen mit sichtbarem Zellkern – die wandernde, phagozytische Zelle, die das Skelett aufbaut, repariert und zugleich das gesamte architektonische Unternehmen mit langsamer, chemischer Präzision zusammenhält.
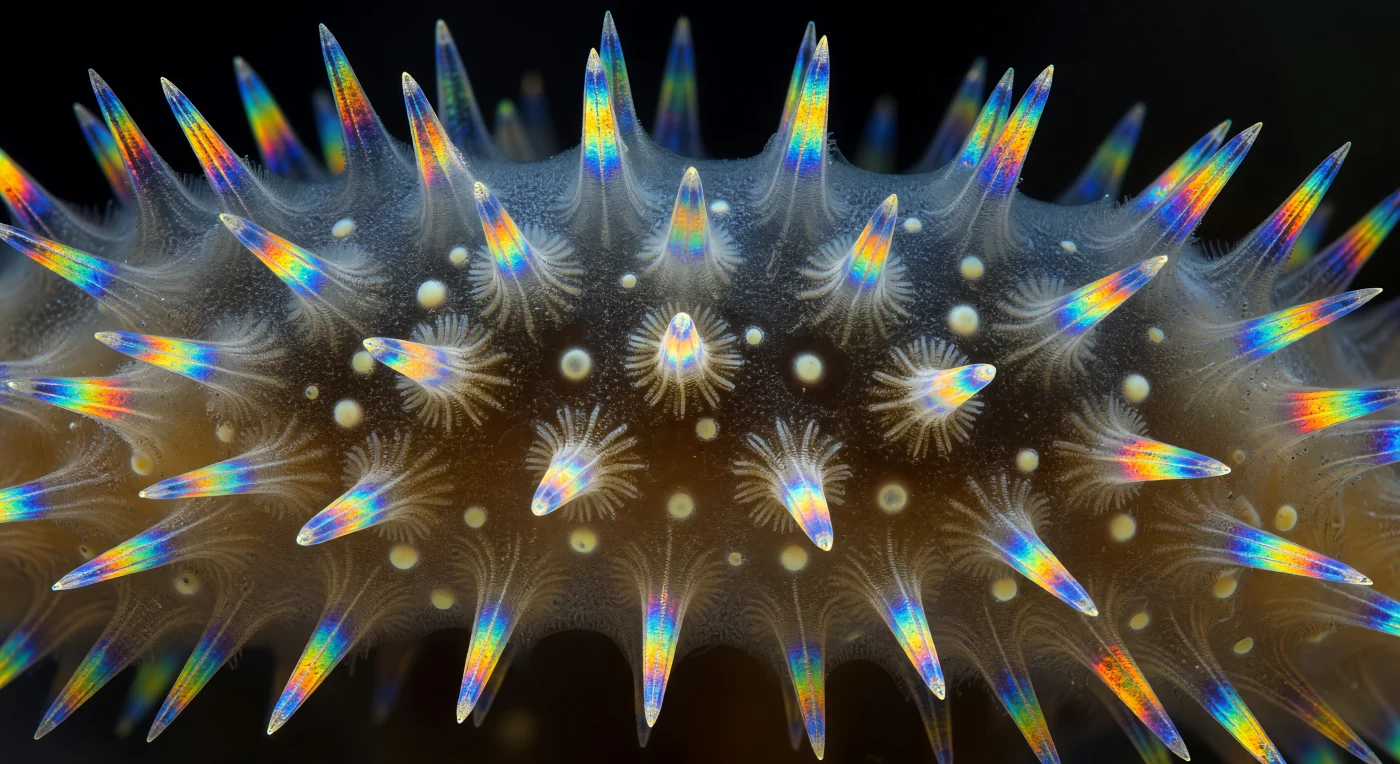
In der Dunkelheit zwischen den Strahlen polarisierten Lichts erwacht die Wand eines winzigen Meeresschwamms — *Sycon ciliatum* — zu einem Spektakel aus lebendigem Mineral und organischer Architektur: Triaktin- und Tetraktin-Spicula aus Kalzit brennen in elektrischem Kobaltblau, Schwefelgelb, geschmolzenem Orange und kaltem Smaragdgrün gegen einen absolut schwarzen Hintergrund, jeder Kristall von innen durch den optischen Effekt der Doppelbrechung entfacht. Die radiale Symmetrie des Schwammgewebes entfaltet sich wie ein Kirchenfenster — zylindrische Radialkanäle, ausgekleidet mit Choanozyten-Schichten, deren Mikrovilli das schwache durchdringende Licht einfangen, getrennt durch Rippen aus lebendigem Gewebe, das von Spicula durchzogen ist wie ein Gerüst aus Edelsteinen. Das Mesohyl zwischen den Kanälen erscheint als ein dichtes, bernsteinfarbenes Gel, granulär und faserig, durchdrungen von einem extrazellulären Matrixnetzwerk, das die molekulare Grundlage des ältesten mehrzelligen Körperbauplans der Tierevolution bildet. Wo sich mehrere Spicula überschneiden, stapeln sich ihre Interferenzmuster zu irisierenden Aureolen — Bernstein, Violett, elektrisches Blaugrün — und erzeugen eine Tiefenperspektive, in der die vorderen Kristalle in rasiermesserscharfer chromatischer Schärfe leuchten, während die hinteren Radialkanäle in schwarze Unendlichkeit versinken, als würde man in das Innere einer lebendigen Kathedrale blicken, die nie für menschliche Augen gebaut wurde.

Im Lichtstrahl des ROV taucht vor einem eine Welt auf, die wie eine erstarrte gotische Kathedrale aus dem Dunkeln wächst: Türme von *Aphrocallistes vastus*, den Glassschwämmen des Nordostpazifiks, erheben sich als transluzente Gittersäulen aus dem grau-weißen Sediment, das von zersplitterten Spicula-Scherben wie von Diamantsplittern übersät ist. Das Skelett jedes Turms besteht aus verschmolzenen Siliziumdioxid-Spiculae, die in einem präzisen hexagonalen Netzwerk verwoben sind – eine biologische Faseroptik, durch die das Flutlicht von unten in jeden Glasstreben wandert und die gesamte Säule in einem warmen, perlmuttfarbenen Schimmer erglühen lässt. Schlangensterne schlingen ihre bändchenartigen Arme durch die Maschenöffnungen des Gitters, ein Rotbarsch verharrt regungslos im Schatten zwischen den Türmen, und am Rand des Lichtkegels verlöscht ein kurzer blau-grüner Biolumineszenzschleier im Schwarz – das Einzige, was sich in dieser vollkommenen, druckerfüllten Stille bewegt. Das Riff, das sich in der Dunkelheit um Hunderte von Metern erstreckt, ist eines der ältesten lebenden Bioherme der Erde: Strukturen, die Jahrtausende brauchen, um zu wachsen, und die das Wasser mit einer Filterpumpleistung von bis zum 20.000-fachen des eigenen Körpervolumens täglich durchströmen lassen.

Du schwebst in der kalten benthischen Grenzschicht über einem Gesteinsgrund, der sich in diesem Maßstab wie ein gewaltiges fremdes Plateau ausdehnt – das verkrustete Korallinenalgen-Substrat zieht sich als zerbrochene magentarote Tundra unter dir hin, seine kalzifizierten Platten von erhöhten tektonischen Graten gesäumt, während Diatomeen-Frusteln wie makellose Glaskathedralen aus dem Biofilm ragen und das diffuse blaugrüne Licht von oben in tausend Facetten brechen. Zwischen ihnen breitet sich eine lebendige Schleimlandschaft aus – transluzente Exopolysaccharid-Fäden der bakteriellen Biohülle fangen das seitlich einfallende Licht und lassen selbst die dünnsten Filme kolloidal schimmern, während die Mikroskulptur jedes Kamms und jeder Vertiefung durch weiche Eigenschatten in greifbarer Tiefe erscheint. Im Zentrum dieses Terrains vollzieht eine frisch abgesetzte kalkige Schwammlarve von etwa 300 Mikrometern Durchmesser eine der grundlegendsten Transformationen des Tierreichs: Ihre ursprünglich hemisphärische Körperform kollabiert in morphogenetischer Inversion nach innen, die Zilien tragenden Zellen ziehen sich an der apikalen Achse in eine wachsende Einbuchtung zurück, während an der Peripherie die zukünftigen Pinacozyten sich bereits zu flachen, pflasterartig angeordneten Zellen ausstrecken und konzentrisch nach außen vordringen wie eine langsame Kristallisationsfront. Der nascente Glykokalyx der Larvenoberfläche fängt das transmittierte Licht an ihrem transluzenten Rand – ein bernsteinfarbenes Leuchten wie durch Buntglas – und die Gesamtszenerie verschmilzt die eisigen Aquamarin-Töne des Wasserkörpers oberhalb mit dem glutroten Karbonat der Algen und dem warmen Bernsteingold der organischen Materie zu einer Welt von überwältigender, lebendiger Präzision.
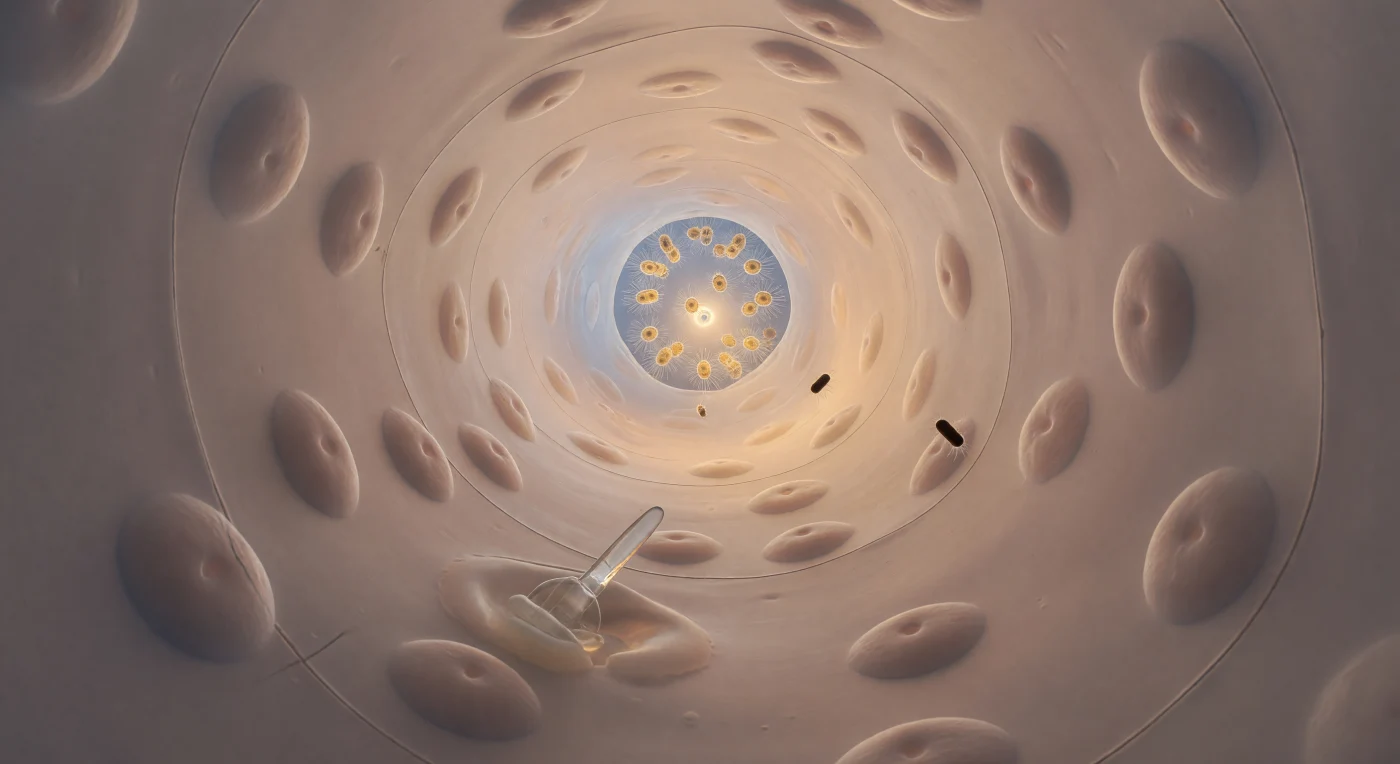
In der Stille vor dir öffnet sich ein lebendiger Schlauch, kaum breiter als ein menschliches Haar siebzigfach gespalten, dessen sanft geschwungene Wände aus hauchflachen Endopinakozyten bestehen — so glatt gepresst gegen das darunterliegende Mesohyl, dass ihre Oberfläche wie polierte Perlmutter schimmert, nur die sanft gewölbten Zellkerne heben sich als gerundete Hügel in der blassrosa Membranlandschaft ab. Das Wasser kriecht in einem trägen, laminaren Stokes-Strömungsregime vorwärts, in dem Trägheit keine Rolle spielt und Viskosität alles regiert — zwei stäbchenförmige Bakterien gleiten wie winzige Mahagonizylinder an dir vorbei, leicht rotierend im Scherbereich nahe der Wand, ein drittes wird vom Brownschen Rauschen aus seiner Bahn getrieben, bevor die Strömung es wieder einholt. Am unteren Wandabschnitt schiebt sich ein Archäozyt mühsam zwischen Zellnaht und eingebetteter Kalknadel hindurch, sein Zytoplasma quillt und zieht sich zurück wie warmes Wachs, während der gläserne Spikel einen hauchzarten Prismaschimmer auf die benachbarte Zelloberfläche wirft. Vierzig Kanaldurchmesser entfernt leuchtet die Prosopyle — eine fünf Mikrometer breite, von zwei sich berührenden Pinakozyten gesäumte Öffnung — wie ein goldenes Portal, durch das der honigwarme Schein der dahinter pulsierenden Choanozyten-Kammer fällt, ein System, das in nahezu unveränderter Form seit sechshundert Millionen Jahren den Ozean durch lebendes Gewebe siebt.
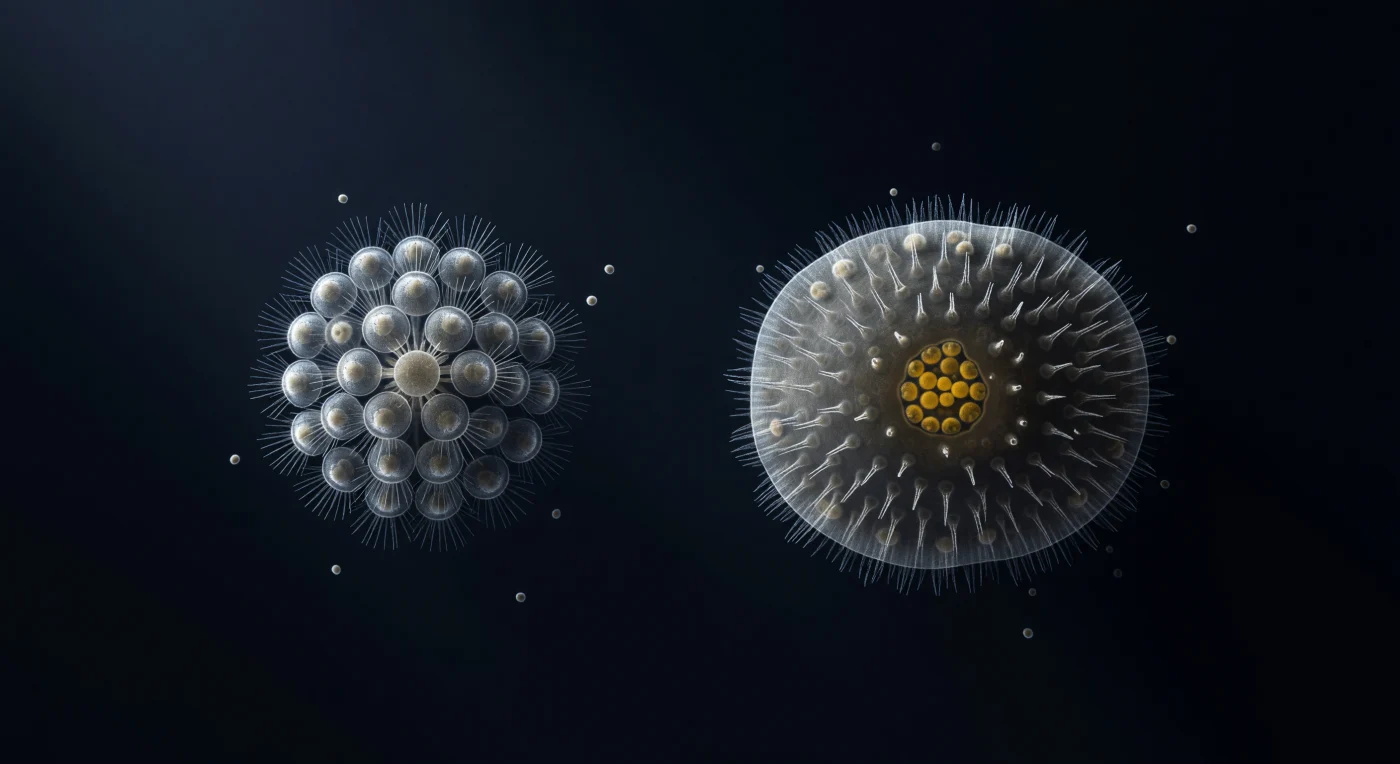
Im tiefsten Blauschwarz eines DIC-beleuchteten Präparats schweben zwei Welten in einem Abstand von kaum hundert Mikrometern voneinander: links die geometrisch makellose Rosette einer *Salpingoeca rosetta*-Kolonie, deren zweiunddreißig Zellen ihre Kragen-Geißel-Einheiten wie silberne Nadeln nach außen recken, ein biologisches Kristall aus lebendigem Glas; rechts die parenchymella-Larve eines kalkigen Schwammes, dicht und opak, ihr konvexer Rücken brennend hell im schrägen Licht, ihr hinteres Ende von warmen Bernsteintönen durchdrungen, wo dottergefüllte Reservezellen wie Glut in einem Raum aus Eis glühen. Das Wasser zwischen beiden ist keine Leere, sondern eine zähviskose, molekular gedrängte Flüssigkeit, in der Schwerkraft keine Rolle spielt und vereinzelte Bakterienschatten lautlos treiben — potenzielle Mahlzeiten für Filtriermechanismen, die in beiden Organismen annähernd identisch gebaut sind. Denn in der Tiefe der Larve zeigen einzelne Zellen bereits die Umrisse von Kragenzellen: Evolution beim stillen Proben einer Körperarchitektur, deren Urform mehr als siebenhundert Millionen Jahre zurückreicht und in dieser einen Aufnahme, im Abstand weniger Atemzüge zweier mikroskopischer Körper, noch immer gegenwärtig ist.

Der Blick fällt auf einen Querschnitt durch eine Süßwasserschwamm-Gemmula – eine Überdauerungsstruktur, die das Tier durch Frost und Trockenheit trägt –, deren dreischichtige Panzerung sich wie das Innere einer aufgesägten Festung entfaltet: außen eine schimmernde Membran aus gespanntem Amber, dahinter eine Palisade aufrecht stehender Amphidisc-Spicula, jede ein hantelförmiges Gebilde aus biogenem Siliziumdioxid, dessen tellerförmige Enden ineinandergreifen wie die Zinken einer miniaturisierten Umzäunung, eingebettet in blasscremeweißes Spongin-Zement. Diese Spicula wachsen nicht aus technologischen Prozessen, sondern werden durch spezialisierte Zellen – Sclerocyten – Atom für Atom in Spongin-Protein gefasst, ihre kristalline Symmetrie ein Produkt molekularer Selbstorganisation bei Körpertemperatur. Dahinter öffnet sich das Innere der Gemmula wie ein von sich selbst erleuchteter Raum: dicht gepackte Archaeocyten, Stammzellen des Schwammes, deren Cytoplasma mit Lipidtröpfchen in tiefem Safrangelb und Kadmiumorange vollgesogen ist – chemische Energiereserven, versiegelt gegen die Außenwelt, bis Temperatur und Photoperiode Keimung signalisieren. Rechts durchsticht ein Micropyle-Kanal die gesamte Panzerung, aktuell von einer Zellsäule verschlossen wie ein Korken in einer Flasche; jenseits der äußeren Membran liegt das Sedimentwasser – trüb, olivgrau, kalt –, und der Kontrast zwischen dieser Stille und dem warmen Bernsteinglühen des Innern gibt dem Ganzen das Gewicht einer im Winter aufgebrochenen Geode.

Vor dir breitet sich der Untergrund eines halb versunkenen Holzstücks aus, überzogen von einem lebendigen, grasgrünen Krusten-Teppich aus *Spongilla lacustris* – einem Süßwasserschwamm, dessen leuchtendes Grün von symbiontischen Grünalgen stammt, die tief in sein lebendes Gewebe eingebettet sind und jeden Lichtstrahl, der durch die bewegte Wasseroberfläche bricht, in Photosynthese verwandeln. Die Textur der Kruste erinnert an Samt, der mit Glasnadeln durchwoben ist: ein feines Geflecht aus Silikatnadeln, den Spicula, die das Skelett des Schwamms bilden und an ihren Spitzen das Licht wie Eiskristalle auffangen, während sie gleichzeitig das gesamte Gewebe stützen und schützen. Zwischen dem lebendigen Grün ragen dunkle, mahagonifarbene Kugeln hervor – die Gemmulae, winterharte Überdauerungsstrukturen, jede etwa einen halben Millimeter im Durchmesser, mit einer radialen Architektur aus Spezial-Spicula besetzt wie die Blütenblätter einer gepanzerten Blume, geduldig wartend in ihrer Starre inmitten der aktiv filtrierenden Zellen ringsum. Kleine Ostrakoden rollen über die Oberfläche wie Saatperlen im Samt, blasse Strudelwürmer gleiten in trägen Bögen darüber hinweg, und über allem wölbt sich das kühle, grün gefärbte Wasser des Baches wie eine belebte Kathedrale aus wandernden Lichtsäulen und Schatten – ein Organismus, dessen Bauprinzip sich seit sechshundert Millionen Jahren nicht verändert hat.

Die äußere Haut des Schwamms breitet sich wie ein leuchtendes, zerklüftetes Pflaster in alle Richtungen aus – ein Mosaik aus flachen, polygonalen Zellen in tiefem Ocker und Safrangelb, gesättigt von Carotinoiden, die das gefilterte Riffwasser in ein warmes, glasiertes Glühen verwandeln. Über diese Fläche verteilt öffnen sich die Ostien als dunkle Einschlüsse unterschiedlicher Weite: Wo sich die Porizytenwände vollständig zurückgezogen haben, fällt der Blick in absolute Schwärze, als schaue man in einen Kaminschlot, während halb geschlossene Öffnungen nur noch als helle, sphinkterartige Schlitze erkennbar sind – gezogen von jenem unsichtbaren Sog, der pausenlos Wasser in das innere Kanalsystem des Tieres befördert, bis zu zwanzigtausend Mal das eigene Körpervolumen täglich. Zwischen den Ostien überzieht ein dreidimensionaler Biofilm aus Stäbchenbakterien, Coccoidclustern und fadenförmigen Cyanobakterien die gesamte Oberfläche wie ein irisierender Flaum, kaum wenige Mikrometer stark, und verleiht dem Terrain eine matte, bereiferte Textur. Aus einem der weitgeöffneten Poren taucht ein kleiner Polychaet auf, seine blassen Segmente biegen sich ins Freie, die Palpen wehen in langsamen Schwingungen durch die Grenzschicht des Wassers. In der oberen rechten Bildseite landet für einen Herzschlag lang ein Copepode – sein glasklarer Panzer bricht das Reiflicht wie eine Linse –, bevor ihn der Druckgradient eines nahen Osculums wieder in die offene Wassersäule ablenkt.
















