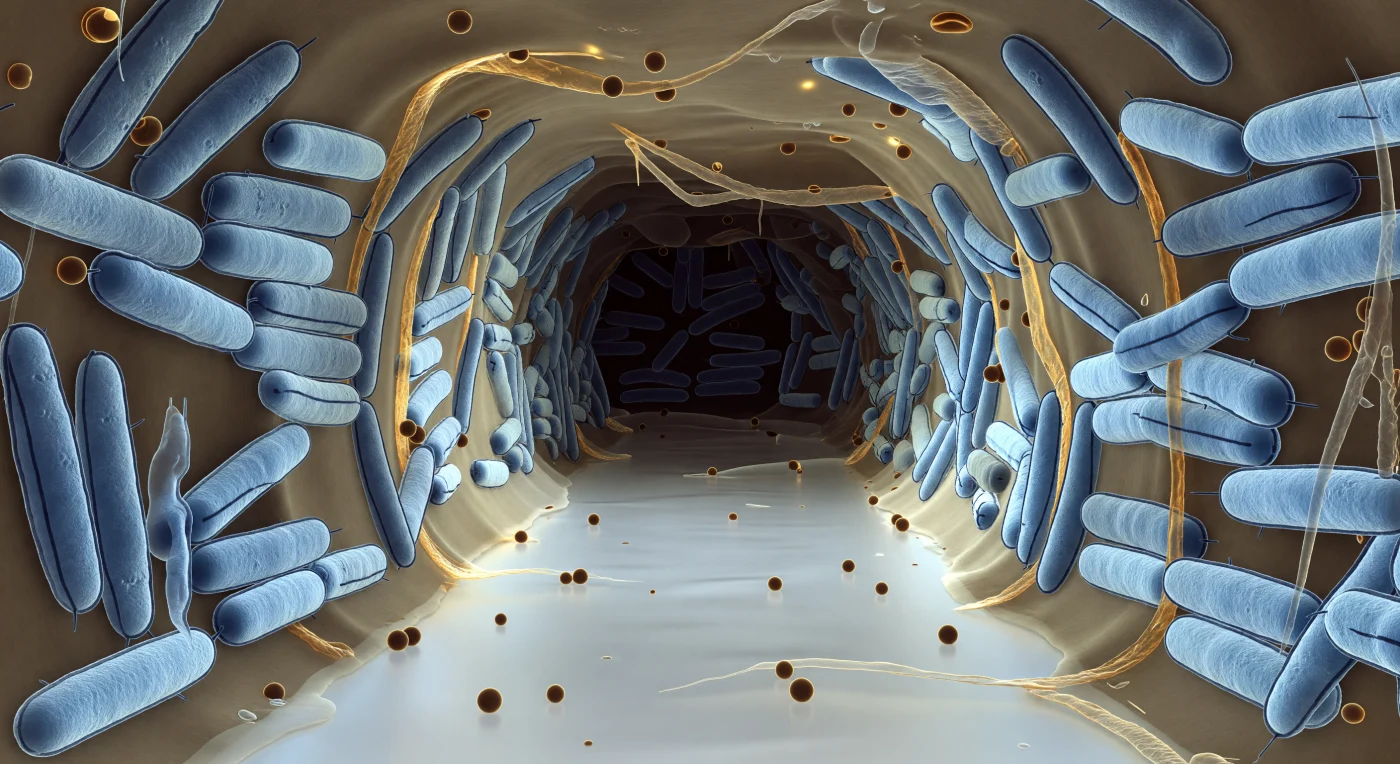
Der Blick fällt in einen lichtdurchflossenen Korridor, der sich zwischen Wänden aus dicht gepackten Bakterienstäbchen in die Tiefe erstreckt – ihre Körper in kaltem Eisblau gehalten, jeder einzelne ein stumpfzylindrischer Koloss, dessen doppelte Außenmembran als zwei haarfeine dunkle Linien entlang der Flanke verläuft, hundertfach gespiegelt bis in den blauen Dunst, wo der Kanal sich verengt und im Schatten versinkt. Das Exopolysaccharid, das diese Gemeinschaft zusammenhält, füllt jeden Zwischenraum wie erstarrter Honig, transluzent und bernsteinfarben, stellenweise zu sehnigen Bündeln gerafft und an den Kanalrändern zu einem Gossamer-Film verdünnt, dessen Oberfläche im diffusen Licht schwach irisiert. Im Fluidraum darunter treiben äußere Membranvesikel wie bernsteinfarbene Perlen – vollständig versiegelte Membranblasen, die molekulare Signale und Enzyme zwischen den Organismen transportieren, ein biochemisches Postnetz innerhalb dieser lebenden Architektur. Was hier als Stille erscheint, ist in Wirklichkeit chemische Aktivität in jedem Punkt: Sauerstoff- und Nährstoffgradienten strukturieren den gesamten Raum, der Kanal selbst ist ein funktionales Organ des Biofilms, ein Versorgungssystem, das durch kollektive biologische Intelligenz entstanden ist, ohne dass je ein Plan existiert hätte.

Im schwebenden Ausharren zwischen Molekülwelten blickt man auf eine Szenerie, die keine irdische Entsprechung kennt: Dutzende von HIV-1-Virionen treiben in der zähen Extrazellularflüssigkeit, jedes ein trüb-bläuliches Kügelchen von 120 Nanometern Durchmesser, dessen Oberfläche mit kleinen goldenen gp120-gp41-Spike-Trimeren besetzt ist – winzige Krönchen aus Glykoprotein, die im diffusen Kryo-Licht warm schimmern wie Laternen auf dunklen Bojen. Das Brownsche Zittern der Virionen ist allgegenwärtig und unaufhörlich, ein thermisches Rauschen, das jede Ruhepause verweigert, während die viskose, proteindurchsetzte Flüssigkeit jede Bewegung dämpft und verlangsamt, als befände man sich in tiefem Polarwasser. Hinter und unter einem erhebt sich die Plasmamembran des T-Lymphozyten wie eine ozeanische Steilwand – nicht flach, sondern in langen, trägen Wellen schwingende Lipiddoppelschicht, durchbrochen von CD4-Rezeptoren und einem Wald aus Glykokalyx-Filamenten, die silbrig ins Licht greifen. Die nächsten Virionen sind bereits in diese Grenzschicht aus wachsender molekularer Dichte eingetaucht, ihre goldenen Spikes auf die Andockstellen der Membran gerichtet, als folge das Geschehen nicht dem Zufall, sondern einer stummen chemischen Zwangsläufigkeit – Bindungsaffinität als Schwerkraft in einer Welt, in der Photonen bedeutungslos sind.

Der Blick richtet sich auf eine Kliffwand aus Biomembran, die sich in gewaltigen Falten über den Beobachter erhebt — die innere Mitochondrienmembran, deren osmiumgefärbte Doppelschicht in sattem Dunkelbraun leuchtet und von Tausenden ATP-Synthase-Komplexen besetzt ist, deren F₁-Köpfe wie kleine Pilzhüte in die Matrix hineinragen. Um den Betrachter herum verdichtet sich das mitochondriale Matrixmilieu zu einem honigfarbenen, quasigelartigen Kolloid — bei einer Proteinkonzentration von über 500 Milligramm pro Milliliter ist dies kein leerer Raum, sondern ein belebtes Gedränge aus TCA-Enzymen, mitochondrialen Ribosomen und superhelikalen DNA-Schleifen, die alle im unaufhörlichen Zittern der Brown'schen Bewegung schwingen. In der Ferne verengt sich die Cristae-Verbindung zu einem golden leuchtenden Engpass, dessen Wände aus dicht gepackten ATP-Synthase-Domen eine nahezu lückenlose Wölbung bilden, durch die warmes Licht fällt wie durch einen biologischen Kathedralbogen. Diese Architektur ist kein statisches Gestein: Die Membran atmet in langsamen Undulationen, hält elektrochemische Gradienten aufrecht und treibt die Synthese von ATP an — dem universellen Energieträger des Lebens — mit einer Effizienz, die keine menschliche Maschine erreicht.
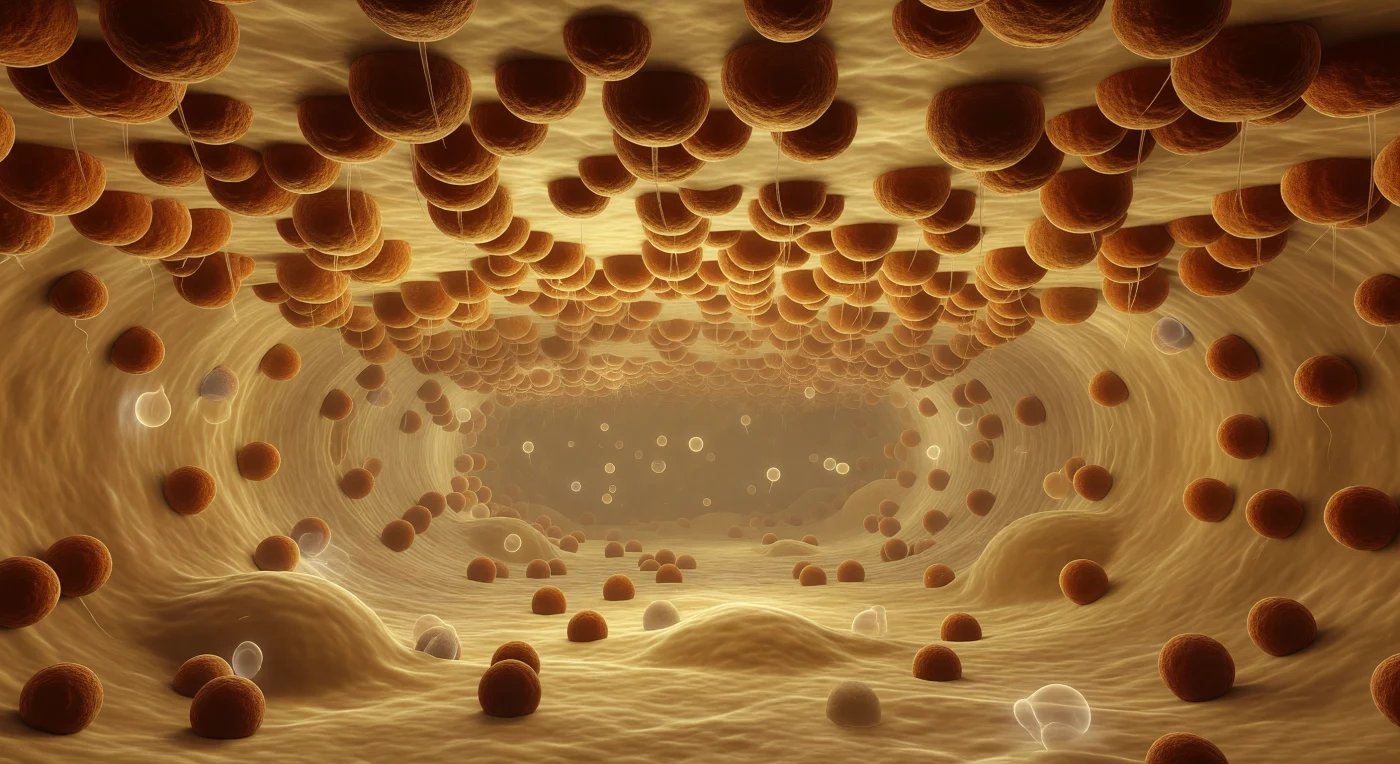
Du treibst lautlos im Lumen des rauen endoplasmatischen Retikulums, umhüllt von einem gleichmäßigen, honigfarbenen Leuchten, das von der wässrigen Umgebung selbst ausgeht — vor dir lösen sich träge treibende Proteinmoleküle wie Schleierwolken in der Tiefe des Korridors auf. Über dir erstreckt sich die Lipiddoppelschicht als endlose, sanft gewellte Decke aus cremefarbenem Ocker, vollständig bedeckt von dicht gedrängt sitzenden Ribosomen, die wie oxidiertes Eisen in Rostbraun und Umber schimmern und deren körnige Oberflächen die zusammengesetzten Natur echter molekularer Maschinerien verraten. Von jedem dieser Ribosomen hängen zarteste Fäden wachsender Polypeptidketten in den Lumenraum hinab, kaum sichtbar im diffusen Licht, bevor sie im proteindichten Dunst verschwinden — jeder dieser Fäden ist ein Protein im Entstehen, durch den Translokationskomplex hindurch in diesen Raum eingespeist. Der Korridor zieht sich in weiter Perspektive fort, begrenzt oben und unten von gleichermaßen ribosomenbedeckten Membranen, die in warmem Bernsteinlicht zu einem fernen Fluchtpunkt zusammenlaufen — eine Fabrik ohne Unterbrechung, ohne Bewusstsein, in jedem Augenblick gleichzeitig überall tätig.

Du schwebst am äußersten Vorposten einer lebenden Zelle, an der hauchfeinen Vorderkante des Lamellipodiums, wo ein dichter Dschungel aus Aktinfilamenten — jedes gerade einmal sieben Nanometer dünn — in präzisen Siebzig-Grad-Winkeln von den Arp2/3-Komplexen abzweigt und ein fraktales, korallenartiges Netzwerk aus elektrischem Blaugrün in die Dunkelheit treibt. Der evaneszente Lichtkegel der TIRF-Beleuchtung streift nur die untersten Nanometer über dem Substrat, sodass die Fokaladhäsionsplaques in warmem Bernstein-Gold aufglühen wie in kaltes Glas eingebettetes geschmolzenes Metall — jene molekularen Verankerungspunkte, an denen Integrine die Extrazellulärmatrix greifen und die gesamte Zugkraft der Zellmigration übertragen wird. Zu beiden Seiten stoßen filopodiale Spitzen wie leuchtende Antennen in den extrazellulären Raum vor, einzelne, gebündelte Aktinstränge, die tastend das unbekannte Terrain vor der vorrückenden Zelle sondieren. Das Netz hinter dir verdichtet sich zu einem ozeanischen Indigodunkel, in dem jede neue Verzweigung eine weitere erzeugt — eine lebende Architektur gerichteter Bewegung, angetrieben durch die ständige Polymerisation an den Plusenden der Filamente und den hydrostatischen Druck, den dieses Wachstum gegen die Zellmembran ausübt.

Vor Ihnen erhebt sich der Kernporenkomplex wie ein gewaltiges Stadttor aus vergoldetem Bronze: ein kreisförmiges Rosettengefüge aus acht symmetrisch angeordneten Proteinkomplexen, eingelassen in die dunkle, doppelschichtige Kernhülle, deren Membranen sich nach beiden Seiten wie antike Gewölbebögen in die Tiefe erstrecken. Die achtfache Radialsymmetrie dieses Molekülportals – kaum 120 Nanometer im Durchmesser – ist kein Zufallsprodukt, sondern das Ergebnis eines präzise assemblierten Ringsystems aus über 500 Proteinkopien, den Nukleaporinen, die gemeinsam eine hochselektive Schleuse zwischen Nukleoplasma und Zytoplasma bilden. Im Zentrum des Kanals hängen FG-Nukleaporin-Filamente wie ein halbdurchsichtiger Perlenhang in die Achse hinein – ungeordnete, phenylalanin-glycin-reiche Sequenzen, die durch transiente hydrophobe Wechselwirkungen eine gel-artige Barriere erzeugen, welche kleinen Molekülen freien Durchtritt erlaubt, während größere Frachten nur mit Hilfe von Importin- und Exportin-Rezeptoren passieren können. Zu beiden Seiten türmt sich Heterochromatin in tief indigoblauen Massen auf, seine dicht gepackten Nukleosomen lichtabsorbierend und schwer zugänglich für die Transkriptionsmaschinerie, während hinter Ihnen das lockerere Euchromatin in lavendelgrauem Dunst schwebt, durchzogen von kondensierten Tröpfchen phasenseparierter Biomoleküle. Sie treiben im Nukleoplasma wie in einem leise bebenden Ozean aus Makromolekülen, getragen von jenem allgegenwärtigen Brown'schen Rauschen, das auf dieser Skala keine Stille kennt.

Vor dir erhebt sich der Granumstapel wie ein Tempel aus Jade — fünfzehn Thylakoidmembranen, präzise übereinandergeschichtet, jede ein dicht besetztes Mosaik aus Photosystem-II- und Lichtsammelkomplexen, deren eingebettete Chlorophyllmoleküle die Membranoberflächen in ein tiefes, inhärentes Smaragdgrün tauchen. Zwischen den Membranscheiben liegen hellgelbe Lumenräume wie leuchtende Mörtelfugen, erfüllt von saurem Fluid, in dem Protonen langsam von einer Seite zur anderen diffundieren — ein unsichtbares elektrochemisches Gefälle, das die ATP-Synthese antreibt. Die Stromathylakoid-Lamellen verlassen den Stapel wie breite grüne Bänder, die sich in der Ferne zu weiteren Granumtürmen wölben und so ein zusammenhängendes Membransystem bilden, das den gesamten Innenraum des Chloroplasten vernetzt. Das Stroma selbst erscheint als opaleszentes Gel, dicht besetzt mit RuBisCO-Komplexen — den unregelmäßigen Enzymblöcken des Calvin-Zyklus — und vereinzelten bernsteinfarbenen Plastoglobuli, Lipidtröpfchen, die als Speicher für Fettsäuren und Tocopherole dienen. Das Licht hat keine einzelne Quelle: Es ist ein diffuses, allgegenwärtiges Grün, das durch Schichten von Chlorophyll gefiltert wird und die gesamte Architektur dieses photosynthetischen Kraftwerks in eine stille, lebendige Lumineszenz hüllt.
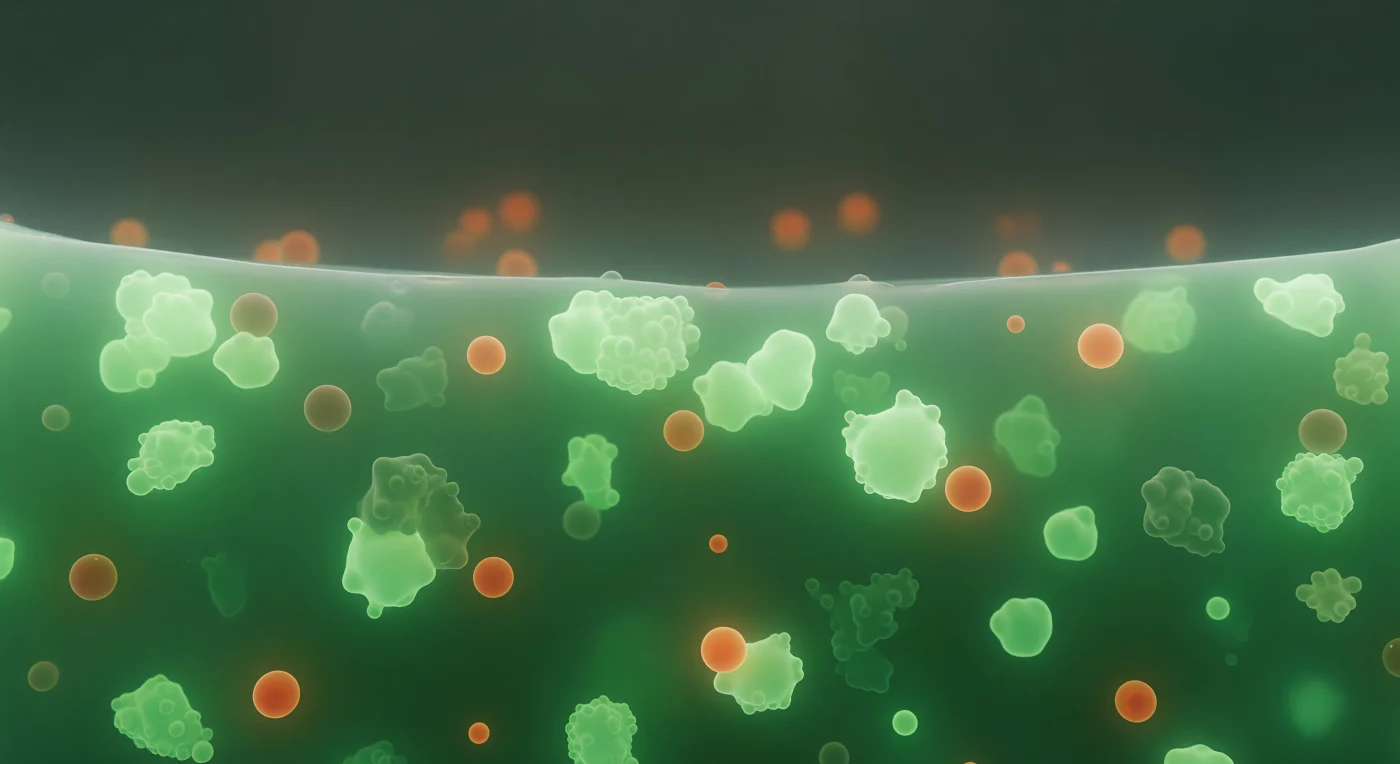
Die Welt, die dich umgibt, ist kein Raum im gewöhnlichen Sinne — sie ist ein viskoelastisches Kondensatinneres, ein membranloser Organell, der nicht durch eine Hülle, sondern allein durch Phasentrennung existiert: das spontane Entmischen zweier flüssiger Phasen, wie Öl in Wasser, aber geformt aus Tausenden verschiedener RNA-Moleküle und RNA-bindender Proteine wie G3BP1, deren kollektive Wechselwirkungen eine dichte, kohärente Materie entstehen lassen, die sich von der umgebenden Zytoplasmaflüssigkeit durch einen einzigen, scharfen Dichteabfall abgrenzt. Der grüne Schimmer, der dich von allen Seiten einhüllt — diffus, gleichmäßig, ohne erkennbare Quelle — ist die Fluoreszenz des GFP-markierten G3BP1-Proteins selbst, eines zentralen Nukleators dieser Stressgranula, die in Augenblicken zellulärer Bedrohung innerhalb von Sekunden bis Minuten assemblieren und mRNA-Moleküle aus dem Translationsapparat herausziehen, um ihre Expression zu pausieren und die Zelle zu schützen. Die wärmer leuchtenden, bernsteinfarbenen Sphären — TIA1-reiche Ko-Kondensate — sind Ausdruck einer weiteren Schichtung der Phasentrennung: innerhalb des Kondensats selbst segregieren bestimmte Proteinspezies in noch dichtere Mikrodomänen, flüssig-in-flüssig, ein Tröpfchen im Tröpfchen. Die Grenze, die du in der Ferne erkennst, wo das grüne Leuchten jäh in nahezu schwarze Leere bricht, ist keine Membran, kein Gerüst — sie ist der thermodynamische Horizont der Phasentrennung, gehalten durch Oberflächenspannung allein, zitternd, durchlässig, und doch scharf wie eine Wand zwischen zwei völlig verschiedenen Zuständen der Materie.

Du schwebst reglos über der zentralen Achse eines bakteriellen Flagellenmotors und blickst senkrecht hinab in eine der kompliziertesten molekularen Maschinen der belebten Welt: konzentrische Ringe aus Bronze und oxidiertem Gold versinken schichtweise in tiefblau schimmernde Membranen, der L-Ring in der äußeren Membran, der P-Ring eingebettet in eine bernsteinfarbene Peptidoglykanlage, der MS-Ring schließlich als skulptiertes, radial geripptes Zentrum aus gediegenem Metall. Siebzehn MotA/MotB-Statorkomplexe drängen sich in nahezu perfekter Radialsymmetrie um den Rotor, massive bleigraue Strebepfeiler, die die innere Membran stützen wie die Stützbögen einer Kathedrale ihr Mauerwerk — jeder Komplex leicht anders ausgerichtet, jede Kontaktfläche mit molekularer Präzision geschliffen. Über dir schraubt sich das Flagellenfilament in einem langen, gleichmäßigen Helix aus dem Bildfeld hinaus, sein Oberfläche von einem kalten, richtungslosen Licht gestreift, während der Haken — kurz und leicht gebogen wie eine Wellenkupplung — Rotor und Filament durch die äußere Membran hindurch verbindet. Das gesamte Ensemble vermittelt keine Starre, sondern mechanische Bereitschaft: Oberflächen, poliert durch Millionen Jahre evolutionärer Selektion, der gesamte Apparat in jedem Augenblick bereit, mit hundert bis tausend Umdrehungen pro Sekunde in der Dunkelheit des Zytoplasmas zu rotieren.

Der Blick richtet sich nach oben durch ein dichtes Gehölz aus Hunderten glatter, tiefblau-cyan schimmernder Zylinder, die wie Säulen eines lebenden Doms in die Höhe streben – es sind die Zilien des Atemwegsepithels, haarfeine Zellfortsätze von nur 200 Nanometern Durchmesser, deren inneres Stützgerüst aus neun Mikrotubulidoubletten und einem zentralen Paar das Epithel zum koordinierten Schlagen befähigt. Zwischen den nächsten Schäften hängen amber-goldene Muzinfäden in langsamen, catenoidalen Bögen – das zähe Schleimnetz des mukoziliären Apparats, das Staubpartikel, Krankheitserreger und eingeatmete Fremdkörper einfängt und durch die Wellenbewegung der Zilien lungenwärts abtransportiert. Diese metachrone Welle ist selbst im Augenblick ihres Einfrierens ablesbar: eine ganze Kolonnade lehnt sich in stummem Gleichschritt nach links, während die benachbarte Reihe bereits wieder aufrecht steht, ein in den Raum geritztes Relief aus sequenzieller Bewegung. Unten erstreckt sich die Epitheloberfläche als warme Ockerflächhe eng verzahnter Zellgrenzen, deren Tight Junctions wie gerillte Dämme aus getrocknetem Flussbett wirken und die epitheliale Barriere zwischen Außenwelt und Körpergewebe abdichten. Was hier atmet, weiß nicht, dass es atmet – und dennoch ist die gesamte Struktur auf einen einzigen Zweck hin organisiert: die unaufhörliche, koordinierte Reinigung des Atemwegs durch das stetige, lebendige Flüstern von Millionen Zilien.
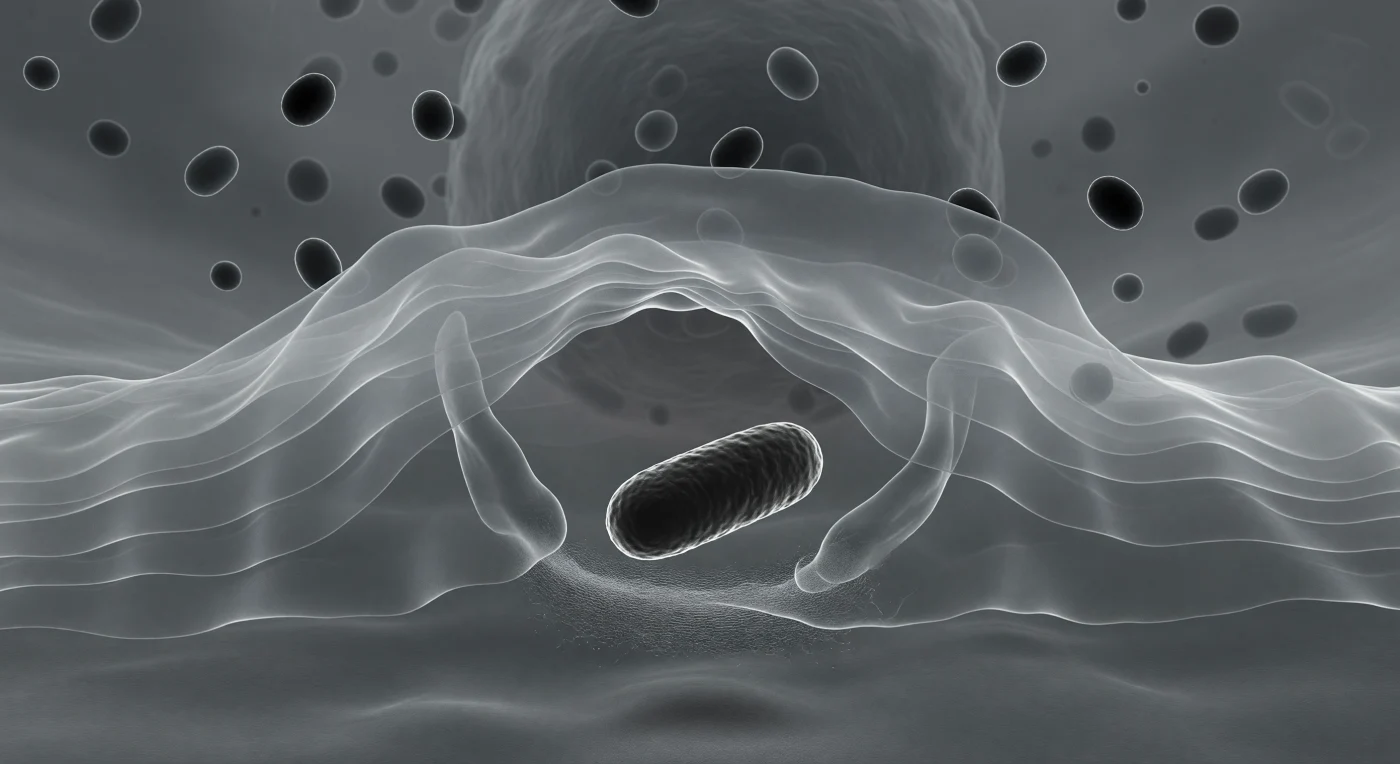
Du befindest dich an der vordersten Front eines lebendigen Einschlussvorgangs: Die lamellipodiale Membranwelle des Makrophagen wölbt sich wie ein gefriergetrockneter Brecher um einen stäbchenförmigen Bakterienkörper, dessen dichte, fast schwarze Silhouette von einem schmalen Beugungssaum umrandet wird, als trüge er seine eigene Aureole. Das transluzente Zytoplasma um dich herum ist weder Flüssigkeit noch Festkörper, sondern ein feinkörniges Aktingeflecht unter viskoelastischer Spannung — dicht genug, um Kräfte mechanisch zu übertragen, porös genug, um als lebendiger Schleier zu wirken, der sich in konzertierten Pseudopodien koordiniert vorwärts schiebt. Hinter dir, tiefer im Zellinneren, hängen lysosomale Granula wie dunkle Kieselsteine im Gel: Sie sind mit hydrolytischen Enzymen gefüllt und warten darauf, mit dem entstehenden Phagosom zu verschmelzen und den Inhalt des Bakteriums zu verdauen — ein Prozess, der in wenigen Minuten abgeschlossen sein wird. Was du erlebst, ist eine der ältesten Schutzreaktionen des Lebens: eine einzelne eukaryotische Zelle schließt sich mit architektonischer Präzision um ein Pathogen, das sie um ein Vielfaches an Komplexität überragt.

Du schwebst im Inneren einer gewaltigen goldenen Mulde — der zentralen Eindellung eines menschlichen Erythrozyten, einer bikonkaven Scheibe von etwa acht Mikrometern Durchmesser, deren Membranoberfläche sich von dir aus in alle Richtungen wie der Boden eines warmen, bernsteinfarbenen Kraters erstreckt. Unmittelbar unter dir ist das Spektrin-Zytoskelett schwach in die Membran eingewoben, ein hexagonales Netzwerk elastischer Filamente, das der Zelle ihre bemerkenswerte Verformbarkeit verleiht — jene Eigenschaft, die es dem Erythrozyten erlaubt, sich durch Kapillaren zu zwängen, die enger sind als er selbst. In der Mitte Distanz türmen sich benachbarte rote Blutkörperchen zu Rouleaux-Stapeln auf, monolithischen Säulen aus aufeinandergepressten Scheiben, entstanden durch die schwachen elektrostatischen Wechselwirkungen ihrer Oberflächen im strohgelben Plasma. Zwischen diesen Zellkolonnen treiben stachelige Thrombozyten — winzige, unregelmäßige Wächter der Gerinnung, ihre Oberfläche mit feinen Fortsätzen besetzt, die im schrägen Licht als helle Reflexionspunkte aufblitzen. Das Licht, scharf und schattenlos wie ein Elektronenstrahl, verwandelt jede biologische Oberfläche in etwas zugleich Vertrautes und Planetarisches — eine Welt aus lebendem Metall und flüssigem Bernstein, vollständig aus Membran und Plasma geformt.
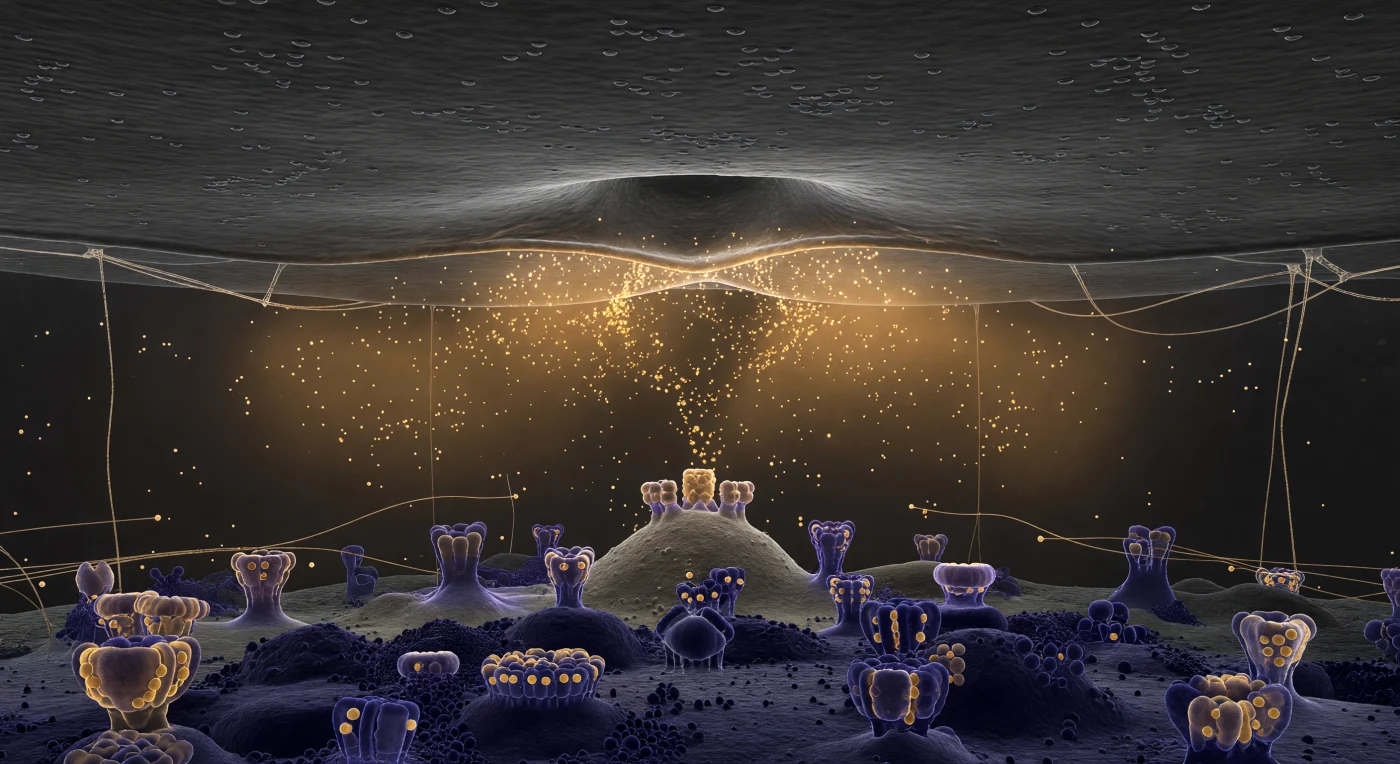
Du schwebst in einem der engsten Kommunikationsräume des Nervensystems – dem synaptischen Spalt – einem nur 25 Nanometer schmalen Korridor, in dem Decke und Boden gleichzeitig sichtbar sind, getrennt durch eine Lücke, die sich kaum weiter anfühlt als die Spannweite ausgestreckter Arme. Direkt über dir hat sich ein synaptisches Vesikel zur Fusion entschieden: Seine Membran verschmilzt mit der präsynaptischen Doppellipidschicht in einer charakteristischen Omega-Form, und aus der entstehenden Fusionspore ergießt sich ein warmer, bernsteinfarbener Nebel – Tausende von Neurotransmittermolekülen, die sich als diffuse Lichtwolke lateral durch den Spalt ausbreiten, dicker nahe der Pore und an den Rändern in Transparenz verlaufend. Zarte Fäden synaptischer Adhäsionsproteine spannen sich wie golddurchwirkte Kabel zwischen Decke und Boden und geben dem aquatischen Medium eine fast strukturelle Tiefe. Unter dir erhebt sich die postsynaptische Dichte als ein architektonisches Feld aus dunkelviolettem, elektronendichtem Gerüst, aus dem AMPA- und NMDA-Rezeptorkomplexe wie uralte Steinformationen in den Spalt ragen und den bernsteinfarbenen Transmitterstrom in einem leisen violett-goldenen Widerschein reflektieren – Bindungsstellen, bereit das chemische Signal in elektrische Aktivität zu übersetzen.
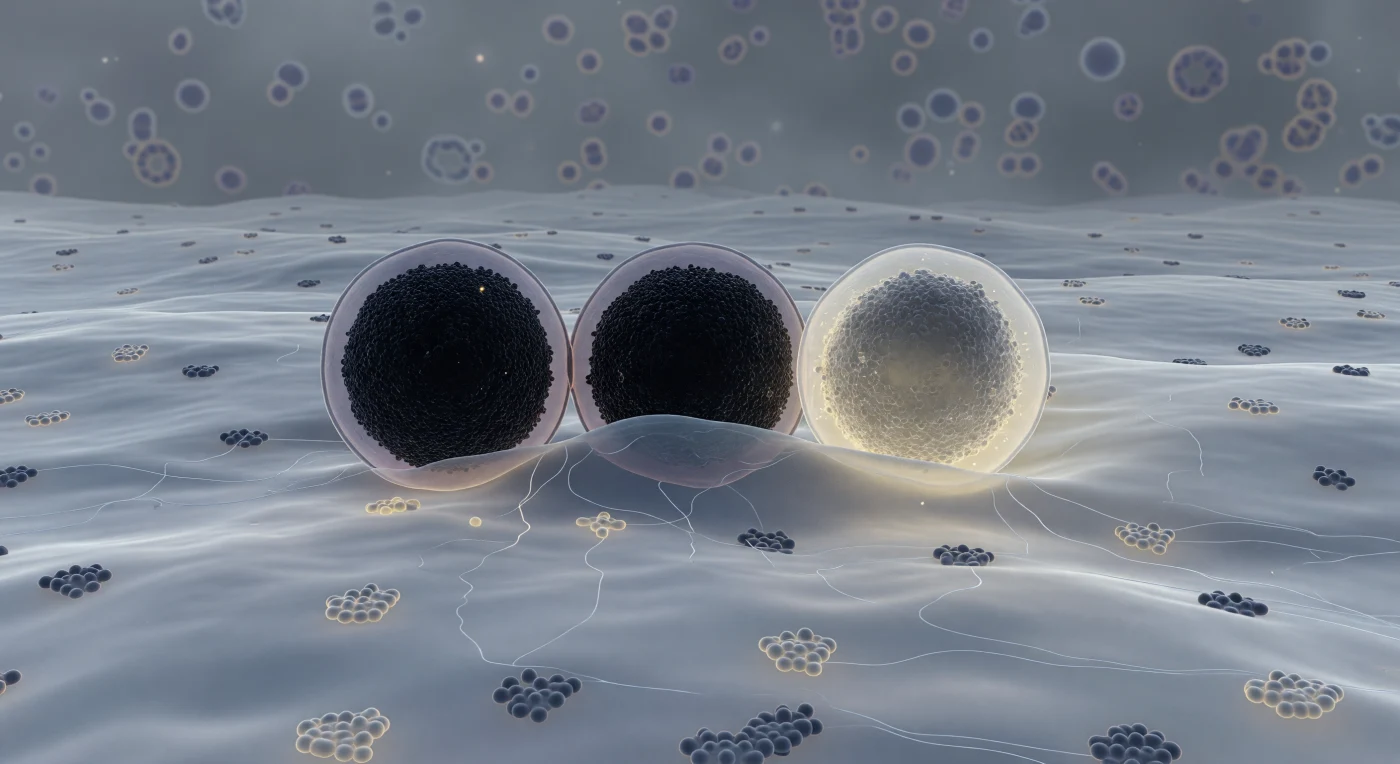
Der Blick gleitet entlang der inneren Membranfläche einer Betazelle des Pankreas, über eine sanft wogende Ebene aus blaugrauem Lipid, in die dunkle Proteinsilhouetten eingebettet sind wie Findlinge in einer stillen Landschaft – jenseits davon, hinter der Membran, öffnet sich ein schwach bernsteinfarbenes Leuchten des Interstitiums. Drei gewaltige Granula dominieren den Vordergrund: Die erste liegt dicht angedockt, ihr Kern ein nahezu opakes, schwarzes Kristallgitter aus Zink-Insulin-Hexameren, umgeben von einem schmalen Hof aus blassem Lavendel, während die beiden Membranen in einer dunklen Naht ununterscheidbar miteinander verschmelzen. Die zweite Granula hat den Punkt der Halbfusion erreicht – die Plasmamembran wölbt sich weich einwärts, ihre Lipide und jene der Granula vermengen sich in einem unbestimmten grauen Saum, der jede individuelle Identität auflöst. Ganz rechts strahlt die dritte Granula bereits in den extrazellulären Raum aus: ihr einst dichter Kern hellt sich von Dunkel zu warmem Elfenbein auf, während Zink-Insulin-Moleküle in den lichtdurchfluteten Bernsteinraum dahinter diffundieren und sich auflösen – ein thermodynamisch unumkehrbarer Moment, der trotz seiner vollkommenen Stille die Spannung eines Atemzugs trägt, der nicht mehr angehalten werden kann.

Der Blick öffnet sich über eine endlose, geometrisch präzise Ebene aus dicht gepackten Zylindern – die Spitzen der Mikrovilli einer einzelnen Darmepithelzelle, jeder Schaft nur etwa 100 Nanometer im Durchmesser, so regelmäßig angeordnet wie die Zellen eines Bienenwabenmusters, ihre actin-gestützten Wände im schräg einfallenden Licht wie gepresstes Wachs leuchtend. Über jedem Schaft erhebt sich der Glykokalyx, ein zarter Flaum unverzweigter Polysaccharidfilamente von nur wenigen Nanometern Dicke, der sich zu einem kontinuierlichen elfenbeinfarbenen Pelz vereint – jene schützende Moleküllandschaft, durch die Nährstoffe wie Glucose und Aminosäuren aktiv in die Zelle transportiert werden, gefiltert und selektiert durch membrangebundene Enzyme und Transporter. Tief zwischen den Schäften verschwinden die engen intervillösen Kanäle in einem feuchten, proteinreichen Schatten, das Cytoplasma des Enterozyten darunter nur als warmes, ockergelbes Leuchten in der Tiefe erahnbar. Was hier gefroren wirkt, ist in Wirklichkeit rastlos lebendig: Ionen driften in langsamer Brownscher Bewegung durch das flüssige Medium, Transportvesikel schnüren sich an Membranen ab, und die gesamte Oberfläche – vergrößert durch Millionen solcher Mikrovilli – verwandelt einen einzelnen Zentimeter Darm in eine absorptive Fläche von unvorstellbarer biologischer Effizienz.

Du schwebs im geometrischen Mittelpunkt einer sich teilenden Zelle, genau auf Höhe der Äquatorialplatte während der Anaphase, und die Welt um dich herum ist eine Kathedrale aus lebendigem Licht: Von zwei fernen Polen strahlen elektrisch-grüne Mikrotubuli-Bündel — markiert mit Alexa-488-konjugierten Antikörpern gegen Tubulin — wie gewaltige Leuchttürme durch die absolute Dunkelheit des Zytoplasmas auf dich zu, ihre Oberflächen schwach längsgestreift, jeder Strang ein polymerisiertes Proteinseil aus Tubulin-Dimeren, der unter mechanischer Spannung steht. Die Kinetochor-Fasern sind die dicksten und hellsten dieser Kabel: gespannt wie Bogensehnen, ziehen sie violett-blaue Chromosomenmassen unaufhaltsam poleward — kondensiertes Chromatin, das in seiner Dichte das gesamte genetische Erbe der Zelle verkörpert. Direkt auf deiner Höhe durchschneidet die Mittelkörper-Zone das Sichtfeld wie ein Balken aus weißgrünem Feuer, eine antiparallele Überlappungszone interpolar verlaufender Mikrotubuli, so dicht gepackt, dass sie alles andere überstrahlt und von einem milchigen Fluoreszenzschleier umgeben ist, der durch die extreme makromolekulare Dichte des Zytoplasmas entsteht. Die gesamte Geometrie dieser Struktur — zwei Pole, eine Äquatorialebene, Dutzende kreuzender Fasern — ist kein Zufall, sondern die präzise mechanische Architektur des mitotischen Spindelapparats, der innerhalb von Minuten die exakte Verteilung von 46 Chromosomen auf zwei Tochterzellen gewährleistet.

Vor dir erhebt sich die Glykokalyx wie ein endloser Unterwasserwald — ein dichtes Geflecht aus blau-silbern schimmernden Proteoglykan- und Glykoproteinketten, die sich zwischen einem halben und zwei Mikrometern über die kaum erkennbare Plasmamembran der Endothelzelle erheben, die selbst nur als dunkle Andeutung tief unten durchschimmert. Die einzelnen Heparansulfat-Stränge verzweigen sich wie winterliche Birkenäste, ihre Oberflächen mit Sulfatgruppen und gebundenem Wasser besetzt, lateral durch zarte Querverbindungen verknüpft, die dem gesamten Gefüge die Qualität eines gefrorenen, leuchtenden Nebels verleihen. Die Glykokalyx ist kein passives Gerüst: Sie reguliert den Zugang von Molekülen zur Endoteloberfläche, vermittelt die mechanische Signalübertragung des Blutstroms, bindet Wachstumsfaktoren und Gerinnungsmodulatoren, und schützt die Membran vor direktem Kontakt mit den zellulären Elementen des Blutes. Dein eigener Schatten — die breite, konvexe Wölbung der herannahenden Erythrozytenmembran — fällt als weiches Dunkel über den Baldachin aus Filamenten und taucht ihre Spitzen von eisblauem Glanz in Indigo, während die beleuchteten Ränder des Waldes in kaltem, ionenartigem Licht erstrahlen. Langsam, unausweichlich dringt deine gebogene Oberfläche in die äußersten Stränge ein, die sich unter dem Andruck leise verwölben — ein Kontakt, der auf molekularer Ebene über Adhäsion, Verformung und Signalweiterleitung entscheidet.
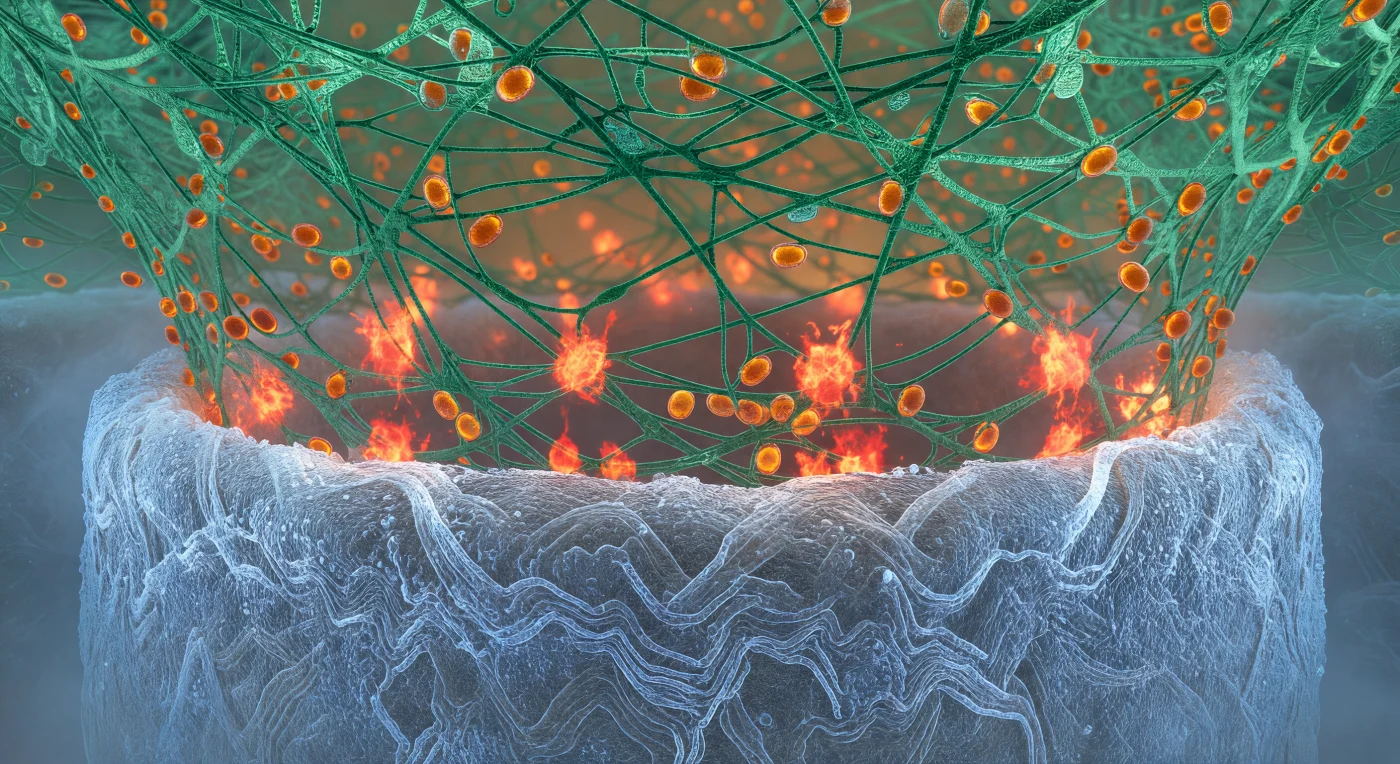
Du stehst eingeklemmt zwischen zwei biologischen Architekturen von gewaltiger Dichte – unter dir wölbt sich die Zellwand des Candida-Hyphas wie der Rumpf eines massiven Schiffes, ihre chitin-reiche Oberfläche von Calcofluor-Weißfärbung in ein kaltes, spektrales Blauweißlicht getaucht, das jeden verschlungenen Polysaccharidstrang zum Leuchten bringt wie kristallisiertes Eis unter arktischem Licht. Von oben senkt sich der Aktinkäfig des Neutrophilen herab als ein dichtes, viridiangrünes Geflecht verzweigter F-Aktin-Filamente, die den Hyphas mit der gespannten Kraft von Haltekabeln umgreifen – ein biologisches Gerüst, das im Verlauf von Sekunden reorganisiert wird, angetrieben durch die ständige Polymerisation und den Abbau einzelner Filamente. An der Kontaktzone zwischen diesen beiden Architekturen explodieren unregelmäßige Ausbrüche reaktiver Sauerstoffspezies in rotorangen Blitzen: Dies ist der oxidative Burst, bei dem NADPH-Oxidase-Komplexe in der Neutrophilenmembran Superoxid produzieren, das zu Wasserstoffperoxid und hypochloriger Säure umgewandelt wird – eine konzentrierte chemische Waffe, die auf engstem Raum gegen die Pilzzellwand entfesselt wird. Bernsteinfarbene azurophile Granula bewegen sich träge durch das grüne Aktinnetz, ihre mit Myeloperoxidase und Defensinen beladenen Membranen nähern sich der Kampfzone wie versiegelte Munitionsdepots kurz vor der Entladung. Diese Szene verkörpert die gesamte Brutalität angeborener Immunität auf einer Skala, wo Chemie unmittelbar zu Gewalt wird.
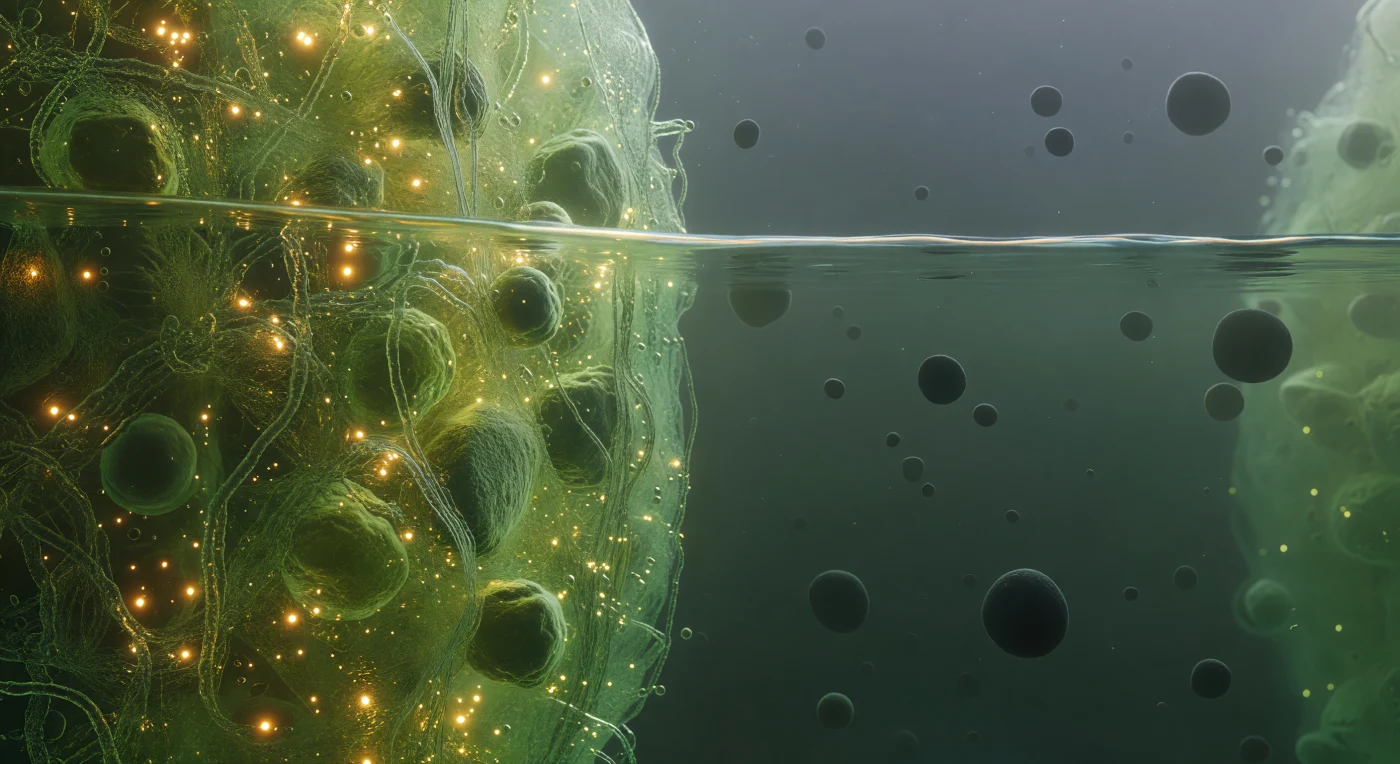
Du schwebst genau an der Grenzfläche zwischen zwei Welten: Zur linken Seite wölbt sich das dichte Innere eines Stress-Granulums als sattgrün-goldenes Leuchten, ein konzentriertes Geflecht aus entangelten mRNA-Strängen und intrinsisch ungeordneten Proteinen, deren Brownsche Bewegungen das Licht zu einem warmen, bernsteinfarbenen Flimmern verdichten. Diese biomolekulare Kondensatphase entsteht durch Flüssig-Flüssig-Phasenseparation – ein thermodynamischer Übergang, bei dem bestimmte RNA-bindende Proteine mit niederkomplexen Sequenzmotiven kollektiv aus dem Zytoplasma heraus in eine dichte, koexistierende Flüssigphase treten, gehalten durch schwache, multivalente Wechselwirkungen statt kovalenter Bindungen. Direkt vor dir zieht sich die Phasengrenze selbst als eine präzise, leicht zitternde Trennlinie durch dein Gesichtsfeld – kein sanfter Gradient, sondern eine echte thermodynamische Diskontinuität, deren Oberflächenspannung Kapillarwellen im Nanometerbereich als irisierendes Schimmern sichtbar macht, als würde Öl zögernd gegen Wasser halten. Nach rechts hin öffnet sich der relative Leerraum des verdünnten Zytoplasmas, ein kühler, blaugrüner Dunst, in dem vereinzelte Ribosomen wie dunkle, matte Felsbrocken treiben und die Entfernungen zwischen ihnen sich anfühlen wie offene Prärie nach der klaustrophobischen Dichte des Kondensats.

Du schwebst in einem feuchten, kaum messbaren Spalt zwischen zwei riesigen Zellwänden, die sich wie die Innenflächen zweier kolossaler Canyons in beide Richtungen biegen – oben öffnet sich das Tubuluslumen plötzlich als schwarze, kavernöse Leere, wie der Schlund eines Ozeangrabeneingangs, schwach erhellt von einer kalten, wässrigen Lumineszenz. Was deinen Blick sofort bindet, ist ein ununterbrochenes, glutrotes Band aus ZO-1- und Claudin-Komplexen, das die gesamte Zellperimeter wie ein in lebendes Gewebe eingeschweißter Metallreifen umschließt – die parazelluläre Barriere der Tight Junction, die verhindert, dass Ionen und Moleküle unkontrolliert zwischen Lumen und Bindegewebe diffundieren, und so die essentielle Polarität des Nierentubulus aufrechterhält. Knapp darunter leuchtet ein zweites, smaragdgrünes Band in sanfterem Licht: die Adherens Junction aus E-Cadherin-Molekülen, deren Ektodomänen über den Interzellularspalt hinweg wie ineinandergreifende Finger verwoben sind und die mechanische Kohäsion des Epithels sichern. Die lateralen Membranen beider Zellen liegen in einer Apposition von kaum 20 Nanometern, sichtbar als zwei parallel verlaufende graphitdunkle Vorhänge, während tief in den Zellkörpern gewaltige kobaltblaue Nuclei wie erleuchtete Kathedralkuppeln durch das Cytoplasma schimmern – das gesamte Bild wie ein Kirchenfenster aus lebendigem Gewebe, betrachtet von innen, aus dem Blei der Dichtungsnaht selbst.




















