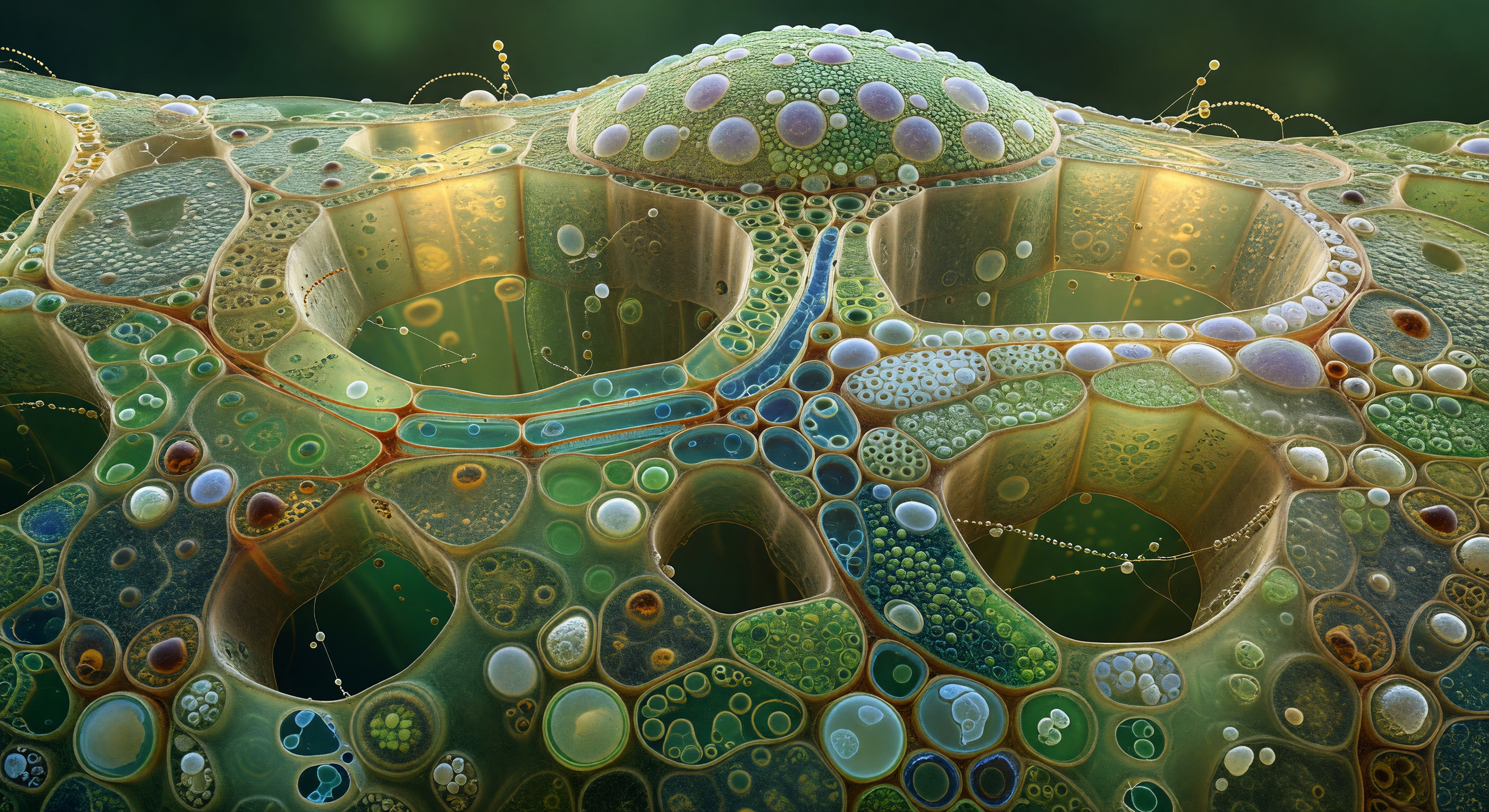
Der Blick geht tief in das Innere eines reifen Xylемgefäßes — ein zylindrischer Hohlraum von etwa 120 Mikrometern Durchmesser, dessen bernsteinfarben leuchtende Wände in obsessiver Regelmäßigkeit mit Hoftüpfeln bedeckt sind, kreisrunde Vertiefungen von rund sechs Mikrometern Breite, jede einzelne mit einem papierdünnen, schimmernden Membranhäutchen bespannt, das einst den Druckausgleich zwischen benachbarten Leitbahnen vermittelte. Diese Wände bestehen aus lignifizierter Cellulose — einem der härtesten biologischen Verbundwerkstoffe, dessen sekundäre Wandverdickungen einen olivgoldenen Schimmer über den tiefen Siennagrund legen — und der gesamte Kanal steht unter negativem hydraulischem Druck, da die Wassersäule, die er trägt, durch Kohäsion im Verbund gehalten wird und aktiv ins Kronendach gezogen wird. Das Gefäß ist vollständig leer: keine Flüssigkeit, nur Vakuum und die physikalische Spannung eines Systems, das durch Kavitation jederzeit kollabieren könnte. Am fernen Ende des Korridors versperrt eine einzige Luftembolie den Lumenquerschnitt vollständig — eine linsenförmige Quecksilberspiegelblase, deren konvexer Meniskus die gesamte Tüpfelgalerie hinter dem Betrachter verzerrt und verkleinert reflektiert, schön wie ein Riss im Kristall und ebenso unerbittlich tödlich für den Wassertransport.

Der Blick nach oben öffnet sich in ein Gewölbe aus lebendigem Glas: Säulen aus Palisadenmesophyllzellen, jede etwa siebzig Mikrometer hoch und fünfzehn breit, steigen dicht gedrängt auf wie die Türme einer versunkenen Stadt, ihre halb durchscheinenden Wände aus Zellulose und Pektin in warmem Bernsteingrün schimmernd, von innen besetzt mit hunderten bikonvexer Chloroplasten, die sich wie smaragdfarbene Kacheln aneinanderpressen und das einfallende Licht in ein kontinuierliches, kühles Jadeleuchten verwandeln. Der Boden unter den Füßen ist eine leicht gewölbte Fläche aus Plasmamembran und Zellwand, wächsern-transluzent, von Zellulosemikrofibrillen in diagonalen Mustern durchzogen wie gefrosteter Jadstein, während zwischen den Säulen schmale, fast schwarze Luftspalten sich in die unbekannte Tiefe des schwammigen Mesophylls hinein öffnen und das Gefühl endloser innerer Kavernen erzeugen. Von direkt oben strömt das Licht durch die Epidermis wie durch mattiertes Glas herab — gleichmäßig, diffus, mit einem schwachen öligen Irisieren der kutikulären Wachsschicht — und taucht das gesamte Spalier in eine Helligkeit ohne harte Schatten, in der nur die allmähliche Verdunkelung zwischen den Stämmen verrät, wie dicht und tief diese Architektur wirklich ist. Hier, wo jede Zellwand als feuchter, biolumineszenter Stab wirkt und jedes Chloroplast seinen Beitrag zur Photosynthese in einem kollektiven chemischen Schweigen leistet, ist Materie zur funktionalen Kathedrale geworden.
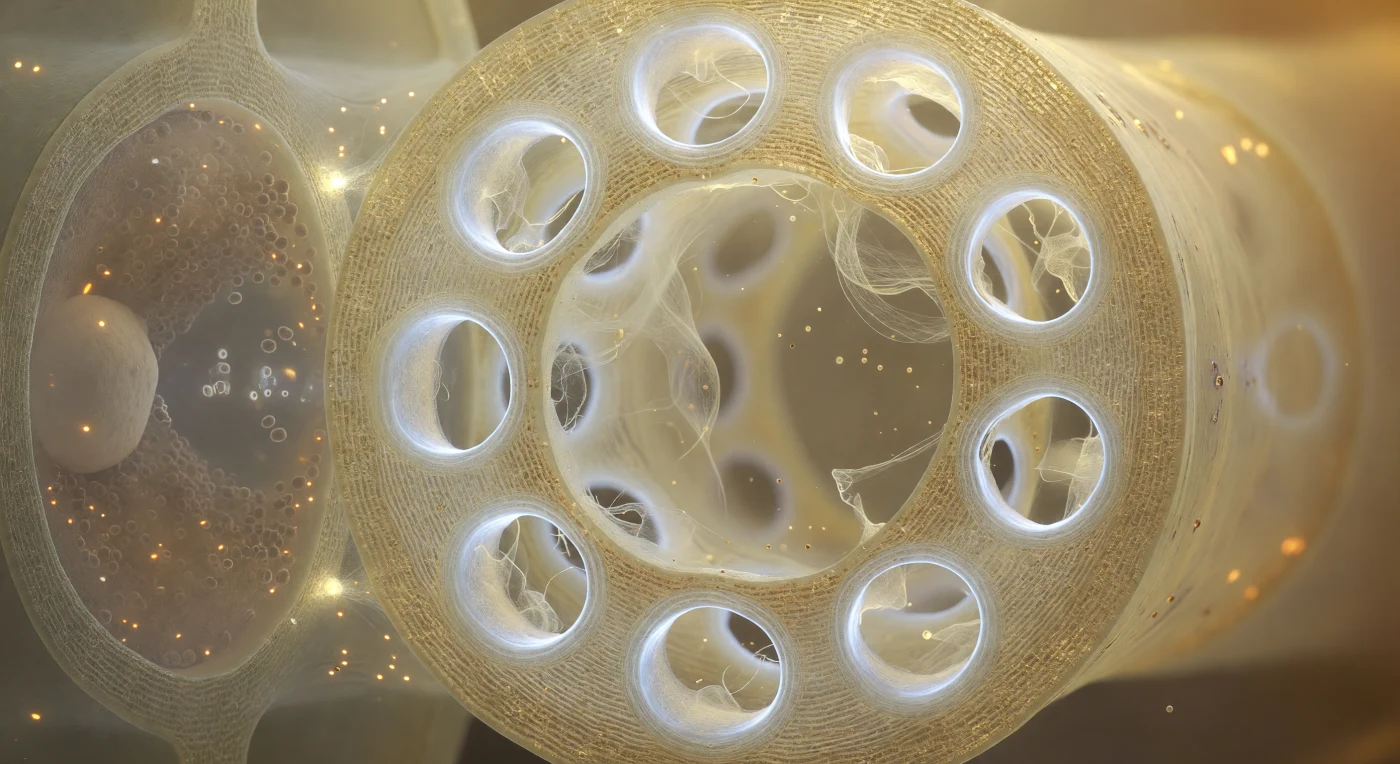
Aus dem Inneren des lebenden Siebröhrengliedes blickt man auf eine Querwand, die das gesamte Gesichtsfeld ausfüllt wie das Rosettenfenster einer Kathedrale — eine dreimicrometer starke Scheidewand aus Cellulose, golden-transparent wie gealterte Bernstein, durchbrochen von zwölf kreisrunden Poren, jede umfasst von einem milchweiß leuchtenden Callosekragen aus dicht gestapelten Biopolymerlamellen, die das Licht des Lumens zerstreuen und kühle, leicht bläuliche Höfe um jede Öffnung zeichnen. Durch diese zwölf Portale treiben P-Protein-Filamente als durchscheinende, cremefarbene Schleier, kaum breiter als ein Bruchteil eines Mikrometers, sanft hin und her schwingend im nahezu unsichtbaren Strom des Phloemsafts, der mit einer Geschwindigkeit von rund einem Meter pro Stunde durch das kolloidale System transportiert — ein Massenfluss, der durch osmotische Druckdifferenzen zwischen Quellorgan und Verbrauchsgewebe angetrieben wird. Links, hinter der dünnen gemeinsamen Lateralwand, drückt sich die Begleitzelle wie ein dunkles, organellengesättigtes Nebenzimmer heran: ihr Zytoplasma fast undurchdringlich von Mitochondrien, Ribosomen und endoplasmatischem Retikulum, ihr blasser Zellkern wie ein Flussstein in braungrauer Dichte, mit dem Siebröhrenglied durch zahlreiche Plasmodesmata verbunden, jene winzigen Lichtpünktchen in der Trennwand, über die Proteine, ATP und Signalmoleküle ausgetauscht werden und ohne die das kernlose Siebröhrenglied nicht funktionsfähig wäre.
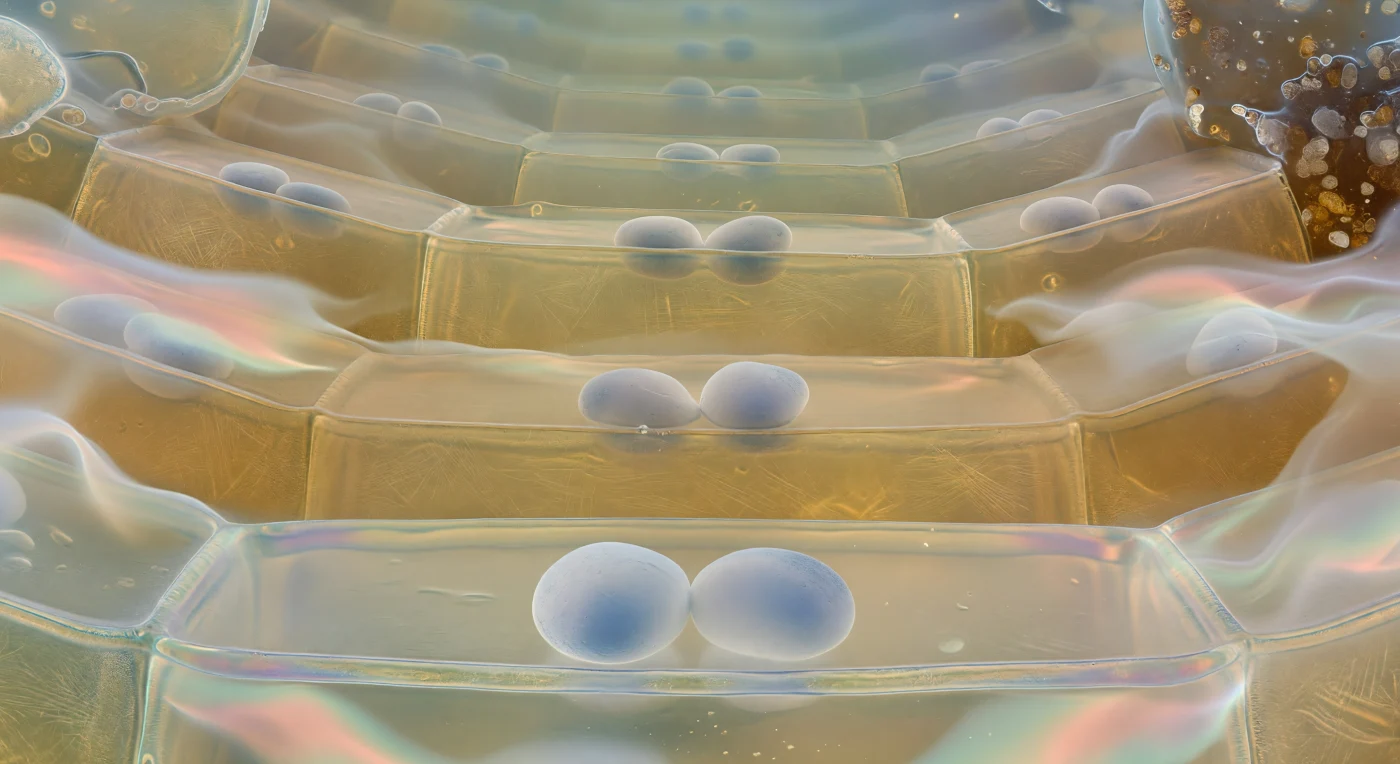
Du schwebst knapp über dem Boden einer Columella-Zelle und blickst durch eine lebende Kathedrale aus bernsteinfarbenem Glas nach oben: Zwei oder drei Amyloplasten-Statolithen liegen direkt vor dir auf der unteren Plasmamembran – dichte, leicht durchscheinende Ovale von der Größe massiver Felsbrocken, ihre Oberflächen kreideweiss und matt, an den Kanten ins Blaugraue schimmernd, wo das Licht hindurchsickert. Die Statolithen sind Stärkekörner innerhalb spezialisierter Plastiden, die als Schwerkraftsensoren fungieren: Wenn die Wurzel kippt, gleiten sie innerhalb von Minuten auf den neuen Zellboden und aktivieren über Mechanosensoren in der Membran die asymmetrische Auxinverteilung, die das Gravitropismus-Wachstum der Wurzel steuert. Über dir wiederholt sich das Muster tier um tier, jede Zellreihe etwas kleiner und schwächer beleuchtet, die Wände aus übereinandergeschichteten Cellulosemikrofibrillen wie rückbeleuchteter Alabaster glühend, bis die obersten Schichten in einem kühlen blaugrünen Dämmerlicht verblassen – das meristematische Gewebe, aus dem diese gesamte Architektur hervorging. Am Rand lösen sich die äussersten Randzellen auf und entlassen Wellen von Schleim ins Extrazellularraum: ein schillerndes Hydrogel-Geflecht aus Polysacchariden, das mineralische Bodenpartikel bindet, Bodenmikroben rekrutiert und den Wurzelvorschub durch den Boden schützend begleitet, während das Licht darin in gespenstischen Spektralbändern aus Lachsrosa und blassem Aquamarin gebrochen wird.

Ein Kalziumoxalat-Druse-Kristall von etwa 55 Mikrometern Durchmesser beherrscht das gesamte Blickfeld — ein mineralisierter Stern mit vierzig einzelnen Facetten, die von einem gemeinsamen Kern radial ausgreifen wie die Speichen eines gotischen Rosettenglases, jede Fläche ein eigenständiges Prisma aus doppelbrechendem Material, das unter gekreuzten Polarisatoren in sattem Kobaltblau, verbranntem Ocker und reinem Gold aufleuchtet, während die umgebende Vakuole im absoluten Schwarz verschwindet. An jedem Grat, wo zwei Facetten aufeinandertreffen, überlagern sich konstruktive Interferenzen zu fast inkandeszentem Licht — ein Effekt, der aus winzigen Wachstumsstufen auf den Kristalloberflächen entsteht, denn Kalziumoxalat scheidet sich nicht gleichmäßig ab, sondern lagert sich in kristallographisch erzwungenen Schichten aus übersättigter Ionenlösung ab. Diese Druse ist kein zufälliges Gebilde, sondern ein metabolisches Abfallprodukt der Pflanze — überschüssige Kalziumionen werden im wässrigen Milieu der Parenchymvakuole mit Oxalat gebunden und als unlösliches Mineral immobilisiert, eine biomineralisierte Gefahrenabwehr, die Herbivoren abschreckt und den Ionenhaushalt reguliert. Am äußersten Rand des Sichtfelds rahmt die Zellwand das Geschehen als zarter Goldstreifen — Beweis, dass diese kristalline Kathedrale vollständig in einer einzigen lebenden Zelle eingeschlossen ist, die unsichtbare Vakuolenflüssigkeit still nach außen drückend.

Von einem Schwebepunkt unmittelbar über dem Scheitel blickt man auf eine sanft gewölbte Kuppel hinab, deren Oberfläche in einem nahezu makellos gleichmäßigen Sechseckraster aus isodiametrischen Zellen gegliedert ist — jede einzelne Zelle kaum zwölf Mikrometer breit, ihre zarten cellulosischen Primärwände zu einem mintfarbenen Elfenbeingitter verbunden, das das diffuse Licht von innen heraus streut wie mattiertes Glas. Im Zentrum jedes Feldes zeichnet sich ein dunkler, ovaler Zellkern ab, dicht und kaum vakuolisiert, eingebettet in ein ribosomenreiches Cytoplasma, das dem Innern der Zelle eine körnige, fastneblige Textur verleiht — denn dies ist das Sprossapikalmeristem, jene pluripotente Keimzone, aus der alle oberirdischen Organe der Pflanze hervorgehen, und die hier freiliegenden Zellen befinden sich in einem Zustand kontinuierlicher mitotischer Bereitschaft. An den Flanken erheben sich zwei Blattprimordien wie goldene Hügelrücken aus dem Plateau des Doms, ihre Zellen bereits in eine gerichtete Elongation übergehend, die Wände wärmer und dicker als das mintfarbene Zentrum, die Grenze zwischen meristematischer und differenzierender Zone über einen nur wenige Zellen breiten Übergangsbereich ausgehandelt. Die gesamte Szene misst kaum einen Wimpernschlag im Durchmesser und bleibt dem bloßen Auge vollständig verborgen, eingeschlossen in der Knospe unter Schuppenblättern — und dennoch trägt diese winzige Kuppel die Bauanleitung für Stängel, Blätter und Blüten, die erst Monate später sichtbar werden.

Der Blick öffnet sich senkrecht nach oben aus dem substomatären Hohlraum heraus, durch eine Architektur, die trotz ihrer Winzigkeit den Eindruck eines gotischen Portals erzeugt: zwei nierenförmige Schließzellen wölben sich wie Gewölbeschlussstein über einem gerade einmal sieben Mikrometer breiten Spalt, durch den das kaltblaue Licht der Außenatmosphäre herabfällt und die Dunkelheit des offenen Porus mit scharfem Kontrast durchschneidet. Jede Schließzelle ist von einem elektrischen Grün erfüllt, das von zwölf Chloroplasten ausgeht, die sich schultergedrängt entlang der verdickten Innenwand reihen und deren Membranstapel das einfallende Licht in eine nahezu eigenständige Lumineszenz verwandeln. Die cuticulären Lippen überragen den Porenrand wie glasige Gesimse, deren wachsartige Substanz das Licht in einen irisierenden Saum aus Gold und blassem Violett bricht – ein optisches Phänomen, das an der Grenze zwischen Materie und Molekulardimension entsteht. Die umgebenden Epidermiszellen wirken dagegen farblos und leer, weitgehend vakuolisierte Fensterscheiben, die das turgeszente Leuchten der Schließzellen noch schärfer hervortreten lassen; sie sind die mechanische Konsequenz eines osmotischen Druckgefälles, das die asymmetrisch verdickten Cellulosemikrofibrillen der Innenwände zwingt, die Öffnung aufzusperren statt sie zusammenbrechen zu lassen. Tiefer im substomatären Hohlraum verlieren sich die unregelmäßigen Lappen des Schwammparenchyms in einem diffusen biologischen Dunst, ihre feuchten Oberflächen von kondensierten Wasserfilmen überzogen, die das Restlicht zu einem glühenden, grünen Nebel zerstreuen.

Du stehst im Inneren der Pflanze selbst – nicht im Holz, nicht in der Rinde, sondern in der hauchdünnen Schicht dazwischen, dort wo das Kambium als kaum wahrnehmbare Membran zwischen zwei sich verfestigenden Welten gespannt ist. Die spindelförmigen Initialzellen um dich herum dehnen sich wie die Schiffe einer Kathedrale aus, ihre Wände so zart wie nasses Seidenpapier, ihr Cytoplasma ein gleichmäßiges Strohgelb, das dich in sanftes Licht taucht; der opaleszente Zellkern der nächsten Zelle hängt wie ein leicht abgeflachter Mond in diesem bernsteinfarbenen Dunst, das Chromatin darin wie Rauch in Harz. Links beginnt das Xylemund seine frisch abgetrennten Tracheiden legen bereits Schicht für Schicht sekundäre Wandmaterialien ab – konzentrische Ringe aus Lignin in Ocker und Rostbraun, die das Licht als stumpfes Messingleuchten zurückwerfen, während die lebenden Innenräume sich in präzise konstruierte hohle Rohre verwandeln, die in bräunlichem Schatten verschwinden. Rechts löst sich die Welt auf: Die Siebelemente des Phloems vollziehen ihre eigentümliche freiwillige Auflösung – Zellkerne verschwinden oder hinterlassen nur gespenstische Schleier, Callose umkränzt die sich öffnenden Siebplattenporen als opaleszente Ringe, und das gesamte Gewebe nimmt eine diffuse, kühle Helligkeit an, als würde es sich der Durchlässigkeit hingeben. Das Kambium selbst, diese beinahe transparente Schicht zwischen Versteinerung und Verflüssigung, ist der stillste Ort im ganzen Organismus – unter ungeheurem osmotischem Druck zusammengepresst und dennoch unerschöpflich generativ, ein Frühlingstakt, der sich mit jedem Teilungsimpuls wiederholt.

Vor dir erhebt sich das Sekretionshaupt eines drüsigen Trichoms der Tomate: vier flach-kuppelförmige Zellen, deren blassgrünes, organellenreiches Cytoplasma sich wie Daumenabdrücke gegen die innere Cuticula-Fläche presst, bilden eine niedrige Krone über einem sechsstufigen Zellstiel, dessen pektinverstärkte Querwände wie dunkle Nähte eines architektonisch präzisen Turms wirken. Über diesen Zellen wölbt sich die Cuticula zu einer gespannten, bernsteinfarbenen Blase auf — ein akkumuliertes Reservoir ätherischer Öle, dessen Oberfläche schräg einfallendes Licht in einem flüssig wirkenden Glanzstreifen entlang ihres Äquators bricht und in dessen Innerem feine Dichtegradient-Schlieren unterschiedliche Terpenoide verraten, die unter wachsender Spannung auf die Grenze zwischen Einschluss und Freisetzung zudrängen. Die umgebende Blattepidermis erstreckt sich wie eine tektonische Ebene in alle Richtungen: die charakteristisch mäandernden antiklinalen Wände der Dicotyledonen-Epidermiszellen bilden ein sanft gepolstertes Relief aus ineinandergreifenden Territorien, über dem sich stäbchen- und plattenförmige Wachskristalle — kaum höher als ein Bakterium — als harte Schattenlinien in das rakenartige Streiflicht einschreiben und die mattbläulich schimmernde Cuticularoberfläche so gedämpft erscheinen lassen, dass die leuchtende Ölblase darüber wie der einzige Himmelskörper in einer wächsernen, grün gefilterten Landschaft brennt.

Der Blick führt tief in einen lebenden Korridor aus gestapelten Zellen, die sich in einer sanft leuchtenden blau-weißen Unendlichkeit verlieren – jede einzelne Zelle ragt rund 250 Mikrometer in die Höhe und ist bis auf einen hauchdünnen zytoplasmatischen Saum vollständig von einer riesigen, wasserklaren Vakuole ausgefüllt, die neunzig Prozent des Zellvolumens einnimmt und unter gewaltiger Turgorspannung steht. Die Zellwände aus laminierten Cellulosemikrofibrillen übertragen das einfallende Licht wie mattiertes Meeresglas, während das lebende Zytoplasma als blassgrüner Film an den Wandinnenflächen klebt – nur gelegentlich verdickt, wo Plasmodesmata die Membranen durchbohren oder ein Mitochondrium wie eine Perle im Netz hängt. Ein einzelner Zellkern, kaum zehn Mikrometer im Durchmesser, treibt wie eine bernsteinfarbene Laterne in diesem Randbereich und macht durch seine winzige Gestalt erst spürbar, wie ungeheuerlich groß der leere, druckgetränkte Raum um ihn herum tatsächlich ist. In der Tiefe des Korridors – Dutzende Zellen weit entfernt – zeichnet sich das zentrale Leitbündel als dunkelindigo-farbene Achssäule ab, deren verholzte Protoxylemwände das Licht schlucken statt es weiterzugeben, ein stiller Orientierungspunkt inmitten der transluzenten Aquarellarchitektur des Streckungsgewebes. Diese Zone ist der Ort, an dem Wasser und Turgor gemeinsam Wachstum erzwingen: Die Vakuolen nehmen Wasser osmotisch auf, dehnen die Zellwände irreversibel aus und treiben den Wurzelspitzenschub voran, ein hydraulischer Mechanismus von stiller, unablässiger Präzision.

Der Blick geht von außen nach innen durch die Außenhaut des Baumes, und was sich entfaltet, ist eine Architektur aus toten Kammern: Korkzellen mit mahagonibraunen, suberingetränkten Wandlamellen, die sich ohne Zwischenraum aneinanderreihen wie Quader in einem Festungsmauerwerk, ihre Lumina vollkommen leer, versiegelt auf allen sechs Flächen, jede Kammer ein lichtloser Hohlraum, der nie wieder Cytoplasma oder Organellen beherbergen wird. Das Suberin selbst scheint zu leuchten, warm wie Cognac im Kerzenlicht, und die Wände steigen mehrfach höher auf, als die eigene Position suggeriert — die Korkzellen sind Räume, keine Zellen, und ihre radialen Kolonnen ziehen sich bis zu einem Horizont, der sich unmerklich krümmt. Dann bricht die Geometrie: Wo die amber-farbenen Reihen enden, erscheint das Phellogen als ein einziger transluzenter Streifen lebender Zellen, dünnwandig und bläulich-grün schimmernd wie nasses Reispapier, ein biologischer Übergang von absolutem Tod zu aktivem Stoffwechsel, der die Erschütterung durch seinen Kontrast allein erzeugt. Seitlich löst sich die Ordnung in einem Lentizellenkanal auf, wo unvollständig suberinisierte Füllzellen lose gepackt sind, ihre Wandfragmente Licht in Gold und Creme brechen und zwischen sich offene Passagen lassen, durch die der Baum tatsächlich atmet — ein kontrollierter Riss in der Festung, nicht Schwäche, sondern Funktion.

Du schwebt im Inneren eines grünen Kathedralen-Tunnels — dem Aerenchym-Luftkanal eines Seerosen-Blattstiels, dessen Wandung aus dicht verschränkten, chloroplastengefüllten Parenchymzellen ein smaragdgrünes Mosaik aus sechseckigen Kammern bildet, jede einzelne rund 200 Mikrometer breit, ihre gemeinsamen Zellwände hauchdünn und bernsteinfarben verstärkt an den Kanten. Direkt vor dir schwebt ein Diaphragma wie eine leuchtende Spitzenscheibe quer über den gesamten Kanalquerschnitt: sternförmig angeordnete, armähnliche Zellen strahlen von einem Zentrum aus nach außen, ihre abgerundeten Spitzen reichen fast — aber nicht ganz — bis zur Kanalwand und lassen polygonale Lücken offen, weit genug, um hindurchzugleiten. Das von hinten einfallende Licht, gestreutes Chlorophyll-Eigenleuchtend oder feuchtigkeitsdiffuses Tageslicht, verwandelt das Diaphragma in ein glühendes, goldgrün gesäumtes Silhouetten-Geflecht von betörender Feinheit. Dünne irisisierende Wasserfilme spannen sich über manche der offenen Polygone und werfen zitternde Regenbogenreflexe — Violett und Kupfer — auf die grünen Zellwände rundum. Tief in beide Richtungen löst sich der Kanal im organischen Dunst auf, seine Wände verblassend von Smaragd zu einem fernen Blaugrün, als blickte man durch feuchten Nebel in ein unendliches, lebendes Rohr.
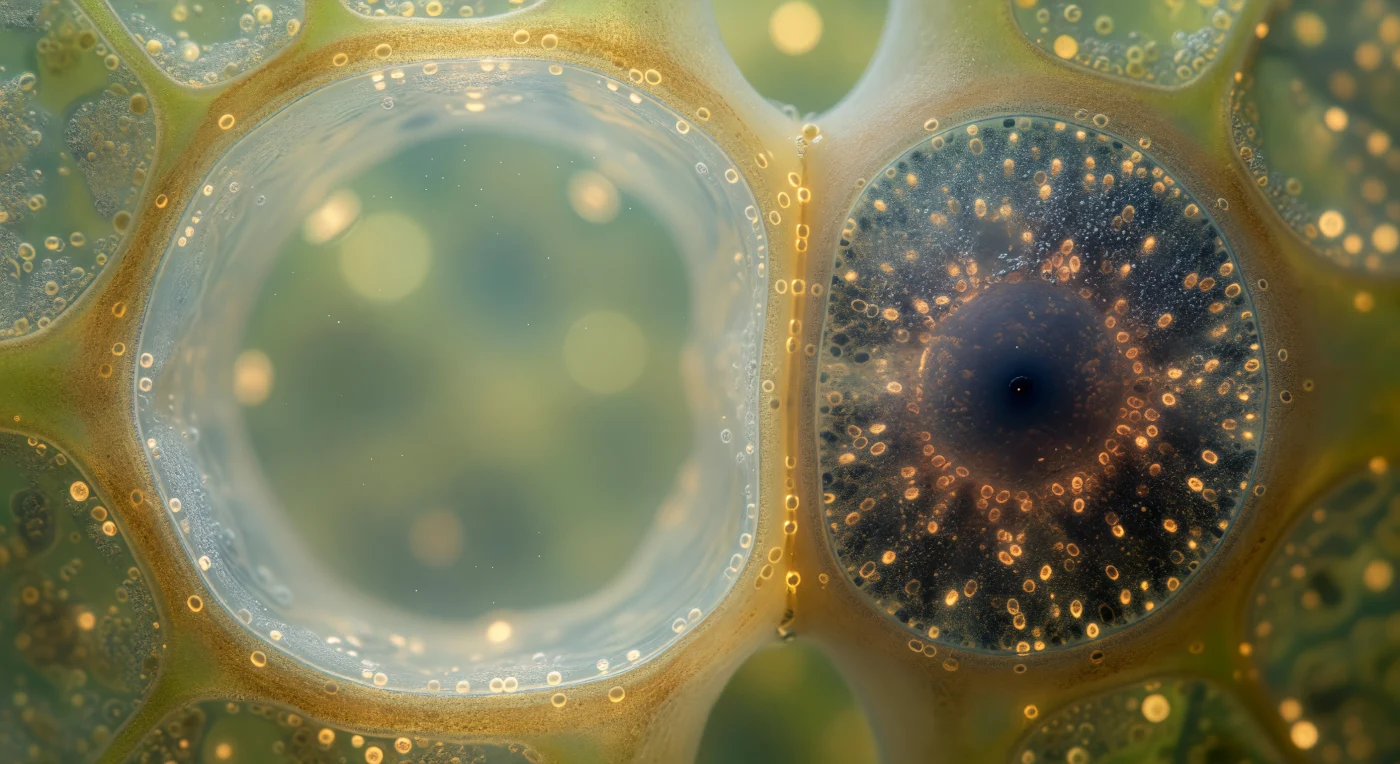
Zwei Welten berühren sich hier an einer einzigen gemeinsamen Wand: links die Siebröhrenzelle, deren Inneres sich wie ein stiller, bernsteingetönter Kathedralenraum ausdehnt — fast leer, mit einer kaum sichtbaren Schicht lebenden Cytoplasmas an der Innenwand, während ein unsichtbarer Strom gelöster Zucker durch das wässrige Lumen fließt. Rechts dagegen drängt sich die Geleitzelle in einem Viertel des Raumes zusammen und ist dabei vollständig ausgefüllt mit einer nahezu undurchdringlichen Dunkelheit aus Mitochondrien, Ribosomen und einem runden, herrschaftlichen Kern — ein biologischer Hochofen, der die Energie liefert, ohne die der Ferntransport im Phloem unmöglich wäre. Diese funktionale Abhängigkeit ist kein Zufall: Siebröhrenzellen verlieren im Laufe ihrer Reife Kern und die meisten Organellen und überlassen ihren Geleitzellen, mit denen sie genetisch identisch sind, die gesamte Stoffwechselverantwortung. Die gemeinsame Wand zwischen beiden ist durchzogen von spezialisierten Plasmodesmen — feine, goldene Perforation im Querschnitt, jede ein molekularer Korridor, durch den ATP, Proteine und regulatorische Signale fließen und die scheinbar so gegensätzlichen Kammern zu einem einzigen, unteilbaren physiologischen System verbinden.

Der Blick entlang der Endodermiszellreihe offenbart eine präzise biologische Grenzarchitektur: prismatische Zellen, jede etwa 30 Mikrometer breit, schließen sich zu einer lückenlosen Ringstruktur zusammen, deren Radiärwände von einem ununterbrochenen Casparyschen Streifen durchzogen werden — einem Gürtel aus Suberin und Lignin, der unter Fluoreszenzanregung in tiefem Bernstein-Orange leuchtet wie erhitztes Metall in einer lebenden Naht. Diese chemische Barriere ist kein bloßes Strukturelement, sondern ein molekulares Kontrollventil: Sie zwingt alle Ionen und Wassermoleküle, die vom Cortex in den Zentralzylinder gelangen wollen, durch das selektiv permeable Cytoplasma der Endodermiszellen selbst — der apoplastische Weg ist hier vollständig versperrt. Hinter dem Betrachter öffnet sich der Cortex in eine lockere, kühl-blaue Parenchymlandschaft mit weiten Interzellularräumen, während sich vor ihm die dicht gepackten Procambialzellen des Steles in komprimiertem Violett-Indigo zusammendrängen. Der leuchtende Streifen hält beide Welten auseinander — still, geometrisch exakt und absolut in seiner Funktion — ein ringförmiges Feuer, das das Innenleben der Wurzel regiert.

Die Welt, die sich vor dir erstreckt, ist aus einem einzigen Material gebaut: Sporopollenin, einem der widerstandsfähigsten organischen Polymere, das die Natur kennt, hier zum netzartigen Exinen-Relief eines Rosenpollenkorns geformt, dessen Grate sich in unregelmäßigen Sechsecken von je etwa 2,5 Mikrometern Breite über die gesamte Oberfläche erstrecken. Die Lumina zwischen den Graten sind keine bloßen Vertiefungen, sondern echte architektonische Kammern, 1,5 Mikrometer tief, ihre Böden in warmem Bernstein versinkend, während das schräg einfallende Licht die Kammern in Schichten aus Ocker und Schatten taucht und die Autofluoreszenz des Sporopollenins wie eine in das Material eingeschlossene goldene Nachmittagswärme nach außen dringt. Quer durch die Landschaft bricht der Colpus auf — eine der drei länglichen Keimöffnungen des Pollenkorns, wo die Exine sich verdünnt, nahezu transparent wird und die Grate in ein flaches, helles Tal auslaufen, das der gesamten Sphäre ihre tricolpate Symmetrie verleiht und zugleich die Zone markiert, durch die der Pollenschlauch beim Keimen austreten wird. Was aus der Ferne wie eine schlichte geometrische Ornamentik wirken mag, ist in Wahrheit das Ergebnis eines physikalisch-chemischen Selbstorganisationsprozesses während der Pollenentwicklung: Die Tapetumzellen des Pollensacks lagern Sporopollenin-Vorstufen nach einem durch den Primexine-Template vorgegebenen Muster ab, sodass jede dieser scheinbar geologischen Unregelmäßigkeiten biologische Notwendigkeit widerspiegelt.
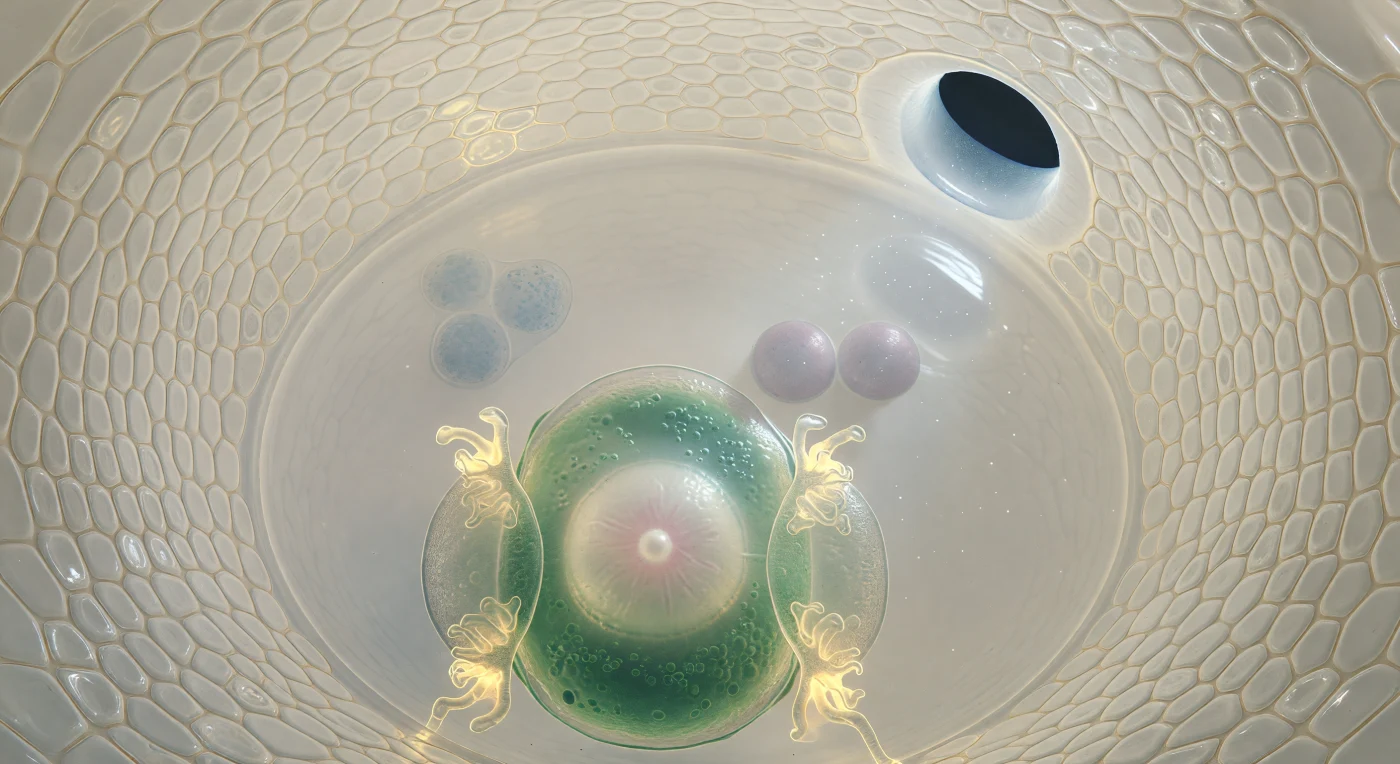
Man befindet sich im Inneren eines Samens-in-Werden – schwebend an der Schwelle der Embryosack-Kammer, umgeben von den geschwungenen Wandungen zweier Integumentschichten, die sich wie die gewölbten Mauern einer lebenden Kathedrale um das Blickfeld schließen und in ihrem cremefarbenen, von innen heraus leuchtenden Gewebe die Grenzen zwischen Zellen als zarte Bernsteinlinien erkennen lassen. Rechts oben öffnet sich die Mikropyle als dunkle Ellipse von kaum fünfzehn Mikrometern Durchmesser, durch die ein kühles Außenlicht in einem einzigen weichen Strahl einfällt und im apoplastischen Fluid schwebende Partikel erfasst. Im Vordergrund dominiert die birnförmige Eizelle mit ihrem alabasterweißen, von einer zarten Doppelmembran umschlossenen Kern, flankiert von den beiden Synergiden, deren feine fadenförmige Wandeinstülpungen an den mikropylaren Spitzen in warmem Bernsteingelb glühen – hochspezialisierte Strukturen, die den späteren Pollenschlauch empfangen und leiten werden. Dahinter öffnet sich die zentrale Zelle in ein kristallklares, nahezu transparentes Cytoplasma, in dessen Mitte zwei fliedergraue Polkerne wie gespiegelte Monde schweben und nach der Befruchtung zu einem triploiden Endospermnukleus verschmelzen werden, während am fernen Chalazapol drei Antipodenzellen als blaugraue Schatten kaum noch erkennbar in der Tiefe des Sacks verblassen.

Gewaltsam an einer unsichtbaren Schwelle schwebend, blickt man gleichzeitig in zwei gegenläufige Architekturen, die aus demselben Holz geschnitzt scheinen und doch grundverschieden sind: links weiten sich die Frühholzgefäße zu dunklen, hohlen Röhren von 250 Mikrometer Durchmesser, monumentale Leitbahnen, die während der Wachstumssaison den Wasserfluss von der Wurzel in die Blattspreite gewährleisteten und deren lignifizierte Wandungen unter polarisiertem Licht wie bernsteingetöntes Glas schimmern. An der unvermittelten Grenze bricht diese offene Welt jäh ab, und das Spätholz zur Rechten ist nahezu massives Gewebe: dickwandige Libriformfasern, deren enge Lumina von nur 15 Mikrometern kaum als Spalten erkennbar sind, speichern in ihren kristallin geordneten Cellulosemikrofibrillen mechanische Energie und leuchten unter dem Analysator in elektrischem Kobaltblau und gediegenem Gold — lebendige Interferenzfarben, die die helikale Feinstruktur der Sekundärwand verraten. Horizontal durch beide Welten ziehen sich die Holzstrahlbänder wie geologische Schichten aus honiggolden schimmernden, abgestorbenen Parenchymzellen, die einstmals Reservestoffe radial transportierten und die strikte saisonale Grenze zwischen Früh- und Spätholz unbeirrt überschreiten. Was man hier sieht, ist das eingefrorene Gedächtnis eines einzigen Jahres im Leben einer Eiche — eine organische Chronik, in der Frühlingsdrang und Sommerhärte in unmittelbarer Nachbarschaft verewigt sind.
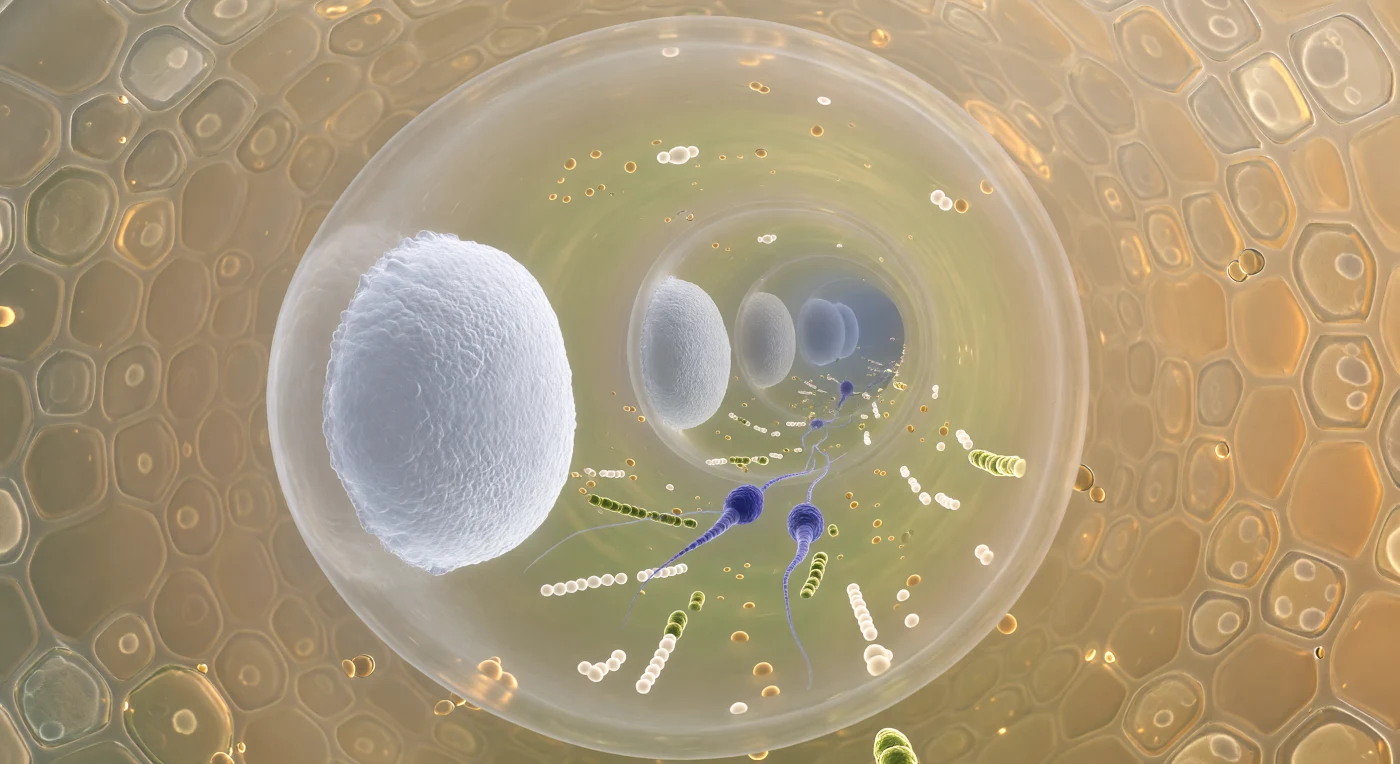
In diesem Moment befindest du dich im Innern eines lebenden Pollenschlauchs, einem biologischen Kanal von kaum zwölf Mikrometern Durchmesser, dessen celluloseverstärkte Wandung – bernsteinfarben getönt und mit Callose durchsetzt – dich wie ein makelloses Glasrohr umschließt. In regelmäßigen Abständen versperren kompakte Callose-Bulkheads den Blick nach vorne: porzellanweiß leuchtende Querwände, deren Oberfläche leicht konvex auf uns zugewölbt ist und deren dichte Polysaccharidfasern ins Blauliche changieren, während jede weitere Scheidewand dahinter blasser und blauversetzter erscheint – eine rückwärts convergierende Kolonnade aus Licht. Zwischen den nächsten beiden Septen strömt das Cytoplasma in aufgestauter Bewegung: Lipidtröpfchen, gelbgrün schimmernde Mitochondrien und Vesikelbündel drängen sich axial voran, und mittendrin treiben zwei indigo-violett gefärbte Spermazellen – fusiform, fünf Mikrometer lang, ihr Chromatin nahezu opak verdichtet – lautlos mit dem gerichteten Cytoplasmafluss in Richtung Eizelle. Die Außenwand des Schlauchs liegt dem leitenden Griffelgewebe unmittelbar an: durch die transparente Wandung sind polyedrische Sekretionszellen sichtbar, honigfarben, randunscharf durch ihre polysaccharidreiche extrazelluläre Matrix, die das gesamte Bild in ein warmes, von außen eindringendes Bernsteinlicht taucht und die weißen Callose-Septen wie schwebende Laternen erscheinen lässt.