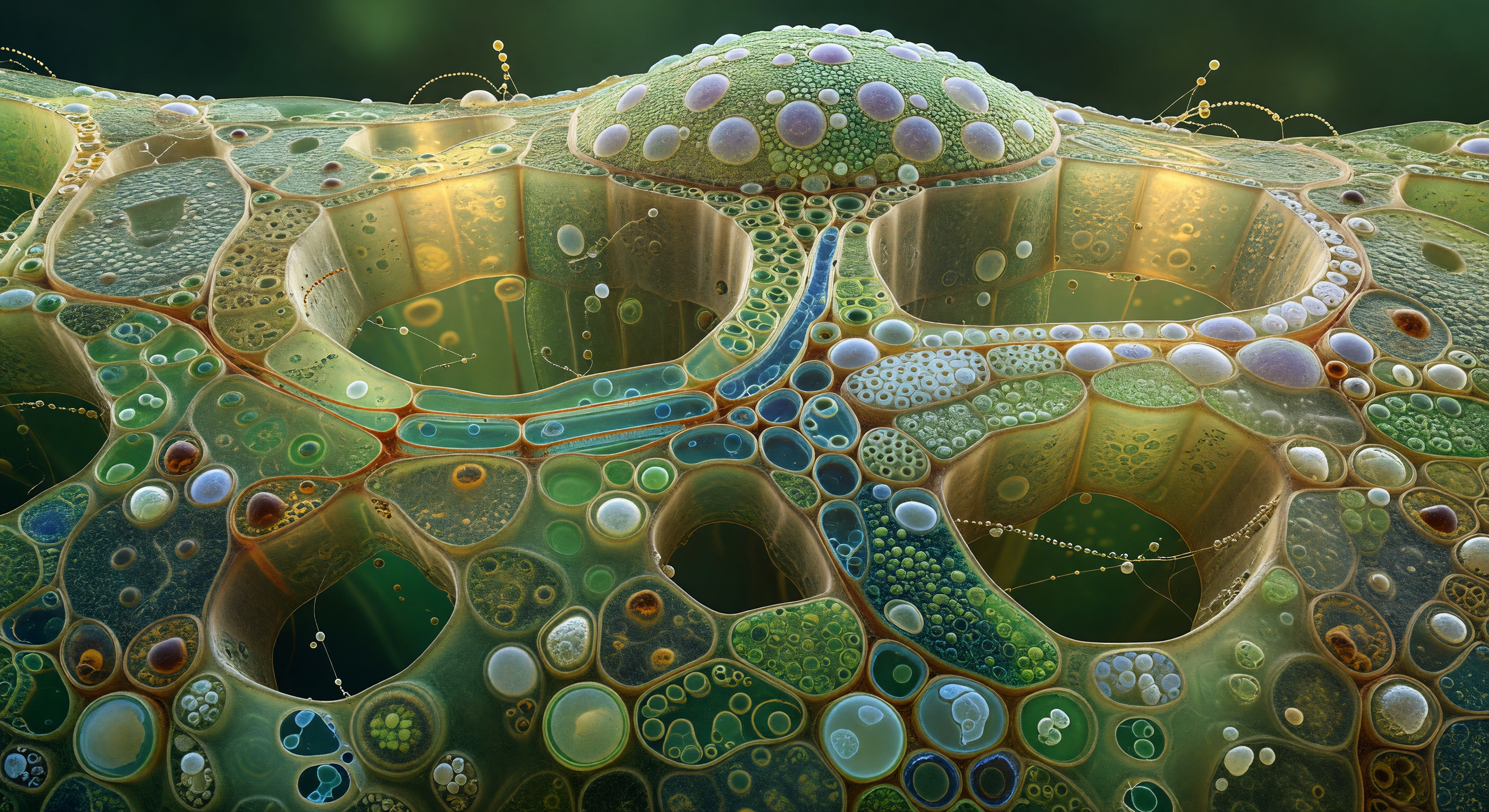
Ci si trova all'interno di un corridoio vuoto di luce ambrata fossile — il lume di un vaso xilematico maturo di angiosperma, le cui pareti lignificate rivestite di centinaia di punteggiature areolate si dispongono in file sfalsate con una regolarità quasi minerale, ogni depressione circolare di sei micrometri orlata da un labbro annulare di cellulosa che cattura il bagliore diffuso emanato dalla parete stessa, come se la rete polimerica di lignina fosse debolmente fosforescente. Al centro di ciascuna apertura si tende una membrana traslucida, sottilissima e leggermente iridescente, residuo della tornitura primaria che un tempo mediava il passaggio dell'acqua tra vasi adiacenti sotto differenziali di pressione capaci di strappare le molecole d'acqua le une dalle altre. Il vaso è completamente vuoto, percorso da una tensione idraulica negativa — non c'è liquido qui, solo la sensazione tattile del vuoto, di un tubo che trattiene l'aria fuori per coesione di una colonna d'acqua che si trova altrove, in salita verso la luce della chioma. All'estremità lontana del corridoio occupa l'intera sezione un'embolia gassosa, una bolla a specchio di mercurio dalla superficie meniscale perfettamente convessa, che riflette in miniatura distorta l'intera galleria di punteggiature alle spalle dell'osservatore — un occhio d'argento nella gola del condotto, immobile, letale per il trasporto dell'acqua, bello come una crepa nel cristallo.

In piedi sul pavimento di membrana plasmatica che riveste il fondo della foglia, levando lo sguardo ci si trova immersi in una foresta di colonne cilindriche di settanta micrometri d'altezza, le cui pareti ambra-verdastre brillano di migliaia di cloroplasti biconvessi disposti come tessere di mosaico vivente — verde cupo al centro, lime acceso ai margini, con le bande dei grana tilacoidi visibili come striature più scure quando la luce li sfiora di taglio. La luce scende dall'alto in modo diffuso e quasi perfettamente uniforme, filtrata dall'epidermide superiore come attraverso vetro smerigliato, trasformando quel soffitto lontano settanta micrometri in una volta iridescente color avorio che suddivide il cielo in poligoni irregolari tracciati dalle pareti anticlinali delle cellule epidermiche. Tra colonna e colonna si aprono crepacci verticali quasi neri — gli spazi intercellulari del mesofillo a palizzata — che suggeriscono caverne laterali che si prolungano verso il mesofillo spugnoso, conferendo alla scena la strana geometria di un canyon costruito interamente di lenti verdi. Ogni superficie è avvolta da un film acquoso sottilissimo che cattura la luce come un velo umido lucente, e dove due cloroplasti si affacciano sul vuoto attraverso uno spazio intercellulare i loro bordi brillano come tubi al neon contro il buio assoluto. È una cattedrale fotosintetica che converte luce in chimica in ogni direzione simultaneamente, struttura e pigmento fusi in un'architettura che non ha equivalenti nel mondo visibile a occhio nudo.
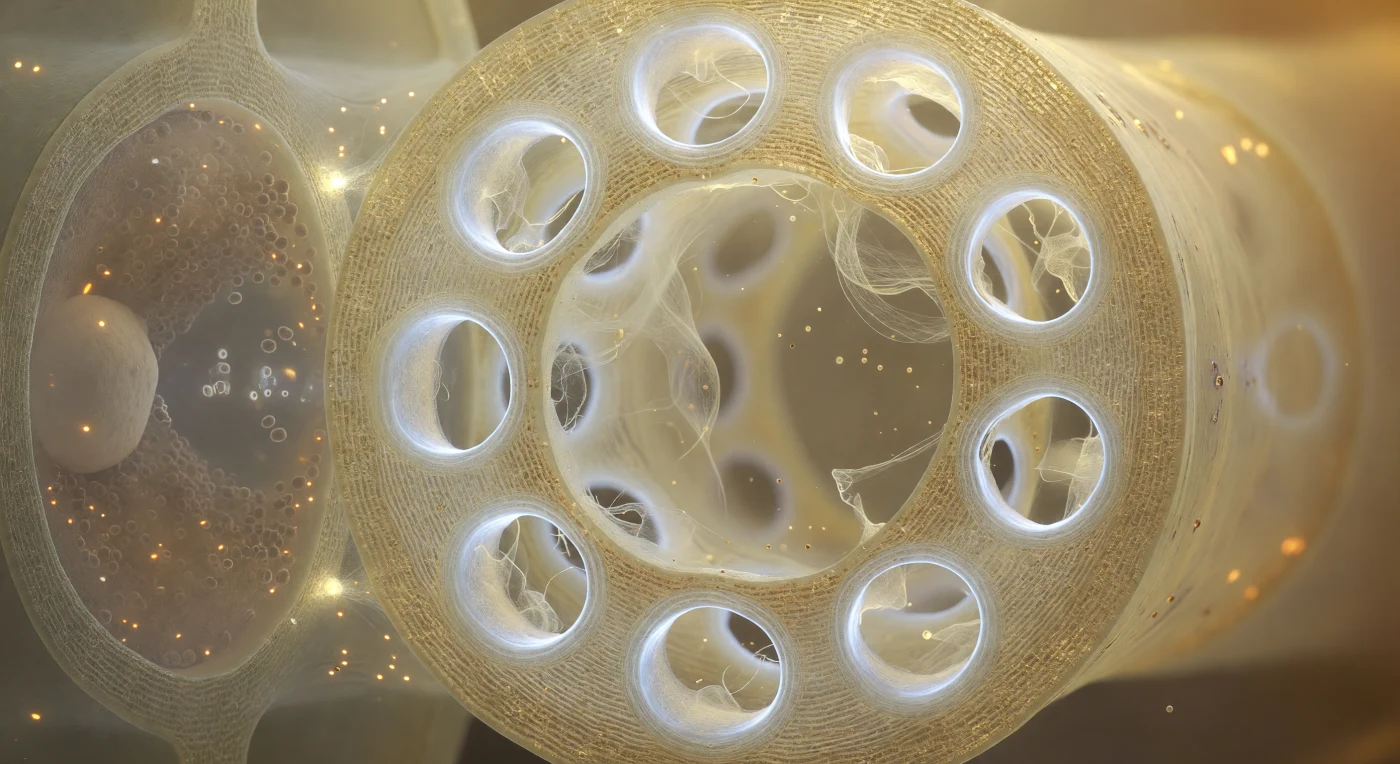
Ci si trova all'interno di un elemento cribroso del floema, sospesi nello spazio cavo del lume come se ci si fosse rimpiccioliti all'interno di una cella vivente: davanti a noi, la parete terminale cribrosa si erge come un antico trittico di cattedrale, tre micrometri di spessore, la sua matrice di cellulosa traslucida come ambra invecchiata, attraversata da dodici pori disposti in una costellazione irregolare, ciascuno orlato da un collare anulare di callosio che irradia una luminescenza biancastra e leggermente bluastra, dove il biopolimero compresso in lamelle concentriche restringe ogni apertura fino a un terzo del suo diametro originale. Attraverso questi portali luminosi, filamenti di proteina P derivano come un reticolo diafano color crema, oscillando impercettibilmente nella corrente quasi invisibile della linfa floematica che pulsa da una camera all'altra, portando saccarosi disciolti e segnali molecolari verso organi lontani — un flusso che percorre circa un metro all'ora su distanze di decimetri o metri. Alla sinistra, attraverso la sottile parete laterale condivisa, la cellula compagna si addensa in una massa quasi opaca: un nucleo pallido come pietra fluviale, mitocondri distribuiti come braci arancioni, un citoplasma granulare e pesante attraversato da connessioni plasmodesmali appena risolte come minuscole perforazioni luminose, cellule metabolicamente iperattive che nutrono e controllano l'elemento cribroso privo di nucleo accanto ad esse. Tutta l'architettura rivela l'essenza del trasporto a pressione osmotica: il caldo ambrato del lume ricco di soluti contro il bianco freddo del callosio che regola ogni flusso, la densità biologica opprimente della cellula compagna a contatto con il vuoto luminoso del tubo cribroso, in un'intimità strutturale che millenni di evoluzione vegetale hanno affinato fino alla precisione del nanometro.
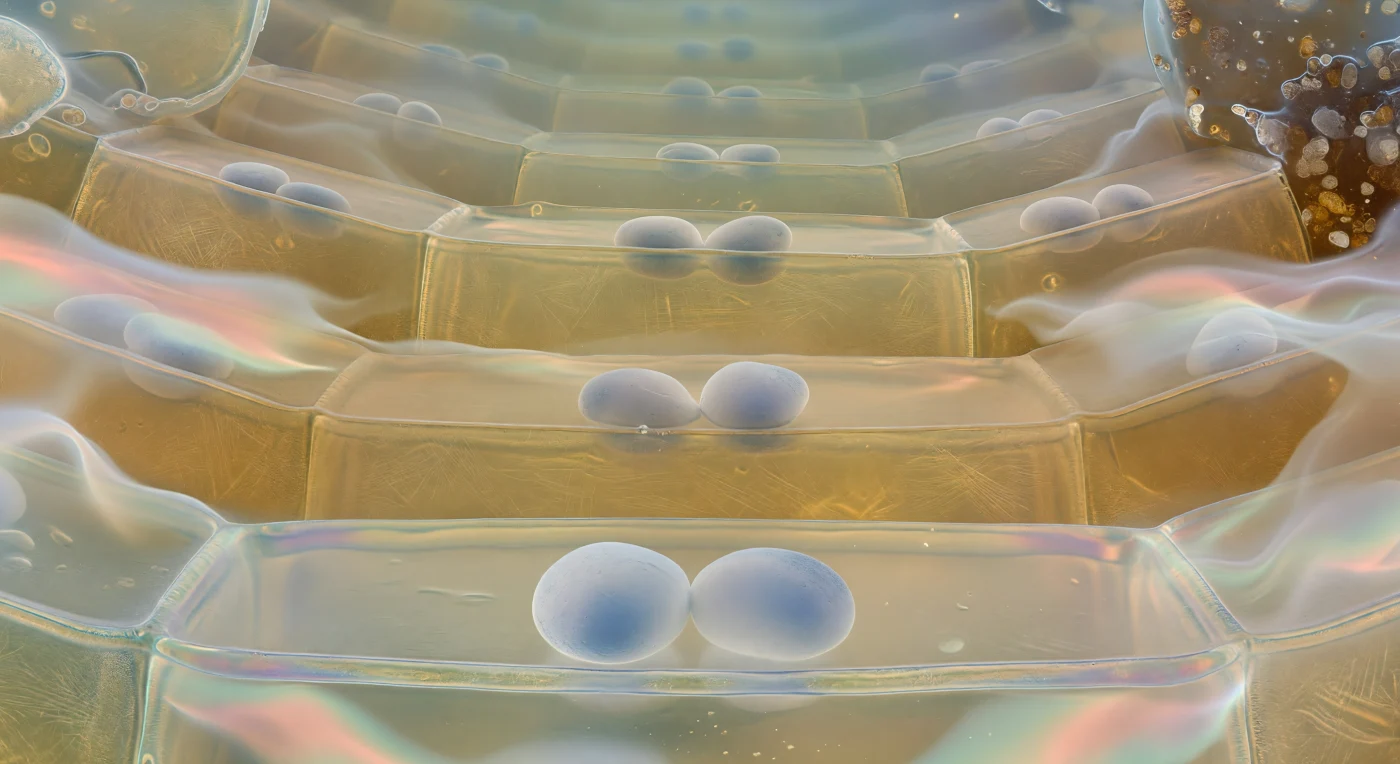
Sospesi appena sopra il pavimento di una cellula della columella, lo sguardo risale verso l'alto attraverso una cattedrale di architettura vivente: i volumi traslucidi si ripetono di livello in livello, pareti di vetro ambrato cosparse di fibre di cellulosa che brillano come alabastro retroilluminato, e i soffitti semitrasparenti lasciano intravedere i propri statocisti come crescenti biancastri immersi in una nebbia dorata. In primo piano, due o tre amiloplasti-statocisti riposano immobili sulla membrana plasmatica inferiore come massi di calcite bianco-grigiastra depositati su una membrana di tamburo iridescente, la loro densità sufficiente a rilevare la direzione della gravità attraverso la semplice forza del loro peso — meccanismo elementare e potentissimo con cui la radice orienta la propria crescita verso il basso. Il citoplasma che li circonda è quasi otticamente puro, appena velato di un calore dorato dove la luce diffusa lo attraversa di sbieco, mentre alle periferie della columella le cellule di confine si sfaldano progressivamente nell'idrogel di mucillagine extracellulare, generando un alone biochimico refrattivo che cattura filamenti spettrali color salmone e acquamarina come olio su acqua ferma. Oltre questa frontiera luminescente, le particelle di quarzo e argilla del suolo premono da ogni lato, le loro superfici bagnate di mucillagine lucida — il mondo esterno, compresso e buio, a pochi micron da questo palazzo di cellule vive che lo respinge con la propria biochimica trasparente.

Nella penombra assoluta creata dai polarizzatori incrociati, il cristallo di ossalato di calcio si erge come una cattedrale minerale di circa cinquantacinque micrometri, i suoi quaranta faccetti irradiati a stella da un nucleo centrale che brucia in colori d'interferenza saturi — blu cobalto intenso lungo le facce più ampie, ambra bruciata e oro puro sulle creste dove due faccetti si incontrano e l'interferenza costruttiva quasi incandesca. Ogni faccetto è un prisma birifrangente distinto, le sue superfici segnate da terrazze di crescita cristallograficamente inevitabili che modulano ulteriormente la luce polarizzata in sottili bande cromatiche invisibili a qualsiasi altra scala. Questo oggetto non respira, non si muove, non metabolizza — è un registro mineralizzato di eventi di saturazione ionica, precipitato lentamente all'interno di un vacuolo di cellula parenchimatica vivente quando la concentrazione di ioni calcio e ossalato ha superato il limite di solubilità, e il parete cellulare di cellulosa che lo circonda, appena percettibile come un tenue bordo oro ai margini del campo visivo, ricorda che questa intera struttura esiste sigillata all'interno di un organismo vegetale. Nient'altro esiste nel campo visivo tranne il cristallo stesso: il mezzo acquoso del vacuolo è annientato nel nero perfetto, ogni fotone in questo ambiente proviene dalla sorgente polarizzata sottostante e genera colore solo dove incontra la materia birifrangente del minerale, trasformando la biologia in spettacolo ottico puro.

Sospesi a poche decine di micrometri sopra la cupola del meristema apicale caulinare, lo sguardo spazia su una superficie quasi piatta ma percettibilmente convessa, rivestita da un mosaico esagonale di cellule isodiametriche del diametro di circa dodici micrometri, i cui sottili setti di parete cellulosica primaria disegnano una griglia color avorio-menta traslucida, simile a un pannello di lanterne interne che diffondono luce da ogni faccia. Al centro di ogni cella brilla, come un ciottolo scuro pressato contro il vetro smerigliato, un nucleo ovale denso e ricco di cromatina — segno inconfondibile di cellule giovani, quasi prive di vacuoli, intasate di ribosomi e macchinario mitotico pronto a entrare in funzione. Ai due lati del plateau si innalzano i primordî fogliari come contrafforti dorato-ambrati, le loro cellule già avviate verso l'elongazione e una geometria sempre meno regolare, mentre la zona di transizione — appena due o tre cellule di larghezza — negozia in tempo reale il passaggio tra il registro isodiametrico del meristema e quello direzionale del primordio. L'intera scena appartiene alla zona più "giovane" dell'organismo: qui la divisione cellulare procede in trenta minuti o poco più, ogni piano di divisione fresco e i tre strati tunicali — L1, L2, L3 — ancora distinguibili dall'orientamento delle pareti appena deposte, mantenuti in equilibrio da segnali ormonali e molecolari che governano la morfogenesi dell'intera pianta.

Guardando verso l'alto dalla cavità substomatica, due cellule di guardia si arcuano sopra di noi come i piedritti di un portale gotico, le loro pareti interne ispessite che incorniciano una fessura luminosa di appena sette micrometri — uno squarcio di cielo aperto che riversa dall'alto una luce bianco-azzurra di forte contrasto. Ogni cellula è gonfia di pressione osmotica, la sua geometria reniforme mantenuta dalla disposizione asimmetrica delle microfibrille di cellulosa, che irrigidisce la parete interna e obbliga il poro ad aprirsi invece di collassare; dodici cloroplasti per cellula, verde intenso e quasi autoilluminati, si dispongono in fila lungo quella parete ispessita come testimoni schierati dalla stessa forza che li ha radunati lì. Le labbra cuticolari sporgono sopra i margini del poro come cornicioni di cera traslucida, rifrangendo la luce in una sottile frangia iridescente dove lo strato ceroso si assottiglia fino a pochi nanometri. Intorno a noi, le cellule epidermiche pavimentali sono pallide e quasi prive di contenuto, spettatori incolori che rendono le cellule di guardia incandescenti per contrasto, mentre verso il basso la cavità substomatica si apre in un labirinto di mesofillo spugnoso, le superfici bagnate dei lobi cellulari che trattengono pellicole d'acqua condensata e diffondono la luce in una foschia biologica luminosa che sfuma gli spazi profondi in verde soffuso.

Ci si trova sospesi all'interno di un corridoio di membrane quasi inesistenti, dentro le cellule iniziali fusiformi del cambio vascolare durante il risveglio primaverile: ciascuna di esse si estende per trecento micrometri come una navata di cattedrale percepita dall'interno, le sue pareti così sottili da sembrare seta bagnata, il citoplasma una luminescenza paglierina continua che avvolge come l'interno di una lanterna velata. Il nucleo più vicino galleggia a metà cellula come una sfera opalescente, la cromatina appena distinguibile come fumo sospeso in resina ambrata, mentre la pressione osmótica che schiaccia queste cellule tra due mondi che si solidificano è silenziosa e immensa. A sinistra, i tracheidi xilematici hanno già iniziato la loro trasformazione irreversibile: depositi concentrici di parete secondaria lignificata si accumulano in bande ocra e ruggine, la materia vivente sostituita da tubi cavi e perfetti che si perdono in un'ombra color ottone antico, una necropoli di ingegneria idraulica. A destra, gli elementi cribrosi del floema si disfano volontariamente — i nuclei svaniscono, il citoplasma si assottiglia in un gel traslucido, e i pori delle placche cribrose si aprono come aloni di callosio opalescente, cedendo ogni solidità alla corrente degli zuccheri in un mondo che diventa permeabile, verde e umido.

Nell'oceano verde-oro della superficie fogliare, si erge davanti a voi una struttura imponente: la testa secretrice di un tricoma ghiandolare di pomodoro, quattro cellule discoidali disposte a corona, ciascuna un cupola traslucida di citoplasma denso di organuli che premono contro la cuticola come impronte digitali nel vetro caldo. La cuticola stessa è stata spinta verso l'esterno in una bolla tesa e lucente — una lente di olio essenziale accumulato, sfumata d'ambra e sottilmente rifrattiva, la cui superficie cattura la luce obliqua con un riflesso liquido e curvo che ricorda il terminatore su una piccola luna; al suo interno, impercettibili gradienti di densità rivelano la stratificazione di diversi composti terpenoidi, tutto tenuto sotto una tensione crescente come una bolla di sapone nell'istante prima di cedere. La colonna cellulare sottostante scende in sei livelli digradanti verso l'epidermide, le pareti condivise marcate da spesse linee di parete primaria cementata dalla pectina, conferendo all'insieme una gravità quasi architettonica. Intorno, la superficie fogliare si estende come una pianura tettonica: cellule epidermiche dai profili sinuosi e intrecciati, tipici delle dicotiledoni, rivestite da una foresta rada di microcristalli di cera cuticolare che proiettano ombre nette nella luce radente, mentre una patina di cera epicuticolare dona alla superficie un opaco riflesso azzurrognolo — tutto attorno alla bolla oleosa che arde luminosa, sospesa tra contenimento e imminente liberazione.

Ci si trova all'interno di una cattedrale vivente che si allunga verso un'infinità azzurra-bianca: la zona di allungamento radicale si apre come un corridoio di camere vacuolari impilate in successione, ciascuna alta circa duecentocinquanta micrometri, le loro pareti di cellulosa che trasmettono la luce come vetro marino smerigliato, tese sotto una turgidità idraulica silenziosa e immensa. Quasi l'intero volume di ogni cellula è occupato da un'unica vacuola centrale colma di fluido limpido come acqua di sorgente, incolore e otticamente perfetto, la pressione osmotica al suo interno — fino a un megapascal — che spinge le pareti verso l'esterno in una geometria arrotondata e contenuta, trasformando ogni camera in un serbatoio pressurizzato che alimenta la crescita per distensione senza richiedere nuova divisione cellulare. Il citoplasma vivo si è ritirato ai margini: sopravvive solo come una pellicola parietale di schiuma verde-mare appena percettibile, premuta contro la faccia interna di ogni parete, e di tanto in tanto un nucleo — una sfera ambrata di una decina di micrometri — galleggia in questo strato marginale come una piccola lanterna all'orlo di un oceano, rivelando con la sua misura la vastità vertiginosa dello spazio che lo circonda. Lontano, al cuore del corridoio, lo stele centrale si presenta come una colonna assiale indaco, più densa e più scura di tutto ciò che la circonda: i suoi elementi vascolari lignificati assorbono la luce trasmessa anziché lasciarla passare, segnando il punto in cui l'acqua risalirà verso il germoglio attraverso capillari sottopressione negativa, trasportata da quella stessa forza di coesione che rende possibile la vita a scala di tutto l'organismo.

Ci si trova all'interno dello spessore radiale della corteccia di un albero, come se ci si fosse fatti strada verso l'interno partendo dalla superficie esterna, e ciò che si vede è un'architettura di precisione assoluta: file e colonne di cellule suberose morte si estendono in ogni direzione, le loro pareti spesse di laminelle suberizzate che brillano di un ambra-mogano caldo come cognac vecchio tenuto contro la luce di una candela, mentre i lumi al loro interno sono vuoti rettangolari ermetici, sigillati su tutte e sei le facce, privi di citoplasma, di organuli, di qualsiasi traccia di vita. Questa è la peridermide, il rivestimento impermeabile prodotto dal fellogeno — un meristema laterale che genera continuamente verso l'esterno cellule suberose morte e verso l'interno il fellogderma vivente — e le pareti ambrate devono la loro impermeabilità alla suberina, un polimero lipidico che esclude l'acqua e i gas con la stessa efficacia di un sigillo di cera su una botte. Poi, bruscamente, il paesaggio si trasforma: l'ambra cede il posto a uno strato sottilissimo di cellule piatte e traslucide, il fellogeno stesso, le cui pareti quasi incolori sembrano carta di riso bagnata e i cui lumi vibrano di un tenue chiarore cianobiotico — la frontiera tra il morto e il vivo, tra la fortezza e il laboratorio. Poco oltre, il fellogderma si apre in ranghi più larghi e arrotondati, con sfumature di verde-clorofilla nei lumi, e a una quarantina di larghezze cellulari di distanza si apre un lenticello: una zona di collasso dove le cellule complementari parzialmente suberizzate si dispongono in modo lasco, lasciando canali aperti attraverso cui la luce filtra obliqua in oro e panna e l'intera parete impermeabile esala il respiro del fusto verso l'esterno.

Ci si trova sospesi nel cuore di un canale aerenchimatico del picciolo di una ninfea, un corridoio cilindrico largo circa 800 µm che si perde in entrambe le direzioni in un'oscurità umida e soffusa, le cui pareti sono tappezzate da un mosaico continuo di cellule clorenchimatiche poligonali, ciascuna larga circa 200 µm, rigonfie di clorofilla e separate da sottilissime pareti cellulosiche ambrate ai bordi: una cattedrale organica, silenziosa e pressurizzata come lo scafo interno di un sottomarino visto dall'interno. Direttamente di fronte, un diaframma stellato occupa l'intera sezione del canale, una struttura a traforo composta da cellule allungate a braccio che si irradiano da un mozzo centrale, i cui apici assottigliati non si toccano, lasciando aperture poligonali abbastanza grandi da attraversarle; retroilluminato da una luce diffusa che filtra dall'altro capo del canale — probabilmente autofluorescenza della clorofilla o semplicemente luminosità che scivola lungo il tessuto — il diaframma si trasforma in una silhouette luminosa bordata di aloni dorati e verde-celadone. L'aerenchyma lacunare che caratterizza le piante acquatiche come le ninfee non è un semplice vuoto strutturale, ma un sistema di canali d'aria interconnessi che facilita il trasporto di ossigeno dalle foglie verso gli organi sommersi, con i diaframmi stellati che fungono da setti di supporto meccanico senza interrompere il flusso gassoso. Alcuni dei vani poligonali del diaframma sono velati da sottilissime membrane d'acqua iridescenti che tremano impercettibilmente, proiettando interferenze di violetto e rame sulle pareti verdi circostanti, mentre il corridoio si dissolve lontano in una nebbia turchese dove il mosaico cellulare si fa impercettibile come le luci di una città vista attraverso la foschia.
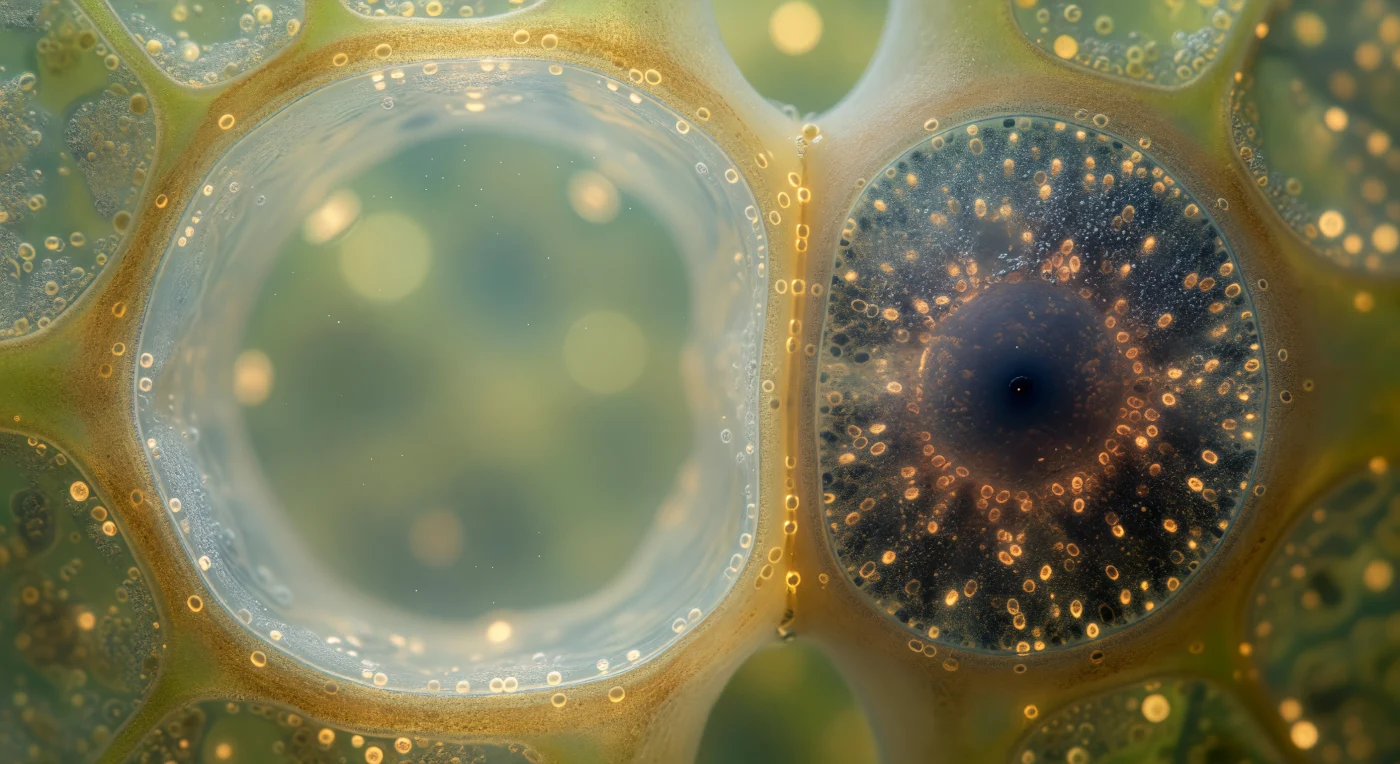
Ci si trova sospesi al confine tra due mondi cellulari radicalmente opposti, immersi nel corridoio vascolare di uno stelo vivente: a sinistra si apre la camera quasi vuota dell'elemento del tubo cribroso, un volume acquoso e traslucido dalle pareti color ambra pallido, percorso da un flusso invisibile di zuccheri disciolti che scorrono lentamente come un fiume sotterraneo, con il citoplasma parietale ridotto a una pellicola madreperlacea appena percettibile lungo quella grande fortezza dorata. Subito a destra, premuta contro quel muro come un'ombra fatta di materia, la cellula compagna occupa uno spazio quattro volte più piccolo eppure stracolmo di urgenza biologica: il citoplasma è un buio denso e quasi opaco, blu-nero e caffè, affollato di mitocondri che emanano calore metabolico come una fucina in miniatura, intramezzati da ribosomi che formano una brina granulare simile a sabbia vulcanica bagnata, con al centro un nucleo tondeggiante e autorevole circondato dal suo alone di cromatina. Sulla parete condivisa tra queste due cellule — un confine di straordinaria intimità biologica — i plasmodesmi si segnalano come perforazioni appena visibili, canali cilindrici nanometrici che attraversano lo strato di circa 200 nanometri come aghi dorati, corridoi di comunicazione tra la cellula-fiume paziente e vuota e la sua instancabile serva metabolica. Intorno a questa diade di luce e ombra, le cellule parenchimatiche retrocedono in un bokeh di verde oliva e chartreuse pallido, umido e cellulare, come se l'intera fisiologia della pianta si fosse disposta per illuminare questo unico, straordinario rapporto di simbiosi.

Osservando questa sezione trasversale dall'interno, ci si trova sospesi al confine esatto tra due regimi biologici: alle spalle, le cellule parenchimatiche della corteccia si aprono in architetture ariose e pallide, attraversate da spazi intercellulari che diffondono una luce azzurra e diffusa come nebbia umida; davanti, la compatta massa violacea dello stele si addensa in una gioia di cellule procambiali dall'intensità quasi minerale. A separarli, la fascia casparia scorre senza interruzione da cellula a cellula come una collana di rame incandescente — un deposito continuo di suberina e lignina incorporato nelle pareti radiali delle cellule endodermali, largo pochi micrometri eppure assoluto nella sua funzione di barriera apoplastica che costringe ogni ione e molecola d'acqua a transitare attraverso il plasmalemma sotto controllo selettivo. Quella luce ambrata e stazionaria non pulsa né vacilla: è la geometria stessa della vita vegetale resa visibile, un sigillo chimico preciso come una saldatura che separa il libero dal controllato, il fuori dal dentro, con l'indifferenza implacabile di un'architettura consolidata nel tempo evolutivo. Stare qui è stare sulla soglia di una delle frontiere più fondamentali della fisiologia vegetale: il luogo dove la pianta decide cosa entra nel suo nucleo vascolare.

Ci si trova sull'equatore di un mondo costruito interamente di bastioni ambrati interconnessi, una rete continua di creste di sporopollenina che forma celle poligonali irregolari, ciascuna larga circa 2,5 micrometri, le cui pareti si alzano in morbide volte dorate profonde fino al bruciato nelle cavità, mentre i lumina tra le creste sprofondano in pozze d'ombra calda come fossero bacini di resina fossile. La sporopollenina — uno dei biopolimeri più resistenti della natura, capace di sopravvivere a milioni di anni di sedimentazione — rivela qui la sua architettura reticolare primaria, scultura molecolare imposta durante lo sviluppo del granulo pollinico nel microsporangio, quando le cellule del tappeto secernono i precursori che si polimerizzano attorno alla microspore in pattern determinati geneticamente. Attraverso la distanza media, la rete di creste si dissolve lungo un canyon pallido e traslucido — il colpo — dove la parete esterna si assottiglia fino a quasi la trasparenza, rivelando una zona di germinazione predestinata attraverso cui il tubo pollinico esploderà quando il granulo raggiungerà lo stigma, spingendo i gameti maschili verso l'ovulo a una velocità di decine di micrometri al minuto. Una luminescenza autofluorescente dorate irradia dall'interno stesso del materiale sotto l'illuminazione radente, trasformando ogni cresta in una lanterna ambrata e ogni fossa in un abisso caldo, rivelando una geometria che governa la vita vegetale a una scala che nessun occhio nudo potrà mai raggiungere.
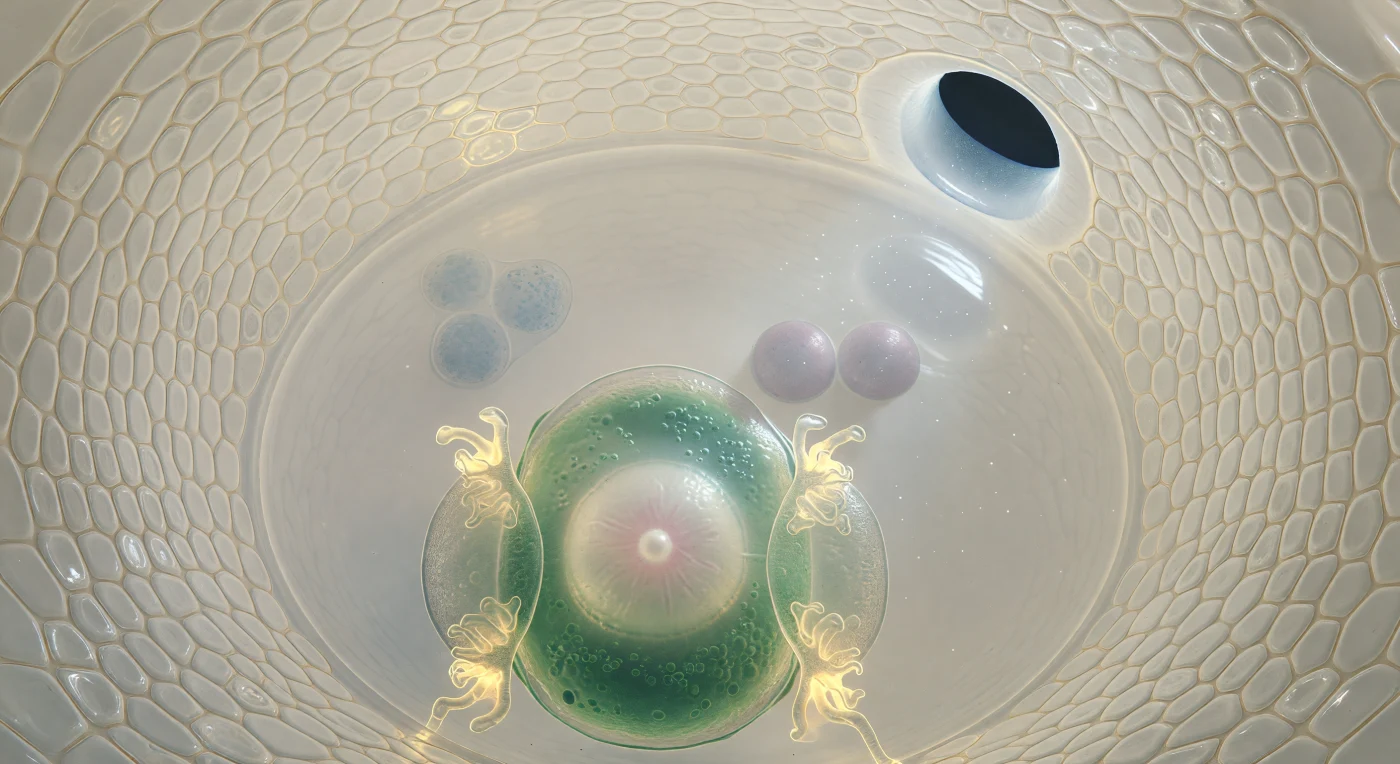
Ci si trova sospesi all'interno di una cattedrale di tessuto vivente, a poche decine di micrometri dalla superficie convessa della cellula uovo: una massa citoplasmatica a forma di pera, dai toni di un giada acquoso che sfuma verso un interno diafano dove il nucleo — sfera luminosa color alabastro venato di rosa pallido — galleggia come una perla in acqua ferma, affiancato dalle due sinergidi le cui ingrossamenti filiformi brillano di un ambra-oro concentrato, lacework membranoso che rimanda la luce come braci. Tutto attorno, i due tegumenti si arcuano come le pareti di un antro d'avorio, mosaico di cellule appiattite e serrate, le loro giunzioni visibili come sottili cuciture ambrate in una traslucenza cremosa che sembra emanare luce propria; in alto a destra, il micropilo si apre come un passaggio ovale di appena quindici micrometri, attraverso cui filtra un fascio di luce esterna che illumina particolato sospeso nel fluido apoplastico. Oltre la cellula uovo, la cellula centrale si espande in una camera cristallina di purezza ottica quasi assoluta, dove i due nuclei polari — sfere grigio-lilla leggermente iridescenti — fluttuano come lune accoppiate in un oceano immobile, mentre all'estremo polo calazale tre cellule antipodali si addensano in un ammasso granulare e sfumato, appena risolto attraverso la profondità trasparente del citoplasma che le separa da noi, avamposto lontano di un mondo che si estende ben oltre la nostra portata.

Ci si trova sospesi esattamente sulla soglia tra due universi opposti, come se si fluttuasse sul bordo di un precipizio tagliato nel vetro ambrato e nel ferro: a sinistra, il legno primaverile spalanca i suoi lumi vascolari — gallerie circolari del diametro di 250 µm, oscure e insondabili come bocche di grotte sottomarine, orlate da aloni ambrati dove le camere dei pori areolati catturano la luce polarizzata in sottili geometrie architettoniche. A destra, senza alcuna transizione graduale, il legno tardivo si chiude su se stesso come un muro: le fibre libriformi si serrano in masse quasi solide, i loro lumi ridotti a fessure di 15 µm che brillano come crepe nell'ossidiana, mentre le pareti secondarie esplodono in colori d'interferenza — blu elettrico, viola e oro brunito — secondo l'orientamento elicoidale delle microfibrille di cellulosa cristallina che le compongono. Attraverso entrambi i mondi, i nastri di parenchima radiale tagliano orizzontalmente il confine come strati geologici nel arenaria, le loro cellule a mattone color miele pallido che ignorano la divisione tra legno primaveriletto e tardivo, portando una luce morbida e opaca in mezzo all'iridescenza caotica delle fibre circostanti. L'intera scena — condensata in un cilindro di quercia pluricentenaria — racconta un anno intero di crescita cambiale: la velocità aperta della conduzione idrica da un lato, la compressione meccanica accumulata dall'altro, due strategie biologiche opposte congelate per sempre in architettura lignificata.
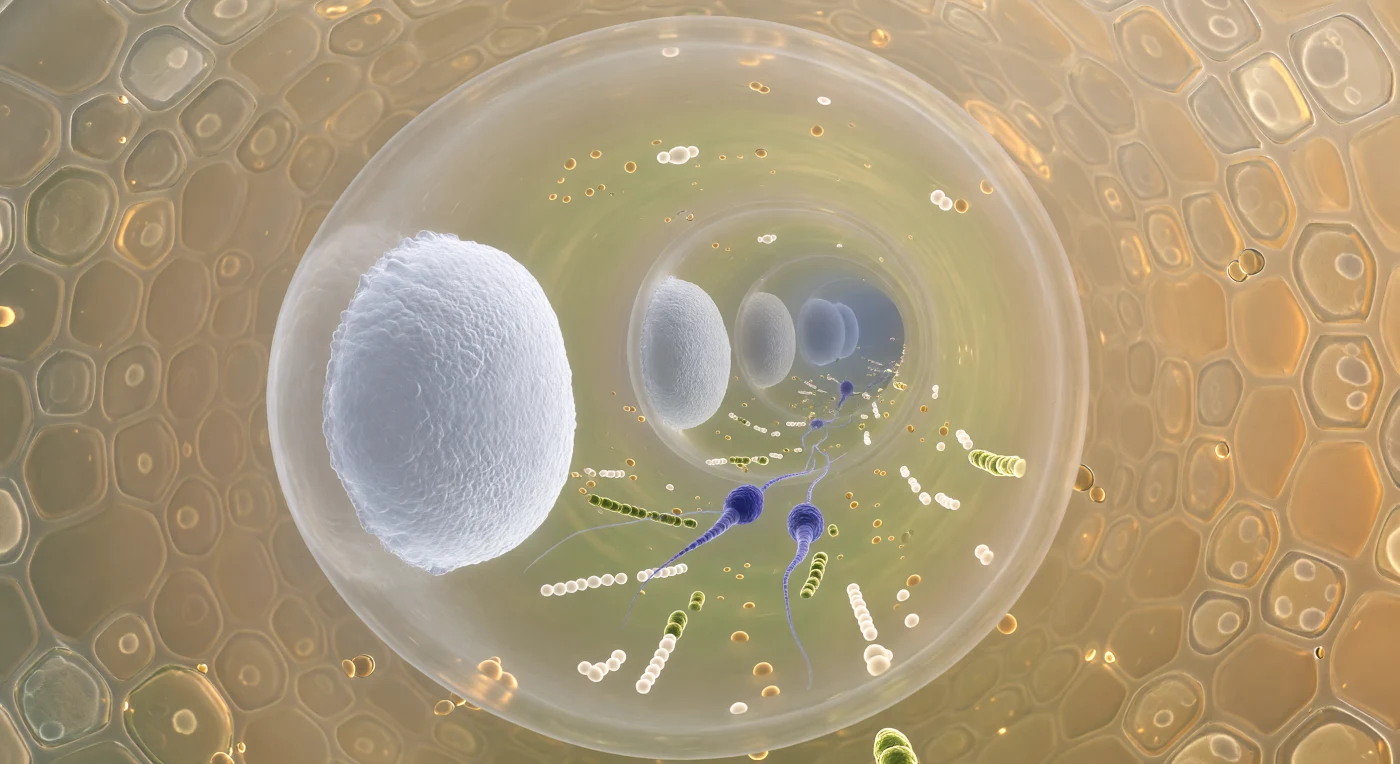
In questo momento esistiamo all'interno di un tubo pollinico in crescita, incanalati in una galleria di soli dodici micrometri di diametro — più stretta di un capello umano — eppure capace di contenere una geografia intera di camere, transito e urgenza biologica. Davanti a noi si ergono i tappi di callosio come bulkhead di una nave microscopica, cilindri di gel polisaccaridico compatto che brillano di un bianco porcellana quasi fosforescente, ciascuno separato dal successivo da circa ottanta micrometri, creando una colonnata di setti luminosi che si perde verso la punta invisibile del tubo. Nel corridoio tra i bulkhead più prossimi, la corrente citoplasmatica trascina un fiume denso di organelli — goccioline lipidiche ambrate, mitocondri giallastri, vesciole in catena — e al centro di questo traffico urgente, due cellule spermatiche fusiformi, lunghe cinque micrometri e colorate di un indaco quasi minerale, vengono portate in avanti senza sforzo verso l'ovulo che le attende. Oltre la parete del tubo, le cellule secretorie del tessuto trasmittente dello stilo premono dall'esterno come un mosaico di masse poligonali dorate, immerse in una matrice polisaccaridica viscosa che diffonde la luce in un caldo alone ambrato, trasformando l'intera scena in qualcosa che ricorda il fondo marino illuminato da un sole pomeridiano filtrato attraverso vetro antico. Quello che si sperimenta qui non è soltanto un fenomeno biologico — è la fecondazione in cammino, la continuità genetica della pianta tradotta in flusso fisico, pressione e materia organizzata con precisione nanometrica dentro un condotto che la mano non potrebbe mai sentire.