
Ti trovi sospeso al bordo di un canyon vivente, le cui pareti si incurvano in entrambe le direzioni come l'interno di un anfiteatro scolpito nel vetro biologico — questa è la docca orale del *Paramecium caudatum*, una specializzazione topografica della pellicola che funziona come un imbuto alimentare permanente, incisa nella superficie della cellula lungo una spirale che termina nel citostoma. Lungo le pareti del canyon migliaia di organelli ciliari composti — membranelle e cirri — battono in onde metacronali sincronizzate a frequenze di 20-40 Hz, generando correnti idrodinamiche che in questo mondo dominato da bassissimi numeri di Reynolds equivalgono a potenti vortici: batteri a forma di bastoncino, luminosi e semitraslucidi, vengono trascinati in spirale verso il basso come detriti risucchiati da un gorgo, incapaci di opporre resistenza alla meccanica collettiva dei dieci mila flagelli. Attraverso la cupola di vetro smerigliato della parete cellulare sopra di te si intravede il macronucleo — una massa reniforme ambrata che preme contro l'ectoplasma, sede delle migliaia di copie genomiche che coordinano il metabolismo di questo singolo protozoo ciliato — mentre più in profondità il citoplasma endoplasmico trasporta vacuoli alimentari a diversi stadi di digestione lisosomiale, sfere scure che derivano dalla stessa trappola ciliare su cui ti affacci. La fossa di assoluta oscurità che pulsa sotto di te — il citostoma — non è una semplice apertura: è il punto dove la membrana cellulare si invagina per avvolgere il pasto batterico in un nuovo vacuolo alimentare, un atto di fagocitosi continua che definisce l'intera architettura di questa creatura.

Sospeso nell'oscurità olivastra sotto la colonna, lo sguardo risale verso l'alto attraverso una cattedrale di luce smeraldo vivente: migliaia di cellule di *Euglena viridis* — ciascuna un fuso di sessanta micrometri, avvolto nella sua pellicola proteica — spiraleggiano in ascesa compatta verso la superficie, dove la luce del giorno filtra diffusa in un disco ambrato circondato da causticità ondulanti. Ogni cellula porta al suo interno nastri di clorofillo disposti ad elica — lamelle di cloroplasti che rifrangono la luce discendente in scintille di verde elettrico e chartreuse — e all'apice anteriore brucia uno stigma terracotta, un ocello di un quarto di micrometro che orienta l'organismo verso la fonte luminosa con la precisione di un sensore fotochimico elementare: è la fototassi positiva, il comportamento collettivo che trasforma questa congrega in una colonna termica di biochimica diretta. Il mezzo stesso non è acqua trasparente ma un brodo di clorofilla diluita, percorso da detriti in moto browniano e da una fluorescenza lime pervasiva — l'emissione collettiva di pigmenti eccitati che stinge il liquido in un vivente tessuto luminoso. Sotto, il verde sbiadisce in oliva, poi in buio immobile; sopra, la massa ascendente di corpi iridescenti si comporta come un unico plume coerente che converte gradiente chimico e luce in ordine biologico emergente.

Vi trovate schiacciati contro un mosaico di frammenti di frustule diatomee — schegge di silice biogenica con le loro reti di pori esagonali che catturano la luce come frammenti di vetrata — mentre sopra di voi si erge uno degli eventi architettonici più straordinari del mondo microscopico: lo pseudopodio avanzante di *Amoeba proteus*, un glacier vivente di ectoplasma che si curva verso il basso come una volta di vetro biologico perfettamente trasparente. Il cappuccio ialino anteriore, opticamente puro, piega e concentra la luce ambiente in archi dorati caldi — caustiche ambrate che scorrono sul substrato davanti a esso come il sole che precede il bordo di una nuvola in transito. All'interno del tubo ectoplasmatico, l'endoplasma avanza in un torrente denso e granulare di bronzo liquido e ambra profonda, ricco di vacuoli alimentari color miele affumicato e granuli rifrangenti che si muovono nel flusso come massi in una piena improvvisa, guidati dal dinamico ciclo sol-gel della citosi amoeboide: il citoplasma si converte in tempo reale da sol fluente a parete strutturale gel ai margini dello pseudopodio. Al confine tra endoplasma ed ectoplasma scintilla una frangia di interferenza iridescente — lavanda pallido e oro tenue che pulsano come olio sull'acqua — una membrana vivente tra due stati della materia, testimonianza di una delle forme di motilità cellulare più primitive e sofisticate dell'intera biosfera eucariotica.
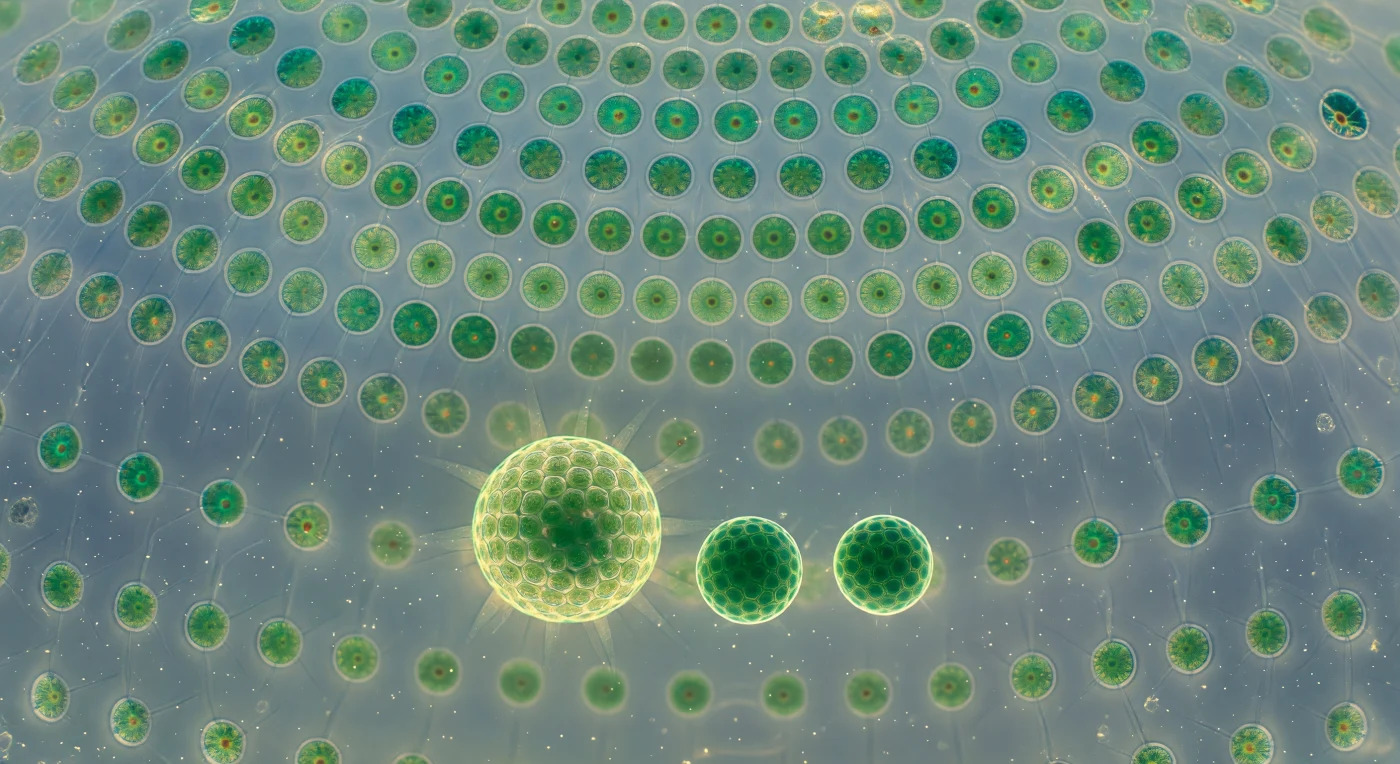
Guardando verso l'esterno dall'interno di questa sfera vivente, il visitatore si trova al centro di una cattedrale del diametro di poco meno di un millimetro, la cui cupola si risolve in un mosaico geodetico di migliaia di cellule somatiche biflagellate, ciascuna un microscopico gioiello verde smeraldo incastonato in una matrice glicoproteica trasparente e collegato ai vicini da filamenti citoplasmatici sottilissimi, quasi invisibili, che percorrono l'intera superficie come una rete di fili d'argento. La luce acquatica filtrata dall'esterno si rifrange attraverso la parete della sfera e si diffonde nell'interno come una luminescenza blu-verde uniforme, mentre ogni cellula irradia il proprio calore clorofilliano con un puntino arancio-ruggine — l'ocello — che brucia come una brace minuscola al centro di ciascun corpo cellulare. I flagelli, invisibili singolarmente, producono insieme uno shimmer metacronico continuo sull'intera superficie interna, un'aurora smeraldo che mantiene la colonia in lenta rotazione stabile nella colonna d'acqua. Sospese nel fluido acquoso dell'interno, tre colonie figlie di dimensioni diverse — una quasi matura e già palpitante di moto proprio, le altre più dense e più opache — galleggiano come pianeti luminosi in una reliquia di vetro, mentre particelle infinitesime disseminate nel liquido intercellulare tremolano per agitazione browniana, trasformando ogni centimetro cubo di questo spazio microscopico in un universo di movimento incessante.

Nel buio assoluto dell'oceano notturno, dove nessun fotone solare è mai penetrato, l'oscurità stessa ha peso e consistenza — poi detonano le prime scariche cerulee, fredde e precise a 490 nanometri, ciascuna della durata di un decimo di secondo, abbastanza da illuminare per un istante la silhouette sferica di un *Noctiluca scintillans*, una cellula dinoflagellata di dimensioni mostruose rispetto a te, la cui membrana plasmatica si incurva come una bolla di sapone tesa che piega e rifrange la propria luce in un alone effimero. All'interno di ogni sfera, un grande vacuolo centrale occupa quasi tutto il volume, mentre ai margini del citoplasma si spengono lentamente le vescicole ricche di luciferina, degradandosi dal blu-bianco al teal profondo man mano che il substrato chimico si esaurisce — e poi il buio risucchia tutto in un istante, come se la luce fosse stata confiscata piuttosto che spenta. Prima che l'oscurità si stabilizzi, una seconda scarica innesca una terza e poi un'altra ancora, propagandosi per disturbo meccanico nell'acqua in un effetto a catena che attraversa la colonna d'acqua come temporale visto dall'interno di una nuvola, ogni lampo blu-verde stampando la propria immagine residua sulla retina mentre i fiocchi di neve marina — aggregati mucillaginosi di frustuli diatomacei — derivano silenziosi attraverso le scariche, disperdendo brevemente la luce ceruleanea in aloni nebbiosi prima che il vuoto oceanico li riassorba.

Guardando direttamente dall'alto nel disco orale di uno *Stentor coeruleus*, ci si trova sospesi sull'orlo di un vortice biologico di incomparabile bellezza: le membranelle composte si dispongono in un anello denso e sovrapposto che ruota in senso orario con una pazienza ipnotica, ciascuna una paletta traslucida di ciglia fuse che cattura la luce come lamelle di vetro impilate, trascinando l'acqua — e tutto ciò che contiene — verso il pozzo buio del citostoma centrale. Il pigmento stentorinico si organizza in striature parallele finissime lungo tutta la pellicola, alternando bande di blu di Prussia intenso e acquamarina pallida con la precisione di un tessuto minerale, mentre batteri e alghe verdi tumultano verso l'interno lungo la spirale logarítmica della doccia orale come detriti catturati ai margini di un pozzo gravitazionale. Attraverso la pellicola semitrasparente, il macronucleo si rivela come una collana di perle opalescenti — lobi refrativi che attraversano verticalmente il corpo cobaltino del protozoo, sospesi nel flusso endoplasmatico accanto a vacuoli alimentari di diverse tonalità di ambra e marrone, ognuno a uno stadio diverso di digestione. L'intera cellula — lunga fino a due millimetri — pulsa con una quasi immobilità geologica del cortex mentre solo le membranelle si muovono con urgenza elettrica, ricordando che in questo mondo dominato da Reynolds bassissimi e dalla viscosità dell'acqua come miele, ogni movimento è una conquista meccanica raffinata da centinaia di milioni di anni di evoluzione.
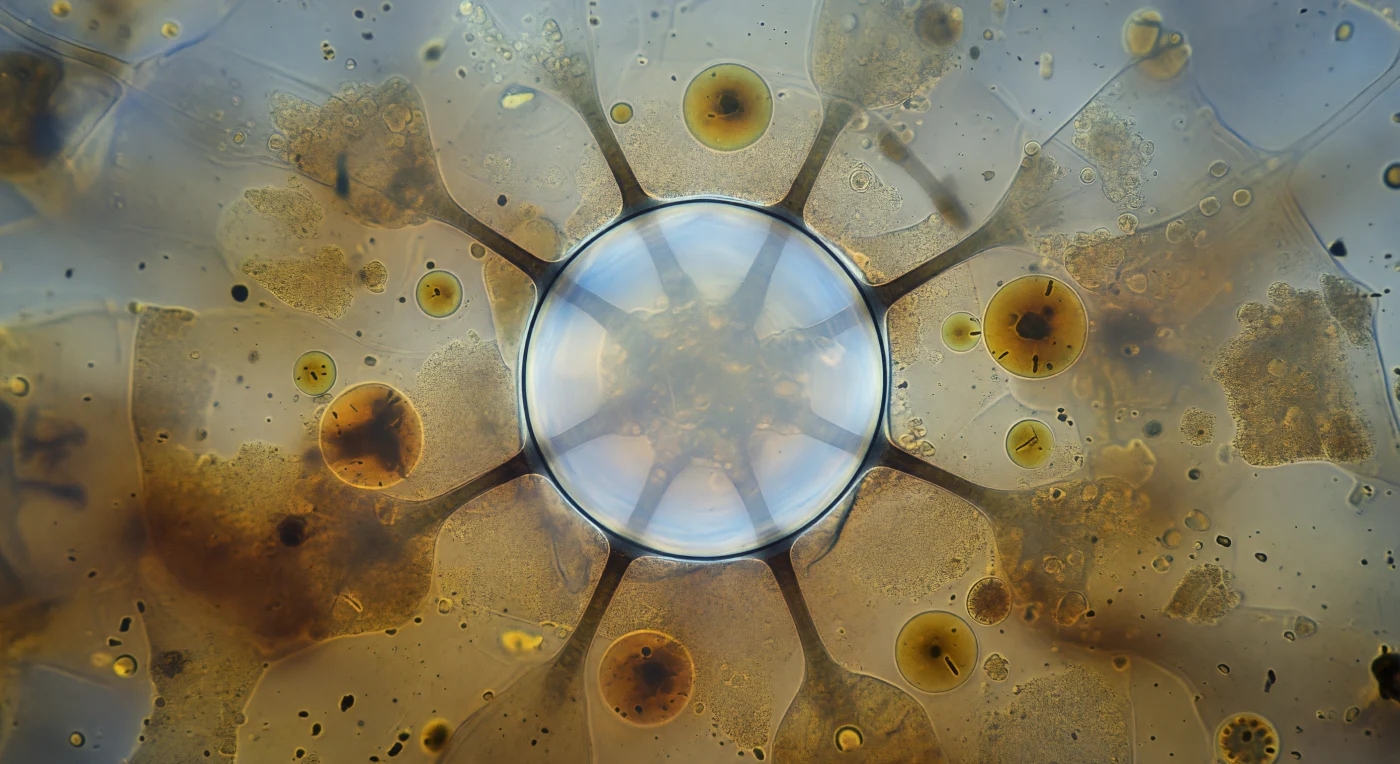
Siamo immersi nel citoplasma di un Paramecium multimicronucleatum, sospesi in un universo viscoso e ambrato dove la luce non ha sorgente ma filtra ovunque come attraverso vetro fumé. In primo piano occupa l'intero campo visivo il vacuolo contrattile: una sfera perfetta di trenta micrometri, la cui membrana sottilissima — appena sette nanometri di doppio strato lipidico — trattiene una colonna d'acqua raccolta in decine di secondi di lavoro osmotico, separando il proprio interno luminoso e latteo dal citoplasma denso e torbido che lo assedia da ogni lato. Sei tubuli nefridiali si irradiano dall'equatore della sfera come raggi oscuri che si perdono nella nebbia granulare dell'endoplasma, incanalando gli ultimi filamenti di acqua citosolica verso il vacuolo già gonfio al limite della rottura. Tutto intorno, vacuoli alimentari ambrati dérivano come lanterne spente, ciascuno contenente residui batterici in diversi stadi di digestione lisosomiale, mentre mitocondri irrisolvibili collettivamente texturizzano il campo come sabbia bagnata in sospensione dorata. L'intera scena è immobile nell'istante prima della sistole: la membrana è tesa alla sua curvatura estrema, il mondo intero trattiene il respiro a un millisecondo dal collasso totale e dall'espulsione violenta di tutto quel carico osmotico verso l'esterno della cellula.
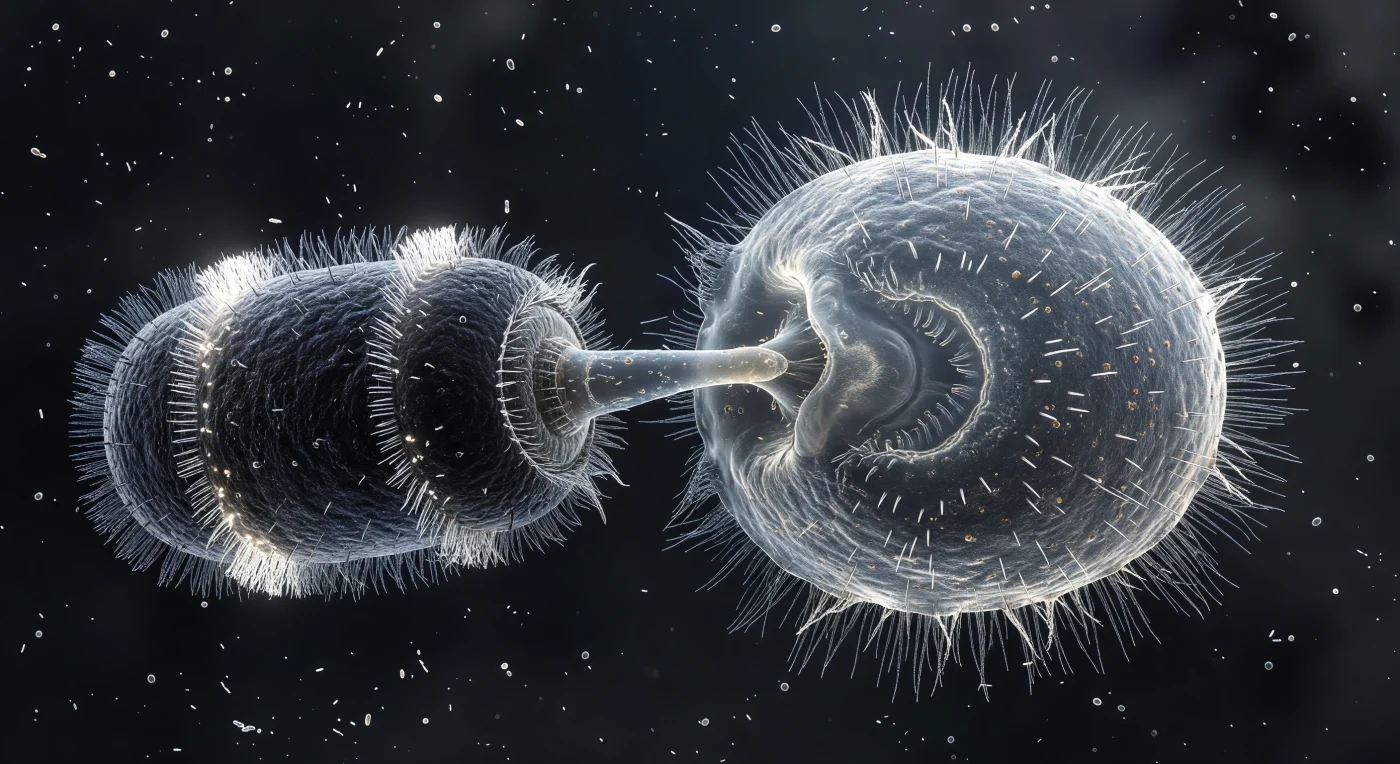
Nel campo visivo appare un incontro di brutalità microscopica congelato in un istante impossibile: a sinistra, il predatore — un cilindro massiccio e scuro, fasciato da due corone luminose di ciglia argentee che ardono come aloni di brina — ha disteso il proprio proboscide fino al punto di contatto con il fianco di un organismo molto più grande, dove la pellicola traslucida cede verso l'interno in una concavità glassata, schiacciata dalla forza biologica pura. Il Paramecium occupa i due terzi destri dell'immagine in tutta la sua magnificenza di cellula-dirigibile: il citoplasma granulare è visibile attraverso l'ectooplasma ialino, i vacuoli alimentari proiettano micro-ombre ambrate nell'interno, e l'intera superficie è esplosa verso l'esterno in una corona di migliaia di filamenti di tricocisti — strutture difensive proteiche sparate in sincronia, ciascuna sottile come vetro filato, l'insieme simile a un'esplosione rallentata di seta ghiacciata. Le ciglia del Paramecium, normalmente coordinate in un'onda metacronale fluida che propulsa l'organismo nell'acqua viscosa come attraverso miele, sono catturate in piena inversione di emergenza — un riflesso comportamentale che si compie in decine di millisecondi — e appaiono scompigliate, alcune splancate lateralmente, alcune arrovolte, la geometria del battito infranta in movimenti individuali frenetici. Il mezzo circostante, un vuoto carbonioso attraversato da nebbia batterica a piani focali variabili, trasforma la scena in un teatro tridimensionale in cui la luce trasmessa illumina entrambi gli organismi dall'interno, trasformando un atto di predazione — Didinium nasutum che si nutre quasi esclusivamente di Paramecia, inghiottendo prede più grandi di sé grazie a una bocca capace di espandersi a dismisura — in un'architettura monumentale di violenza biologica resa eterna dalla fotografia.

Nell'oscurità blu-verde di questo mondo sub-millimetrico, il guscio calcareo di un foraminifero si erge come un'architettura monumentale di calcite bianca lunare — le sue camere globulari disposte in una spirale logaritmica bassa, luminose come marmo scolpito, le suture tra esse tracciate con precisione geometrica sulla superficie traslucida. *Ammonia tepida* è un foraminifero bentonico comune nei sedimenti costieri poco profondi, capace di costruire la propria conchiglia multicamerale — il test — per accrezione di carbonato di calcio in condizioni di bassa energia idrodinamica, proprio come quelle di questo fondale siltoso che si estende in ogni direzione come un deserto d'ambra pallida. Ciò che rende quest'organismo una trappola fantasma è la sua rete di reticulopodi: filamenti citoplasmatici quasi invisibili che si diramano e rianastomizzano in ogni direzione, tradendo la propria presenza soltanto attraverso il movimento — procissioni di granuli organellari color ambra che scorrono bidirezionalmente lungo queste vie di vetro quasi prive di spessore, verso il guscio e lontano da esso. A sinistra, una frustula di diatomea — le sue pareti di silice incise da matrici di pori alla nanoscala che diffrangono la luce blu-verde in labili scintille prismatiche — è trattenuta da più filamenti convergenti e trascinata lentamente verso l'apertura del foraminifero, come preda su una ragnatela fatta di vetro vivente. Ai propri piedi, i granuli di sedimento sono enormi: quarzo, lamelle di mica con superfici a specchio, pellet fecali colonizzati da nubi batteriche grigie appena percettibili — una geologia in miniatura che ricorda, nella sua complessità stratigrafica, quella di qualsiasi paesaggio terrestre.

Sospeso nella penombra acquatica, lo sguardo risale verso quella volta ambrata che domina l'intero cielo visibile: la cupola di *Arcella vulgaris*, un igloo chitinoso largo quasi duecento micrometri, la cui parete semitrasparente si illumina di un oro caldo e profondo là dove la luce trasmessa filtra attraverso le regioni più sottili, sfumando verso un ambra bruna al bordo equatoriale più spesso. Al centro preciso della cupola, incorniciata da un labbro scuro di materiale chitinoso, l'apertura si apre verso il basso come un portale circolare, un tunnel dal quale quattro lobopodi ialini scendono lentamente nell'acqua — cilindri di ectoplasma perfettamente trasparenti, quasi di vetro, che captano la luce trasmessa in un biancore freddo e lunare contro il calore dell'ambra sovrastante, estendendosi con la lenta viscosità propria di un fluido in cui l'inerzia non esiste e ogni movimento costa fatica molecolare. La chitina che forma questo guscio organico — sintetizzata dall'organismo stesso e agglutinata in una struttura autoportante — è percorsa a scala micrometrica da una finissima granulosità come lacca antica, mentre attorno a noi l'acqua non è vuota ma brulicante di frammenti vegetali in decomposizione e batteri che derivano in gruppi, tutto immerso in quella qualità di luce diffusa e calda che trasforma la scena in qualcosa di simile a una cattedrale di resina illuminata dall'interno.

Ci si trova sospesi appena fuori dalla parete pellicolare di un *Paramecium bursaria*, il corpo dell'organismo che occupa l'intero campo visivo come una volta di vetro ambrato attraverso cui si intravede un mondo interiore straordinariamente verde: centinaia di endosimbionti *Chlorella* — dischi compatti di quattro micrometri, ciascuno modellato dalla luce DIC in una moneta tridimensionale con bordo illuminato e mezzaluna d'ombra — tappezzano il citoplasma in una mosaico così fitto da evocare, con precisione botanica, la volta di una foresta osservata dal basso. Ogni *Chlorella* è ospitata volontariamente all'interno della cellula ospite attraverso un'endosimbiosi stabile che fa dell'ameba ciliata al tempo stesso animale e pianta, capace di ricavare carboidrati fotosintetici dai suoi inquilini in cambio di protezione e mobilità. In profondità, tra le correnti citoplasmiche dorate che scorrono nei canali tra simbionte e simbionte, emerge il macronucleo come una radura chiara — un corpo reniforme di grigio-lavanda translucido che governa l'espressione genica quotidiana della cellula — mentre ai margini esterni la pellicola si sfuma in un'aureola di ciglia argentate che battono a decine di hertz trascinando il Paramecio attraverso l'acqua come una nave coperta di remi.
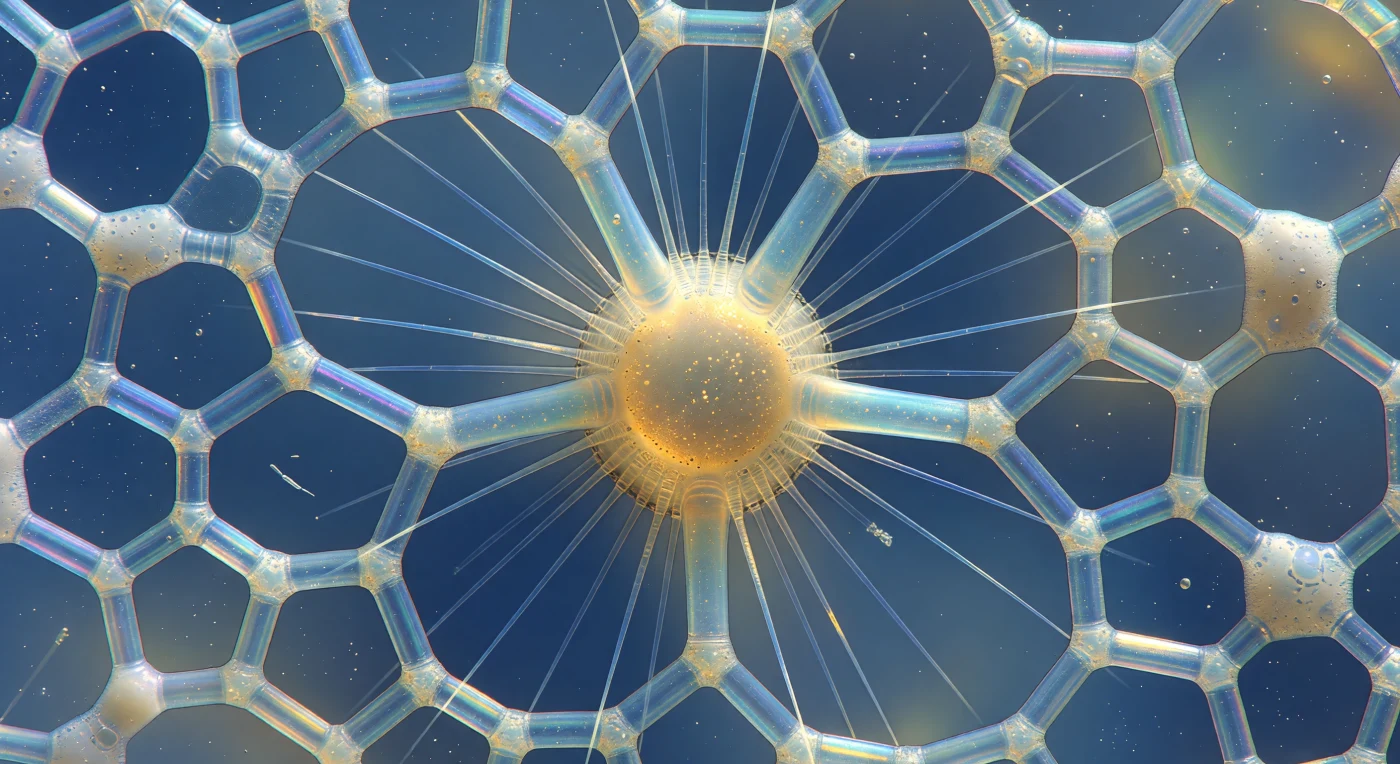
Ci si trova sospesi nell'acqua oceánica tropicale a pochi micrometri dal fianco equatoriale di un radiolario policistino, e l'intero campo visivo è occupato da un'architettura di silice amorfa — opale biologico fabbricato dall'organismo stesso — che si curva e si perfora intorno allo sguardo come la navata di una cattedrale sommersa, ogni trave larga appena due micrometri eppure capace di frantumare la luce discendente in frange d'interferenza che scorrono dal violetto agli angoli acuti fino al cobalto lungo i montanti più larghi, fino all'ambra calda dove la silice si ispessisce ai nodi di giunzione. Attraverso ciascuna delle finestre esagonali e pentagonali del reticolo, l'oceano aperto si risolve in una sfumatura di azzurro cerúleo profondo, trasformando lo scheletro intero in un reliquiario illuminato tenuto contro un crepuscolo perpetuo, mentre al suo centro la capsula centrale arde di una luminosità densa color miele — membrane proteiche appena visibili come un bordo più scuro, e all'interno un lento rimescolio granulare di gocce lipidiche e cristalli di solfato di stronzio che scintillano come scintille d'oro. Gli axopodi si irradiano verso l'esterno come aghi di vetro perfettamente rettilinei, rigidi e rifrangenti, alcuni che svaniscono nell'azzurro e altri che captano la luce di traverso e lampeggiano bianco-argento come fili tesi, mentre tra le spine più esterne uno strato di ectoplasma vacuolato si aggrappa in bolle traslucide, ciascuna un piccolo obiettivo che raccoglie e distorce i colori interferenziali in punti luminosi fugaci — e un singolo bastoncello batterico che tumba attraverso il poro esagonale più vicino misura, involontariamente, la vera scala di questa cattedrale minerale.

Ci troviamo appena al di sopra di un pavimento di sedimento che si estende verso un orizzonte luminoso e diffuso, immersi in una luce acquosa e fredda che filtra attraverso ogni frammento di silice come se provenisse da un sole remoto e nascosto, trasformando l'intera scena in un mosaico spettrale di oro pallido, cobalto e rosa madder che si sposta ad ogni minima variazione della nostra prospettiva. Intorno a noi si ergono i resti di migliaia di frustule diatomee — tamburi cilindrici di *Cyclotella* crollati come colonne di marmo, carene pennate di naviculoidi inclinate come scafi di navi affondate, triangoli di *Triceratium* e sezioni di *Coscinodiscus* che emergono dal substrato come detriti architettonici di cristallo — ciascuno composto di silice amorfa con la traslucenza lattiginosa di un opale, i cui array di pori nanometrici proiettano ombre a pizzo finissimo sul limo sottostante. Questa non è una scena di morte silenziosa: tra le rovine, flagellati ambrati derivano nel volume d'acqua come piccole ellissi dorate, e un eliozoario *Actinophrys* è sospeso come un lampadario vivente, i suoi assopodi — aste rigide irradiate in ogni direzione, sostenute da fasci di assonemi — catturano la luce trasmessa e bruciano come fibre ottiche tra le guglie di vetro, un organismo singolo che presiede sul campo di cristalli come se fosse il custode ultimo di questa cattedrale silenziosa e iridescente.
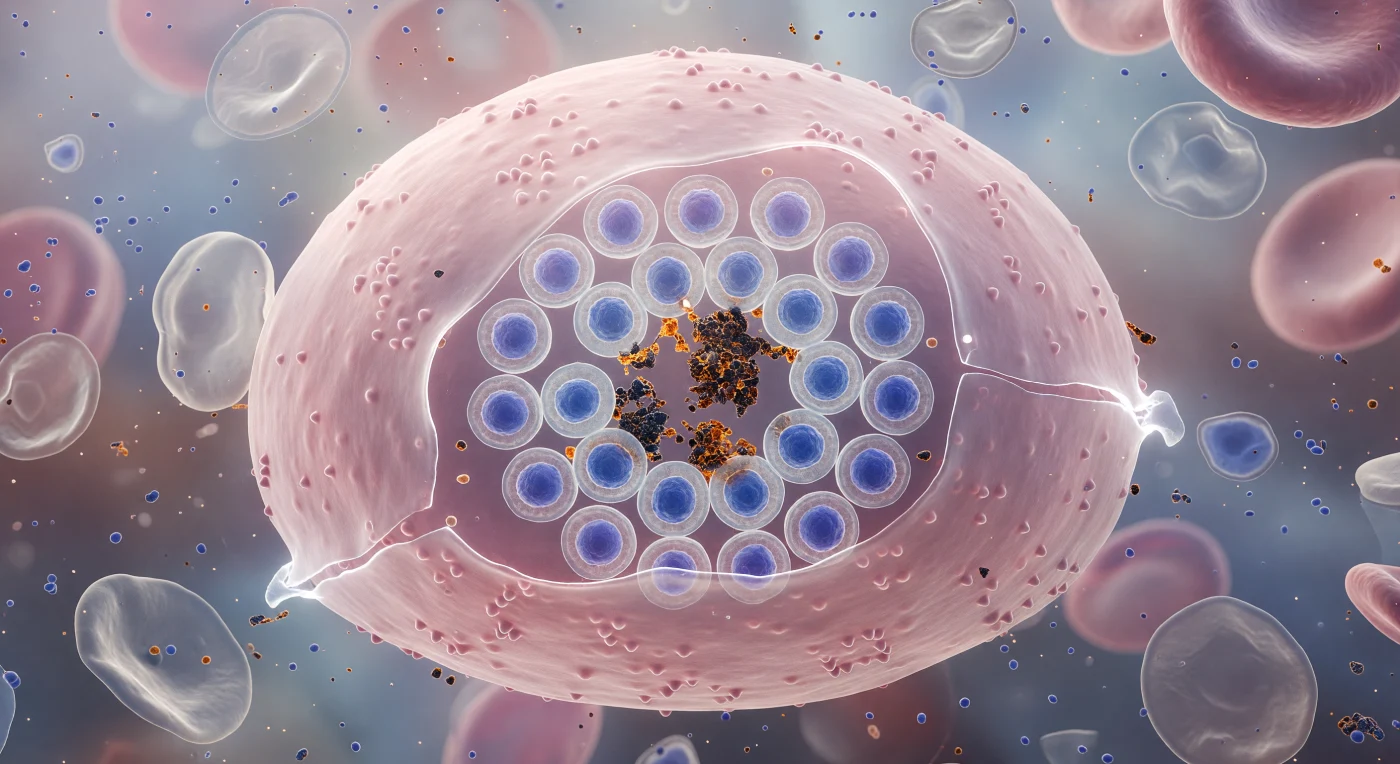
Ci si trova sospesi contro la membrana rigonfia di un eritrocita infetto, un'immensa cupola rosa-traslucida che si curva in ogni direzione come lo scafo di un dirigibile sul punto di cedere: attraverso di essa si intravede una rosetta di ventiquattro merozoiti di *Plasmodium falciparum*, disposti con precisione geometrica intorno a un nucleo centrale di granuli di emozoina color ambra bruciata, i loro nuclei colorati nel blu cobalto più intenso, come pietre preziose incastonate in una struttura floreale sul punto di esplodere. La cellula ospite è stata interamente consumata: il parassita ha digerito l'emoglobina, cristallizzandone i sottoprodotti ferrici in emozoina — chimicamente inerte, otticamente densa, l'unica struttura che sopravviverà alla rottura imminente. La pressione osmotica accumulata all'interno ha assottigliato la membrana fino alla quasi-trasparenza in certi punti, dove essa trema impercettibilmente, luminosa e fragile come vetro soffiato, mentre le proiezioni proteiche esportate dal parassita punteggiano la superficie come colline basse su una pianura rosa. Attorno, cellule fantasma già svuotate derivano come involucri accartocciati nella penombra azzurrina del plasma, testimonianze silenziose dei cicli di invasione precedenti; il mezzo intercellulare è velato di frammenti molecolari in sospensione browniana, i detriti biochimici di rotture già avvenute. L'intera scena è sospesa nell'ultimo istante prima che la membrana ceda e i merozoiti vengano liberati nel torrente sanguigno, pronti a invadere nuove cellule.

Ci si trova sospesi a pochi centimetri sopra quella che sembra una pianura continentale di ambra incandescente: la superficie thecale di *Ceratium tripos*, un dinoflagellato corazzato le cui placche di cellulosa si estendono in ogni direzione come altipiani illuminati da una luce interna, ciascuna delimitata da creste di sutura geometricamente precise che ricordano le scarpate di faglie tettoniche, la loro superficie segnata da striature parallele e interrotta a intervalli regolari da minuscoli pori scuri, pozzi perfetti che penetrano negli strati lamellari della teca. Attraverso il campo visivo si apre il cingulum equatoriale come un canyon di cobalto-indaco, le sue pareti che tagliano di netto il caldo paesaggio ambrato per rivelare in sezione la struttura cellulosica della teca — laminae concentriche, architettura organica stratigrafica —, mentre nel fondo della gola, quasi invisibile nell'ombra, il flagello trasversale giace avvolto in spirale come un nastro silenzioso, appena tradito da un filo di iridescenza pallida. La placca è composta da polisaccaridi cellulosici che la cellula sintetizza e assembla con precisione molecolare in un'armatura che la protegge pur lasciando filtrare verso l'esterno la luce calda metabolicamente generata al suo interno, così che l'intera superficie brilla di un oro bruciato in contrasto con la traslucidità acquatica blu-verde della colonna d'acqua circostante. A sinistra, il corno apicale si innalza come una guglia monumentale della stessa materia ambrata, curva e maestosa, fino a scomparire oltre i limiti del frame — ricordando che questa singola cellula, immobile nell'oceano, porta su di sé una geometria che l'evoluzione ha perfezionato da centinaia di milioni di anni.
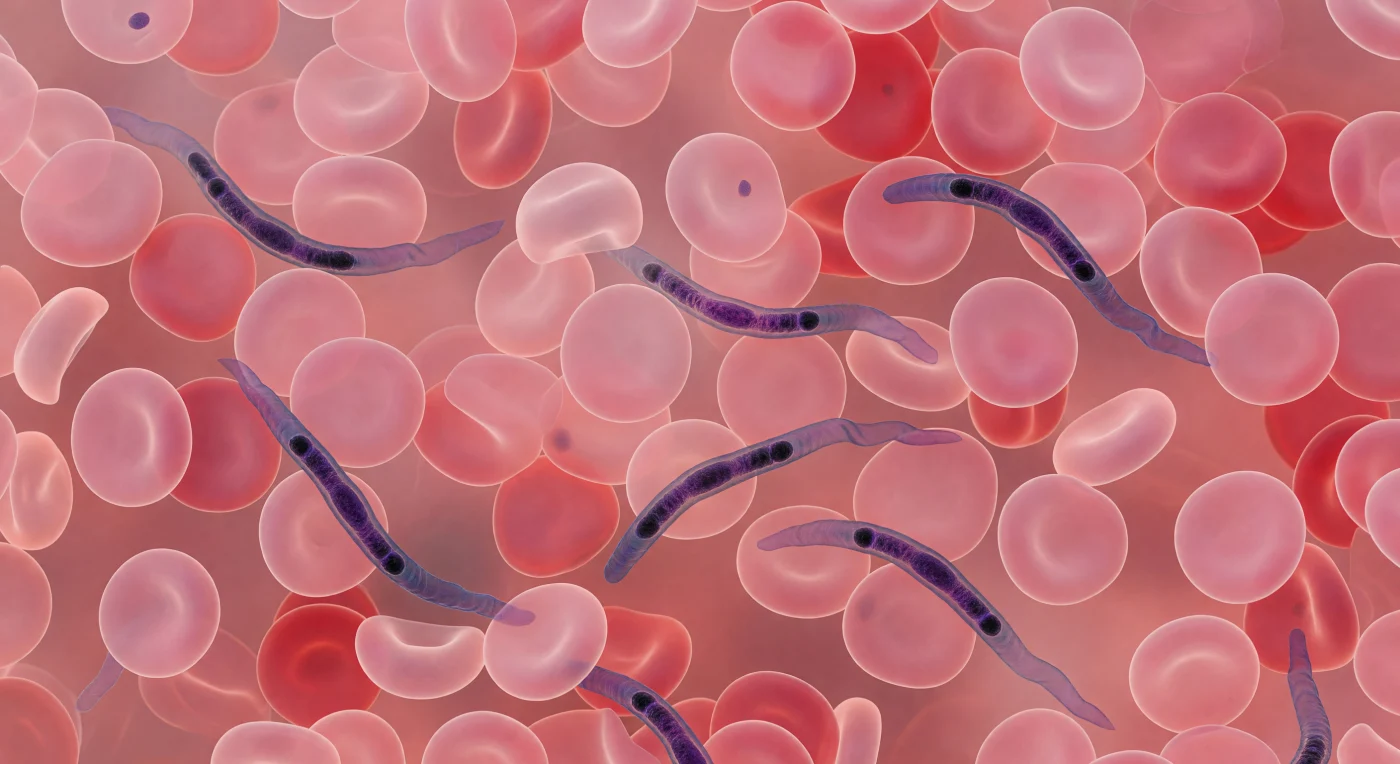
Immersi nel flusso vivo di un capillare sanguigno, lo sguardo si perde in ogni direzione tra una folla soffocante di dischi biconcavi color rosa-corallo — ogni globulo rosso un cuscino traslucido di sette micrometri, così denso da trasformare l'intera profondità di campo in una nebbia tepida di geometrie carnose che si sovrappongono e si pressano senza lasciare alcuno sfondo visibile. Tra questi boulders di emoglobina si insinuano, come calligrafia vivente, diversi Trypanosoma brucei: organismi eucarioti flagellati lunghi fino a trenta micrometri, la cui membrana ondulante corre lungo il corpo come un nastro di seta indigo, propagando onde laterali che spingono il parassita attraverso i corridoi più stretti tra i globuli, sfruttando le stesse viscosità del plasma che a questa scala rendono il nuoto più simile a un lento scivolare nel miele che a qualsiasi moto inerziale. All'interno di ciascun corpo parassitario, il colorante Giemsa rivela due condensazioni cromatiche quasi nere — il nucleo, più grande e centrale, e il cinetoplasto, una struttura mitocondriale compatta carica di DNA extracromosomico situata all'estremità posteriore come un seme scuro — entrambi testimoni di una biologia cellulare straordinariamente sofisticata nascosta in un organismo invisibile a occhio nudo. La scena intera — rosa, viola, indaco — è quella di un'invasione silenziosa: i tripanosomi navigano con grazia tra cellule ospiti ignare, in quel momento in cui la patologia e la bellezza microscopica coincidono perfettamente.

Sospesi a duecento micrometri sotto la pellicola superficiale di uno stagno, il mondo sopra di voi è un soffitto di mercurio ondulante — l'interfaccia aria-acqua che restituisce come specchio frantumato ogni fotone diffuso dalla comunità sottostante — mentre la luce pomeridiana filtra attraverso quella membrana in colonne ambrate che proiettano causticali dorate scivolanti lentamente su organismi in perenne moto. Direttamente davanti a voi, una folla di Euglena occupa il piano intermedio come siluri smeraldo da quindici a ottanta micrometri, i loro cloroplasti così densi da saturare la luce trasmessa di un verde botanico cupo, mentre le striature proteiche del pellicolo generano una sottile iridescenza metallica lungo i fianchi; fra loro, le cellule di Chlamydomonas brillano come lanterne di giada, ciascuna con il suo punto di colore più intenso nell'intera scena — il macchiato granulo carotenoide dello stigma rosso mattone che arde come una brace. I Coleps rotolano lentamente tra le forme fotosintetiche, armati di un mosaico di placchette calcaree che frammentano la luce in mille sfaccettature come porcellana frantumata, mentre Chilomonas semitrasparenti derivano come ovali di vetro ottico nel fumo bluastro della coltre batterica che ammorbidisce ogni contrasto in profondità, e un frammento di filamento di Spirogyra attraversa il campo visivo come una trave di vetro, la sua spirale di clorofilla ancora visibile come elica verde-giada nell'interno cilindrico. L'intero paesaggio è un istante congelato di densità cinetica — ogni superficie bagnata e rifrangente, ogni organismo una piccola lente che trasforma la luce ambrata dello stagno in qualcosa di più complesso e vivo.

Siamo prigionieri all'interno della larva nauplio, guardando verso l'esterno attraverso la sua corazza di chitina color ambra-arancio, le placche rigide e scanalate che si incurvano ai margini della visione come le pareti di una cattedrale tinta. Attorno a noi — da ogni direzione, in modo quasi invisibile — si estende la rete reticolosa di *Globigerina bulloides*, una foraminifera planctonica il cui test calcitico domina la distanza in alto a destra come una fortezza di gesso bianco-crema, le sue centinaia di aperture superficie punteggiata da cui emergono fili pseudopodiali larghi appena 0,2–0,5 µm, traditi soltanto dagli incessanti treni di vescicole ambrate e mitocondri scuri che scivolano lungo ogni filamento verso il corpo centrale. Il mezzo acquoso non è vuoto ma una sospensione colloidale di neve marina, cellule batteriche e materia organica disciolta che ammorbidisce i contrasti oltre qualche centinaio di micrometri, lasciando che i fili più prossimi brillino brevemente d'argento prima di dissolversi di nuovo nell'azzurro-verde pervasivo. Non c'è violenza né movimento brusco: i filamenti si contraggono con una geometria meccanica silenziosa, restringendosi e irrigidendosi impercettibilmente mentre la tensione convergente trascina la larva, millimetro dopo millimetro, verso la struttura calcarea indifferente che attende in lontananza.

Sospesi in questo blu cobalto, i veri protagonisti della scena sono gli Acantari — organismi unicellulari il cui scheletro interno, composto da venti spicole di solfato di stronzio disposte secondo una simmetria geometrica assoluta, rifrange la luce discendente in aureole prismatiche di bianco ghiaccio, violetto pallido e oro spettrale, come stelle cadute e congelate nel loro esplodere. Le spicole stesse mostrano una birifrangenza interna che scompone la luce polarizzata in bande arcobaleno sottili come fili di seta, mentre il corpo cellulare centrale — una sfera di citoplasma ambrato appena risolta — irradia assopodi trasparenti che catturano la luce come filamenti d'argento nell'acqua vischiosa. Tra questi organismi, le lorichee dei tintinnidi pendono come piccoli vasi di cristallo inclinati, costruiti da particelle minerali agglutinate, e i fiocchi di neve marina — aggregati di muco, detriti organici e frammenti di colonie — derivano lentamente attraverso il campo visivo a profondità focali diverse, caldi nei toni ambra contro il freddo imperioso del blu. Questa colonna d'acqua aperta a venti metri di profondità non è uno spazio vuoto ma un universo abitato, dove la geometria minerale e la fragilità organica coesistono sospese nella luce filtrata che discende dalla superficie come attraverso una cattedrale senza pareti né soffitto visibile.

Distesa davanti a te come un continente dimenticato, la superficie del fango essiccato si incrina in un mosaico di placche poligonali separate da crepacci profondi — canyon di argilla ocra e sienna scura che precipitano nell'ombra come gole di un pianeta arido. Luce obliqua e dorata radente ogni asperità rivela il contrasto fondamentale di questo mondo: la superficie minerale frantumata, matta e granulare, contro la perfezione levigata delle cisti protiste sparse sui pianori — sfere di Colpoda ambrate e traslucide, ognuna una gemma biologica a doppia parete che intrappola un sottile alone luminoso di aria tra il rivestimento chitinoso esterno e la membrana interna, proiettando un'ombra ellittica morbida sulla superficie spezzata. I gusci di Arcella siedono come piccoli elmi di chitina scura, le loro aperture sigillate da un tappo translucido di membrana cistale, la superficie finemente stipata di subunità proteiche geometriche visibili solo a questa scala intima. Tra questi vasi solitari di vita sospesa, le colonie di Euglena in palmella interrompono la pianura austerea come macchie di muco essiccato — fogli traslucidi e rugosi, tinti di verde-oro spento dove i cloroplasti dormienti conservano ancora il loro pigmento, i bordi arricciati che catturano diversamente la luce obliqua rispetto all'argilla minerale circostante, segnali biologici di una sopravvivenza nascosta nell'attesa silenziosa del ritorno dell'acqua.




















