
Du schwebst am Rand eines gewaltigen Spiralcanyons — die Mundrinne eines *Paramecium caudatum* —, dessen gläsern-transparente Wände sich in einem weiten Bogen wie das Innere eines lebenden Amphitheaters um dich wölben, im Phasenkontrastlicht in stechendem Silberweiß gegen den kohleschwarzen Hintergrund leuchtend. Tausende von Zilienorganellen — dichtgedrängte Membranellen und Cirri — schlagen in donnernden, synchronisierten metachronen Wellen, die wie langsam rollende Brecher eine nach der anderen die Canyonwände hinabgleiten und einen kontinuierlichen Sogstrudel erzeugen, der stabförmige Bakterien in goldweißem Lichtreflex spiralförmig in die Tiefe zieht, hinein in die pulsierend-schwarze Öffnung des Cytostoms. Die Pellicle unter deinen Füßen — eine fein längsgestreifte, metallisch schimmernde Membran, verstärkt durch Proteinkämme im Ektoplasma — gibt dem gesamten Organismus seine halbstarre Form, während hinter der gewölbten Zellwand der Makronukleus in warmem Bernsteinton leuchtet, eine nierenförmige Masse, die im diffusen Granularlicht des Endoplasmas wie ein Himmelskörper durch Milchglas scheint. Tiefer im Zellinneren treiben dunkle Nahrungsvakuolen wie Gewitterwolken — jede eine versiegelte Verdauungssphäre auf einem anderen enzymatischen Zeitplan —, während du spürst, wie das gesamte Medium um dich, zäh wie Honig und durchdrungen von Brownscher Bewegung, nicht von Schall, sondern allein von Druck, Chemie und dem rastlosen mechanischen Takt zehntausend schlagender Zilien geformt wird.

Du schwebst reglos unter einer aufsteigenden Säule aus *Euglena viridis*, die sich wie ein lebendiger Smaragdturm in das diffuse Goldlicht der Wasseroberfläche hineinschraubt — jede einzelne Zelle ein sechzig Mikrometer langer Spindelkörper, dessen spiralförmige Chloroplastenbänder ein so gesättigtes, elektrisches Grün ausstrahlen, dass das gesamte Medium um dich herum zu einem blassen Limettenhauch aufleuchtet. Dieser kollektive Phänotyp ist keine Zufälligkeit: Die Zellen folgen dem Licht durch Phototaxis, gesteuert vom winzigen terrakottaroten Stigma nahe ihrer Vorderseite — einem Photorezeptorfleck von kaum einem Viertelmikrometer Durchmesser, der im Zusammenspiel mit dem darunterliegenden Photorezeptor die Geißelbewegung moduliert und so jeden Organismus präzise nach oben lenkt. Die Pellicle jeder aufsteigenden Zelle, ein halbstarres Proteinkorsett direkt unter der Plasmamembran, fängt das Streulicht wie geölte Seide und lässt die gesamte Kolonne als langsam rotierende Säule facettierter Juwelen erscheinen, während in der Tiefe unter dir der Limettengrün-Dunst zu öliger Schwärze versinkt, wo weder Licht noch Bewegung die Stille durchdringen.

Der Blick von unten, aus dem Mosaikboden zersplitterter Diatomeenfrusteln heraus, wird von einer einzigen gewaltigen Struktur beherrscht: dem vorrückenden Pseudopod von *Amoeba proteus*, der sich wie ein Gletscher aus lebendigem Glas über den Betrachter wölbt, seine hyaline Spitze eine optisch makellose Kuppel aus Ektoplasma, die das Umgebungslicht zu warmen Kaustikbögen bündelt und sie wie Vorboten einer Flutwelle über den Kieselsäureschutt darunter wandern lässt. Durch die transparente ektoplasmatische Röhre hindurch ist das Innere wie durch ein Vergrößerungsglas sichtbar: das Endoplasma strömt als dichter, granularer Fluss aus flüssiger Bronze vorwärts — Nahrungsvakuolen wie geräucherter Honig, Mitochondrien wie gesplitterte Kupfersplitter, Granula, die wie Felsbrocken in einer Sturzflut trudeln. An der Sol-Gel-Grenze, dort wo das fließende Cytoplasma in Echtzeit zum starren Wandmaterial erstarrt, schimmert ein lebendiger Interferenzstreifen aus blassem Lavendel und warmem Gold, ein irisierendes Grenzphänomen zwischen zwei Aggregatzuständen desselben biologischen Materials. Das Licht, das die gesamte Zellmasse durchquert, wirft pulsierende Kaustiknetze auf den Diatomeenfriedhof darunter, während die Tiefe des Teichwassers dahinter zu einem warmen, organischen Braun-Grün-Dunst zerfließt, in dem Bakterienspäne unsichtbar zittern.
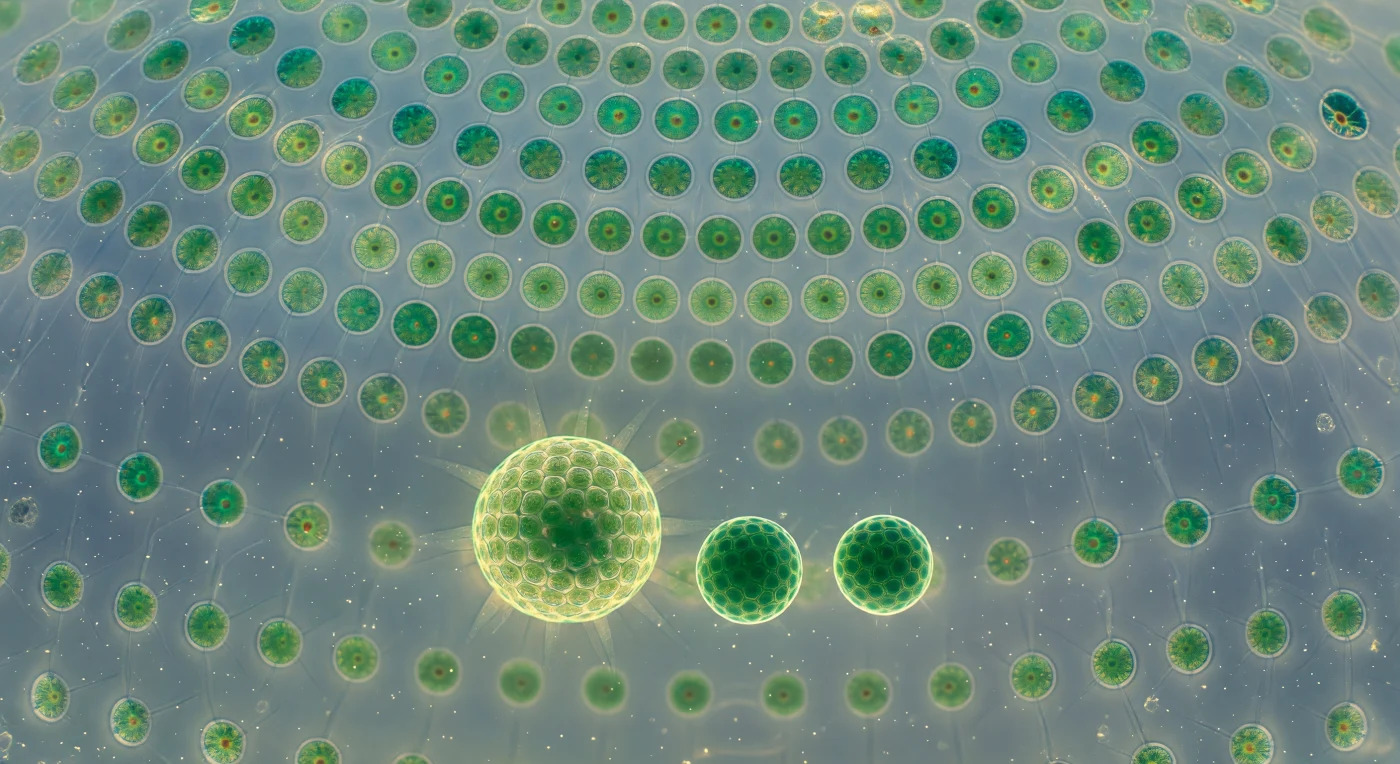
Im geometrischen Zentrum dieser lebenden Kuppel schwebend, blickt man durch eine Wand aus transparenter Glykoproteinmatrix nach außen, in der tausende biflagellate Somazellen wie Smaragde in bernsteinfarbenes Glas eingelassen sind – jede einzelne ein vollständiges Lebewesen von rund zehn Mikrometern, durch haarfeine Zytoplasmabrücken mit seinen Nachbarn vernetzt und so die gesamte Kolonie zu einem einzigen koordinierten Organismus zusammenfügend. Das Innere dieser Hohlkugel – *Volvox globator*, eine der komplexesten Kolonialformen unter den Grünalgen-Protisten – ist erfüllt von einem kühlen, blaugrünen Schimmer, der entsteht, wenn Tageslichtstrahlen durch das überlagernde Teichwasser und die leicht lichtbrechende Matrixwand gefiltert werden, während der synchrone Flagellenschlag aller Somazellen an der Innenfläche ein nicht endendes, metallisch glänzendes Polarlichtflimmern erzeugt, das die Kugel sanft rotierend durch die Wassersäule treibt. Im klaren Innenfluid hängen drei Tochterkolonien unterschiedlicher Reife wie leuchtende Planeten in einer gläsernen Reliquienkapsel: die größte bereits ein vollständig ausgebildetes, golden-grünes Miniaturabbild der Mutter, die mittlere noch jadegrün und zelldicht, die kleinste kaum mehr als eine stille Hohlkugel gleichmäßig smaragdener Zellen ohne funktionierende Geißeln. Diese Schachtelung von Kolonien innerhalb einer Kolonie markiert einen der eindrücklichsten Belege für den evolutionären Übergang zwischen Einzelligkeit und echter Vielzelligkeit – die Arbeitsteilung zwischen sterilen Somazellen und reproduktiven Gonidien ist hier bereits vollzogen, eingebettet in eine Matrix, die nicht Gewebe, aber auch nicht mehr bloße Ansammlung ist.

In absolutem ozeanischem Dunkel – nicht dem weichen Dunkel eines geschlossenen Raums, sondern dem schweren, salzigen, dreidimensionalen Nichts tiefen Meerwassers – detoniert eine eiskalte Lichtexplosion: ein Noctiluca-scintillans-Zelle, kaum zwanzig Mikrometer entfernt, entlädt in einem Zehntel Sekunde ihr gesamtes chemisches Lichtpotenzial, und die Biolumineszenz brennt in einem präzisen Cerulean-Blau bei 490 Nanometern durch das Schwarz wie ein winziges, gefangenes Wetterleuchten. Für diesen Bruchteil einer Sekunde ist alles sichtbar: die gallertartige Kugel der Zelle, groß wie ein kleines Planetoid in dieser Welt der Mikrometer, ihre Plasmamembran ein schimmernder Meniskus, der das eigene Licht in sich zurückbricht, während im Innern die große zentrale Vakuole wie ein Öllampenglas glüht und die Luciferin-haltigen Vesikel am Zellrand von Blau-Weiß zu tiefem Türkis verblassen, während die Reaktion ihr Substrat erschöpft. Dann greift das Dunkel zurück wie ein zugeschlagener Deckel – doch noch bevor Stille sich setzt, löst drei Zelllängen entfernt eine neue Entladung aus, und dann wieder eine dahinter, die Kettenreaktion wandert durch mechanische Erschütterung im Wasser fort und lässt einen Noctiluca-Körper nach dem anderen für je ein Zehntel Sekunde aufleuchten: eine treibende Ansammlung kalter blauer Laternen, zwischen denen Flocken aus marinem Schnee – aggregierte Schleim- und Diatomeenfragmente – in den Lichtblitzen auftauchen, kurz ein nebliges Cerulean-Halo streuen und wieder verschwinden, während das Wasser selbst eine Textur aus überlagerten Nachbildern annimmt, blau-grün wie Gewitterwolken von innen, ein Sturm ohne Himmel und ohne Ende.

Wir blicken senkrecht hinab in den geöffneten Oralscheibendes eines *Stentor coeruleus* – ein lebendiger Strudel von solcher Tiefe, dass er wie ein biologischer Abgrund wirkt, ein blaugrüner Trichter, dessen spiralförmig angeordnete Membranellen das umgebende Wasser in einem gleichmäßigen, hypnotischen Uhrzeigersinn nach innen ziehen. Die dicht gestaffelten, fusionierten Cilienpaddel fangen das von unten einfallende Licht wie übereinandergeschichtete Glaslamellen, während die Stentorin-Pigmentgranula in feinen parallelen Striationen – tiefes Preußischblau wechselt mit blassem Aquamarin – die Randzone der Scheibe wie ein schimmerndes Gewebe erstrahlen lassen. Durch die halbtransparente Pellikel des sich nach unten erstreckenden Trompetenkörpers ist die Makronucleus-Kette zu erkennen: eine Perlenschnur opaleszenter, schwach leuchtender Loben, die sich wie gefrorene Flusstropfen durch das körnige, bernsteinfarbene Zytoplasma fädeln. Bakterienstäbchen und grüne Algenpartikel trudeln entlang der Spiralströmung ins Innere, blitzen kurz als goldene und chlorophyllgrüne Lichtpunkte auf, bevor sie im dunklen Zytostom verschwinden – verschluckt von einem einzelnen, geduldigen Organismus, dessen gesamtes Wesen darauf ausgerichtet ist, die umgebende Welt in sich hineinzuziehen.
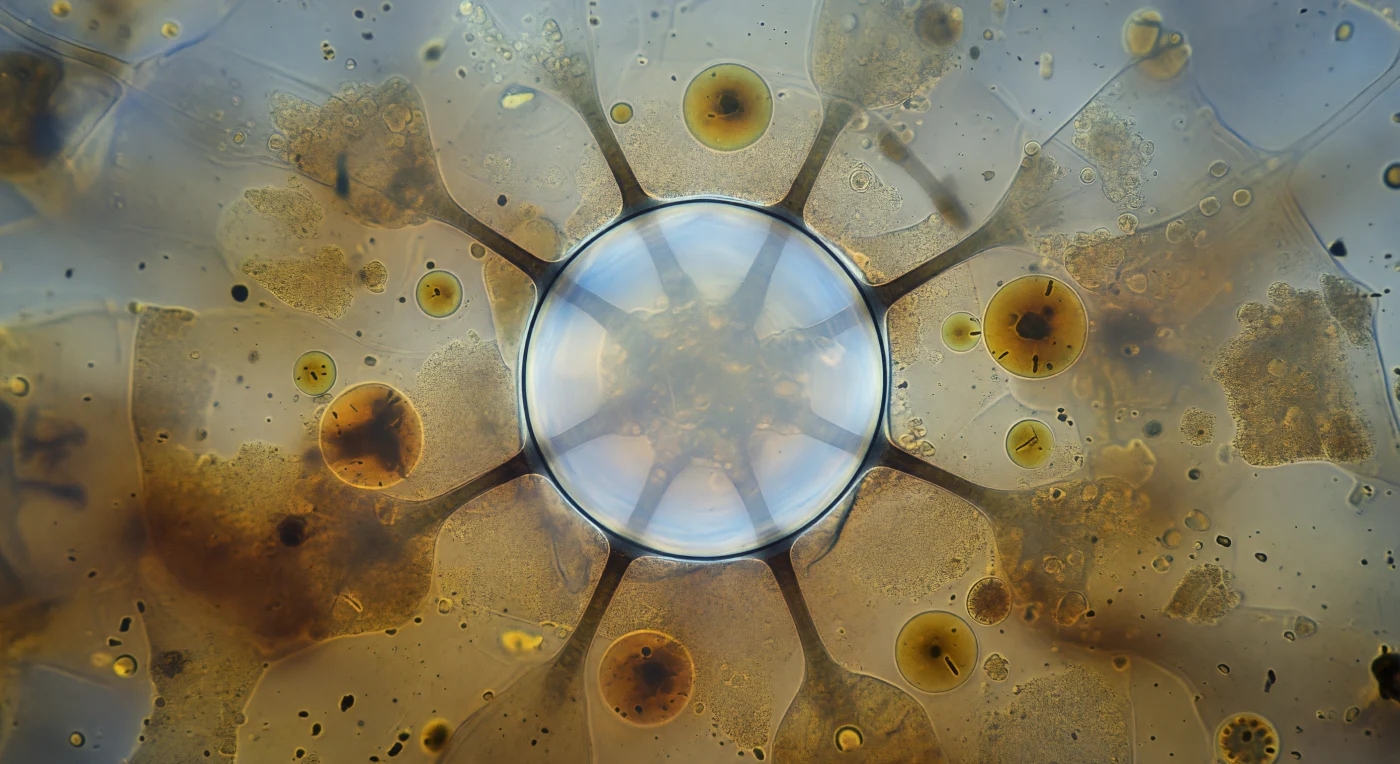
Wir befinden uns im Innern eines lebenden Einzellers, schwebend in der zähen Halbdunkelheit des Cytoplasmas von *Paramecium multimicronucleatum*, und die kontraktile Vakuole beherrscht das Blickfeld wie eine vollkommene Glaskuppel — dreißig Mikrometer im Durchmesser, ihre Membran kaum mehr als eine Silberlinie aus Oberflächenspannung, das gepresste Wasser in ihrem Innern mit einem blässlich-aquamarinblauen Glanz leuchtend, der aus der Reinheit des angesammelten osmotischen Drucks selbst zu kommen scheint. Sechs nephridiale Tubuli strahlen von ihrem Äquator aus wie dunkle Speichen, die sich in den granulären Nebel verlieren — röhrenförmige Kanäle aus gefalteter Membran, die in diesem letzten Atemzug vor dem Kollaps die äußersten Fäden cytoplasmatischen Wassers aus dem Endoplasma einsaugen. Die kontraktile Vakuole ist das osmoregulatorische Organ des Ciliaten: ein evolutionärer Kompromiss mit dem Süßwasser, das unaufhörlich durch die Plasmamembran eindringt und in rhythmischen Systolen hinausgepumpt werden muss, um die Zelle vor dem Platzen zu bewahren. Aus dem Mittelgrund driften unregelmäßige, bernsteinfarbene Nahrungsvakuolen heran — gefüllt mit den Geisterumrissen halb verdauter Bakterien, deren Zellformen im sauren Milieu lysosomaler Verdauung bereits zerfallen —, während das gesamte Cytoplasma in einem kaum wahrnehmbaren Druckstrom aus Granula und winzigen Mitochondrien langsam kriecht und das Bild von einem atemlosen Moment durchzogen ist: die Kuppel an ihrer äußersten Grenze, eine Millisekunde vor dem vollständigen, schlagartigen Zusammenbruch.
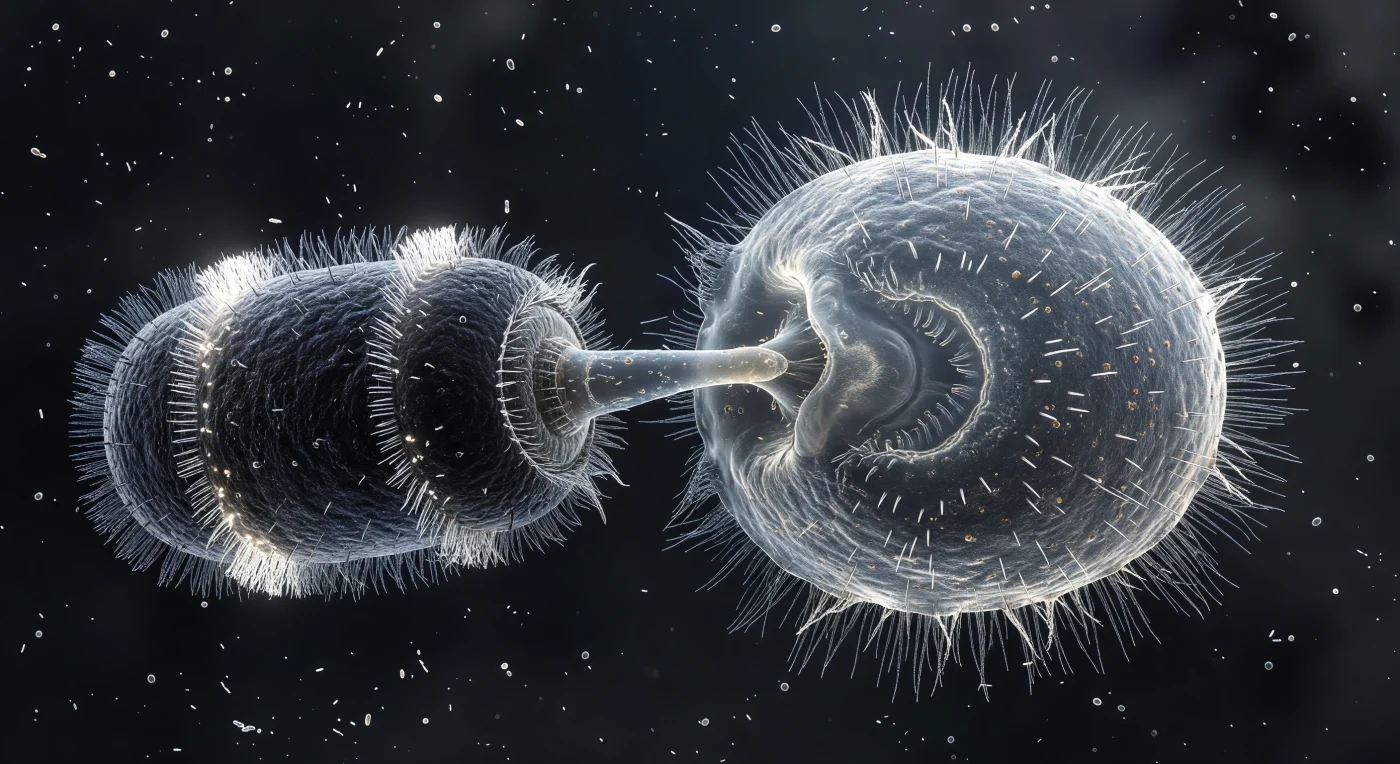
In der Mitte des Gesichtsfelds trifft ein gedrungener, fassförmiger Räuber auf seine Beute: Didinium nasutum hat seinen Rüssel vollständig ausgestreckt und presst dessen Spitze in die Flanke eines weit größeren Parameciums, dessen Pellikel an der Kontaktstelle sichtbar eingedellt und zu einer glasig-dünnen Mulde verformt ist. Als Antwort auf diesen mechanischen Einschlag hat das Paramecium binnen Millisekunden Tausende von Trichocysten entladen — feine Proteinfäden, die sich wie ein Strahlenkranz aus gesponnenem Glas mehrere Körperlängen weit in das umgebende Medium erstrecken und die Zelle in eine kalte, helle Explosionswolke hüllen. Die Wimperntracht des Parameciums ist aus dem geordneten metachronen Wellenschlag herausgerissen: einzelne Cilien spreizen sich seitwärts oder knicken zurück, ein Zeichen des akuten Fluchtverhaltens, das in der Realität nur zehn bis zweihundert Millisekunden dauert. Beide Organismen leuchten von innen — Zytoplasma, Nahrungsvakuolen in Bernstein- und Brauntönen, hyalines Ektoplasma — während ein feiner Schleier aus Bakterienstäbchen und -kokken im nahezu schwarzen Medium Tiefe erzeugt und daran erinnert, dass dieser Augenblick biologischer Gewalt sich in einem dreidimensionalen Flüssigkeitskontinuum ereignet, das auf diesen Längenskalen die Viskosität von Honig besitzt.

Dicht über dem Sediment schwebend, blickt man hinauf zu einer mächtigen, kreideweißen Kalkarchitektur, die das gesamte Blickfeld ausfüllt: das Gehäuse einer lebenden *Ammonia tepida*, einer Foraminifere, deren logarithmisch gestapelte Kammern im blaugrünen Durchlicht wie geschliffener Mondstein leuchten, die feinen Nähte zwischen den Kammern in präzisen Bögen verlaufen und die Apertур wie ein dunkler Höhleneingang wirkt, aus dem das Leben selbst herausdringt. Von dort breitet sich in alle Richtungen über den ockerfarben-trüben Meeresboden ein kaum sichtbares Netz feinster Reticulopoden aus — biprotoplasmatische Filamente, die durch bidirektionale Ströme bernsteinfarbener Organell-Granula verraten werden, welche in dichter Prozession zur Schale hin und von ihr fort fließen und das Reticulopodennetz als lebendige Transportinfrastruktur erkennbar machen. Links wird eine Diatomee mit ihren lichtbeugenden Silikatstrukturen von mehreren konvergierenden Strängen gehalten und millimeterweise, unmerklich langsam, wie in einem Netz aus lebendigem Glas, zur Apertур hin transportiert. Das Sediment zu Füßen besteht aus Quarzkörnern von Felsbrocken-Ausmaßen, Glimmerplättchen, die kalte Lichtblitze zurückwerfen, und von Bakterien besiedelten Kotpellets, während die gesamte Szene in jenem diffusen blaugrünen Schimmer badet, der das Wasser selbst als Lichtmedium enthüllt und die nahezu unsichtbare Geometrie der Geisterfalle spürbar macht, noch bevor man sie wirklich sieht.

Schau hinauf, und die gesamte Welt über dir ist aus bernsteinfarbenem Harz gegossen: der gewölbte Chitinpanzer einer *Arcella vulgaris* spannt sich wie ein flaches Iglu über den Blickraum, seine Wände halbtransparent und warmgolden leuchtend, wo das Durchlichtfeld durch die dünnsten Schichten fließt und an den dickeren Rändern zu tiefem Rostbraun abdunkelt. Das Material dieser Schale ist kein Mineral, sondern ein organisches Biopolymer – ein selbst abgesondertes Chitin-Proteingefüge, das dem Organismus eine starre, formstabile Hülle verleiht, während er sich darunter frei bewegt. Im Zentrum der Wölbung öffnet sich die Apertur: eine präzise kreisrunde Öffnung, von einem scharf abgesetzten Rand eingerahmt wie ein Tunnelmund, durch den vier hyaline Lobopodia langsam herabgreifen – glasklare, dickwandige Ektoplasmazylinder, deren Oberflächen im Licht schimmerig-bläulich schillern und in deren Innern winzige Granula wie eingeschlossene Staubteilchen treiben. Um dich herum schwebt das fragile Inventar eines nährstoffreichen Süßwassers: goldbraune Pflanzenreste, schwebende Bakterienstäbe, und die diffuse Helligkeit des Durchlichtmikroskops, das dieser Szene die warme Atmosphäre einer mit Harz-Glas überdachten Laterne verleiht.

Der Blick durch die leicht gewölbte, bernsteingolden schimmernde Pellicle eines *Paramecium bursaria* eröffnet eine Welt von überwältigender botanischer Dichte: Hunderte von *Chlorella*-Endosymbionten füllen das Cytoplasma so lückenlos mit ihren sattgrünen, münzförmigen Zellen, dass das Innere an ein von unten betrachtetes Blätterdach erinnert, bei dem die einzelnen Scheiben — jede etwa vier Mikrometer im Durchmesser — in gestaffelter Tiefe verblassen und die zwischen ihnen durchscheinenden Cytoplasmakanäle wie flüssiges, zitronengoldenes Licht leuchten. Diese Endosymbiose ist keine zufällige Vergesellschaftung, sondern eine vererbte, funktionelle Partnerschaft: Die Algen betreiben Photosynthese im Körperinneren des Wirts und versorgen ihn mit Kohlenhydraten, während *Paramecium* die *Chlorella*-Zellen vor Verdauung schützt und ihnen Nährstoffe und CO₂ liefert — ein vollständiges Miniatur-Ökosystem in einem einzigen Zellkörper von kaum 150 Mikrometern Länge. Das differentielle Interferenzkontrast-Licht modelliert jede Algenzelle zu einem dreidimensionalen Relief aus hellem Vorderrand und schattigem Halbmond, während tief im Inneren der nierenförmige Makronukleus als blassgrau-lavendelfarbene Lichtung inmitten des grünen Gewirrs auftaucht, ruhig und strukturgebend wie ein Auge im Sturm. An der äußersten Zellgrenze streift die Cilienkrone das durchfallende Licht zu einem silbrigen Hof aus zitternden Fäden — ein atmosphärischer Saum, der den harten Übergang zwischen lebendigem Organismus und dem wässrigen Außenmedium in etwas fast Atmosphärisches auflöst.
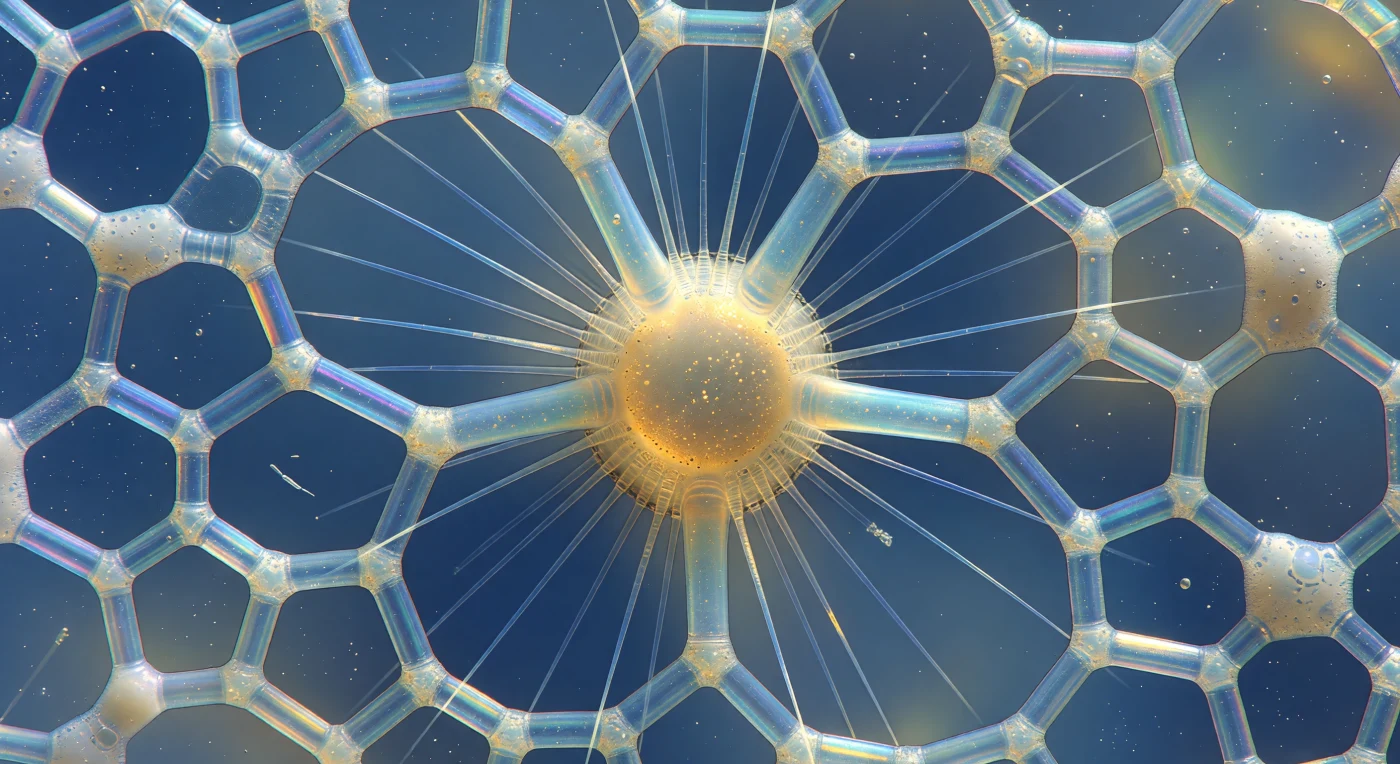
Die Welt, die sich vor dir entfaltet, ist eine aus reinem Mineralgehäuse gebaute Kathedrale: ein perfekt gefertigtes Gitterwerk aus amorphem Opal-Silizium, dessen einzelne Streben kaum zwei Mikrometer dick sind und dennoch das diffuse blaugrüne Tiefseelicht in schillernde Interferenzfarben zerlegen — violett an den spitzen Winkeln, kobaltblau entlang der breiten Balken, warmgolden an den verdickten Knotenpunkten. Jede hexagonale und pentagonale Pore ist ein Fenster in den offenen Ozean dahinter, und durch diese Öffnungen treibt gelegentlich ein Bakterium, das sich taumelnd um seine eigene Achse dreht und damit das wahre Ausmaß dieser Architektur unwillkürlich bezeugt. Dies ist das Skelett eines polyzystinen Radiolariers, eines einzelligen Organismus, der sein Silikatgehäuse durch biologische Selbstorganisation mit mathematischer Präzision aufbaut und darin Strontiumsulfat-Kristalle als Ballast sowie Lipidtröpfchen als Auftriebsreserve speichert. Vom zentralen Kapselmembran aus strahlen die Axopodien — steife, lichtbrechende Zytoplasmafortsätze, gestützt durch ein Axonem aus parallel angeordneten Mikrotubuli — wie kristallene Nadeln in alle Richtungen, während zwischen den äußersten Skelettspitzen ein unregelmäßiger Saum vakuolisierten Ektoplasmaplasmas haftet, dessen winzige Bläschen die Interferenzfarben des Gitters zu flüchtigen Lichtpunkten bündeln und wieder auflösen.

Der Blick gleitet knapp über einen Sedimentboden, der sich bis zu einem diffusen, leuchtenden Horizont erstreckt – ein endloses Trümmerfeld aus geometrisch vollkommenen Glassplittern, jedes Fragment die leere Schale eines einzelligen Lebewesens, das Jahrhunderte oder Jahrtausende zuvor gestorben ist. Zylindrische Frustulen liegen gestürzt wie Marmorsäulen eines versunkenen Tempels, ihre Porenarrays – jede Perforation schmaler als eine Lichtwellenlänge – verwandeln den einfallenden Schimmer in kobaltblaue und goldene Interferenzfransen, die sich über den Silt verschieben, sobald der Beobachter auch nur um Bruchteile seine Perspektive ändert. Das Material selbst ist amorphes Opal-Siliziumdioxid, von lebenden Kieselalgen über enzymatisch gesteuerte Biomineralisation aus gelöster Kieselsäure des Wassers präzipitiert, so dass jedes dieser geometrischen Objekte – Cyclotella-Trommeln, naviculoide Schiffskiele, sternförmige Triceratium-Dreiecke – eine biologische Ingenieurleistung von kristallographischer Präzision darstellt. Im Mittelfeld treibt ein Actinophrys-Heliozoon wie ein schwebender Kronleuchter zwischen den Ruinen, seine axopodialen Strahlen – durch Axonem-Mikrotubulibündel versteift und faseroptisch das blaue Durchlichtleuchten einfangend – in alle Richtungen ausgestreckt, während bernsteinfarbene Flagellaten mit kaum sichtbaren Geißelschlägen die Korridore zwischen den Frustulentürmen durchqueren. Die Stille dieses Feldes ist trügerisch: was als mineralische Ruinenlandschaft wirkt, ist zugleich ein aktiver Lebensraum, in dem chemische Gradienten, Brownsche Molekularbewegung und die viskosen Kräfte des Wassers jeden Millimeter des Raums zwischen den Glastrümmern physikalisch strukturieren.
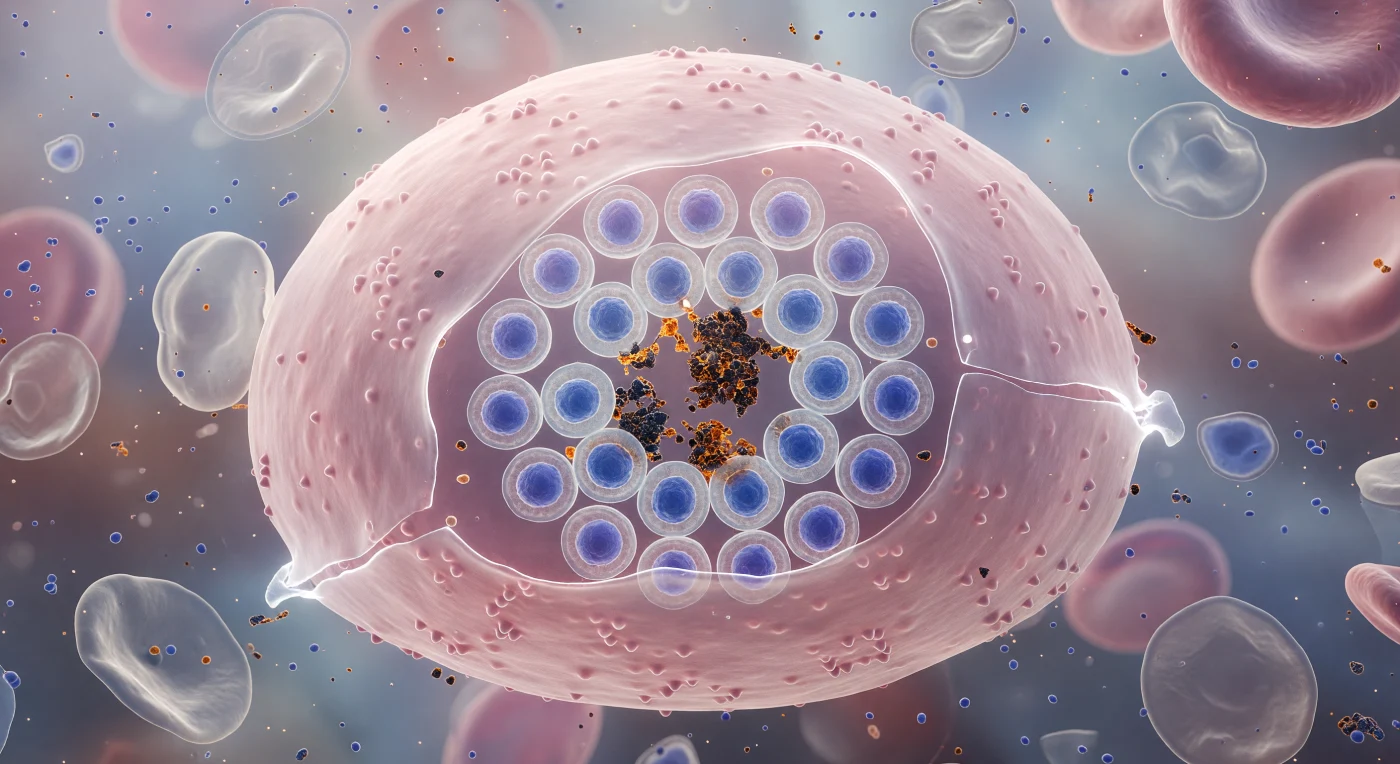
Die gesamte Szene ist eine einzige Sekunde vor dem Zerfall erstarrt: Man schwebt unmittelbar vor der geschwollenen Außenmembran einer infizierten roten Blutzelle, einem riesigen, blassrosa gewölbten Dom, dessen Lipiddoppelschicht an den dünnsten Stellen zu einer fast transparenten Hülle ausgedünnt ist und kaltes Licht wie hinterleuchtetes Glas durchlässt. Im Inneren ist die gesamte Wirtszelle von vierundzwanzig *Plasmodium falciparum*-Merozoiten besetzt, die sich in einer geometrisch präzisen Rosette anordnen — jeder Parasit ein kompaktes Oval mit tiefkobaltblauem Kern, der sich von seinem blassen zytoplasmatischen Hof absetzt, das Ganze ein lebendiges Rad aus Invasion und Verdichtung. Im Zentrum dieser Anordnung liegen Klumpen aus Hämozoin-Malariapiement, dunkelbraune, kristallisierte Rückstände der Hämoglobin-Verdauung, hart und unveränderlich wie gesplitterter Bernstein, die einzigen Strukturen, die den bevorstehenden Zerfall überdauern werden. Die Membranoberfläche ist mit charakteristischen Proteinknoten übersät — erhöhten Auswölbungen, entstanden durch vom Parasiten exportierte Proteine, die das Zytoskelett des Wirts umgebaut haben — während benachbarte Geisterzellen, bereits geplatzt und leer, als faltige, matte Hüllen im biochemisch getrübten Medium treiben. Die chromatische Spannung zwischen dem warmen Lachsrosa der sterbenden Membran und dem kühlen Juwelblau der dagegen drängenden Parasitenkerne ist zugleich von bedrängender Schönheit und unausweichlicher Gewalt.

Die Welt unter dir erstreckt sich in alle Richtungen wie ein erdfarbenes Kontinent: Die Theka von *Ceratium tripos* bedeckt deinen gesamten Horizont, ihre cellulosischen Platten in warmem Bernstein und gebrannter Siena leuchtend, während das kühle blaugrüne Durchlicht des DIC-Mikroskops von unten durch das lebendige Zellinnere filtert und jeden polygonalen Panzer zu einer strahlenden Kachel aus organischem Gold verwandelt. Die Nahtlinien zwischen den Platten verlaufen wie tektonische Schollengrenzen, scharf und geometrisch präzise, ihre erhöhten Grate werfen schwache Schatten auf die gefurchten Oberflächen darunter, die ihrerseits von parallelen Mikrorippen und regelmäßig gesetzten Poren durchzogen werden — eine zelluläre Architektur, die mit der Sorgfalt von Sedimentgestein geschichtet ist. Quer durch das Bildfeld schneidet der äquatoriale Cingulum wie ein tiefer Canyon aus Kobaltindigo, seine Wände senkrecht in die Dunkelheit abfallend, während in seinem Schatten das Querflagellum wie ein schlafendes Band liegt, kaum sichtbar als schwacher irisierender Faden im Blaudunkel. Am linken Bildrand steigt ein monumentales Apikal-Horn aus demselben Bernsteinmaterial auf, krümmt sich majestätisch aus dem Rahmen und lässt seine Spur als langen Schatten über die angrenzenden Theka-Platten fallen — ein lebendiges Skelett aus Cellulose, das dieser einzelligen Zelle die geometrische Würde eines Architekturdenkmals verleiht.
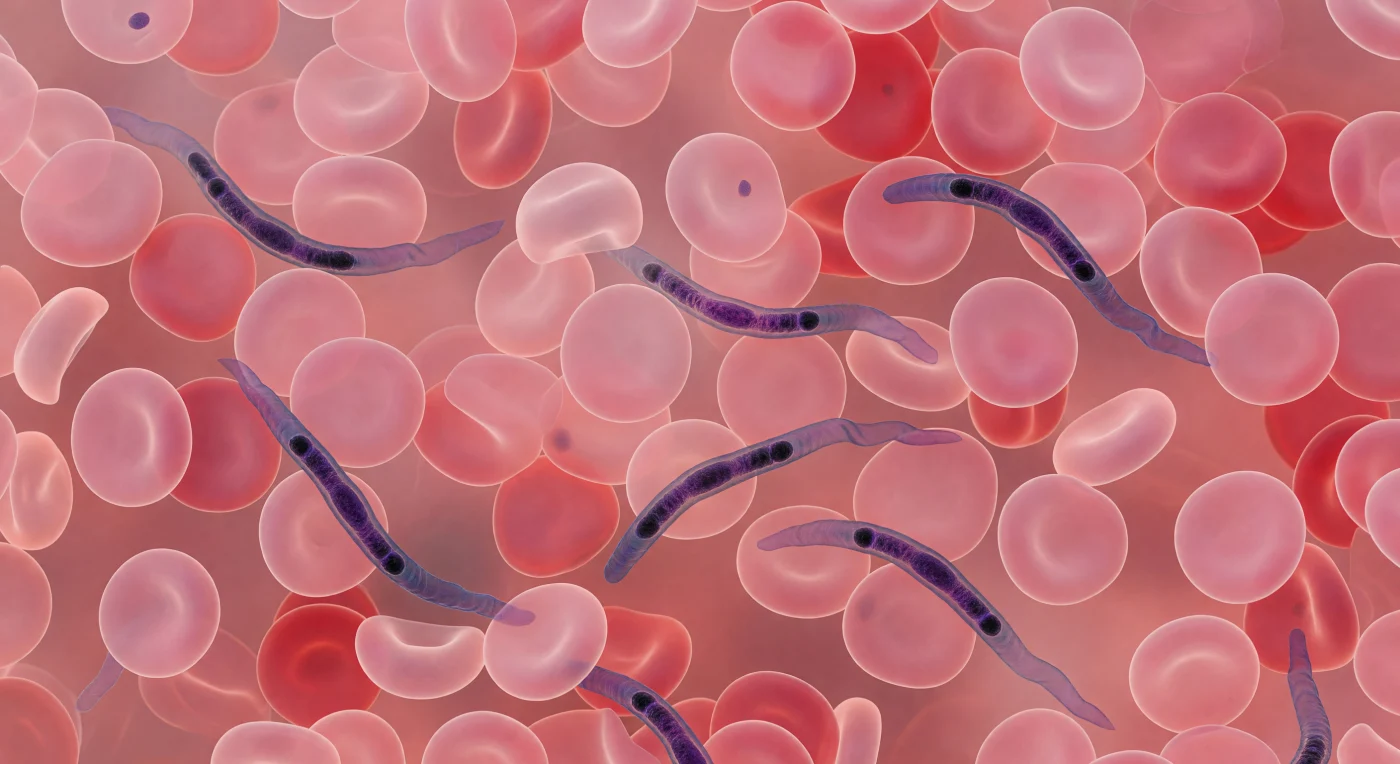
Der Blick öffnet sich in ein klaustroph obisches Universum aus roséfarbenen Scheiben — jede Erythrozyte ein weiches, bikonkaves Kissen, an seinem gedünnten Zentrum von einem warmen Lichtschimmer durchdrungen, an seinem Rand zu einem tieferen Karminring verdickt —, die sich in jede Richtung stapeln und drängen, bis das gesamte Gesichtsfeld zu einer endlosen fleischfarbenen Tapete verschwimmt. Zwischen diesen Scheiben winden sich mehrere Trypanosoma brucei wie lebendige Kalligraphie: ihre 15 bis 30 Mikrometer langen Körper tief blauviolett gegen den rosafarbenen Grund, angetrieben von einer wellenartig flatternden Flagellarmembran, die sich wie ein seidenes Band an ihrer Flanke entlangkräuselt und bei jeder Wellenausbreitung in Lavendel und Indigo aufleuchtet. Innerhalb jedes Parasitenkörpers markieren dichte chromatische Kondensationen den Zellkern in der Körpermitte sowie den kompakten, fast schwarzen Punkt des Kinetoplasts am hinteren Ende — jenes mitochondriale DNA-Depot, das Trypanosoma als Kinetoplastida auszeichnet und das Ziel moderner Antiparasitika ist. Die Giemsa-Färbung sättigt die gesamte Szene mit ihrer charakteristischen Stahl-Violett- und Karminpalette, während das biologisch-diffuse Licht durch das Plasma fällt wie durch Bernsteinsglas und jede Zelle mit einem zarten Glanzpunkt auf ihrem Rand hervorhebt — eine intime, schwebende Stille, durch die sich die Trypanosomen wie Schlangen zwischen Felsen hindurchschlängeln, ihre Membranwellen das einzige gerichtete Bewegen in einer Welt aus sanftem Druck und gedrängtester Enge.

Mitten in der Neustonschicht eines Teiches — jener wenige Hundert Mikrometer dünnen Welt unmittelbar unter der Wasseroberfläche — schwebt man inmitten einer Gemeinschaft lebender Körper, die das bernsteinfarbene Nachmittagslicht in hundert verschiedene Richtungen brechen und streuen. Die Unterseite der Oberflächenspannung wölbt sich wie eine quecksilberne Decke über allem, ein zitterndes Spiegeldach, das jeden nach oben gestreuten Photon zurückwirft und dabei kausale Lichtbänder erzeugt, die wie langsame Scheinwerfer über die treibenden Organismen gleiten. Vor einem drängen sich Euglena-Spindeln — smaragdgrüne, metallisch schimmernde Torpedos mit einem Pellicle aus spiralförmig angeordneten Proteinstreifen, die das Licht in feine Beugungsfarben zerlegen —, während zwischen ihnen Chlamydomonas-Zellen wie kleine Jade-Laternen leuchten, jede mit einem ziegelroten Augenfleck aus gebündelten Carotinoidgranula, dem gesättigtsten Farbpunkt im gesamten Bild. Coleps-Zellen taumeln als geometrisch gepanzerte Tonnen durch das Gewimmel, ihre Calciumcarbonat-Plättchen fragmentieren das Licht in winzige Glanzpunkte wie gesplittertes Porzellan, während dahinter Chilomonas-Zellen als bläulich-weiße, fast glasklare Ovale treiben und der allgegenwärtige Bakterienrauch die Tiefe in ein weiches, kühles Dämmern auflöst. Diese ganze Szene ist kein Zufall, sondern das Ergebnis phototroper Vertikalwanderung, chemischer Gradienten und der niedrigen Reynolds-Zahlen einer Mikrowelt, in der Trägheit keine Rolle spielt und jede Bewegung unmittelbar von der Viskosität des Wassers gedämpft wird — ein perpetuum mobile aus Flagellen, Cilien und fließenden Pseudopodien, eingefroren in einem einzigen goldenen Augenblick.

Aus den orangefarbenen Tiefen des eigenen Körpers schaut man heraus: Chitinplatten, warm bernsteinfarben und leicht irisierend, rahmen das Blickfeld wie die Bleifassung eines Kirchenfensters, während dahinter das kalte Blaugrün des offenen Meerwassers liegt, durchzogen von treibenden Partikeln und dem diffusen Schimmer organischer Schwebstoffe. Fast unsichtbar — und gerade deshalb so unheimlich — spannen sich die Retikulopodien von *Globigerina bulloides* in alle Richtungen, fadenförmige Strukturen von kaum 0,2 bis 0,5 µm Durchmesser, die sich nur durch das ununterbrochene, perlschnurartige Fließen von Organellen und Vesikeln entlang ihrer Länge verraten, eine Art granularer Verkehr, der stetig auf die kreideweiße Kalzit-Schale in der blauen Ferne zuströmt. Jene Schale — vielschichtig gekammert, mineralisch matt glänzend, vier- bis fünfmal so groß wie der gefangene Nauplius — dominiert den Hintergrund wie eine mittelalterliche Festung aus Kalziumkarbonat, kühl und gleichgültig, während ihre Fäden sich geometrisch präzise zusammenziehen, jeder Strang leicht versteifend, die Gesamtbewegung so langsam wie das Schließen einer Hand. Es gibt keinen Lärm, keine Hast, keine Gnade — nur die stille Mechanik eines Netzes, das längst zugezogen ist.

Im blauen Herz des offenen Ozeans, zwanzig Meter unter der Oberfläche, blickt man aufwärts in eine Kathedrale aus kobaltblauem Licht – Sonnenstrahlung, die durch das Meerwasser auf eine einzige Wellenlänge von 460 Nanometern reduziert wurde und nun in sanften, volumetrischen Schäften herabströmt. Durch dieses leuchtende Blau schweben Acantharier wie explodierte Sterne in der Stille: Jede Zelle trägt zwanzig radial ausstrahlende Spiculae aus Strontiumsulfat, deren Kristallgitter das einfallende Licht in prismatische Koronen aus Eisweiß, blassem Violett und spektralem Gold zersplittern, während feine Axopodien zwischen den Mineralstäben wie Seidenfäden im Blau zittern. Verstreut zwischen diesen geometrischen Strahlensystemen hängen Tintinniden-Loricae in schrägen Winkeln – glasklare, vasenförmige Hüllen aus agglutinierten Coccolithen, an ihrer offenen Mündung kaum aufgelöste Wimpernkränze als leuchtender Bewegungshauch angedeutet. Dazwischen treiben bernsteinfarbene und cremefarbene Marineschnee-Flocken aus Schleim und Detritus träge durch das Sichtfeld, ihre weichen, organischen Konturen ein stiller Gegensatz zur kristallinen Präzision der Spiculae – gemeinsam bilden sie eine lebendige Lichtsäule ohne sichtbaren Boden und ohne sichtbare Decke.

Über einer ausgetrockneten Teichsohle erstreckt sich eine polygonale Landschaft aus Tonplatten, deren Bruchkanten wie Schluchten in den Schatten abfallen — ein Wüstenplateau in Miniatur, dessen Oberfläche aus verdichtetem Mineralkorn und eingetrocknetem organischen Material besteht, aufgebrochen durch die Physik des Wasserentzugs in ein Mosaik aus Sienna, Ocker und tiefem Umbra. In diesen rauen Untergrund gebettet liegen die Zysten der Protisten wie handgeschliffene Juwelen: Die Colpoda-Zysten ruhen als doppelwandige Bernsteinkugeln auf den Platós, ihr äußerer Chitinmantel von einem hauchfeinen Flüssigkeitsspalt vom inneren Membransack getrennt, sodass jede Kugel im schrägfallenden Licht einen zarten Lichtsaum trägt, der lebende Komplexität verrät, während der Organismus dahinter seinen Stoffwechsel auf nahezu null gedrosselt hat. Arcella-Gehäuse — chitinbraune Halbkuppeln, deren Mündungen mit einem blassen Zystenwall verschlossen sind — sitzen an den Rissrändern wie versiegelte Helme, ihre Protein-Untereinheiten als winzige geometrische Textur spürbar, und zwischen ihnen breiten sich Euglena-palmella-Kolonien in eingetrocknetem Schleim aus: olivgoldene, crinklige Folien, die sich an ihren Rändern vom Substrat lösen und im streiflichten Licht einen biologischen Glanz zeigen, der sich klar vom matt-mineralischen Chaos ringsum absetzt. Diese Überlebensformen sind keine passiven Relikte, sondern hochentwickelte Konstrukte — doppelte Membranen, biochemisch inerte Hüllstoffe, kondensiertes Chromatin — die auf den nächsten Wasserfilm warten, um die Uhr wieder anlaufen zu lassen.




















