
Vous flottez au bord d'un canyon en spirale d'une ampleur écrasante — le sillon buccal d'un *Paramecium caudatum* — dont les parois de verre vivant s'incurvent de chaque côté comme les gradins d'un amphithéâtre taillé dans la matière cellulaire elle-même, la pellicule environnante captant la lumière disponible comme une membrane argentée et métallique, striée de crêtes protéiques longitudinales parcourant l'ectoplasme en bandes parallèles. Des milliers d'organites ciliaires — membranelles et cirres disposés en rangées serrées — battent en vagues métachronales synchronisées qui dévalent les parois du canyon comme des déferlantes lumineuses, chaque cycle de frappe se propageant vers le bas en une iridescence ondulante, chariant dans le vortex induit des bactéries en bâtonnets translucides qui pivotent sur elles-mêmes et spiralent inexorablement vers la fosse cytostomale, cette ouverture de noirceur absolue qui pulse faiblement au fond. Au-dessus, la paroi cellulaire translucide s'arque en dôme de verre dépoli, et à travers elle le macronoyau rayonne d'un ambre chaud — une présence réniforme imposante, rétroéclairée par la luminosité granulaire diffuse du cytoplasme — pendant que plus profondément dans l'endoplasme, des vacuoles digestives dérivent comme des nuages sombres à différents stades d'une digestion dont l'alchimie enzymatique, silencieuse et inexorable, se mesure non en sons mais en gradients chimiques et en pression mécanique.

Vous planez en dessous d'une colonne vivante d'*Euglena viridis* qui s'élève vers la lumière, chaque cellule fuselée de soixante micromètres traçant une spirale ascendante dont la pellicule protéique capte le jour diffus filtré depuis la surface en éclairs successifs d'émeraude et de chartreuse. La phototaxie positive qui gouverne ce rassemblement est orchestrée par le stigma, cette tache oculaire terracotta visible près de l'apex antérieur de chaque cellule — un organite photorécepteur qui module le battement du flagelle selon l'intensité et la direction de la lumière, guidant l'organisme vers la zone euphotique où la photosynthèse est la plus productive. Le milieu lui-même n'est pas un simple liquide mais un bouillon chlorophyllien jaune-vert parcouru de tressaillements browniens, dans lequel chaque corps cellulaire agit comme une lentille convergente faible, déviant la lumière ascendante et créant sur sa surface aborale de minuscules secondes brillances qui font paraître la colonne entière auto-luminescente. La masse des chloroplastes en rubans hélicoïdaux, visibles à travers la membrane translucide comme une architecture de jade feuilleté, rappelle que ces eucaryotes unicellulaires pratiquent à la fois la photosynthèse oxygénique et une motilité flagellaire sophistiquée — une double stratégie trophique que les biologistes nomment mixotrophie. En dessous de vous, la brume vert-olive s'épaissit vers une obscurité dense et immobile, là où aucune cellule n'est plus visible et où le poids chimique du milieu semble absolu.

Vous êtes écrasé contre un cimetière de silice — des fragments de frustules de diatomées brisées dont les réseaux de pores hexagonaux captent la lumière comme des éclats de vitrail enchâssés dans un sédiment sombre et organique. Au-dessus de vous, un événement architectural unique submerge le regard : le pseudopode d'*Amoeba proteus* s'avance comme un glacier coulé dans du verre vivant, son capuchon hyalin d'une transparence optique parfaite concentrant la lumière ambiante en arcs dorés et chauds qui voyagent sur le substrat en avant de lui, annonçant sa progression comme le soleil précède le bord d'un nuage. À l'intérieur de ce conduit biologique, l'endoplasme jaillit en torrent — une rivière granuleuse de bronze liquide et d'ambre profond chargée de vacuoles alimentaires, de mitochondries brillant comme des éclats de cuivre, la frontière sol-gel scintillant en une frange d'interférence iridescente, lavande pâle et or doux, là où le cytoplasme se convertit en temps réel de l'état fluide à la paroi rigide de l'ectoplasme. La lumière traversant la masse du pseudopode projette sur le cimetière de diatomées des réseaux caustiques pulsants, tandis que l'ensemble du corps de l'amibe — ce grand tremblement de cytoplasme ambré — se fond loin en arrière dans la brume végétale tiède de la colonne d'eau, chaque membrane un film arc-en-ciel, chaque granule un joyau captant son propre spectre privé à l'intérieur d'une seule cellule en mouvement.
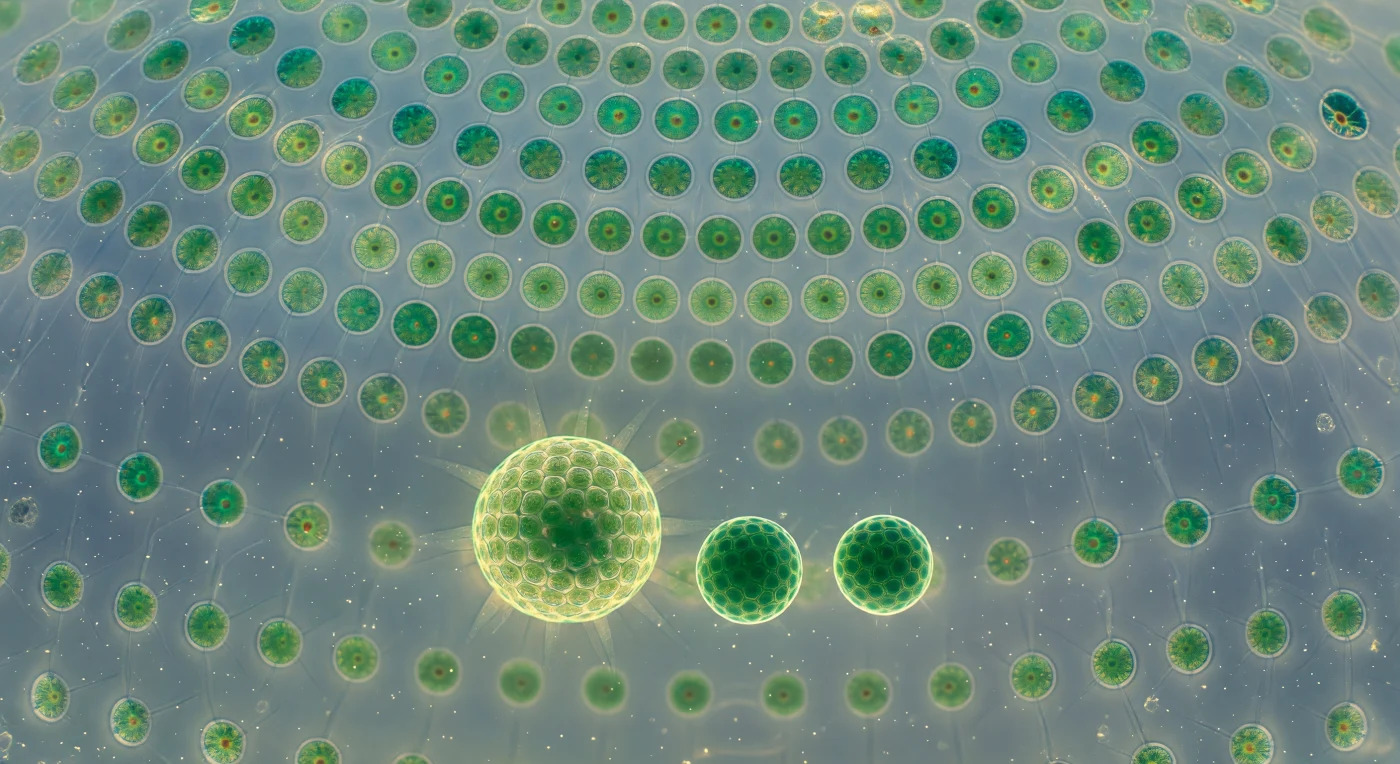
Au centre géométrique de cette sphère vivante, le regard s'élève vers une voûte de verre organique dont la courbure se perd dans une profondeur lumineuse : des milliers de cellules somatiques biflagellées s'inscrivent dans la paroi de glycoprotéines translucide comme des émeraudes sertiesn dans de l'ambre pâle, chacune reliée à ses voisines par des filaments cytoplasmiques d'une ténuité presque irréelle, qui ne se révèlent qu'en captant la lumière comme de fines lignes d'argent. Cette architecture coordonnée est celle d'un organisme colonial eucaryote, *Volvox globator*, dont les quelques milliers de cellules somatiques partagent une matrice extracellulaire commune et synchronisent le battement de leurs flagelles en une onde métachronale continue — une aurore d'émeraude qui parcourt la face interne du dôme en lentes pulsations et entraîne la rotation de l'ensemble de la sphère dans la colonne d'eau. Chaque cellule porte en elle un unique point de rouille ardente, l'eyespot, organe photorécepteur orientant la nage de la colonie vers la lumière selon un gradient chimiosensoriel collectif. Suspendues dans le fluide aqueux de la cavité interne, trois colonies filles de tailles décroissantes dérivent comme des planètes retenues dans une châsse de cristal — la plus grande déjà pourvue de sa propre paroi frémissante, la plus petite encore immobile, sphère de cellules en attente d'un battement qui n'a pas encore commencé.

Dans l'obscurité absolue de l'océan profond, là où aucun photon solaire n'a jamais pénétré, une explosion froide et céruléenne déchire le néant : une cellule de *Noctiluca scintillans* vient de décharger ses organelles à luciférine, libérant une lumière à 490 nanomètres qui révèle l'espace d'un dixième de seconde la sphère gélatineuse translucide, sa large vacuole centrale luisant comme une lanterne de verre dépoli, son mince film membranaire courbant la lumière en un bref halo avant que les ténèbres ne confisquent tout. La décharge mécanique se propage dans l'eau visqueuse et déclenche une réaction en chaîne : cellule après cellule s'embrase à son tour, chaque flash révélant un instant la silhouette d'une sphère voisine, le filament fin d'un tentacule, l'ombre d'une vacuole digestive contenant un reste de diatomée à demi dissous, avant que l'obscurité ne se referme avec une brutalité totale. Entre les détonations lumineuses, des flocons de neige marine — agrégats de mucus et de frustules brisées — dérivent en silence, et parfois l'un d'eux entre dans le faisceau d'un nouvel éclair et diffuse la lumière céruléenne en un halo brumeux fugace, rappelant que cette eau noire n'est pas vide mais peuplée d'une matière organique en suspension constante, un océan vivant que seul le feu froid de ces organismes unicellulaires rend, par intermittence, visible.

Suspendu au bord exact du disque oral, on plonge le regard dans la gorge spiralée d'un *Stentor coeruleus* : un vortex vivant de plusieurs centaines de micromètres de diamètre, tapissé de membranelles translucides qui battent en concert pour aspirer l'eau environnante vers un puits cytostomal sombre comme le fond d'un abîme. La jante du disque irradie d'un bleu-vert froid, les granules de stentorine disposés en striations parallèles alternant Prusse profond et aigue-marine pâle sous la pellicule semi-rigide, tandis que des tiges bactériennes et des algues verdâtres tourbillonnent en spirale logarithmique avant de disparaître dans le funnel cellulaire. Sous le disque, le corps en colonne cobalt s'enfonce dans la brume ambrée du milieu aqueux, sa transparence laissant deviner un ruban de lobes opalescents — le macronoyau en chapelet — qui file verticalement à travers l'endoplasme granuleux, ponctué de vacuoles digestives brun-ambre à différents stades. Tout autour du vortex, des frustules de diatomées et des protistes plus petits dérivent à la lisière du courant, satellites maintenus en orbite précaire à l'exact équilibre entre la traînée visqueuse du milieu — ici l'inertie ne compte plus rien — et la succion inexorable des cils en mouvement.
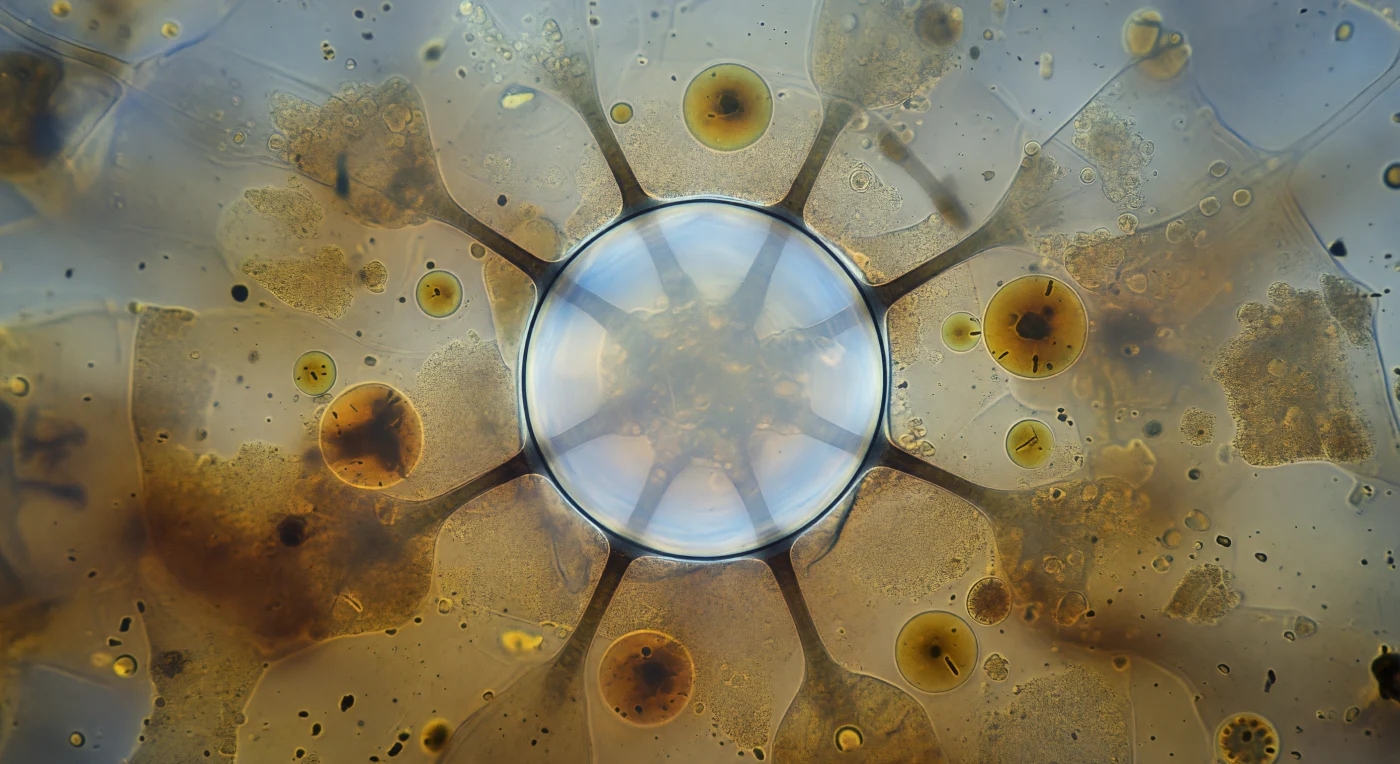
Au cœur de ce monde translucide et visqueux, la vacuole contractile occupe le champ comme une coupole de verre vivant — sphère de trente micromètres suspendue dans la tension absolue de sa propre pression osmotique, membrane si mince qu'elle n'existe qu'à peine, juste un frémissement argenté séparant l'eau pure et lumineuse de l'intérieur du cytoplasme ambré et grenu qui presse de toutes parts. Six tubules néphridiens rayonnent depuis son équateur comme des rayons sombres se perdant dans le brouillard granulaire de l'endoplasme, chacun ayant acheminé pendant de longues secondes les derniers volumes d'eau cytosolique vers cette chambre de collecte, accomplissant le travail fondamental de l'osmorégulation dans un organisme dépourvu de tout rein, de toute membrane basale, de tout épithélium de transport. Les vacuoles alimentaires dérivent dans le champ moyen — sphères irrégulières d'ocre et d'ambre contenant les fantômes de bactéries à demi digérées, leurs intérieurs assombris là où la chimie lysosomale a déjà accompli sa dissolution silencieuse. L'ensemble de la scène est chargé d'une tension proprement physique : la membrane vacuolaire, portée à sa courbure limite, ne tient plus qu'à l'équilibre précaire entre la pression hydrostatique intérieure et la résistance élastique du film lipidique — et dans une fraction de milliseconde, tout ce volume, toute cette lumière contenue, s'effondrera vers le pore excréteur dans une systole totale et instantanée, expulsant l'eau en excès hors de la cellule avant que le cycle recommence, inlassablement, toutes les dix à soixante secondes, pour toute la durée de cette vie minuscule et précise.
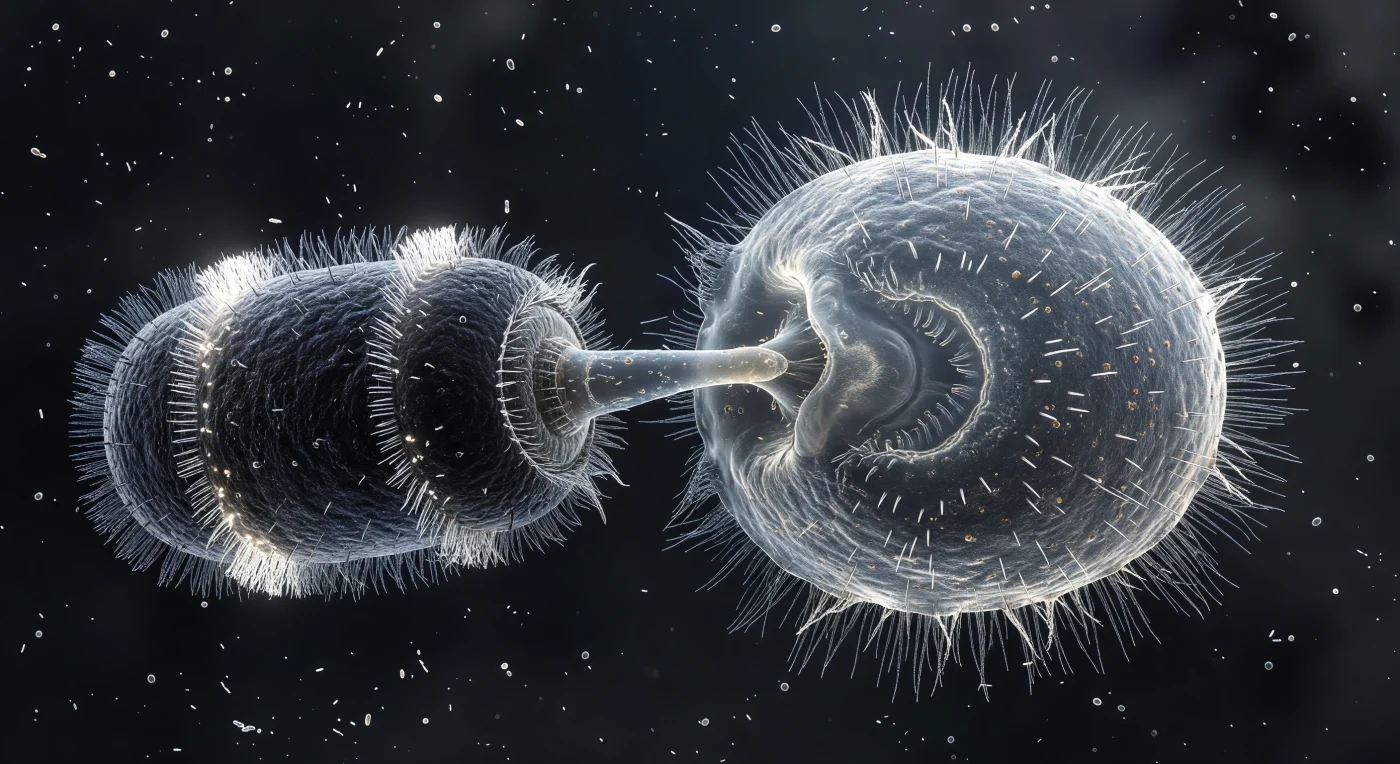
Au centre gauche du champ, un cylindre sombre bandé de deux couronnes ciliaires lumineuses s'est projeté contre un organisme voisin : c'est un *Didinium nasutum* dont la trompe, entièrement déployée, s'enfonce dans le flanc translucide d'un *Paramecium caudatum*, creusant une concavité vitreuse là où la pellicule se déforme sous la pression mécanique. En réponse à ce contact catastrophique, le paramècie a déclenché en une fraction de seconde la décharge simultanée de ses trichocystes — des milliers de filaments protéiques cristallins, normalement rangés en fuseau sous la membrane, qui se dévissent explosivemen dans le milieu aqueux pour former un halo radiant de fils de verre figés à leur extension maximale, défense évolutive qui n'arrêtera pourtant pas ce prédateur spécialisé. Les cils du paramècie, rompant leur onde métachronale coordonnée, se sont éparpillés en une frange désordonnée de battements inversés — réflexe de fuite enclenché trop tard, capturé ici à l'échelle de la dizaine de millisecondes. Dans le vide charbonneux alentour, une brume bactérienne de bâtonnets et de coques dérive en suspension à différents plans focaux, rappelant que cet instant de prédation se joue dans un milieu à nombre de Reynolds infinitésimal, où la viscosité gouverne tout mouvement et où la violence biologique se mesure en micronewtons.

Au ras du sédiment, sous une lumière bleue-verte froide qui semble émaner de l'eau elle-même plutôt que d'une source identifiable, l'architecture calcaire d'une *Ammonia tepida* se dresse comme un monument de craie sculptée — ses chambres globulaires empilées en spirale logarithmique luisent d'une blancheur laiteuse presque minérale, leurs parois légèrement translucides laissant deviner l'ombre chaude du cytoplasme intérieur, et l'aperture s'ouvre à la face ombilicale comme la bouche d'une caverne bordée de matière organique ambrée. Rayonnant depuis cette ouverture vivante dans toutes les directions sur la surface du sédiment, le réseau de réticulopodes se déploie en une architecture fantôme presque invisible — des filaments de verre étiré qui ne trahissent leur existence que par les granules organellaires ambrés circulant en processions bidirectionnelles le long de leurs autoroutes transparentes, certains convergeant vers la coquille, d'autres s'en éloignant, transformant ce piège en pur mouvement. À gauche, une frustule de diatomée — ses parois de silice gravées de réseaux de pores nanométriques qui dispersent de furtifs éclats prismatiques — est maintenue par plusieurs brins convergents et lentement convoyée vers l'intérieur, comme une proie prise dans une toile d'araignée faite de verre vivant. Les grains de sédiment autour de soi ont des dimensions de rochers — quartz ronds, lamelles de mica aux surfaces de miroir, pelotes fécales colonisées par une brume grise de bactéries trop petites pour être résolues individuellement — et le tout baigne dans cette lumière diffuse et enveloppante qui transforme la calcite en pierre de lune et rend le monde entier sensible non par la vue, mais par le mouvement de ce qui le traverse.

Suspendu dans l'eau douce trouble, regard levé vers le haut, on contemple la face intérieure d'un édifice vivant : le test d'*Arcella vulgaris*, une coupole de chitine organique teintée d'ambre qui s'étend d'un bord à l'autre de l'horizon visible, semi-transparente, laissant filtrer la lumière transmise en une lueur chaude dorée là où ses parois s'amincissent, s'assombrissant vers un bourrelet équatorial épais et profond. Au centre exact de cette voûte, l'ouverture aperturale descend comme un puits circulaire bordé d'un liseret chitineux plus sombre, un portail d'à peine cinquante micromètres de diamètre à travers lequel quatre lobopodia hyalins s'avancent lentement vers le bas — cylindres d'ectoplasme absolument transparents, presque vitreux, captant la lumière en un éclat bleu-blanc froid qui contraste avec la chaleur ambrée de la coque. Ces pseudopodes progressent au rythme d'un à dix micromètres par minute, une extension quasi géologique à cette échelle, gouvernée non par l'inertie mais par la viscosité dominante d'un monde à très faible nombre de Reynolds, où l'eau elle-même se comporte comme un milieu épais et résistant. Autour, des fragments de matière organique décomposée dérivent dans l'illumination diffuse, et le détritus brunâtre du substrat rappelle que cette créature d'une centaine de micromètres vit tapissée contre un fond où elle se nourrit par phagocytose, tendant ses lobopodia vers des proies bactériennes invisibles à cette résolution.

Vous vous trouvez suspendu à la surface incurvée d'un *Paramecium bursaria*, la pellicule se dressant devant vous comme une verrière de cathédrale aux nervures d'ambre pâle — une membrane architecturale tendue dont les stries longitudinales captent la lumière transmise en fines lignes d'argent, frontière translucide entre l'eau extérieure et un monde intérieur d'une densité végétale stupéfiante. Au-delà de cette paroi, des centaines de *Chlorella* — chacune un disque de chlorophylle d'à peine quatre micromètres, sculpté par la lumière en contraste interférentiel en une monnaie vert forêt à demi-éclairée — tapissent le cytoplasme si étroitement que l'intérieur ressemble à une canopée vue d'en dessous, une voûte continue de vert saturé qui n'est que la traduction visible d'une symbiose photosynthétique transmise de génération en génération, chaque Chlorella fournissant des sucres à son hôte en échange d'un abri métabolique. Là où la population de symbiontes se fait légèrement moins dense, la lumière traverse en canaux citrins et ambrés — le sol cytoplasmique glissant entre des vacuoles réfractantes comme une rivière dorée dans une forêt trop serrée — et au centre, le macronucleus émerge en clairière lavande, pâle et granuleux, entouré de toutes parts par la forêt verte. À la périphérie extrême, les cils vibrant sur la pellicule extérieure ne sont plus que lumière : une frange argentée et atmosphérique, comme des embruns retenus un instant avant de retomber, signalant à chaque battement — vingt à quarante fois par seconde — que cette architecture intérieure monumentale n'est pas un cristal figé mais un organisme vivant en déplacement actif dans son monde aqueux.
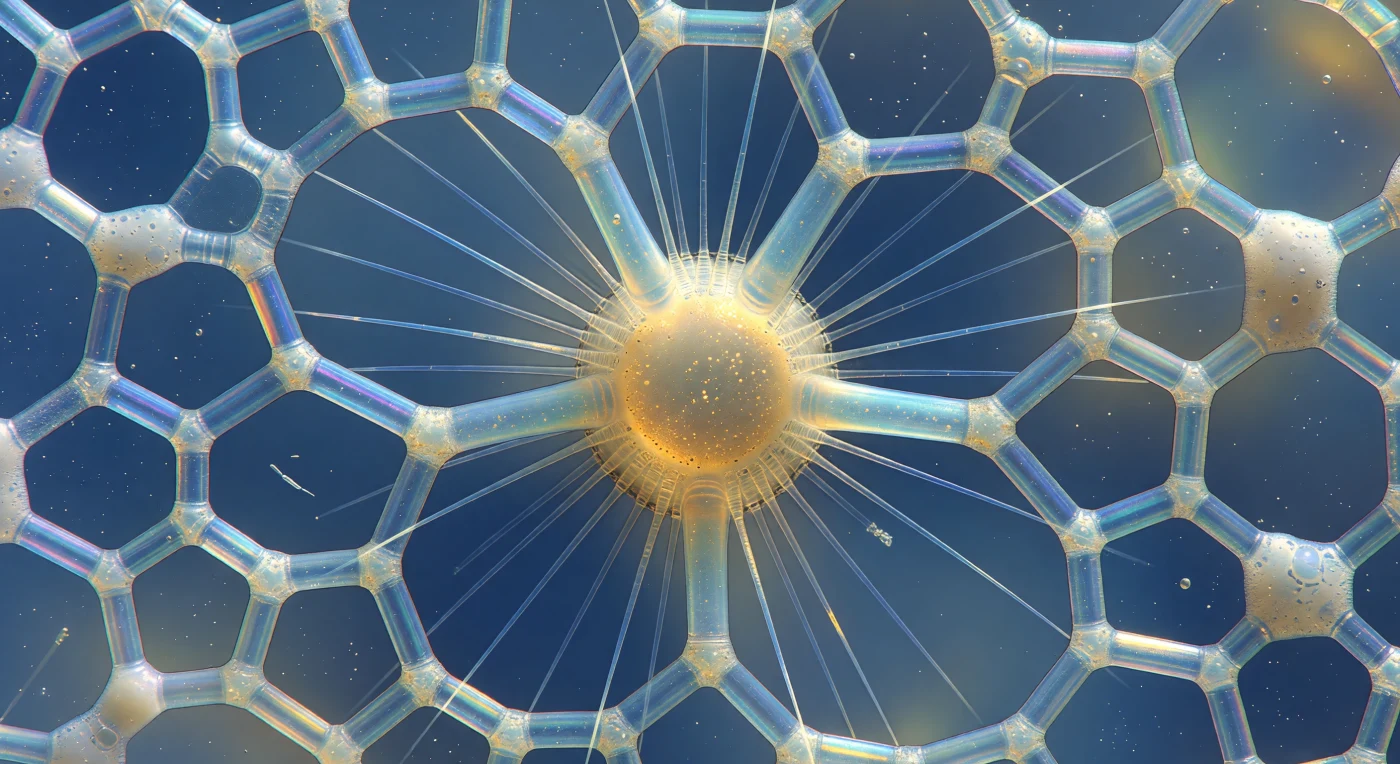
Vous vous trouvez suspendu dans les eaux ouvertes de l'Atlantique équatorial, face à face avec une architecture minérale que l'évolution a perfectionnée depuis cinq cents millions d'années : le squelette de silice amorphe d'un radiolaire polycystine, dont les travées — chacune épaisse de deux micromètres à peine, fines comme du fil de verre filé — fragmentent la lumière descendante en franges d'interférence qui glissent du violet profond au bleu cobalt, puis s'enflamment en or pâle aux nœuds où la silice s'épaissit, transformant chaque pore hexagonal et pentagonal en une fenêtre illuminée sur l'océan céruléen derrière. Au cœur de cette cathédrale engloutie, la capsule centrale brûle d'une luminosité ambrée et résineuse, délimitée par une membrane protéique perforée à travers laquelle on devine le lent tourbillon granulaire du cytoplasme, parsemé de gouttelettes lipidiques et de cristaux de sulfate de strontium — le lest minéral de l'organisme — qui s'allument comme des étincelles d'or dans la pénombre. De cette capsule irradient les axopodes, filaments de verre parfaitement rectilignes qui traversent la dentelle siliceuse et s'étendent dans l'eau libre comme des aiguilles cristallines réfractant la lumière en éclats prismatiques, tandis qu'entre les dernières épines du squelette une mousse de ectoplasme vacuolisé s'accroche en globules translucides, chaque vacuole agissant comme une minuscule lentille qui concentre et déforme les couleurs interférentielles en points lumineux fugaces. Une bactérie en bâtonnet — un corps dont la taille mesure quelques dixièmes de micromètre — culbute en bout-à-bout dans la plus grande ouverture hexagonale de la paroi, offrant par sa présence involontaire la seule mesure vraie de ce silence froid et photonique, de cette architecture minérale que l'organisme unicellulaire secrète et habite simultanément, vivant et cathédrale à la fois.

Au ras d'un plancher de silice qui s'étend jusqu'à un horizon lumineux et diffus, le regard traverse un champ de ruines architecturales d'une précision de cristal taillé : frustules de diatomées écroulées les unes sur les autres, cylindres et navettes et triangles de verre opalin dont les réseaux de pores — chaque perforation à peine une fraction de micron — decomposent la lumière transmise en franges d'interférence dorées, cobalt et rose, peignant le sédiment d'une mosaïque spectrale mouvante. Cette silice n'est ni franchement transparente ni franchement opaque, mais possède la translucidité laiteuse et précieuse d'une opale, parcourue de micro-fractures internes qui fragmentent la lumière en arcs prismatiques, tandis qu'entre les grandes ruines une poudre fine de stries brisées et de valves détachées scintille comme un silt de verre pilé. Au-delà des premières rangées de débris, des corridors de colonnes empilées s'enfoncent dans un brouillard bleu-blanc qui suggère que ce champ s'étend à l'infini dans toutes les directions, chaque frustule mesurant de vingt à cent cinquante micromètres et pourtant constituant à lui seul une cathédrale de géométrie ornementale. À la lisière des ruines, un héliozoaire Actinophrys flotte en pleine colonne d'eau comme un lustre de verre suspendu, ses axopodes rayonnant en tiges rectilignes qui captent la lumière transmise et brillent comme des fibres optiques entre les débris de silice, pendant que des flagellés ambrés dérivent alentour, leurs corps ellipsoïdaux dorés captant l'éclat froid et omniprésent de ce monde entièrement fait de lumière réfractée.
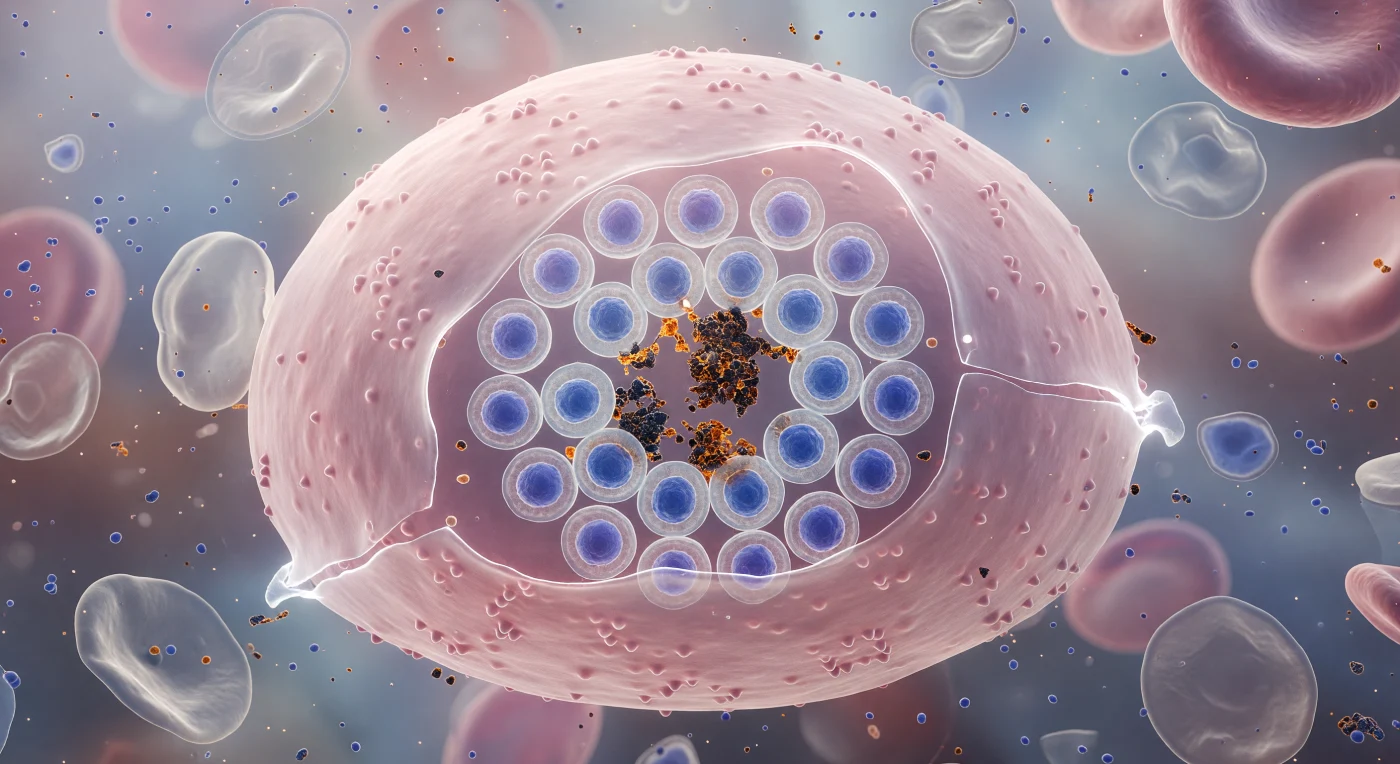
Vous planez contre la paroi bombée d'un globule rouge infecté, une vaste coupole d'un rose translucide tendue jusqu'à la quasi-transparence par la pression mécanique de ce qu'elle contient — vingt-quatre mérozoïtes de *Plasmodium falciparum* disposés en rosette géométrique précise, leurs noyaux teints d'un bleu cobalt intense pressés contre la membrane de l'intérieur comme des pierres serties dans un médaillon fragile. Au centre de cette roue vivante, des amas d'hémozoïne — cristaux brun-noir issus de la digestion de l'hémoglobine de l'hôte, résidus métaboliques inertes et durs comme des gemmes — réfractent la lumière ambiante en brefs éclats d'ambre chaud au milieu du froid bleu-violet dominant. Le cytoplasme érythrocytaire a été intégralement consommé, remplacé par cet assemblage parasite d'une précision presque architecturale, et là où la bicouche lipidique s'est amincie jusqu'à l'extrême, la membrane vibre imperceptiblement sous la pression osmotique accumulée — au-delà, des cellules fantômes froissées dérivent, enveloppes grises et mates, témoins des ruptures précédentes. Toute la scène est suspendue dans la dernière fraction de seconde avant l'effraction : lorsque la membrane cédera, ces vingt-quatre parasites se déverseront simultanément dans le tissu environnant, chacun prêt à envahir un nouvel érythrocyte et à relancer un cycle qui, multiplié à l'échelle d'un organisme entier, produit les fièvres tierces caractéristiques du paludisme à *falciparum*.

La surface s'étend dans toutes les directions comme un continent d'ambre vivant — les plaques thécales de *Ceratium tripos* couvrent l'ensemble du champ visuel, chacune un vaste polygone de cellulose lumineux, baigné par la lumière transmise en bleu-vert qui traverse l'intérieur métabolique de la cellule et ressort transformée en miel brûlé, en sienna chaud, comme si la matière organique elle-même était en fusion. Les sutures entre les plaques forment des escarpements géométriques d'une précision saisissante — des crêtes surélevées qui divisent le territoire en mosaïques pentagonales et hexagonales, projetant de légères ombres sur des surfaces striées de micro-nervures parallèles, interrompues à intervalles réguliers par de minuscules pores circulaires traversant l'épaisseur de la paroi cellulosique en couches lamellaires visibles dans la translucence de la coupe. Le cingulum équatorial traverse la scène comme un canyon cobalt-indigo, ses parois tombant abruptement dans l'ombre, et au fond de cette tranchée obscure le flagelle transverse repose en spirale silencieuse, ne se révélant qu'en un mince fil d'iridescence pâle contre le bleu profond. À l'extrême gauche, la corne apicale monte en spirale majestueuse hors du cadre, portant la même armure d'ambre et de pores, tandis que derrière elle l'eau libre se dissout en translucidité atmosphérique — le milieu aquatique rendu presque immatériel par l'éclairage diffus, infiniment loin de cette citadelle de cellulose vivante.
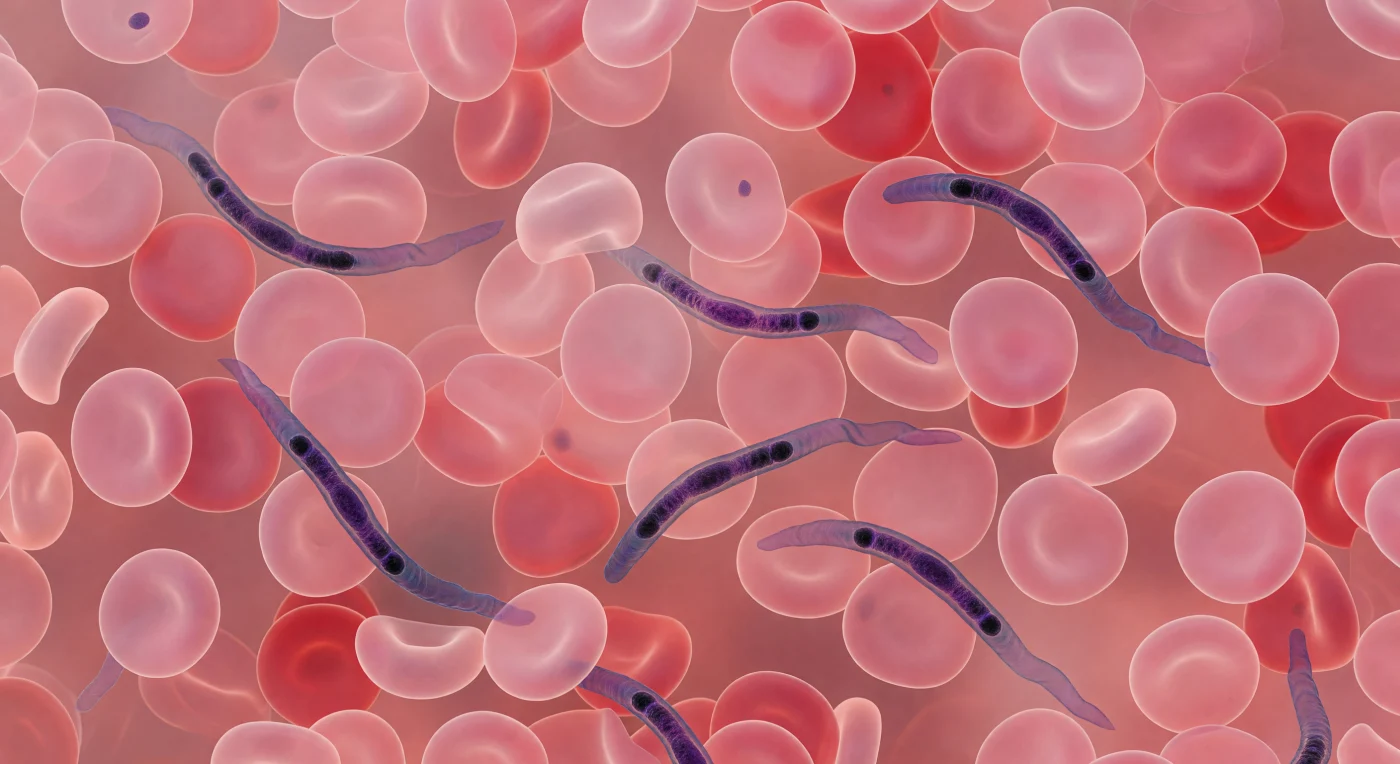
Dans ce couloir de chair rose que constitue le flux sanguin, la vue est entièrement saturée de disques biconcaves érythrocytaires — chacun une galette de sept micromètres, translucide en son centre aminé, s'épaississant en un tore carmin vers le bord, empilés et pressés dans chaque plan de profondeur jusqu'à former un papier peint de géométrie rosée, à la fois claustrophobe et infini. Entre ces boulders de membrane, plusieurs Trypanosoma brucei se faufilent en arcs sinueux d'un bleu-violet soutenu, leurs corps de quinze à trente micromètres ondulant grâce à la membrane flagellaire latérale — un ruban de soie irisée dont chaque propagation de vague constitue l'unique source de mouvement dirigé dans ce monde de pression douce et d'immobilité rose. À l'intérieur de chaque parasite, le noyau et le kinétoplaste — ce corpuscule compact d'ADN mitochondrial propre aux kinétoplastidés — se détachent comme des concentrations presque noires dans la cytoplasme violet acier, le kinétoplaste tapi près de l'extrémité postérieure tel un noyau de fruit sombre. La coloration de Giemsa, standard de diagnostic du paludisme et des trypanosomoses, révèle cette architecture chromatique avec une précision de watercolor humide : le parasite responsable de la maladie du sommeil se trahit ainsi dans le sang de son hôte humain, serpentant entre des cellules dix fois plus petites que lui, invisible à l'œil nu mais décisif pour la survie de l'organisme tout entier.

Au cœur du film neustonique d'un étang de plaine, à quelques centaines de micromètres à peine sous l'interface air-eau, le regard traverse une foule serrée d'organismes unicellulaires qui transforment le moindre photon en matière vivante : des fusées émeraude d'Euglena glissent en tournant sur leur pellicule irisée, des Chlamydomonas portent chacune un œil-spot rouge braise comme une braise caroténoïde, tandis que des Coleps roulent lentement, leurs mosaïques de plaquettes carbonatées éparpillant la lumière ambrée en éclats de porcelaine blanche. Au-dessus, la surface du film forme un plafond de mercure ondulant — la tension superficielle y est une force gigantesque à cette échelle, une paroi invisible qui courbe la lumière en rubans caustiques coulissant sur la communauté comme des projecteurs au ralenti. L'eau elle-même n'est pas vide mais une suspension dorée d'acides humiques, de flocons de cellulose effondrée et d'un brouillard bactérien bleuté qui atténue les lointains comme une brume légère, rappelant que dans ce monde de Reynolds infinitésimal, la viscosité règne en maître et chaque battement de flagelle est une lutte contre un milieu aussi épais que du miel.

Dans la lumière bleu-verte du large pélagique, nous regardons vers l'extérieur à travers notre propre exosquelette d'ambre — les plaques de chitine orangées se courbent aux bords du champ de vision comme les parois d'une lanterne translucide, pendant que trois paires de pattes larvaires tressaillent contre quelque chose que l'œil refuse d'accepter comme réel : les réticulopodes de *Globigerina bulloides*, des filaments de 0,2 à 0,5 µm à peine, trahis uniquement par le trafic continu de vésicules et de particules mitochondriales qui défile le long de chaque fil comme des perles sur un courant invisible. La géométrie du piège est ce qu'il y a de plus troublant — chaque thread capte brièvement la lumière froide et directionnelle, scintille en argent-blanc, puis disparaît avant de réapparaître avec une nouvelle pulsation de cargo granulaire, les fils convergent de toutes les directions vers notre corps, leur tension contractile imperceptiblement mais inexorablement resserrée. Dans le lointain bleu-vert, le test calcaire de la foraminifère domine comme une forteresse de craie — sphérique, chambré, couvert de centaines d'apertures minuscules d'où émergent ces fils mortels, sa surface de carbonate de calcium d'un blanc mat et crémeux, froide et indifférente. Il n'y a ni violence ni mouvement brusque : seulement la lente mécanique d'un piège déjà fermé, et le milieu aqueux lui-même — colloid de neige marine en dérive brownienne, bactéries éclairées comme des étincelles, matière organique dissoute teintant d'ambre le bleu-vert ambiant — qui efface doucement tout contraste au-delà de quelques centaines de micromètres.

Au-dessus de vous, la colonne d'eau s'ouvre comme une nef de cathédrale immergée : deux mètres de mer ont filtré le spectre solaire jusqu'à ne laisser survivre que le bleu à 460 nanomètres, une lumière cobalt électrique qui descend en faisceaux volumétriques traversés de matière organique dissoute, transformant l'océan en quelque chose de vivant et de lumineux. Les Acantharia flottent à tous les étages de ce volume — chacune bâtie autour de vingt spicules de sulfate de strontium rayonnant en symétrie géométrique stricte selon la loi de Müller, et ces cristaux biréfringents brisent la lumière descendante en couronnes prismatiques de blanc glacé, de violet pâle et d'or spectral qui auréolent chaque organisme comme une explosion figée. Entre les spicules, le corps cellulaire est une sphère translucide d'ambre gris d'où s'élancent des axopodes aussi fins que des fils de soie, captant la lumière en filaments argentés, tandis que dans le lointain cobalt d'autres Acantharia se réduisent à de minuscules étincelles prismatiques se dissolvant dans le gradient bleu. Des loricas de tintinnides ponctuent la colonne à des angles obliques — tubes hyalins faits de coccolithes agglutinés, ambrés à leur base, quasi-transparents à leur ouverture où les cils composés se devinent à peine, fantôme lumineux d'un mouvement suspendu. Entre tous ces organismes, des flocons de neige marine couleur crème et ambre dérivent lentement à travers le champ, leurs contours organiques et irréguliers tranchant avec la précision géométrique des cristaux minéraux, rappelant que cette colonne de lumière vivante est à la fois une architecture et un festin, un milieu où la prédation, la sédimentation et la photosynthèse se négocient dans le silence bleu.

Sous vos pieds, une plaine fracturée de limon brun s'étend à perte de vue — une carte géologique en miniature dont les plaques d'argile ocre et sienna sont séparées par des crevasses abyssales où persiste, presque imperceptible, une haleine d'humidité résiduelle. Sur ces plateaux minéraux, une lumière dorée rasante révèle des formes parfaitement lisses : des kystes de *Colpoda*, sphères d'ambre translucide à double paroi chitineuse, reposent sur le substrat granuleux comme des perles polies, chacune projetant une ombre elliptique précise dans la lumière oblique, tandis que des tests d'*Arcella* — coupoles stipplées d'une géométrie protéique fine, leur ouverture scellée d'un bouchon nacré — s'adossent au bord des crevasses comme de petits casques abandonnés. Entre eux, des agrégats d'*Euglena* en stade palmella forment des voiles de mucilage desséché, froissés et légèrement brillants, leurs chloroplastes assoupis retenant encore un reflet olive-doré dans l'aridité uniforme. Chaque kyste incarne une victoire de l'évolution sur le chaos : une vie entière comprimée dans une armure biologique imperméable, suspendue dans un silence métabolique en attendant que l'eau revienne.




















