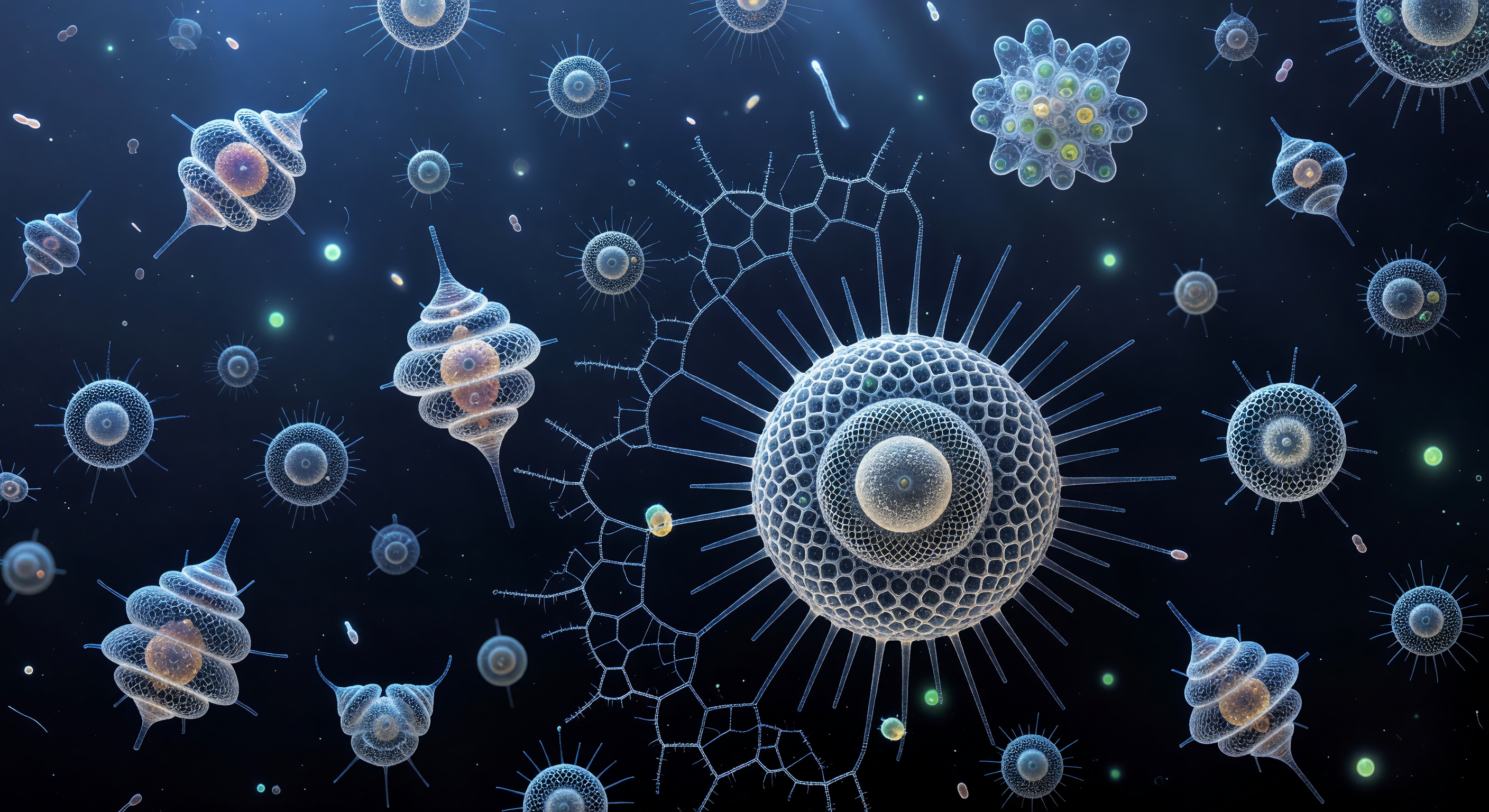
Wer hier steht, steht nirgendwo – schwebend im Herz eines Wesens, das kleiner ist als ein menschliches Haar, und doch öffnet sich ringsum eine Kathedrale aus gefrorenem Licht. Die Wände dieser Kuppel bestehen aus amorphem Opal, dem biogenen Siliziumdioxid, das *Actinomma asteracanthion* Stunde um Stunde aus dem Meerwasser abgeschieden hat, und ihre hexagonalen Poren – kaum breiter als ein Bakterium – wirken wie Präzisionslinsen, die das kalte Tiefseelicht in prismatische Höfe zerlegen: zartes Violett an den Streben, warmes Aquamarin in der Mitte. Drei konzentrische Gitterschalen nisten ineinander, jede etwas offener gearbeitet als die vorherige, und die zwölf triradiat verzweigten Stacheln durchstoßen alle drei Lagen wie die Rippen eines gotischen Gewölbes, ehe sie als kristalline Nadeln im indigoblauen Ozean verschwinden – Strukturen, die das Tier aus einer Lösung heraus mineralisiert hat, reguliert durch Vesikelmembranen, die die Siliziumquelle präzise formen. Hinter dem Beobachter pulsiert das Endoplasma des Zellkerns in warmem Bernsteingelb, ein organischer Gegenpol zur kalten Geometrie der Schalen, während draußen, jenseits der äußersten Kuppel, der mitternachtsblaue Ozean in hunderte winzige Linsenfenster gefasst ist und jede Pore eine leicht anders gebrochene Ansicht des Abyssus zeigt, als bewohne man das Facettenauge eines unmöglichen Mineralorganismus.

In der Mitte einer schwarzen, druckvollen Stille schwebt man knapp außerhalb eines lebenden Acantharia-Einzellers — eines Vertreters der Radiolarien, der nicht aus Siliziumdioxid, sondern aus Strontiumsulfat (Zölestin) seinen zwanzigstrahligen Kristallstern aufbaut, einem Mineral so selten im ozeanischen Kontext, dass die Zelle zu seinen Lebzeiten nahezu den gesamten verfügbaren Strontiumvorrat der umgebenden Wassermasse bindet. Unter simuliertem Kreuzpolarisationsfilter explodieren alle zwanzig Stacheln gleichzeitig in vollständig verschiedenen Interferenzfarben — elektrisches Cyan, gesättigtes Magenta, tiefes Kobaltblau, glutreiches Gold —, weil die kristallographische Ausrichtung jedes einzelnen Stachels relativ zur Polarisationsebene leicht abweicht und so die Gangunterschied der ordentlichen und außerordentlichen Strahlen eine andere Wellenlänge auslöscht, was Birefringenz als lebendige Spektralmalerei sichtbar macht. Zwischen den blitzenden Kristallruten spannen sich die Myonemkabel — kontraktile Proteinfasern, die keinem bekannten Muskeltyp gleichen — als kaum sichtbare dunkle Schatten, die die geometrische Symmetrie der Stacheln unter Spannung halten und das Gesamtgefüge bei Reiz innerhalb von Sekunden zusammenziehen können. Im Zentrum liegt die Zentralkapsel als warmes, tabakbraunes Oval, dicht besetzt mit Zooxanthellen, deren Chlorophyllpigmente ein rostgoldenes Leuchten aussenden — und das gesamte Wesen hängt allein in vollständiger Dunkelheit wie ein brennendes Geometrieobjekt, ein lebendiger Lüster aus Kristall und Cytoplasma, der sich selbst beleuchtet.

Wir schweben knapp über einer gewölbten Mineralebene, die sich in alle Richtungen erstreckt wie der Boden eines fremden Planeten aus Glas — die äußere Gitterwand einer lebenden Spumellaria-Zelle, deren Kieselsäuregerüst sich als präzises Mosaik aus Sechsecken und Fünfecken vor uns ausbreitet, jede Porenmündung zu einer leicht leuchtenden Lippe aus Opalquarz aufgeworfen, die Streben tief wasserglastransparent, an den Knotenpunkten von schräg einfallendem DIC-Licht zu harten Silberpunkten aufgehellt. Aus jedem Porenrand erhebt sich ein starres Axopodium senkrecht in die Dunkelheit über uns — ein Wald aus kristallinen Speeren, jeder Schaft von inneren Mikrotubulbündeln längs gestreift und von Interferenzfarben gesäumt, einem hauchdünnen Spektralband aus Türkis, Bernstein und blassem Magenta, das wie eine Neonnaht die volle Länge des Schafts hinaufläuft. Diese Axopodien sind keine passiven Strukturen, sondern aktive Fangorgane: sie leiten erbeutete Beute über cytoplasmatisches Streaming — mit einer Geschwindigkeit von etwa ein bis fünf Mikrometern pro Sekunde — entlang ihrer Mikrotubulschienen in Richtung der Zelle, und tatsächlich schleichen an drei der nächsten Speere bernsteinfarbene Nahrungsvakuolen langsam nach innen, jede ein dicht gepacktes, membranumhülltes Päckchen verdauter Beute, das wie eine Laterne in der Mitternachtsdunkelheit des umgebenden Meerwassers leuchtet. Die Szene verbindet Kathedralengeometrie, Korallenriff und Mineralkosmos in einem einzigen stillen Augenblick an der Grenze zwischen Tier, Mineral und offenem Ozean.

Der Blick richtet sich aufwärts durch ein Bauwerk, das kein Menschenhand je errichtet hat: ein konischer Tunnel aus amorphem Opal-Siliziumdioxid, dessen Wände in Armreichweite schimmern und durch spiralförmig angeordnete elliptische Poren das Licht des offenen Ozeans als zitternde aquamarinblaue Flecken ins Innere lassen, die sich auf den Mineralrippen überlagern wie in einem lebenden Glasfenster. Fünf übereinander gestapelte Septen steigen in erzwungener Perspektive empor, jedes eine ringförmige Siliziumwand mit einem zentralen Foramen, die Öffnungen mit jeder Etage kleiner werdend, bis das oberste nur noch ein Nadelstich intensiven Türkislichts ist. Das Material selbst ist weder Glas noch Kristall, sondern etwas dazwischen – milchig-transluzent, mit einem Brechungsschimmer, der jeden eintreffenden Lichtstrahl in weiche kaustische Ringe faltet, während ein schleimiger Zytoplasmafilm die inneren Gitterrippen mit irisierendem Schein überzieht und dort, wo Zytoplasmafäden Rückstände hinterlassen haben, das Siliziumdioxid in warmem Bernsteinton gegen das vorherrschende Blau leuchtet. Durch einzelne größere Poren ist draußen der Geisterschatten eines Axopodiums zu erkennen – ein gerader kristalliner Faden, der als leuchtende Speiche ins aquamarinblaue Außen reicht, bevor er im Dunst des offenen Wassers verblasst. Am Scheitelpunkt der Welt steht, in perfektes Schwarz gegen das gleißende Blau silhouettiert, der apikale Stachel wie eine obsidiane Nadel.

Der Blick fällt senkrecht hinab auf eine Ebene aus Silizium und Stille, die sich nach allen Seiten bis zum Horizont erstreckt wie die Ruinen einer versunkenen Stadt – hunderte radiolarer Skelette, Schulter an Schulter in bleigrauen Ton gepresst, ihre kugelförmigen Gitterwerke und konischen Kammern unter einem schräg einfallenden Elektronenstrahl in hartem Hell-Dunkel-Kontrast erleuchtet. Jede geometrische Pore eines Spumellaria-Tests – konzentrische Siliziumsphären noch ineinandergeschachtelt, zwei Millimeter breit – wirft einen tiefschwarzen Schattenkanal senkrecht in die Tiefe, als schaue man durch die Fenster einer ertrunkenen Kathedrale; daneben liegt ein Nassellaria-Helm umgestürzt, seine segmentierten Kammern wie zerdrückte Kühltürme gestapelt, der Apikalstachel noch aufwärts gerichtet und mit mineralischen Überwachsungen bedeckt. Diese Skelette sind die Überreste von Organismen, die seit dem Kambrium das Pelagial bewohnen, deren amorphe Opal-Tests nach dem Tod jahrtausendelang durch die Wassersäule sanken – kaum mehr als einen bis zehn Meter pro Tag – und sich schließlich in radiolaren Tiefseeschlammen akkumulierten, wo geologischer Druck haarfeine Risse in die Testwände trieb und Tonpartikel wie Schutt in gebrochene Fenster trieben. Es gibt keine Farbe, keine Wärme, nur die gnadenlose Klarheit der Elektronenoptik: eine Nekropole aus mathematischer Präzision, komprimiert zu grauem Sediment am Rand der Sichtbarkeit.
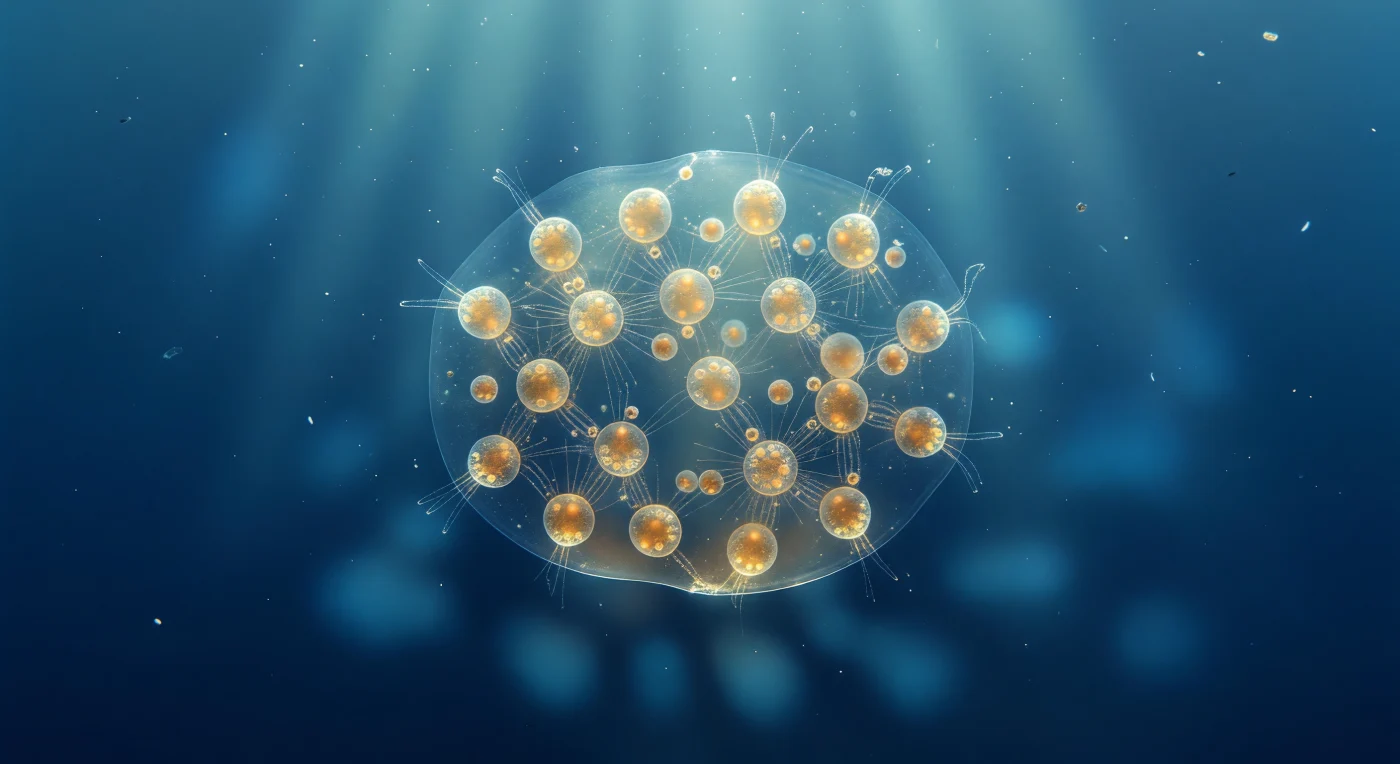
Vor dir schwebt eine Welt aus fast nichts — ein acht Millimeter großes Ellipsoid aus Schleim und Licht, so transparent, dass es eher eine Verdickung des Ozeans selbst zu sein scheint als ein Lebewesen. Die koloniale Sphaerozoum-Ansammlung hängt reglos im tropischen Oberflächenwasser, gehalten von den Lipidvakuolen ihrer Zellen, und ihr Inneres offenbart sich wie das Innere einer Glaskugel: Dutzende goldbrauner Einzelzellen, jede dreihundert Mikrometer weit, leuchten als warme Bernsteinlaternen durch das gallertartige Gewebe, ihre Farbe von dicht gepackten symbiotischen Dinoflagellaten gesättigt, die einfallendes Sonnenlicht in Honig und Ocker verwandeln, bevor es weiter in die Tiefe dringt. Von jeder Zelle strahlen Axopodien als nahezu unsichtbare kristalline Fäden aus — erst wenn ein Lichtbündel sie im richtigen Winkel trifft, flackern sie zu silbernen Nadeln auf und verweben sich zu einem zarten Netz, das die gesamte Kolonieinnenwelt durchzieht, ohne ein einziges Skelettelement aus Silica zu benötigen. Die Kolonie selbst wirkt als schwache biologische Linse: Das Sonnenlicht bricht an ihrer gewölbten Grenzfläche, läuft konvergierend durch die transparente Gallerte und entwirft darunter ein sich langsam verlagerndes Kaustikmuster aus helleren und dunkleren Blautönen, das in den indigo werdenden Tiefraum hinabwandert — ein schwebend treibendes Buntglasfenster in einem stillen, grenzenlosen Dom aus Wasser.
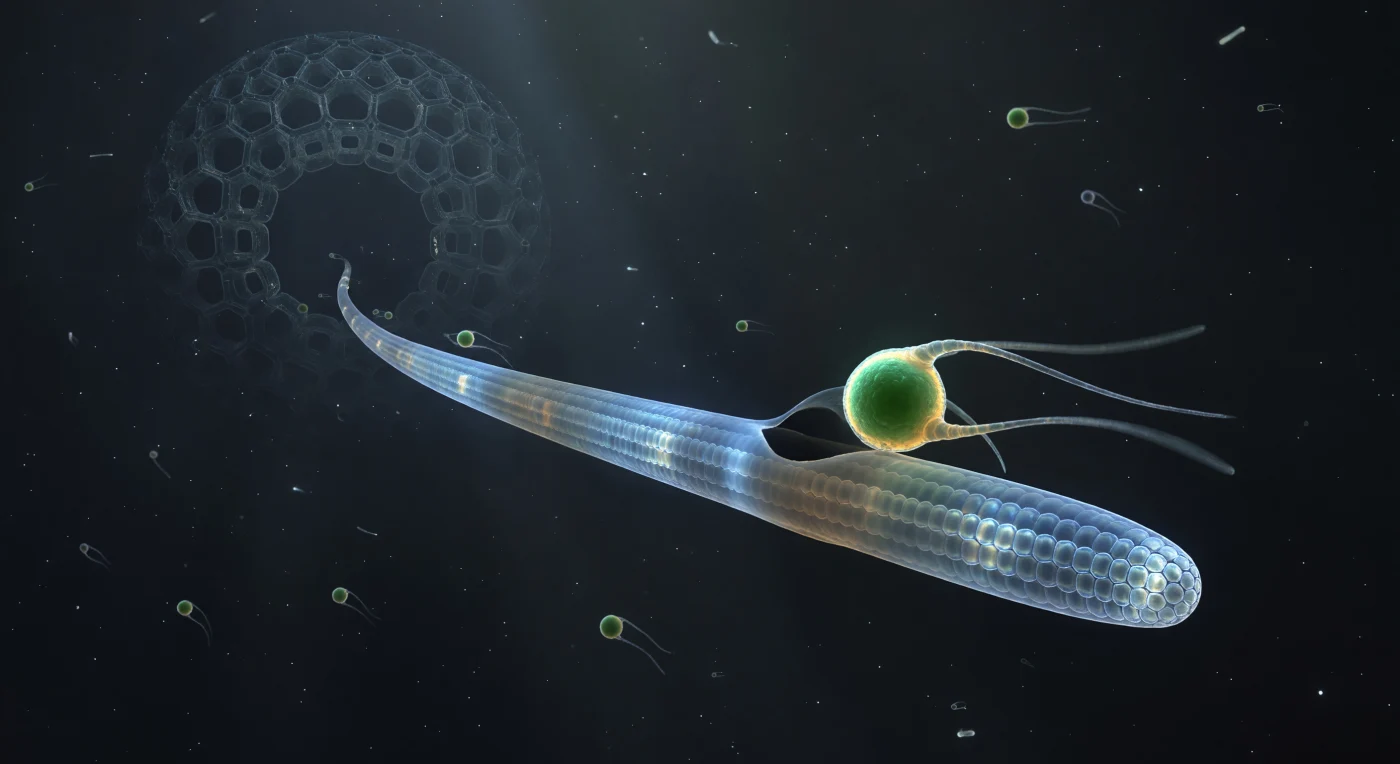
Im Herzen dieser Szene berührt sich eine winzige, smaragdgrüne Kugel – eine Micromonas-Geißelalge kaum drei Mikrometer groß – mit dem gläsernen Speer eines Axopodiums, und in diesem Bruchteil einer Sekunde entscheidet sich ihr Schicksal. Das Axopodium, innen von gebündelten Mikrotubuli in wabenhafter Geometrie durchzogen, leuchtet mit kaltem, blaugrünem Schimmer, während am Kontaktpunkt eine dunkle Membransichel beginn, sich wie eine erste Grad eines langsamen Sonnenfinsternis um die autofluoreszierende Beute zu wölben – sichtbares Zeichen einer bereits ausgelösten biochemischen Maschinerie der Einverleibung. Weit hinter dieser Begegnung steigt das sechseckige Silikatgitterwerk des Radiolars wie eine außerweltliche Kathedrale aus dem Dunkel: jedes Pore ein dunkles Fenster in einer Architektur, die hier Dimensionen eines gewaltigen Bauwerks annimmt. Entlang des Axopodiums treiben blasse Vesikel wie gedämpfte Laternen tiefer ins Zellinnere – frühere Mahlzeiten, deren einst leuchtende Pigmente zu Rost und Ocker verblichen sind, während die Verdauung still voranschreitet. Das gesamte Bild schwimmt in einem volumetrischen Dunkel, das keine Lichtquelle kennt außer den Organismen selbst – jeder emittiert genau so viel Licht, wie seine Chemie verlangt.
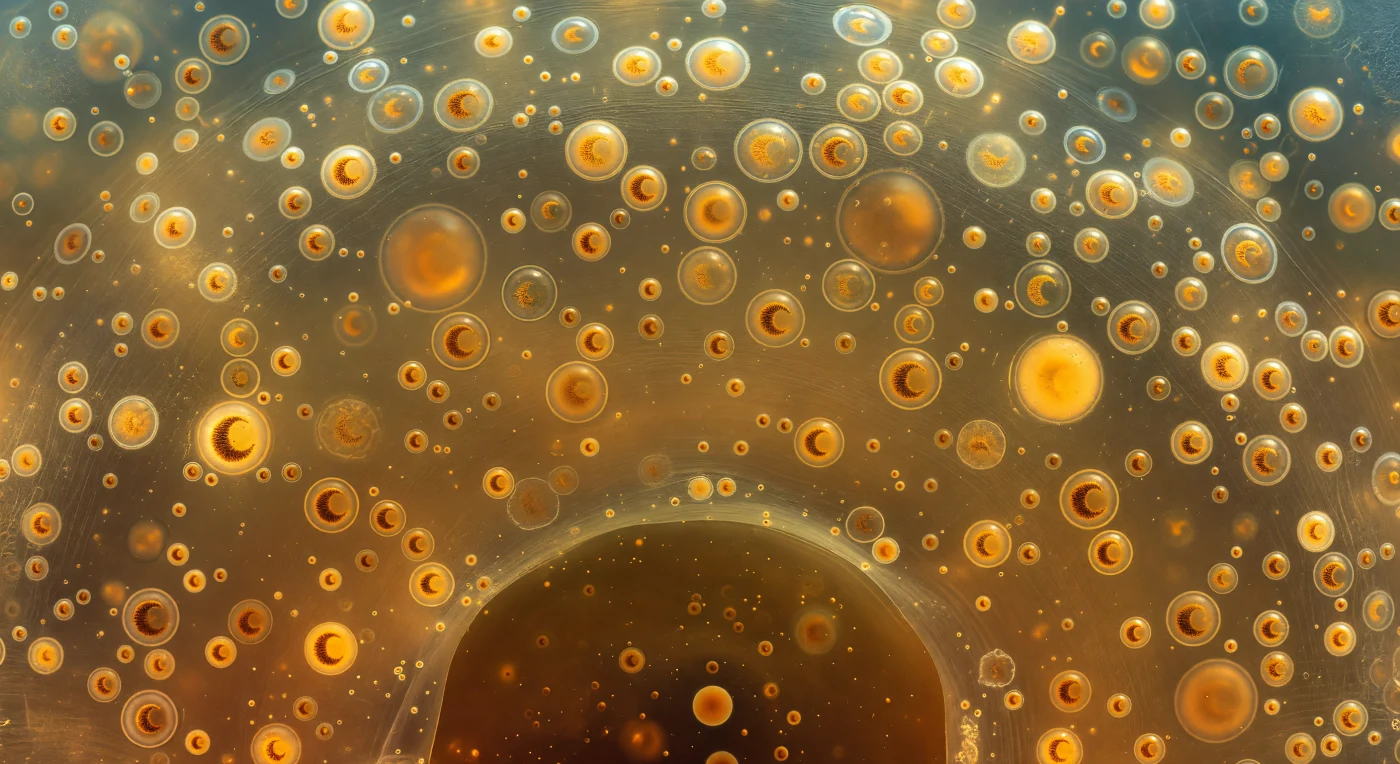
Im Inneren der Calymma einer kolonialen Collodarie bist du von einem lebenden Gel umschlossen, das warm und vollständig um dich herum drückt wie amber Honig – weder flüssig noch fest, sondern in einem Zustand zitternder Schwebe zwischen beiden. In alle Richtungen hängen Zooxanthellen frei im Raum: goldbraune Kugeln von zehn bis fünfzehn Mikrometern Durchmesser, so zahlreich, dass sie das Sichtfeld füllen ohne sich zu berühren, jede mit einem sichtbaren, halbmondförmigen Kern aus dichterem Ocker-Braun, der sich wie eine Mondsichel durch das Zellinnere zieht – Dinoflagellaten-Symbionten, die dem Wirt über Photosynthese Kohlenhydrate liefern und dafür Nährstoffe und Schutz erhalten. Die Lipidvakuolen des Ektoplasmas, bis zu vierzig Mikrometer groß, lenken das von oben einfallende blaue Ozeanmeerlicht in warmes Bernstein um und beugen es zu goldenen Kaustikringen, die sich hinter jedem klaren Tropfen auf die nächste Schicht Symbionten legen. Das gesamte Innere wirkt wie ein biologischer Hohlraum mit Domgeometrie, abgedichtet nach innen durch die schwach sichtbare Wölbung der Zentralkapsel – einer glykoproteinreichen Membran, die das dichte Endoplasma von der transparenten Welt der Symbionten trennt und die fundamentale Zweiteilung des Radiolarienkörpers markiert.
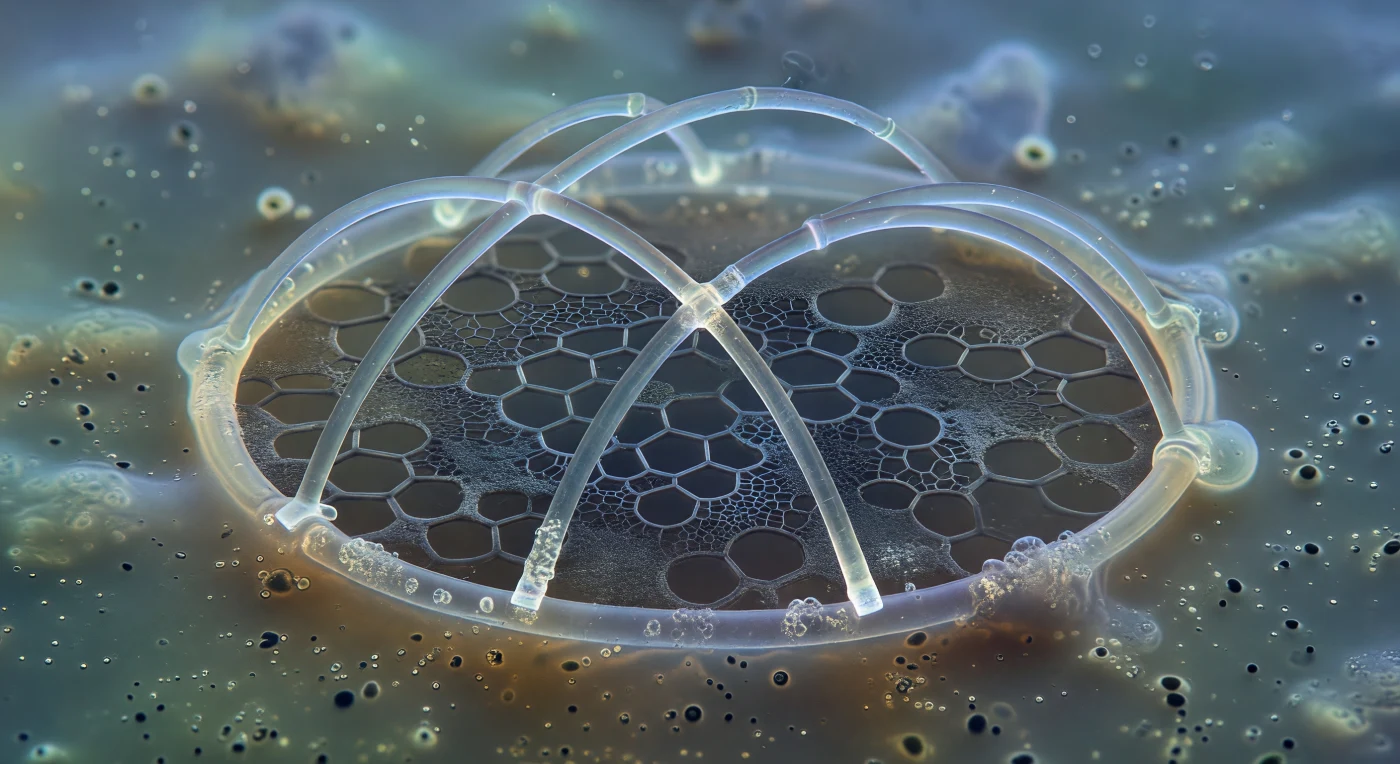
Der Blick fällt auf einen Nascent-Skelett aus Kieselsäure, der sich wie die Rippen einer halbfertigen Kathedrale aus dem trüben, bernsteinfarbenen Zytoplasma herausschält – zwei gekreuzte Primärbalken und ein gebogener Sagittalring, bereits glashart und beinahe farblos, mit kühlen, irisierenden Halos, die das blaugrüne Streulicht in schmale optische Kränze verwandeln. Dabei handelt es sich um die früheste Mineralisierungsphase einer *Pterocorys*-Schale: Amorphes Siliziumdioxid wird innerhalb spezialisierter Silizifizierungsvesikel abgeschieden und folgt dabei einem organischen Proteingerüst aus Glykoproteinfasern, das der Mineralstruktur vorauseilt und bereits die zukünftige Geometrie der Poren als sechseckige Leerstellen in mattem Grau vorzeichnet, noch bevor ein einziges Siliziumatom ihren Rand berührt hat. Dieses Gerüst ist kaum sichtbar – ein Abdruck des Zukünftigen, der Licht eher schluckt als reflektiert, und dessen Präzision um so erstaunlicher wirkt, als die gesamte Zelle von Brownscher Molekularbewegung durchzittert wird, von taumelnden Lipidtröpfchen, dem unscharfen Vorbeiziehen von Mitochondrien und einer Viskosität, die jede Bewegung in Zeitlupe verwandelt. Was sich hier abspielt, ist kein beiläufiger Vorgang: Das fertige Gehäuse wird seinen Erbauer um Hunderte von Millionen Jahren überdauern – eingebettet in Tiefseetone als mineralisches Zeugnis eines einzelnen Augenblicks des Lebens.

Die gesamte Welt besteht hier aus einer einzigen gewölbten Fläche – der Innenseite der Siliziumablagerungsvesikel, einer membranösen Kammer, in der die Radiolarie ihr mineralisiertes Skelett Schicht um Schicht aufbaut. Über dem Betrachter zieht sich die Silikalemma als messerscharfe dunkle Doppellinie in einem weichen Cremeweiß, das von allen Seiten durch die Membran dringt wie Tageslicht durch Reispapier; darunter kriecht eine blasse, grauweißliche Silicagel-Front mit der Geduld erkaltender Lava über ein rostfarbenes Geflecht aus silaffinähnlichen Proteinfibrillen, deren Terrakotta-Wärme unter den vordringenden Mineralschichten langsam zu tiefem Sienna abdunkelt. Die Silizifizierung ist kein abrupter Vorgang, sondern ein graduelles Einschließen: Die Gelfront durchdringt das Proteingitter wie eine Flut, die über feuchten Sand steigt, und wandelt ein biologisches Gerüst in dauerhaften, amorphen Quarz um – denselben Werkstoff, aus dem das gesamte Skelett des Organismus besteht und der nach dem Tod des Tiers jahrmillionenlang im Meeresgrund erhalten bleibt. Im Bernsteinlicht des umgebenden Cytoplasmas dahinter leuchten ferne Organellen als gefärbte Flecken – ein kobaltblaues Mitochondrium, ein smaragdgrünes Granulum –, stille Zeugen eines Mineralisierungsprozesses, der sich in diesem abgeschlossenen Hohlraum, Nanometer für Nanometer, in vollständiger Stille vollzieht.

Der Boden unter deinen Füßen ist eine gekrümmte Ebene aus blassem Aschengrau – amorphes Opal, kein Kristall, die Oberfläche mit einem matten Glanz wie gefrostetes Borosilikatglas unter schrägem Licht, und doch bei genauerem Hinsehen feinkörnig bis auf die Nanometerskala. Das hexagonale Porentesselat erstreckt sich in jede Richtung bis zum sichtbar gebogenen Horizont: jede Öffnung ein nahezu perfektes Sechseck von rund fünfzehn Mikrometern Durchmesser, dessen erhöhte Siliziumlippenränder scharfe Schatten in die Tiefe der Poren werfen, wo das Licht zu absolutem Schwarz versinkt – mehr Oberfläche ist Leere als Materie, und du stehst auf einem Gitterwerk aus Brücken über abgrundtiefe Brunnen. Sechs massive Stacheln erheben sich in gleichmäßigen Abständen aus den Kreuzungsknoten des Gitters, jeder ein triradiales Obeliskmonument aus extrudiertem Siliziumdioxid, dessen Basis glatt in das Gitter übergeht und dessen Spitze vierzig bis fünfzig Mikrometer über dem Boden in der kalten, gerichteten Beleuchtung glänzt – von hier aus wirken sie wie Kathedraltürme, die aus einer mineralischen Wüste wachsen. *Hexacontium* ist ein polycystines Radiolarie aus der Gruppe der Spumellaria, dessen konzentrische Kugelschalen aus biogenem Opal (SiO₂·nH₂O) in intrazellulären Silifizierungsvesikeln abgeschieden werden – ein Skelett, das seit dem Kambrium in den Sedimenten der Weltmeere erhalten geblieben ist, eine geometrische Notwendigkeit des Lebens in den Tiefen des Ozeans, hier freigelegt und erstarrt im Vakuum des Rasterelektronenmikroskops.

Du schwebst reglos in einer Wassersäule, die kälter und schwerer ist als alles, was die Oberfläche kennt, und rings um dich vollzieht sich ein lautloser Abstieg aus Mineralglas: Nassellaria-Gehäuse in konischen, glockenförmigen und pagodenartigen Gestalten sinken auf allen Seiten gleichzeitig herab, jedes zwischen hundert und vierhundert Mikrometern groß, doch bei diesem Maßstab wie Kathedralen aus amorphem Opal, deren hexagonale Porengitter das letzte mesopelagische Licht in kalte blaustahlfarbene Splitter zerlegen. Wo eine Zelle noch lebt, drückt das Zytoplasma bernsteinfarben und ockergelb gegen die Innenwand des Gitterwerks und lässt jeden durchbrochenen Stab wie ein Fenster in einem Kirchenfenster aus organischer Wärme leuchten — ein biologisches Glühen, das vollständig von mineralischer Kälte umschlossen ist; die leeren Gehäuse daneben sind aschfahl und still, ihre Kammern mit Meerwasser gefüllt, die Porenreihen offen wie Augenhöhlen in einem Schädel aus gesponnenem Glas. Zwischen all diesen sinkenden Formen treiben Flocken aus marinem Schnee — Aggregate aus Schleim, toter organischer Substanz und abgestoßenem Zytoplasma — auf spiralförmigen Bahnen durch das gesättigte Indigo der Tiefe, gelegentlich an einem hervorstehenden Radiolarienfortsatz hängenbleibend und sich wieder lösend, ihre halbdurchsichtigen Körper von unsichtbarer Biolumineszenz zu einem perlmuttartigen Schimmern erweckt. Die Geometrie dieser Welt ist nicht zufällig: Jede Form hier ist das Ergebnis von Hunderten Millionen Jahren evolutionärer Selektion auf präzise Siliziumabscheidung, und die Skelette, die jetzt an dir vorbeisinken, werden eines Tages auf dem Ozeanboden zu radiolaritischem Tiefseesediment werden — Archiv und Grabmal zugleich.

Der Blick durch das Polarisationsmikroskop öffnet sich auf eine versteinerte Welt, die zugleich intim und unermesslich wirkt: ein dichtes Mosaik aus rekristallisierten Kieselgerüsten — kugelförmige Spumellaria, kegelförmige Nassellaria, unter Jahrmillionen lithosphärischen Drucks zu blassen Chalzedon- und Mikroquarz-Formen zusammengepresst — das sich wie die Ruinen einer versunkenen Stadt in alle Richtungen erstreckt. Das von unten einfallende polarisierte Licht diffundiert durch die gesamte komprimierte Masse und verleiht jedem Test einen geisterhaften, von innen kommenden Schimmer, als wäre Mondlicht in gefrorenem Glas eingefangen. Rostbraune und dunkelkarminfarbene Hämatitflecken bluten durch die Zwickel zwischen den Tests — die mineralisierten Überreste einstiger meeresweiter Porenwässer, die das Gestein wie eingetrocknetes Blut durchziehen. Was sich hier zeigt, ist kein bloßes Gestein, sondern das verdichtete Archiv eines Jurassischen Ozeans: 150 Millionen Jahre Sedimentation, Diagenese und tektonischer Druck in einem einzigen Dünnschliff, dessen jede Einzelform einst ein winziger pelagischer Organismus war, der in einem Meer trieb, das längst von der Erdoberfläche verschwunden ist.

Der Blick gleitet durch eine Finsternis, die nicht nach Wasser aussieht, sondern nach Weltraum – das gekreuzte Polarisatorenpaar hat alles Umgebungslicht ausgelöscht und lässt nur das leuchten, was die mineralische Architektur der Organismen selbst abstrahlt. Über das gesamte Sichtfeld von zwei Millimetern verteilen sich Acantharia-Zellen wie gleichzeitig zündende Feuerwerkskörper: Ihre zwanzig Strontiumsulfat-Spiculae – jede ein birefringenter Kristallstab – verwandeln das polarisierte Licht durch Interferenz in satte Spektralfarben, sodass eine Zelle in Magenta und Kobaltblau brennt, die nächste in elektrischem Türkis und tiefem Violett, jede mit einer unverwechselbaren chromatischen Identität, die ihrer ikosaedrischen Symmetrie entspringt. Dazwischen treiben die Spumellaria als gespenstische Gitterarchitektur – ihr amorphes Opalsilikat erzeugt keinerlei Interferenzfarben und erscheint stattdessen in kaltem Zinngrau gegen das Schwarz, ihre konzentrischen Kugelkäfige mit hexagonalen Poren dennoch von atemberaubender Detailpräzision, wie gotische Kathedralen in Silbernebel eingefroren. Wo ein Acantharia-Stachel eine dieser Schalen berührt, flackert kurz ein Bernsteinlicht auf – das birefringente Material drückt dem Berührungspunkt seine Farbe auf, ein letzter Kontakt zweier sehr verschiedener Mineralstrategien des Lebens.

In der vollkommenen Dunkelheit zweitausend Meter unter der Meeresoberfläche schwebst du in einem Raum, den Licht normalerweise nie erreicht – nur dein Scheinwerfer schneidet als schmaler blau-weißer Kegel durch das druckgesättigte Wasser und lässt *Aulacantha scolymantha* aus dem Nichts hervortreten: fünfhundert hohle Kieselnadeln, die radial nach allen Seiten ausgreifen wie die eingefrorene Explosion eines gläsernen Kronleuchters, jede Nadel ein lichtleitendes Röhrchen von kaum zwei Mikrometern Durchmesser, das den Strahl aufnimmt und an der Spitze als kaltes blaugrünes Glühen wieder abgibt – eine sphärische Konstellation selbstleuchtender Koordinaten im absoluten Vakuum des Tiefseeschwarzens. Im Zentrum dieser Strahlenschar liegt das Phaeodium, eine opake, dunkelbraune Masse aus halbverdautem organischen Material, die das Innere des Organismus wie ein Kern aus kompakter Schwärze versiegelt und die zarte opaline Maschenstruktur der Kapselwand nur in flüchtigen Silberfäden sichtbar werden lässt, wenn das Licht sie streift. Das gelartige Calymma zwischen Kern und Nadelfeld – durchsetzt von winzigen Vakuolen, die den Strahl in diffuse Punkte zerstäuben – verleiht dem Organismus eine eigentümliche Dichte inmitten der Leere, während thermische Unruhe und Brownsche Bewegung die äußersten Nadelspitzen in einem Zittern halten, das weniger wie Leben wirkt als wie das ruhlose Atmen der Kälte selbst.
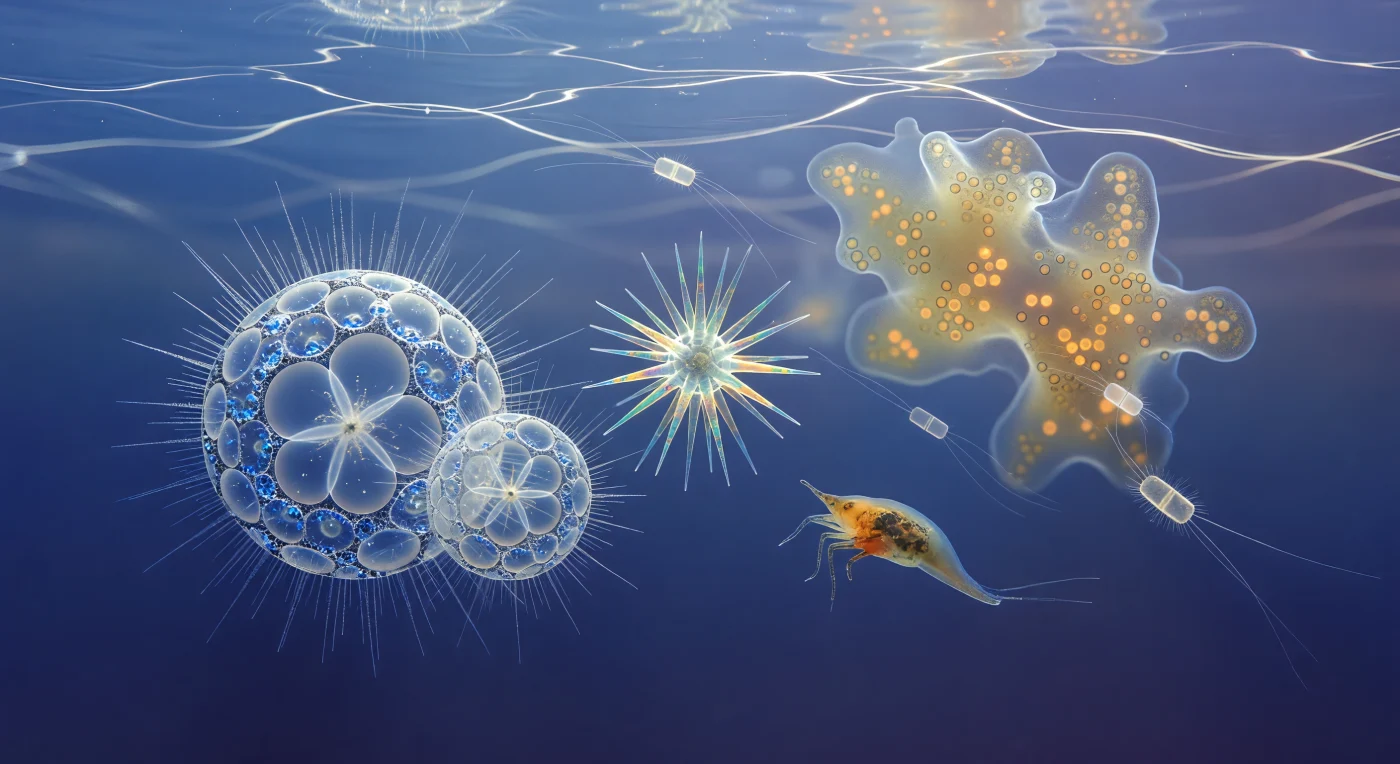
Schwebend in dreißig Metern Tiefe im tropischen Pazifik, auf die Größe einer einzelnen Radiolarienzelle geschrumpft, öffnet sich ringsum ein Kosmos aus Glas und lebendigem Licht: Die Sphaerozoum-Individuen zu deiner Linken hängen wie gotische Kathedralen aus gehauchtem Opalkiesel im Wasser, ihre ineinandergeschachtelten Gitterschalen von hexagonalen Poren durchbrochen, die jeden Kaustikenstrahl von der Oberfläche in kalte blaue Funken zersplittern, während ihre Axopodien-Koronen — mikrometerdünne Mikrotubuli-Nadeln, gestützt von kristallinen Axonemen — als silbrige Heiligenscheine aufleuchten, sobald das zitternde Schleppenwerk der Oberflächenkaustiken sie überstreicht. Hinter dir treibt die Collodarien-Kolonie als warme Bernstein-Nebelwolke heran, ihre zentimetergroße Gallertmatrix von tausenden eingebetteter Dinoflagellaten-Symbionten orange-golden durchglüht, ein biologisches Laternenlicht, das scharf gegen das kühle Blauindigo des offenen Wassers absticht. Die Acantharia daneben dreht ihre zwanzig Strontiumsulfat-Stacheln — arrangiert in präziser ikosaedrischer Symmetrie — langsam durch den Lichtfall, und ihre Doppelbrechung lässt die Stacheln in elektrischem Türkis, Bernsteingelb und Altrosa aufflackern, als wären sie aus lebendiger Seifenhaut gebaut. Zwischen allem gleiten Chaetoceros-Diatomeen wie mattierte Glasweberschiffe dahin, ihre Kieselsäure-Frusteln von haardünnen Setae verlängert, und ein Copepoden-Nauplius — von hier aus so gewaltig wie ein Schulbus — schlägt seine drei Beinpaare in zeitlupenlangsamen Bögen, während das Wasser selbst nie aufhört zu sprechen: ein zitterndes Netz aus weißer Lichtkalligraphie, das unablässig von der Oberfläche herabschreibt und die gesamte lebendige Szene in ständige, traumhafte Bewegung taucht.