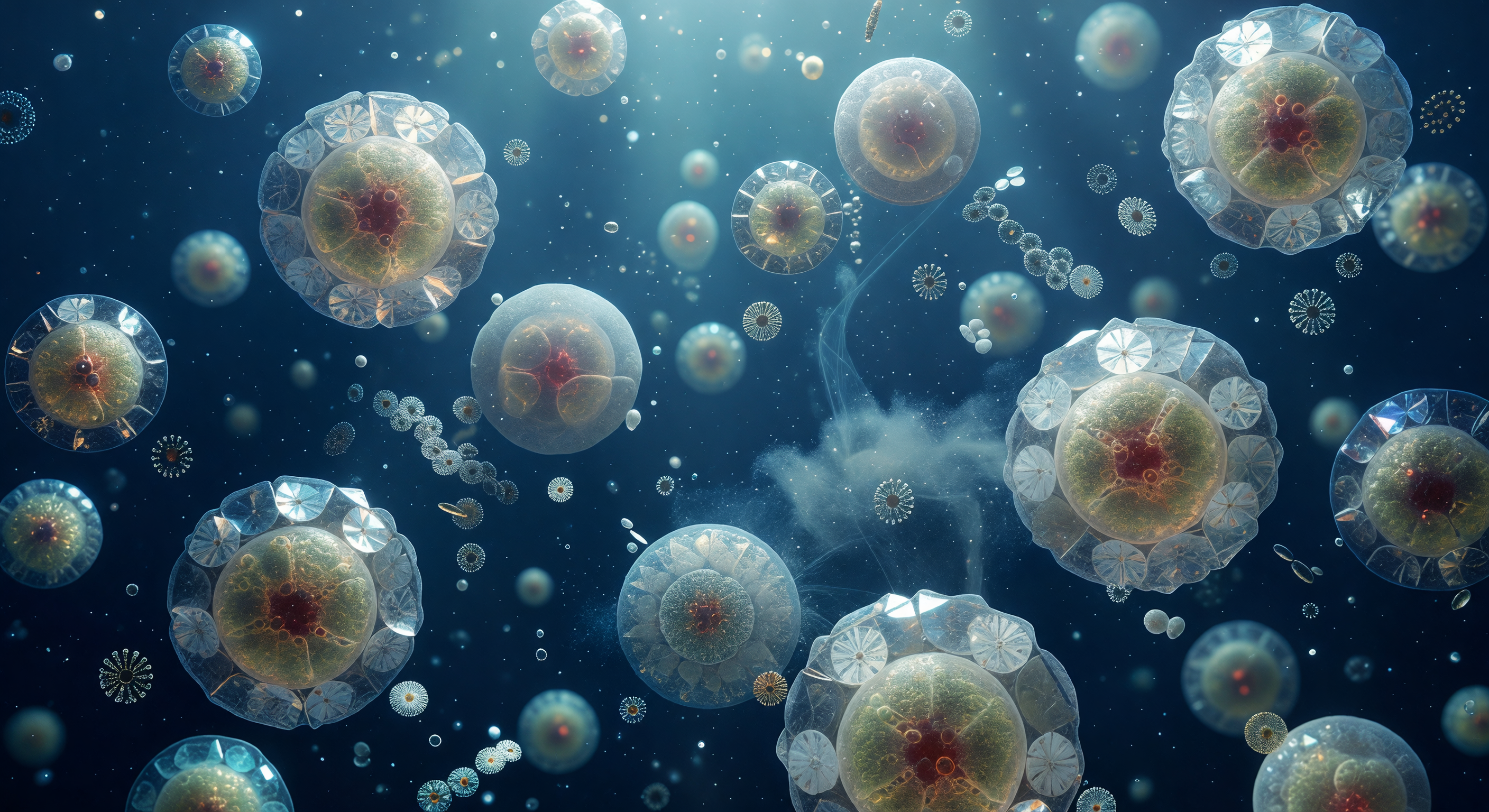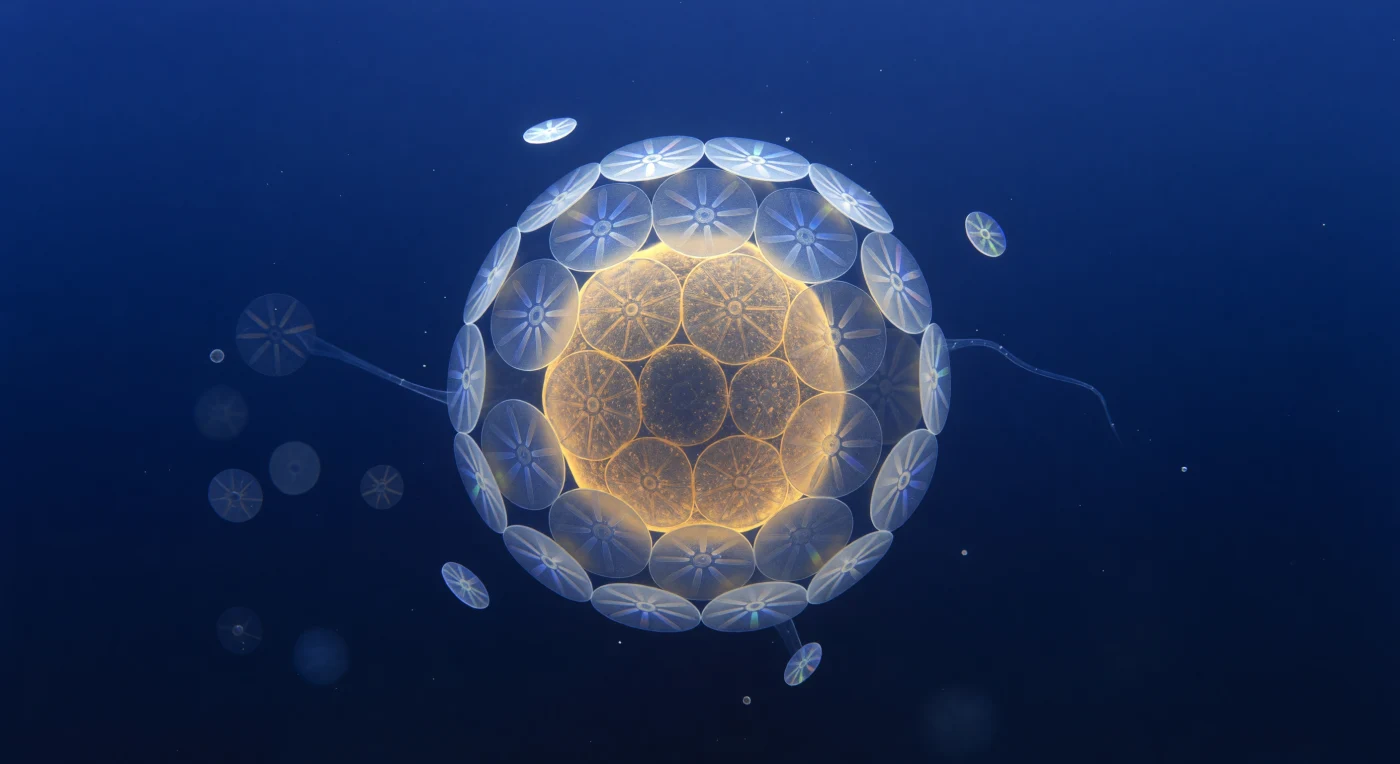
Der Blick fällt vollständig auf eine einzelne *Emiliania huxleyi*-Zelle, die wie ein bernsteinfarbener Mond das gesamte Sichtfeld ausfüllt: ein kaum acht Mikrometer messender, warm leuchtender Körper, dessen Chloroplasten ein honigfarbenes Licht nach außen diffundieren lassen, während eine Rüstung aus zwanzig ineinandergreifenden Kalzitkartuschen — den Coccolithen — die Zelle mit uhrmacherischer Präzision umschließt. Jede dieser kristallinen Kalkscheiben ist selbst ein winziges Prisma, das das von weit oben herabfallende 480-Nanometer-Licht in kurze spektrale Aufblitze bricht: Eisblau geht in Violett über, ein Hauch Mintgrün flackert an einer Kristallkante auf und erlischt sofort wieder. Im Wasser ringsum, dessen Ultramarin keine terrestrische Entsprechung kennt — ein Blau, das schon Meter Meeressäule gefiltert und verdichtet hat —, treiben einzelne losgelöste Coccolithen als winzige Lichtscheiben durch die Wassersäule und rotieren langsam im thermischen Rauschen der Brownschen Bewegung. Diese Zelle ist gleichzeitig Bauwerk und Seifenblase: eine biologisch mineralisierte Architektur, die aus gelöstem Calciumcarbonat in einem Prozess sekretiert wird, der Millionen von Jahren geologischer Kalkablagerungen antreibt — und die dennoch bei der geringsten mechanischen Störung zerfällt.
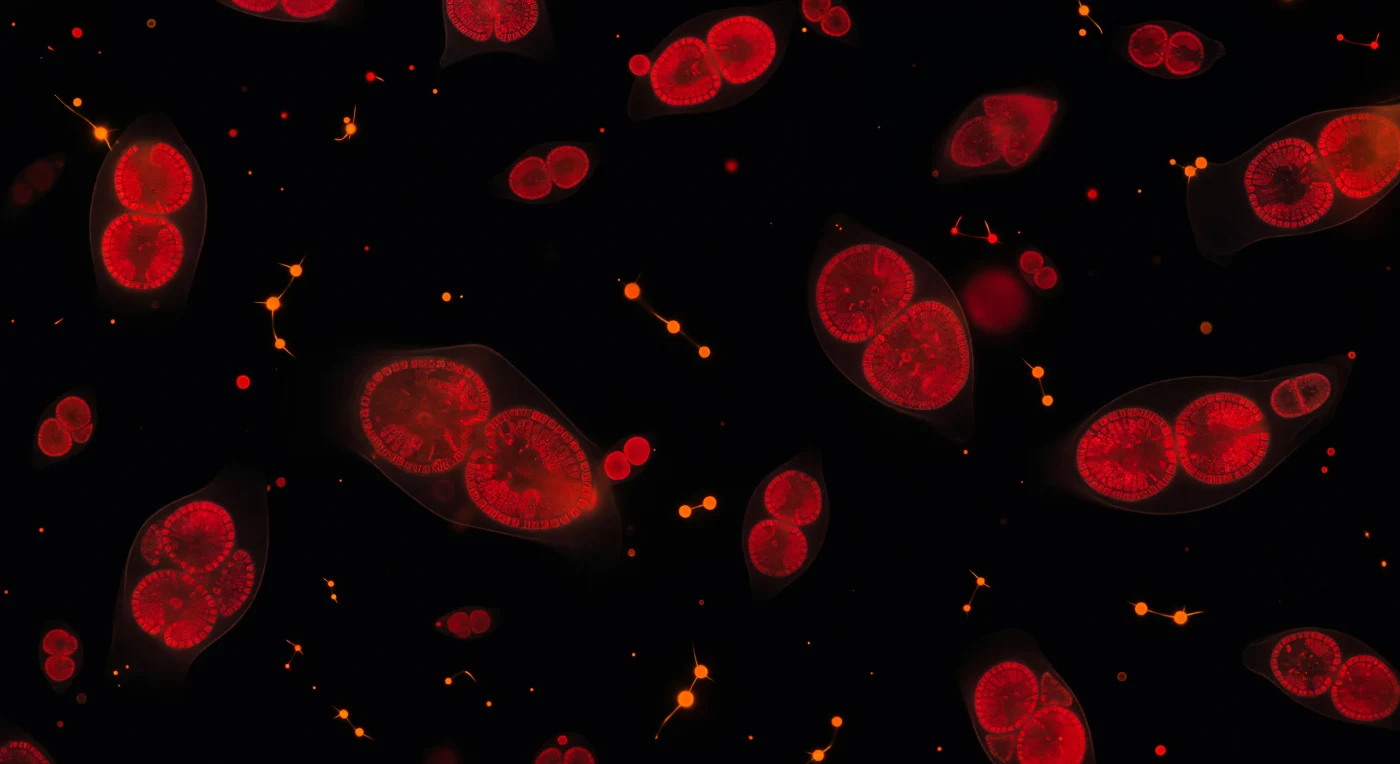
In absoluter Dunkelheit, gemessen in wenigen Mikrometern, schweben wir in einer Welt ohne Horizont und ohne spürbares Gewicht – nur das langsame, quellenlose Treiben der Brownschen Molekularbewegung umgibt uns. Rund um uns brennen Dutzende Phytoplanktonzellen wie tiefkarmesinfarbene Glut, ihre Chlorophyll-Autofluoreszenz bei 680 nm erzeugt ein konzentriertes, sattgesättigtes Scharlachrot, das nicht leuchtet wie eine Lampe, sondern glüht wie Kohle im vollen Brand; innerhalb jeder Zelle zeichnen sich die doppellappigen Chloroplasten als paarige, nierenförmige Strukturen ab, deren innere Thylakoidmembranen das Licht schichtweise auffangen und es an den dicksten Falten ins Burgunderrote vertiefen. Zwischen den kreumesinroten Eukaryoten tauchen vereinzelt scharfe orangefarbene Funken auf – Cyanobakterien, deren Phycoerythrin-Fluoreszenz heißer und greller brennt als das Chlorophyllrot der umgebenden Zellen, einige als einzelne leuchtende Punkte, andere in Paaren oder kurzen Kettenanordnungen, die wie winzige Konstellationslinien durch das schwarze Medium ziehen. Das Medium selbst ist unsichtbar, verrät sich aber durch schwache Aureolen aus gelöstem organischem Material und Membranvesikeln, die das zelluläre Licht streuen und die Dunkelheit gerade so weit strukturieren, dass wir wissen: Wir hängen in Flüssigkeit, nicht im Vakuum – in einem Universum aus einem einzigen Wassertropfen, in dem diese glühenden Körper die einzige Quelle von Farbe, Wärme und Orientierung sind.

Das Wasser um dich herum ist kein Wasser mehr: Du stehst brusttief in einer lebenden Mineralsuspension, so undurchsichtig wie verdünntes Kreidegemisch, denn jeder Milliliter birgt bis zu zehn Millionen Kokkolith-Scheiben aus Kalzit, deren mikroskopische Geometrie das Licht nach wenigen Zentimetern vollständig zurückwirft und die Oberfläche in ein blendendes Jade-Weiß taucht. *Emiliania huxleyi*, die häufigste Coccolithophoride der Weltmeere, baut jede ihrer 2–4 Mikrometer großen Kalzitplatten in einem präzisen biochemischen Prozess auf — Kalziumionen strömen in spezialisierte Vesikel, wo Kristalle Atom für Atom wachsen, bevor die fertigen Kokkolith-Räder durch Exozytose an die Zelloberfläche geschleust werden. Langmuir-Windstreifen ziehen sich in regelmäßigen Abständen von zwei bis vier Metern als cremefarbene Bänder über die Oberfläche, jedes ein sichtbarer Fingerabdruck gegenläufig rotierender Walzenwirbel knapp unter der Wasseroberfläche, die die leichtesten Partikel in kondensmilchfarbene Linien verdichten. Am Horizont schneidet die Blütengrenze wie eine gezogene Linie durch das Bild — links das kreidige Türkis der lebendigen Kalzit-Wolke, rechts das plötzlich fremdartig wirkende Tintenschwarz offenen Ozeans, dessen Transparenz nach der opaken Biosphäre hinter dir fast unwirklich erscheint. Du stehst inmitten eines biogenen Wettersystems, das sich über tausende Kilometer erstreckt, den Strahlungshaushalt der Atmosphäre messbar verändert und nach dem Absterben der Zellen als Kalzitregen in die Tiefsee sinkt — dort, wo es über Jahrmillionen zu Kreide wird.
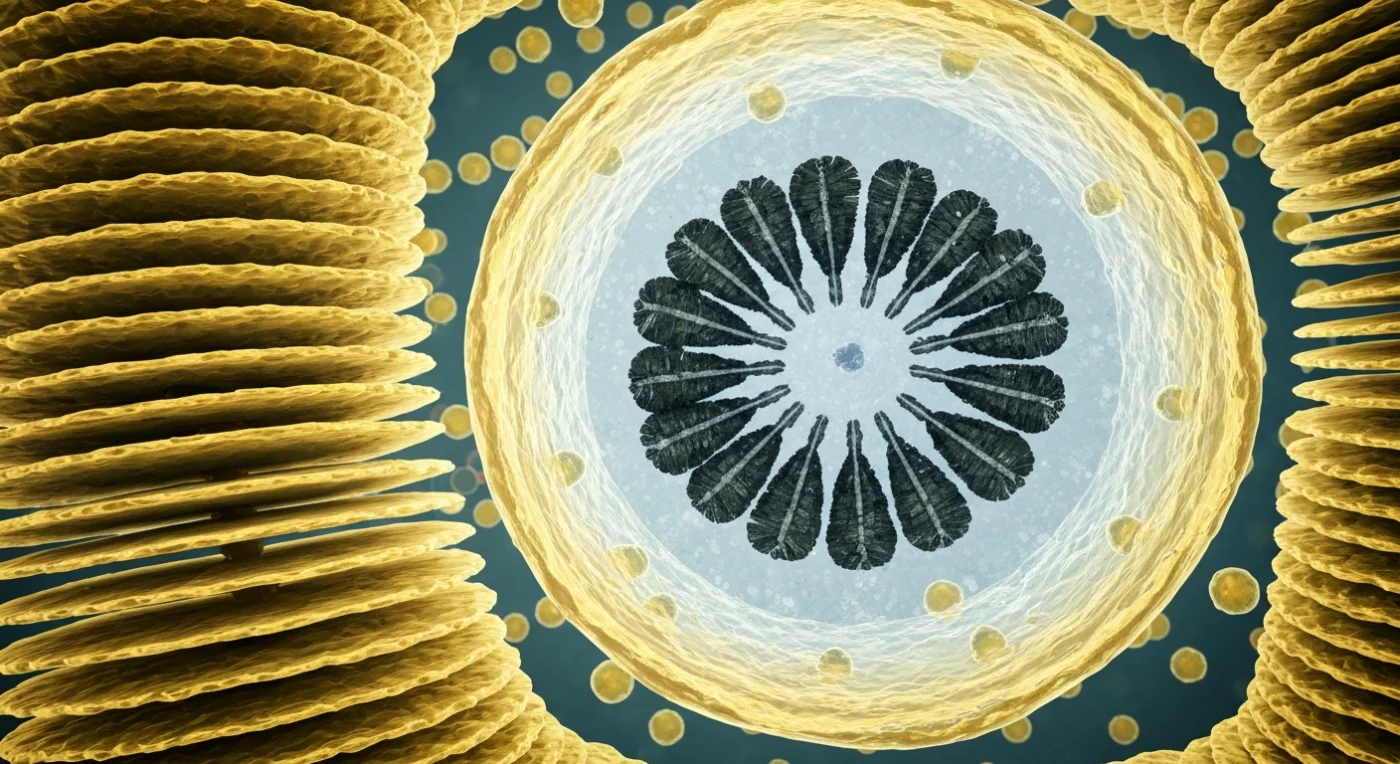
Im Inneren dieser winzigen Zelle erstreckt sich vor dir eine Welt aus präzise gestapelten Membranen – die Golgi-Zisternen erheben sich wie übereinandergelegte Blätter aus getriebenem Bernsteinglas, jede einzelne kaum mehr als einige zehn Nanometer dick, warm-golden leuchtend in der diffusen Helligkeit des Zytoplasmas. An ihrer trans-Seite blähen sich Membranausstülpungen zu kugelförmigen Vesikeln auf, die sich abschnüren und langsam, mit der trägen Unvermeidlichkeit einer Welt ohne nennenswerte Trägheit, durch das dicht besetzte Zytoplasma driften – jedes ein Frachtschiff, beladen mit Kalziumionen und Vorläufermolekülen, die auf ihre Bestimmung warten. Vor dir beherrscht die Coccolithenvesikel das Blickfeld wie eine riesige industrielle Kuppel: eine einzelne membranumschlossene Kammer, in deren kaltem, blaugrau schimmerndem Inneren sich auf einer gespenstisch-irisierenden Polysaccharidscheibe ein Kalzitkranz formt – dreißig und mehr hexagonale Prismen aus dunklem Anthrazit, radial angeordnet mit einer Präzision, die eher einer mathematischen Notwendigkeit als einem Zufall gleicht. Ein Quadrant bleibt offen, die Kristalle dort noch roh an ihren Enden, ihre Wachstumsfronten scharfkantig unterbrochen, während Kalziumionen in unsichtbaren Pulsen durch die Vesikelmembran strömen und die Mineralisierung in Echtzeit voranschreitet. Das dichte Gewimmel von Ribosomen auf den Oberflächen des endoplasmatischen Retikulums, die gelegentlichen orangeroten Impulse passierender Mitochondrien, die Bräune des granulären Hintergrunds – all das verdichtet sich zu dem Eindruck eines vollständig besetzten, schweigend arbeitenden Innenraums, in dem aus dem Meer Stein gemacht wird, Molekül für Molekül.

Vor dir schwebt ein Gebilde, das im Dunkel aus sich selbst heraus leuchtet: eine Kokkolithmosphäre, deren fünfzehn ineinandergreifende Kalzitradreifen eine nahezu perfekte Kugel bilden, jede Platte verwandelt vom kreuzpolarisierten Licht in ein strahlendes Mandala aus leuchtendem Weiß und samtschwarzem Extinktionskreuz. Die Kalzitprismen jedes einzelnen Kalkplättchens – winzige Rhomboeder, die der lebende Organismus Ion für Ion in der Kälte des Ozeans aufgebaut hat – zeigen ihre Doppelbrechung als erste Ordnung Weiß, das so intensiv wirkt, als habe es inneren Druck, während an den verdickten Speichenrändern dünnfilmische Interferenz ein warmes Elfenbein-Gold aufsteigen lässt. Um diese zentrale Sphäre herum treiben freie, abgestoßene Kokkolithmosphären in alle Richtungen und bilden eine Konstellation geometrischer Einzelwelten: jede Platte kaum drei Mikrometer im Durchmesser, flach wie getriebene Folie, doch kristallographisch so präzise gebaut wie ein Kathedralenfenster. Tiefe entsteht einzig durch die abnehmende Schärfe der ferneren Plättchen, die nächsten hart und klar in ihren Extinktionsgrenzen, die äußersten zu weichen Lichtschlieren aufgelöst, sodass der schwarze Raum trotz jeglicher fehlender Referenz als ein Volumen von beträchtlicher Ausdehnung lesbar wird – ein Kronleuchter, errichtet von etwas Lebendigem, treibend drei Kilometer über dem Meeresboden.
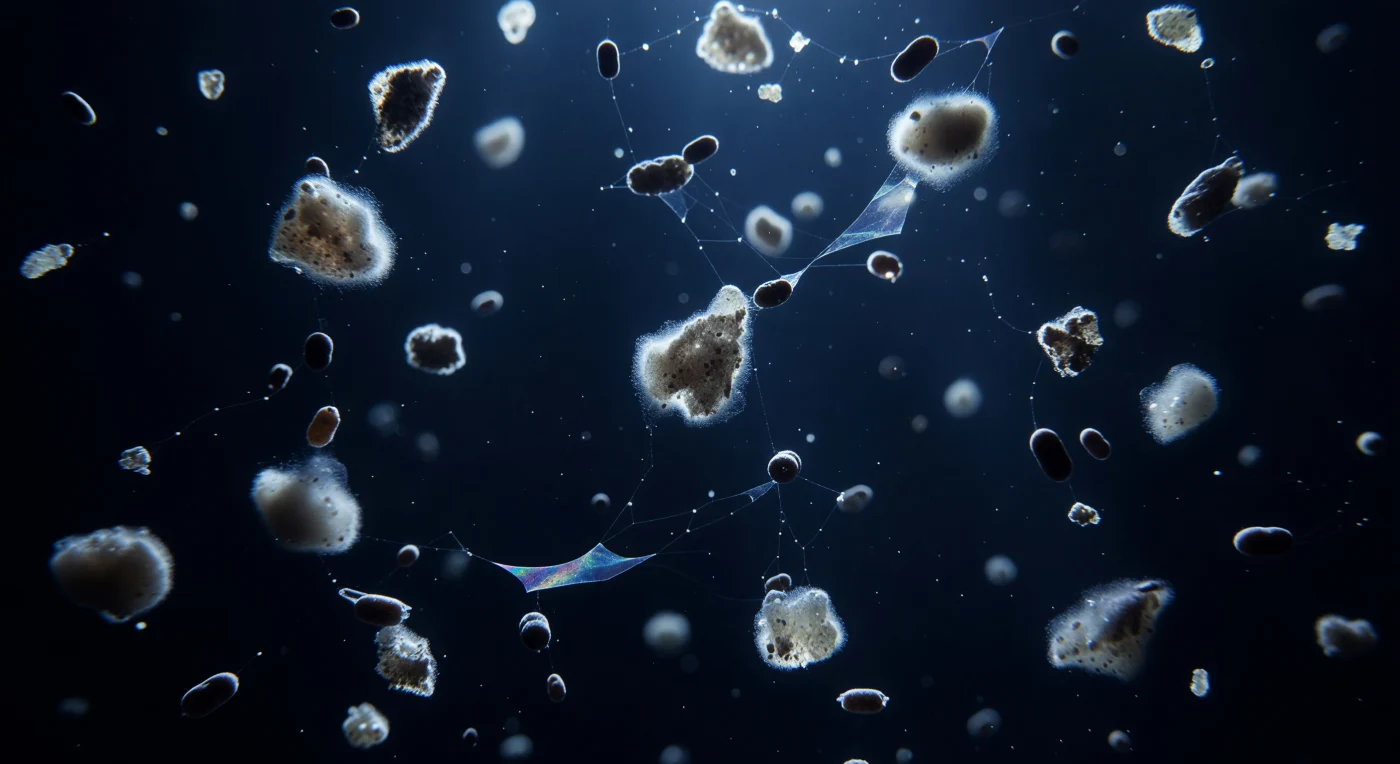
Im tiefblauen Dunkel in 200 Metern Tiefe zieht eine stumme Prozession herab: wattige, grau-braune Aggregate aus zerschellten Coccolithen, toten Kieselalgenschalen, Schleimfäden und verdautem Zellmaterial treiben in äußerster Zeitlupe abwärts, jede Flocke von den letzten gedämpften Photonen aus der euphotischen Zone in ein kühles, blau-weißes Schimmern gehüllt, da die eingebetteten Kalzitplättchen das Restlicht zwischen 450 und 490 Nanometern zurückwerfen. Zwischen diesen Wolkenfetzen organischer Erinnerung schießen dunkelbraune, zylindrische Kotpillen weitaus schneller und gerader hinab, dicht und wächsern, als hätten sie die Schwerkraft effizienter begriffen als ihre porösen Nachbarn. Fast unsichtbar verbinden TEP – transparente Exopolymerpartikel, ausgeschieden von Algen und Bakterien – die Aggregate in zitternden Schleiernetzen, die sich nur an ihren Rändern als irisierender Hauch verraten, eine kollabierte Seifenblasenarchitektur zwischen dem Treibgut. Diese biologische Pumpe, die seit Hunderten von Millionen Jahren kohlenstoffreiches Material in die Tiefe befördert und in Sedimenten wie den Kreidefelsen von Dover archiviert, vollzieht sich hier als lautloses, gravitätisches Schneien – der Ozean schreibt seinen Kohlenstoffhaushalt Flocke für Flocke in die ewige Dunkelheit.
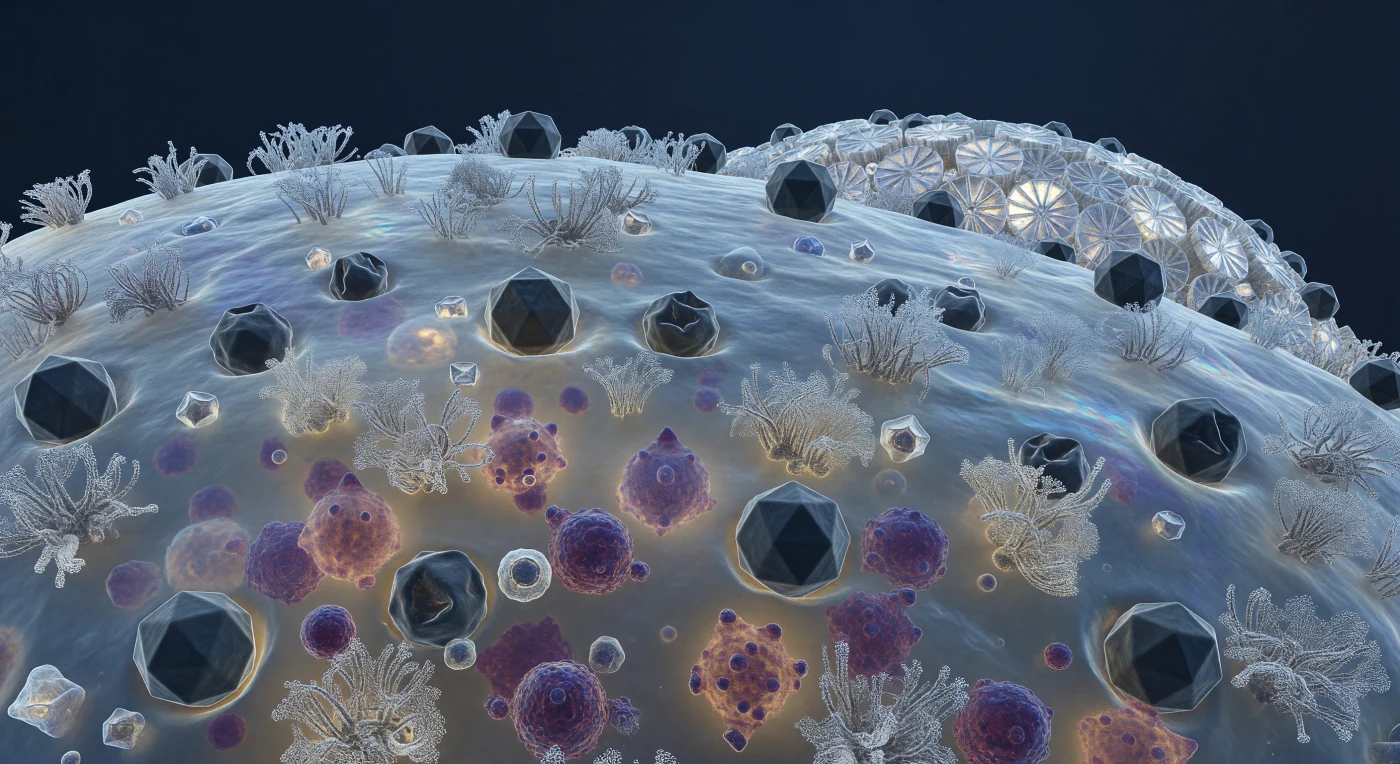
Die gesamte Welt, die sich vor dem Betrachter erstreckt, ist die sanft gewölbte Außenhaut einer einzigen Zelle – eine halbdurchsichtige, blaugraue Membran, die unter dem molekularen Zittern der Brownschen Bewegung leise bebt und von dichten Wäldern aus glykoproteinbesetzten Rezeptorclustern durchbrochen wird, die wie verwitterte Korallenformationen aus der Lipiddoppelschicht emporragen. Gegen diese biologische Landschaft pressen sich an Dutzenden von Stellen dunkle, schiefergraue ikosaedrische Viruskapsiden – jede ein geometrisch präzises, zwanzigflächiges Gebilde von rund 200 Nanometern Durchmesser –, manche noch makellos scharf an den Kanten, andere sichtlich kollabiert und wie zerdrückte geodätische Kuppeln in sich zusammengesunken, nachdem sie ihr Erbgut in die Wirtszelle injiziert haben. Wo Kapsid auf Rezeptor trifft, zieht sich die Membran in flache Mulden zurück, ein stilles mechanisches Nachgeben, das die molekulare Präzision dieser Invasion sichtbar macht. Durch die milchig-bernsteinfarbene Membranwand hindurch drängen sich im Inneren dichte, dunkelviolette und magentafarbene Massen – neu assemblierende Virionen in fabrikartigem Maßstab, deren wachsende Zahl das Cytoplasma von innen ausbeult und die Zellwand nach außen wölbt wie ein überfüllter Sack. Im Hintergrund, wo die Membrankurve sich dem Horizont der Kalkschale nähert, ragen die weißen Calcitplatten der Coccolithen wie keramische Strebepfeiler auf – kristalline Räder von makelloser Geometrie, die das spärliche Licht in prismatische Blitze zersplittern, während die Zelle, von innen überschrieben und von außen besetzt, in aller Stille an ihrer eigenen molekularen Grenze aufgerieben wird.

Im tiefsten Blau des offenen Ozeans, hundert Meter unter der Oberfläche, schwebt der Betrachter inmitten eines lebendigen Zwielichts: Das Wasser selbst scheint zu leuchten, durchdrungen von einem spektral engen Kobaltblau bei 475 Nanometern, das kaum zwei Prozent der Oberflächenintensität erreicht und dennoch ausreicht, um Dutzende von Phytoplanktonzellen als warme olivgoldene Laternen gegen das kalte Indigo sichtbar zu machen. Dinoflagellaten hängen im Wasserfeld wie bernsteinfarbene Glühkörper, ihre Amphiesma-Panzerung schwach prismatisch schimmernd, während Diatomeen-Ketten aus biogenem Siliziumdioxid in losen Spiralen treiben und ihr goldbraunes Innenleben wie komprimierte Glut aufleuchten lassen – all das konzentriert sich in der tiefen Chlorophyllmaximalschicht, wo Nährstoffgradient und Lichtminimum sich zum optimalen Wachstumshorizont überlagern. Ein Marineeschneeflocken-Aggregat sinkt langsam vorbei – in diesem Maßstab so groß wie ein Gebäude –, ein durchscheinendes Gewirr aus Exopolymerfäden, leeren Coccolithen-Kalkplatten und Kotballen, das im Gegenlicht des blauen Schimmers über ihm fast luminesziert, bevor es in das tiefere Indigo darunter entschwindet. Noch weiter unten verblassen die letzten weißen Funken weiterer Schneeteilchen im ausklingenden Licht, und die Grenze zur aphoten Zone löst sich nicht als Linie, sondern als allmärliges Erlöschen der Wärme auf – bis nur noch das Blau bleibt und dann das Nichts.

Vor dir erhebt sich *Ceratium tripos* wie eine bernsteinfarbene Kathedrale im Indigoschwarz des Ozeans — ein einziges Lebewesen, dessen drei hohle Kalksporn-Hörner sich fast einen halben Millimeter weit erstrecken und deren wände dünn genug sind, um das erste zögernde Licht der Dämmerung hindurchzulassen, das von der Grenzfläche zwischen Luft und Wasser zwei Körperlängen über dir in breiten rosa-stählernen Säulen herabfällt. Die amphiesmatischen Platten, die den Zellkörper bedecken, fügen sich wie ein Wabenmosaik aus schwach irisierenden Paneelen zusammen, und im Inneren pulsieren die Chloroplasten — warme, goldbraune Scheiben — mit jedem prismatischen Lichtbogen, den die Kapillarwellen der Oberfläche über den Rumpf der Zelle streichen. Am Äquator der Zelle schlägt das Quergeissel in seiner cingulären Rinne einen unsichtbaren Rhythmus, der sich als silberner Schimmer manifestiert, kaum wahrnehmbar, aber beständig — ein mechanisches Wunder auf der Grenze zwischen dem Sichtbaren und dem Erahnbaren. In der Mitteldistanz, wo in Wirklichkeit nur drei bis vier Zentimeter Wasser liegen, überragt ein Ruderfußkrebs die Szene mit der schweigenden Wucht eines Glaswolkenkratzers: durch seinen transparenten Körper hindurch erkennt man das gegliederte Urosom, die gefrorenen Ruderantennen, und zwischen euch beiden treiben vereinzelte Coccolithen — winzige Kalkräder von zwei bis vier Mikrometern — in der Brownschen Bewegung und entzünden sich kurz als kalte Funken im wachsenden Licht.

Der Betrachter ist vollständig eingetaucht in eine so dicht besiedelte Suspension aus *Ostreococcus tauri*-Zellen, dass das Wasser selbst zur lebendigen Substanz wird – ein jadegrüner Nebel ohne Horizont, ohne Boden, ohne Decke, der sich in jede Richtung ins Unendliche erstreckt. *Ostreococcus tauri* ist der kleinste bekannte freilebende eukaryotische Organismus überhaupt, mit einem Zelldurchmesser von nur 0,8 Mikrometern, der damit an die Wellenlänge des sichtbaren Lichts selbst heranreicht und die Grenze zwischen Teilchen und Welle verwischt. Jede dieser kugelförmigen Zellen trägt einen einzigen riesigen Chloroplasten, der den Zellkörper nahezu vollständig ausfüllt – ein dunkles Jadegrün, das bei Anregung in tiefes Chlorophyll-Rot aufleuchtet und das umgebende Medium kollektiv färbt, als würde man Seeglas gegen das Licht eines Wintertages halten. Die Brownschen Bewegungen sind absolut und allgegenwärtig: Kein Zelle steht still, das gesamte Feld atmet in einem probabilistischen Rhythmus thermischer Strömungen, und Tiefe löst sich nicht als Distanz auf, sondern als Farbsättigung – nahe Zellen als leuchtende Laternen, entfernte bereits als Geister, die in der kollektiven Glut des Nebels verschwimmen. In dieser Suspension, so dicht, dass die mittlere freie Weglänge der Photonen kürzer ist als der Abstand zwischen benachbarten Zellen, wird der Organismus ununterscheidbar vom Medium: Der Nebel *ist* das Leben.
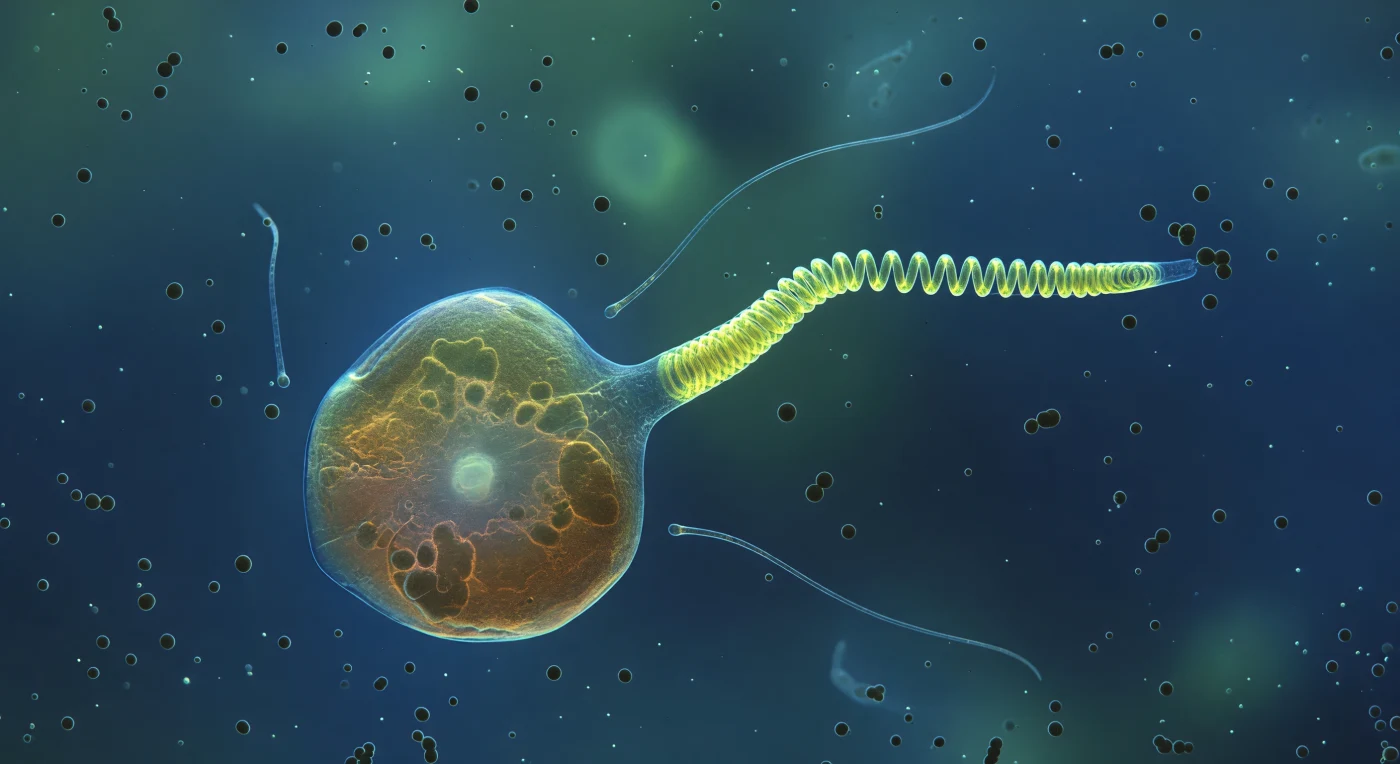
Vor dir entfaltet sich eine Welt aus ozeanblauem Licht, diffus und kalt, als wäre man tief in ein fluoreszierendes Gewässer eingetaucht – überall präsent und doch ohne erkennbare Quelle. Eine einzelne *Chrysochromulina*-Zelle füllt den Blick wie ein zitternder Bernsteinglobus: halbdurchsichtig, golden-braun, mit sichtbaren Chloroplasten als dunkle Lappen hinter der schimmernden Plasmamembran und einem blassen, leuchtschwachen Zellkern im Inneren. Aus einem Pol der Zelle schießt das Haptonema in seiner dramatischen Verwandlung hervor – der proximale Teil bereits zu einer straffen, neongelb-grünen Helix zusammengefaltet, der distale Abschnitt noch als steifer Stab, gerade am Knicken, die gespeicherte Biegeenergie eines extrazellulären Mikrotubuli-Bündels in einem einzigen biophysikalischen Moment entladen. Die beiden Geißeln treiben seitlich der Zelle wie silberne Fäden im Medium – entspannt und nahezu durchsichtig, ein ruhiger Kontrast zur Gewalt des Haptonema-Rückstoßes. In ihrer unmittelbaren Nähe clustern matte Kugeln von etwa einem Mikrometer Durchmesser – Bakterien, die im chemischen Gradienten der größeren Zelle treiben wie stumme Planeten um einen leuchtenden Stern, während das Wasser selbst mit gelöster organischer Substanz und Membranvesikeln milchig schimmert und in der Ferne ins Kobaltblau verschwindet.

Von der Bugspitze des Forschungsschiffs aus öffnet sich ein Anblick, der kaum glaublicher wirken könnte: unmittelbar unter dem Geländer verläuft eine fast chirurgisch scharfe Grenzlinie, auf deren einer Seite tiefes Indigo-Kobalt in scheinbar bodenlose Transparenz taucht, während auf der anderen Seite ein opakes, kalkig-türkisfarbenes Wasser leuchtet, als wäre gemahlener Kalkstein in Gletscherschmelze aufgelöst worden. Diese seltsame innere Lumineszenz entsteht, weil Milliarden von Coccolithophorenzellen – winzige, 5 bis 10 Mikrometer große Algen der Art *Emiliania huxleyi* – ihren Körper mit geometrisch präzisen Kalzitplatten gepanzert haben, deren 2 bis 4 Mikrometer breite Kristallscheiben das Sonnenlicht isotrop in alle Richtungen zurückwerfen wie mikroskopische Prismen. Die Langmuir-Zirkulation hat den Oberflächenschaum in parallele weiße Windstreifen geordnet, die genau entlang der Scherzone der beiden Wassermassen verlaufen, während ein Basstölpel sich mit geschlossenen Schwingen in die produktive Grenzlinie bohrt und beim Eintauchen einen Schwall milchweißen Wassers aufwirft, der im tief stehenden Nachmittagssonnenlicht für einen Herzschlag lang aufblüht. Ein kaum wahrnehmbarer Schwefelgeruch – Dimethylsulfid, freigesetzt von gestressten Zellen – liegt in der Luft, das Zeichen jenes biogeochemischen Prozesses, durch den diese Blüte nicht nur das Licht, sondern letztlich auch das Klima berührt.

Der Sedimentkern vor dir ist eine gepresste Bibliothek des Meeres — ein Querschnitt von zehn Zentimetern, der Jahrmillionen komprimierter Tiefseegeschichte enthält, geschichtet in Laminae aus Cremeweiß und gebrochenem Elfenbein, die unter dem schrägen Seitenlicht wie die Jahresringe eines unvorstellbar langsamen Lebens aufleuchten. Du existierst auf der Ebene einer einzelnen Kalkscheibe, eines winzigen geometrischen Rades von kaum drei Mikrometern Durchmesser — eines Coccolithen, der Panzerschuppe einer einzelligen Alge, die vor zehn Millionen Jahren im Licht der Meeresoberfläche photosynthetisierte, bevor sie absank und sich in diesem dichten Labyrinth aus interlockenden Kalzitkristallen zu einem Gestein verdichtete, das geologisch wirkt, aber einmal lebte. Die Strahlen des Lichts fallen schräg durch die Sedimentsäule wie spätnachmittägliche Sonne durch gefrostetes Glas und werfen scharfe Mikroschatten über die erhabenen Ränder jedes Rades, sodass die Matrix zu einer Landschaft von Kratern und Bögen wird, durchzogen von Zonen leicht dunklerer Einträglichkeit — den Spuren glazialer Epochen, in denen tonartige Mineralien die Kalzit-Ooze unterbrachen und die biologische Produktivität der Oberflächenwasser zurückging. Was hier zurückbleibt, ist die obsessiv genaue Geometrie des Lebens: Speichenanordnungen und Randarchitekturen, die ein Paläoozeanograph noch im tiefsten Diagenesegrad als *Emiliania* oder *Calcidiscus* erkennen würde — Identitäten, eingeschrieben in Kristallsymmetrie und bewahrt durch die Gleichgültigkeit des tiefen Meeresbodens.
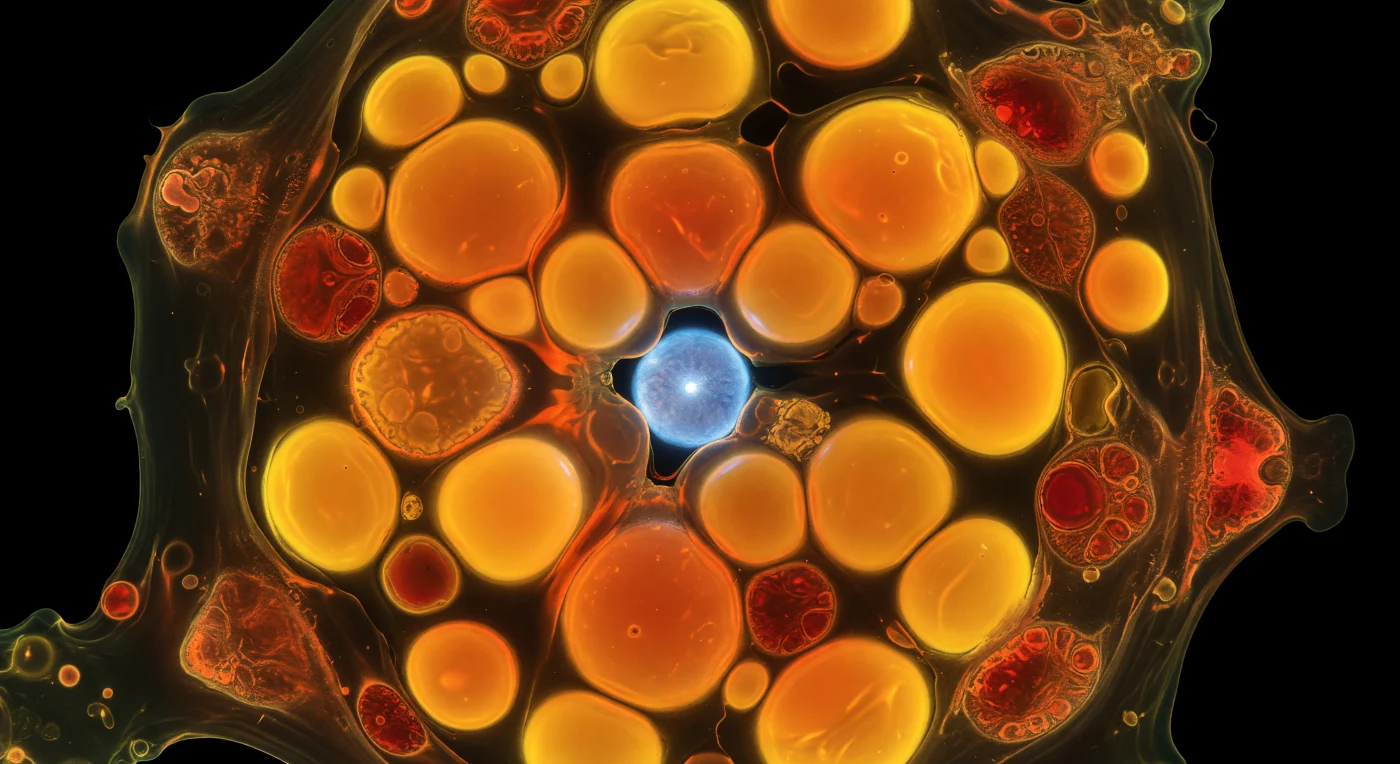
Der Blick taucht ein in das Innere einer einzigen, stickstoffgehungerten Zelle, die sich in ein leuchtendes Chaos verwandelt hat: Überall drängen sich riesige, kugelförmige Lipidtröpfchen aneinander, jedes in einem intensiven Orange-Gold brennend, das nicht von außen beleuchtet wird, sondern von innen strahlt — Nilrot, eingelagert in jedes neutrale Lipidmolekül, verwandelt jedes Tröpfchen in eine selbstleuchtende Laterne. Diese Fettkugeln sind das Ergebnis einer metabolischen Umleitung: Wenn Stickstoff knapp wird, stellt *Emiliania huxleyi* die Proteinsynthese zurück und lenkt Kohlenstoffflüsse stattdessen in Triacylglyceride, die sich als dichte Speicherreservoirs im Cytoplasma anhäufen, bis sie die gesamte Zellarchitektur neu ordnen. An den Rändern dieses orange glühenden Gedränges haben sich die Chloroplasten zurückgezogen — ihre Chlorophyll-Autofluoreszenz noch ein mattes Karminrot, wie abkühlende Glut neben einem Feuersturm, ihre Thylakoidmembranen zusammengedrückt zwischen vordrängenden Öltröpfchen. Irgendwo im Inneren, durch eine schmale Lücke zwischen bernsteinfarbenen Kugeln kaum sichtbar, leuchtet der Zellkern in kühlem DAPI-Blau — ein ferner, stiller Mond, eingeschlossen in einer Welt, die ausschließlich von ihrem eigenen Licht erhellt wird, während draußen, jenseits der Plasmamembran, absolutes Schwarz herrscht.

Die Hände des Betrachters schneiden durch das schwarze Wasser wie Klingen, und an jedem Punkt des Kontakts bricht Licht aus der Dunkelheit hervor – kein Schein, keine Reflexion, sondern Eigenleuchten, präzise auf 460 Nanometer geeicht, ein Blau von solcher Sättigung, dass es unwirklich wirkt, als hätte das Meer eine Farbe angenommen, die dem sichtbaren Spektrum eigentlich nicht gehört. Was hier leuchtet, sind Millionen von *Lingulodinium polyedra*-Zellen, jede sechs bis zwölf Mikrometer groß, jede ausgestattet mit Scintillonen – membranumschlossenen Kammern voller Luciferase und Luciferin, die auf mechanischen Druck reagieren wie Auslöser einer Waffe, die seit dem Präkambrium gespannt ist. Der Druckwelle einer bewegten Handfläche folgt eine Kaskade biochemischer Entladungen, die sich von Zelle zu Zelle ausbreitet und die Geometrie unsichtbarer Strömungen – Wirbel, Eddies, Turbulenzen – als leuchtendes Diagramm in die Dunkelheit schreibt. Fünfzig Meter entfernt zieht das Kielwasser eines längst verschwundenen Bootes als strahlend blau-weißer Strom über das Wasser, ein Fluss aus verdichtetem Leben, so hell, dass seine Ränder scharf erscheinen wie Schnitte. Über dem Betrachter gibt es keinen Horizont mehr, keinen Mond, keine Sterne – nur das Wasser selbst kennt noch seine eigene Grenze, und es bezeichnet sie in kaltem biologischem Feuer.
Im Abstand von zwei Millimetern schwebt der Betrachter vor einem Körper, der weniger wie ein Tier als wie ein lebendes Instrument aus Glas wirkt: der Copepode *Calanus*, dessen chitinöser Panzer so transparent ist, dass der smaragdgrüne Darmschlauch und die dicht gepackten bernsteinfarbenen Eicluster durch drei Schichten durchsichtiger Cuticula leuchten, von durchfallendem Ozeanblau von innen beleuchtet wie eine Laterne aus Eis. Die Maxillipeden – federartig angeordnete Anhänge aus haarfeinen Setae – vibrieren am Rand des Sichtfelds und fangen einzelne Coccolithophoren-Zellen der Art *Emiliania huxleyi* ein, deren Kalzitplatten in konzentrischen Ringen kalten Silberlichts aufblitzen, bevor sie von den Mundwerkzeugen zermalmt werden und als Glitzerwolken winziger Zwei-Mikrometer-Scheiben in die Wassersäule explodieren. Das umgebende Wasser ist keine Leere, sondern eine Suspension aus türkisweißem Licht – bis zu zehn Millionen abgelöste Coccolithen pro Milliliter streuen die verfügbare Helligkeit zu einem leuchtenden Dunst, in dem ganze Coccosphären wie gepanzerte Miniaturplaneten in langsamen Spiralbahnen auf den Fresswirbel zutreiben, ihre geometrischen Kalzitgehäuse von Silber zu Gold zu eisigem Weiß wechselnd, während sie sich drehen und dem Sog gehorchen. Die Tiefe hinter dem Copepoden löst sich nicht in Schwärze auf, sondern in eine unendliche blauweiße Atmosphäre, in der jede weitere Schicht etwas heller leuchtet als die vorherige – das Blütengewässer so dicht mit gestreutem Kalzit gesättigt, dass es in alle Richtungen als Nebel wirkt und jede Vorstellung von Entfernung auflöst.

Im tiefen Ozean, zwischen fünf Mikrometer voneinander entfernt wie zwei Welten, schweben diese beiden Zellen der Emiliania huxleyi im gleichen Wassergrau – und könnten dabei kaum verschiedener sein. Die diploide C-Phase-Zelle zur Linken ist vollständig gepanzert: eine Kokkolithmosphäre aus cremefarbenen Kalzitplatten, deren trigonale Kristallklingen das diffuse Blaulicht von oben in kalte, prismatische Funken zurückwerfen, die gesamte Oberfläche eine Architektur aus Radialspeichen, ineinandergreifenden Schilden und kleinen zentralen Öffnungen – ein lebendes Mineral, das im dunklen Wasser leuchtet. Unmittelbar daneben zeigt die haploide N-Phase-Zelle das nackte Gegenteil: keine Schale, nur eine weiche, transluzente Membran aus grünlichem Creme, hinter der Chloroplasten ihr gedämpftes Bernstein-Jade-Glühen abgeben, und aus deren Basis zwei Geißeln wie nasse Glasfäden in eleganten Sinuswellen ausschlagen, eingefroren im Augenblick maximaler Auslenkung, zwischen ihnen das hauchzarte Haptonema als kaum sichtbare Federspirale. Diese beiden Zellformen gehören zum gleichen Lebenszyklus – die gepanzerte Zelle pflanzt sich durch Meiose fort und kann die ungeschützte Geißelzelle hervorbringen, die sich ihrerseits durch Sexualreproduktion wieder zur diploiden Phase zusammenfindet, ein Wechsel, den die Ozeane seit über 200 Millionen Jahren vollziehen. Im Hintergrund treiben vereinzelte losgelöste Koccolithen als winzige weiße Lichtfunken durch das Ultramarin – und erinnern daran, dass Milliarden solcher Platten seit Jahrmillionen auf den Meeresgrund sinken und dort zu den Kreideschichten wurden, die heute ganze Küsten formen.

Der Blick von unten auf die Kreidefelsen von Dover ist ein Schwindel erregender Sturz rückwärts in die Zeit: Die fast senkrechte Wand steigt in schwindelerregende Höhe auf, ihr Weiß so intensiv im schrägfallenden Nachmittagslicht, dass die Oberfläche selbst zu leuchten scheint – ein retinales Nachbild gegen den blaugrauen Himmel über der Nordsee. Was wie poröser Stein wirkt, ist in Wirklichkeit eine biologische Kathedrale: komprimiertes Kalkoplankton, Milliarden einzelner Coccolithen – die winzigen Kalkscheiben, die einst Mikroalgen wie *Emiliania huxleyi* panzerten –, die über Millionen von Jahren auf den Meeresboden sanken und sich zu dieser biogenen Karbonatsäule verfestigten, die heute hunderte Meter aufragt. Die dunklen Flintzonen, die wie Tuschelinien quer durch das blendende Weiß ziehen, sind diagenetische Geister, chemische Signaturen längst vergangener Meeresböden, Schweigen in hartem Glas eingeschlossen – jede Schicht ein Atemzug geologischer Zeit zwischen aufeinanderfolgenden Blüteperioden. Eine einzelne Eissturmvogel, kaum einen Zentimeter groß in der Distanz, sitzt regungslos auf einem Felsvorsprung auf halber Höhe und macht die schiere Vertikale plötzlich körperlich greifbar: Dieses weiße Monument ist nicht Gestein, sondern geronnenes Leben – ein Archiv unsichtbarer urzeitlicher Ozeane aus Licht, Kalzium und stiller, massenhafter Drift.