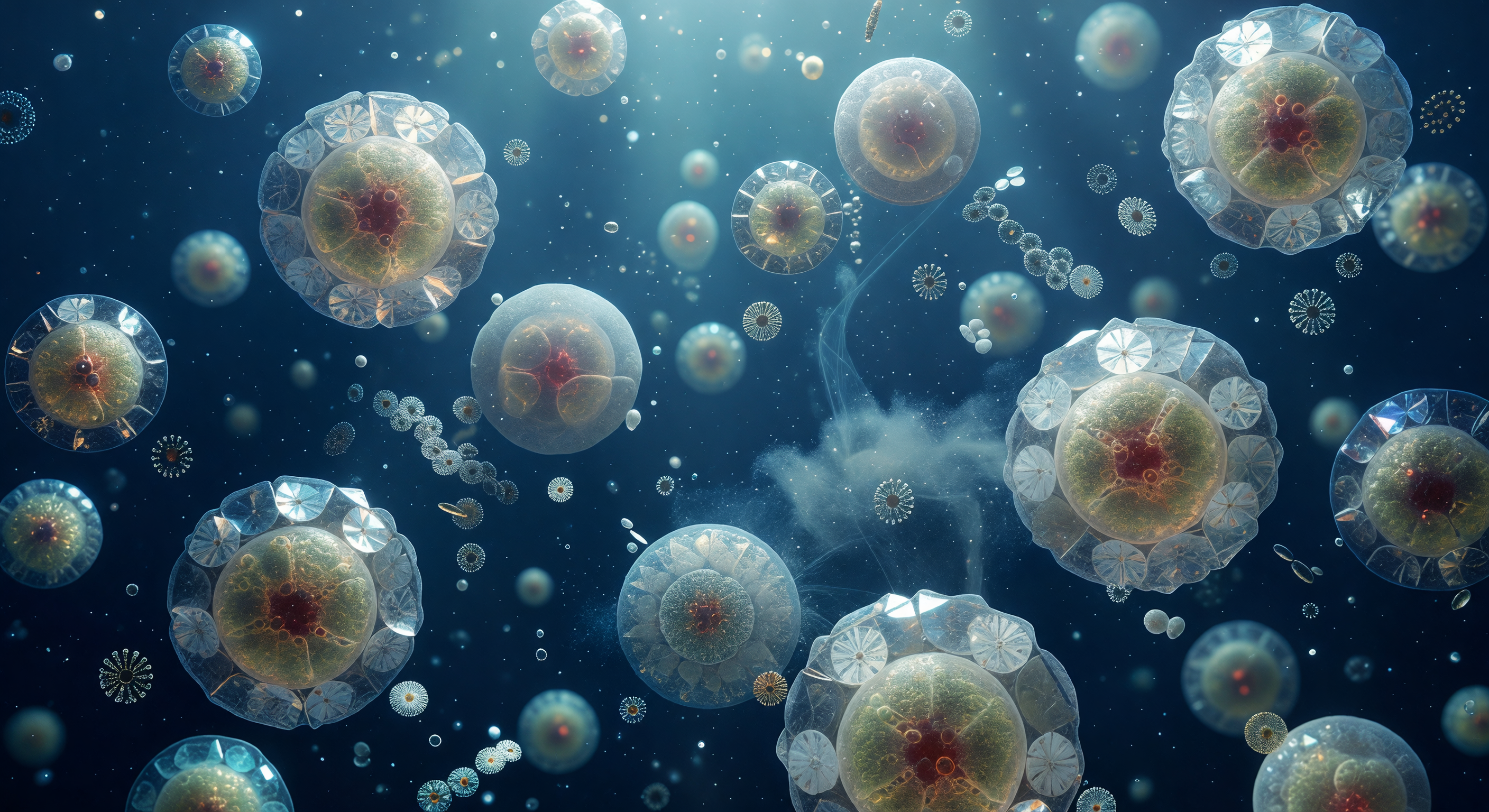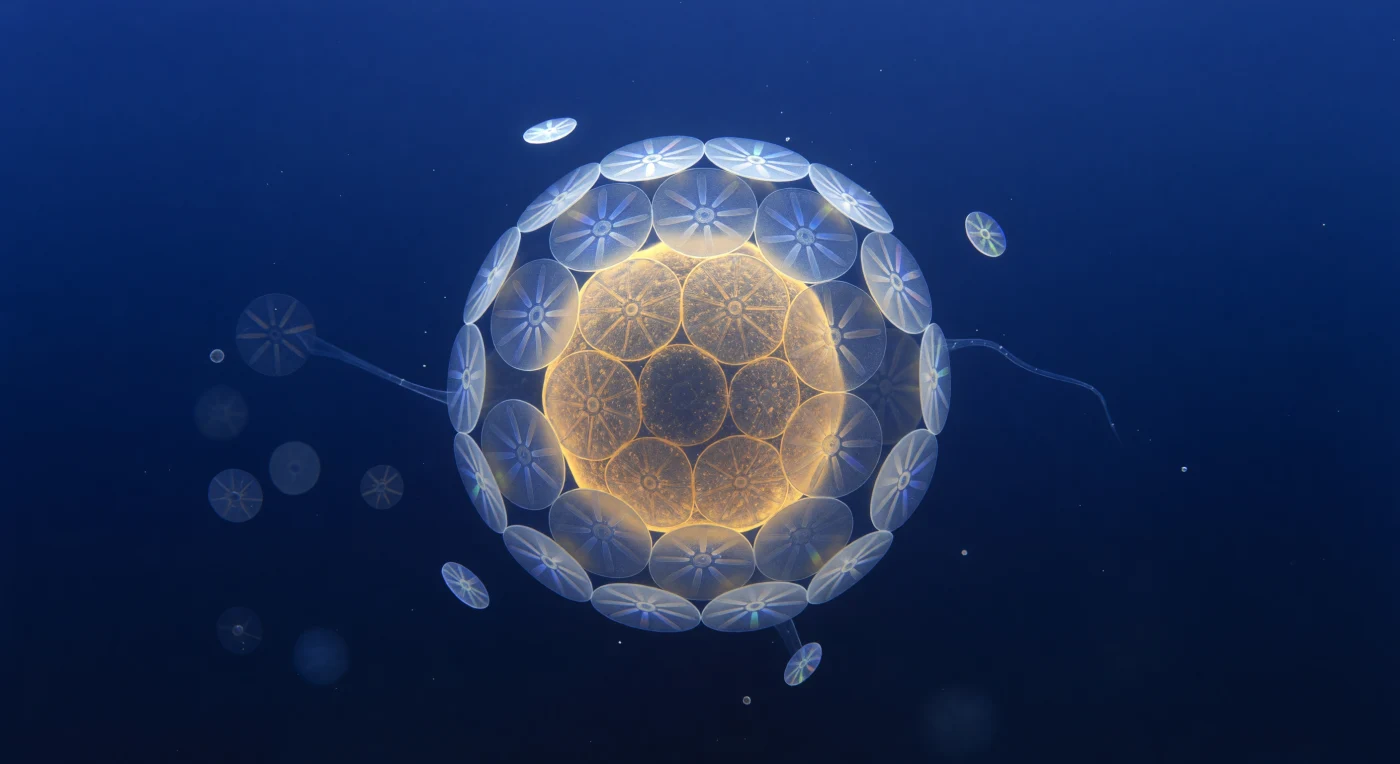
Ci si trova sospesi nell'azzurro più profondo dell'oceano, a pochi istanti di distanza da una singola cellula di *Emiliania huxleyi* che occupa l'intera visuale come una piccola luna ambrata: il suo corpo traslucido irradia una luce calda e dorata dall'interno, dove i cloroplasti stipati proiettano aloni di zafferano attraverso la membrana plasmatica, mentre tutto intorno l'armatura di venti coccoliti in calcite si intreccia con la precisione di un orologiaio, ogni raggio cristallino che cattura la luce diffusa a 480 nanometri proveniente da molto in alto e la frammenta in fugaci arcobaleni di ghiaccio blu, verde menta e violetto. Questi piatti a forma di ruota di carro — ognuno largo quanto metà del proprio corpo — sono il prodotto di una biomineralizzazione straordinariamente controllata: la cellula sintetizza i cristalli di calcite all'interno di vescicole specializzate e li estrude uno a uno sulla propria superficie, costruendo uno scudo che al contempo riflette la luce eccessiva e protegge il contenuto cellulare. Appena oltre la sfera, quattro coccoliti distaccati ruotano lentamente nel rumore termico browniano, ciascuno un dischetto luminoso che cattura e rilascia lampi prismatici mentre tumula nella colonna d'acqua; più lontano, i contorni fantasmatici di altre coccosphere emergono dall'indaco impenetrabile, e un filamento trasparente di polimero extracellulare attraversa il campo visivo come filo di vetro filato. L'intera scena respira una fragilità impossibile — un'architettura simultaneamente solida come il calcare e delicata come una bolla di sapone, destinata, dopo la morte cellulare, a depositarsi sul fondo oceanico e, nel corso di millenni, a comporre le stesse scogliere bianche che segnano le coste del mondo.
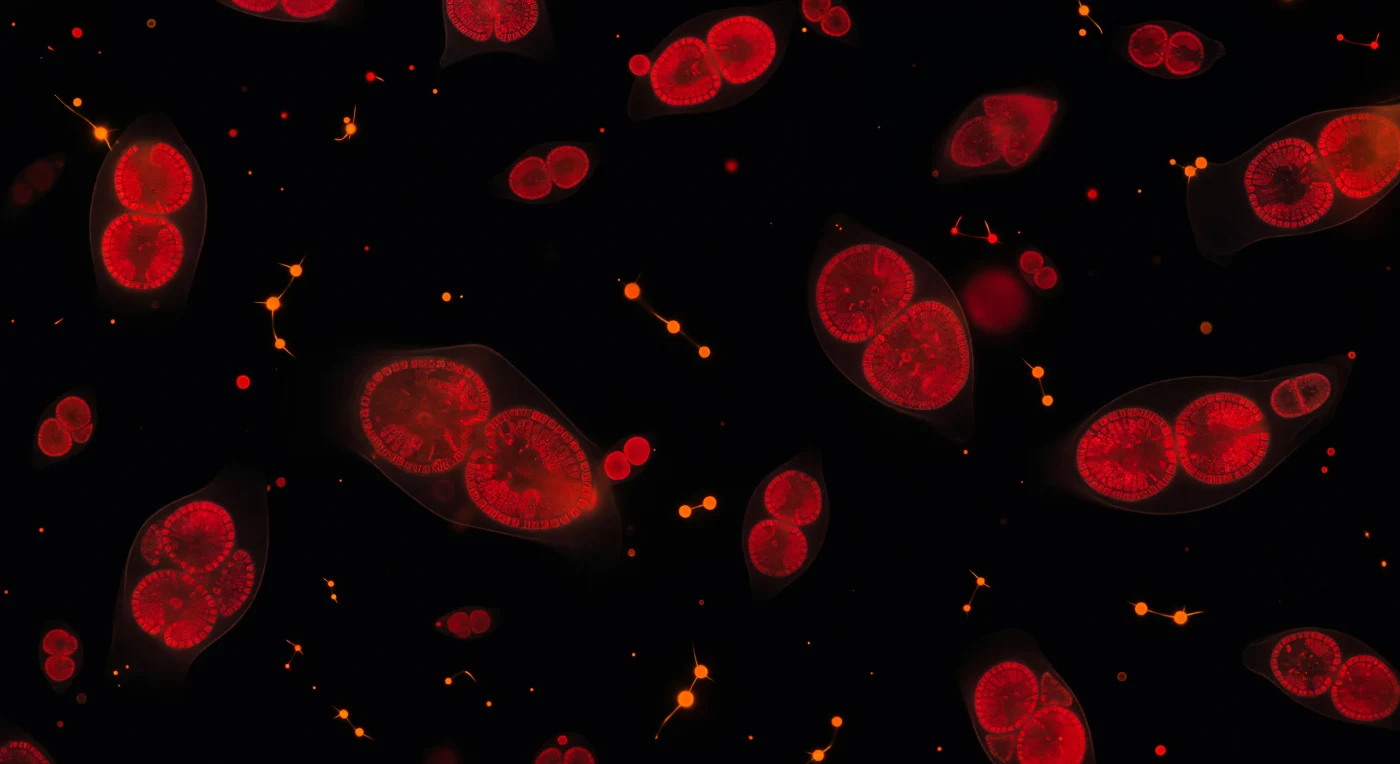
In un'oscurità assoluta misurata in milionesimi di metro, decine di cellule fitoplanctoniche ardono come braci di carminio profondo, la loro autofluorescenza clorofilliana a 680 nm l'unica fonte di luce in un vuoto tridimensionale senza orizzonte né gravità percepibile. All'interno di ciascuna cellula, i cloroplasti a doppio lobo si risolvono come forme reniformi scarlatte bilateralmente simmetriche, dense di pigmento, le membrane tilacoidee impilate in lamine che approfondiscono il rosso verso il bordeaux nei punti di maggiore spessore. Tra le masse cremisi, cianobatteri fotosintetici procarioti punteggiano il nero come scintille arancioni nitide — la ficoeritrина brucia con una cromaticità più calda e immediata rispetto alla clorofilla delle cellule eucariote, alcune in file concatenate che tracciano minuscole linee costellari nel mezzo invisibile. Tenui aloni rossastri attorno alle cellule più vicine tradiscono la presenza del fluido sospensivo — vescicole di membrana e materia organica disciolta che diffondono i fotoni cellulari in sottili corone di un micron — confermando che non siamo nel vuoto cosmico ma in una goccia d'oceano dove questi organismi fotosintetici rappresentano il fondamento della catena trofica marina e un motore primario del ciclo globale del carbonio. Il campo visivo intero, con le cellule più lontane ridotte a rubini appena percettibili, genera un'illusione stellare autentica: una nebulosa compressa in dimensioni invisibili a occhio nudo.

Ci si trova immersi fino al petto in un oceano che non è più acqua ma una sospensione minerale vivente, opaca come gesso diluito, dove ogni millilitro contiene decine di milioni di minuscole ruote di calcite prodotte da *Emiliania huxleyi* — coccolitofore il cui diametro non supera i dieci micrometri, eppure capaci, in miliardi, di trasformare centinaia di chilometri di Atlantico settentrionale in una distesa di giada bianca visibile dallo spazio. La superficie si estende in ogni direzione come una lastra di porcellana luminescente, striata da lunghi nastri color latte — i windrow di Langmuir — che segnano in superficie il lavoro silenzioso di vortici controrotanti accoppiati appena sotto la pelle del mare, i quali concentrano le particelle più leggere in filamenti ordinati ogni due o quattro metri. Guardando verso il basso, il corpo scompare dopo pochi centimetri in un bianco-verde impenetrabile e radioso, poiché la luce retrodiffusa dai cristalli di calcite perde ogni direzione e il mare diventa la sua propria sorgente luminosa. All'orizzonte, il margine del bloom taglia il mondo con precisione geometrica: a sinistra il bianco-turchese calcificato, a destra il blu cobalto dell'oceano aperto, trasparente e buio come inchiostro per contrasto, come se due pianeti diversi fossero stati premuti l'uno contro l'altro. Nell'aria aleggia un lieve odore di dimetilsolfuro — quel profumo verde e marino che le cellule rilasciano lisando, segnale chimico della senescenza del bloom e, ironicamente, del suo contributo alla chimica dell'atmosfera globale.
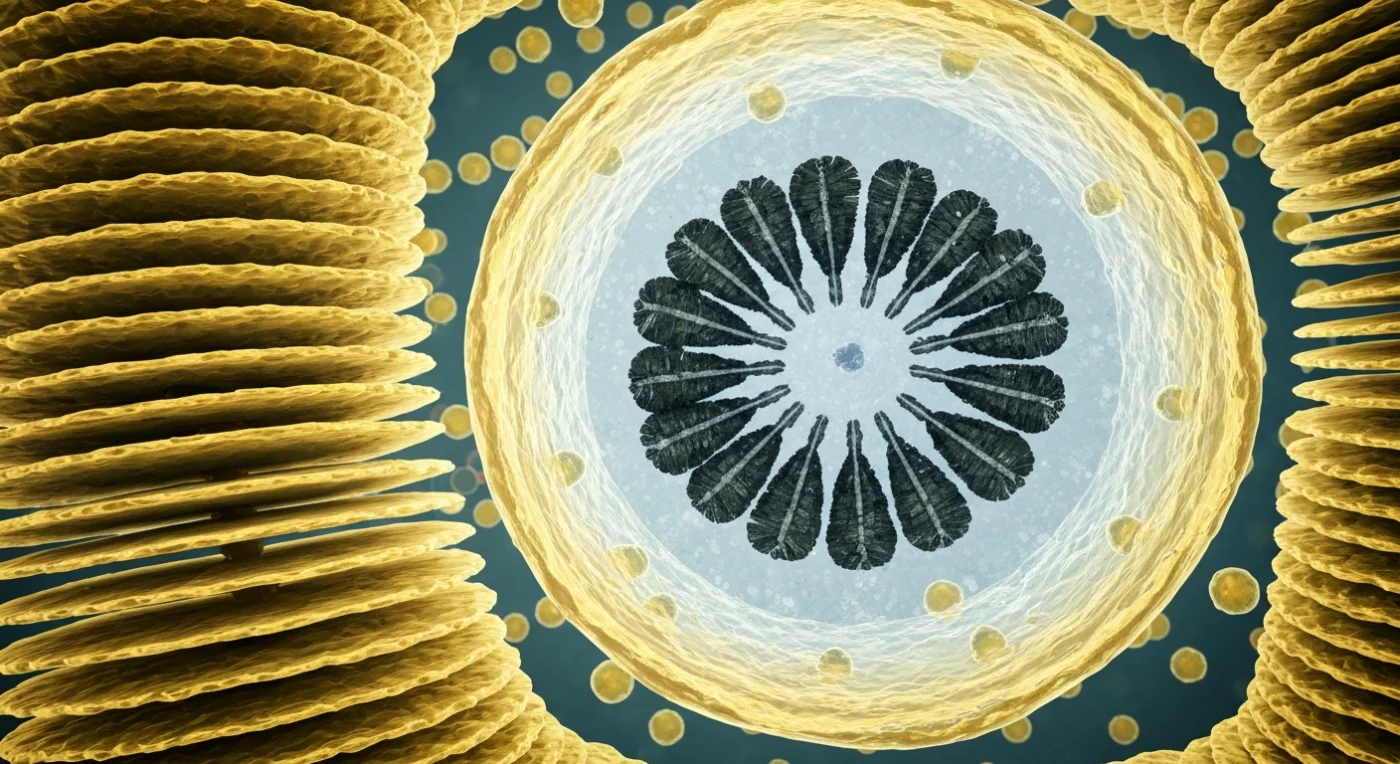
Ci si trova sospesi all'interno di una cellula vivente, immersi in un paesaggio che non lascia un solo angolo vuoto: le cisterne del Golgi si innalzano come lamine di vetro ambrato battuto a martello, ciascuna spessa appena qualche decina di nanometri, disposte in file parallele con una regolarità che evoca un'architettura intenzionale, quasi liturgica. Dalle loro facce trans si gonfiano bolle membranose che si staccano lentamente e migrano attraverso il citoplasma come lanterne alla deriva, cariche di precursori di calcite destinati alla grande camera di assemblaggio. Davanti a noi domina la vescicola coccolitica — una cupola traslucida di colore ambra caldo il cui interno irradia un freddo chiarore blu-grigio — e al suo interno, su una base polisaccaridica sottile come seta di ragno, un anello nascente di prismi di calcite si assembla in tempo reale, con i cristalli più giovani ancora spigolosi e grezzi dove la mineralizzazione continua in pulsioni invisibili di ioni calcio. I ribosomi punteggiano ogni superficie del reticolo endoplasmatico come una costellazione fitta e vellutata, e occasionalmente un mitocondrio allungato attraversa il campo visivo con un bagliore arancione-rosso, le sue creste visibili come corrugazioni interne. Questo è il luogo in cui *Emiliania huxleyi* costruisce pietra dal mare, in assoluto silenzio, con una precisione che precede qualsiasi ingegneria umana di centinaia di milioni di anni.

Sospesi nel vuoto assoluto, senza orizzonte né gravità, si apre davanti agli occhi uno spettacolo che sfida ogni senso di proporzione: una cocosfera arde come un sole conquistato, quindici ruote di calcite intrecciate in una sfera quasi perfetta, ciascuna trasformata dalla luce polarizzata in un mandala radiante dove la croce di estinzione maltese — nero vellutato e assoluto — è circondata da un bianco di prima ordine così intenso da sembrare quasi solido, con accenni di oro pallido e avorio arancione ai bordi ispessiti dei raggi, dove le differenze di percorso ottico spingono la birifrangenza appena oltre la soglia cromatica. Ogni coccolite è una struttura biologicamente precipitata, formata ione per ione all'interno di vescicole intracellulari specializzate, composta da trenta e più prismi romboedrici di calcite disposti in simmetria radiale — un'architettura cristallografica che la cellula vivente assembla nel buio freddo dell'oceano, a decine di metri sotto la superficie. Attorno alla cocosfera centrale deriva una costellazione di coccoliti liberi, ciascuno un disco ellittico di tre micrometri di diametro, piatto come lamiera battuta eppure ornato come una cattedrale cristallografica, alcuni di taglio — sottili falci luminose in atto di ruotare — altri frontali, con la piena simmetria geometrica del loro pattern a raggiera visibile nel chiarore birifrangente. La profondità del campo nero si misura unicamente nella progressiva perdita di nitidezza dei coccoliti più lontani, ridotti a morbide scie luminose, così che l'intera scena si rivela come uno spazio volumetrico di considerevole estensione, eppure privo di qualsiasi riferimento fisico oltre a queste ruote ardenti — frammenti di un organismo che ha plasmato la chimica del carbonio oceanico per decine di milioni di anni, e la cui morte in massa precipita lentamente verso i fondali trasformandosi, in millenni, nei banchi di gesso bianco che affiorano nelle scogliere di Dover.
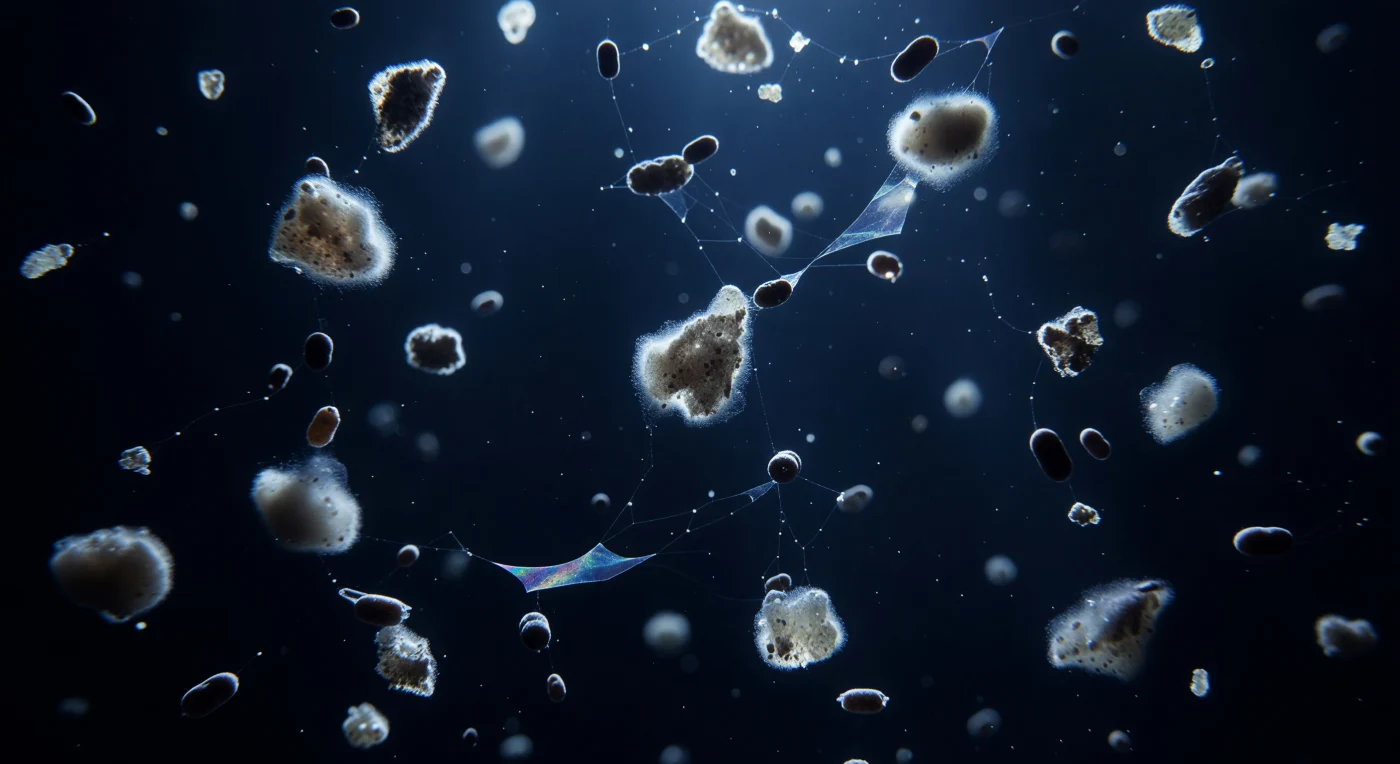
Sospeso a duecento metri di profondità, il visitatore si trova immerso in una colonna d'acqua indaco quasi priva di luce, attraversata da un lento e incessante corteo di fiocchi biancogrigi che scendono dall'alto come frammenti di nuvola strappata. Ogni aggregato di neve marina — da uno a quattro millimetri di diametro — è una cattedrale compressa di coccolithi calcitici, frustuli di diatomee morte, mucillagini e detriti cellulari, costruita nel corso di giorni di lenta aggregazione nella zona eufotica soprastante; i rari fotoni residui che filtrano dall'alto ne incendiano i bordi in un alone azzurro-bianco tra i 450 e i 490 nanometri, trasformando ogni fiocco in una piccola lanterna fantasma che porta con sé la propria luce nell'abisso. Tra i fiocchi, cilindrici pellet fecali color bruno scuro cadono tre-dieci volte più veloci, compatti come proiettili, mentre tra aggregato e aggregato le particelle di esopolimero trasparente — TEP — si tendono in veli quasi invisibili, rivelando la propria presenza solo come un'iridescenza al limite della percezione, ragnatele di materia biologica sospese nel buio. L'intera scena obbedisce a una grammatica verticale assoluta: tutto scende, sempre verso il basso, in una processione glaciale che trasforma la colonna d'acqua in un archivio vivente del carbonio oceanico, un blizzard biologico che cade senza testimoni da centinaia di milioni di anni.
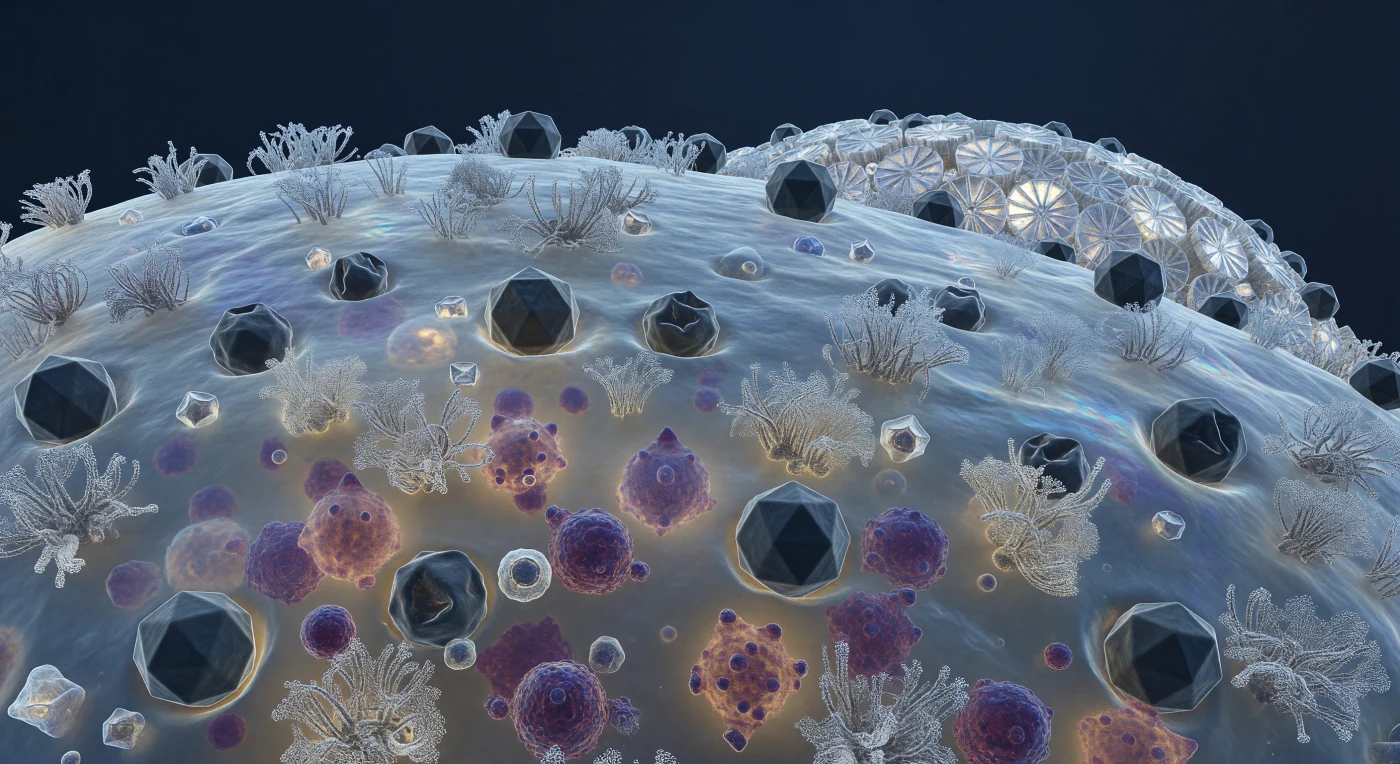
La superficie di questa cocolitofora si estende davanti a noi come un vasto altopiano biologico, la membrana traslucida e fremante per l'agitazione browniana che non cessa mai, cosparsa di foreste di glicoproteine recettoriali che si innalzano come formazioni coralline avvolte da zuccheri molecolari. Contro questo paesaggio vivo si appoggiano decine di capsidi virali icosaedrici — i cocolitovirus EhV, particelle di circa 200 nanometri — in ogni stadio dell'assalto: alcuni geometricamente perfetti con le loro venti facce triangolari che catturano la luce fredda degli abissi, altri già collassati su sé stessi come cupole geodetiche forate dopo aver iniettato il proprio genoma nella cellula ospite. Attraverso la parete membranosa, translucida come vetro ambrato appannato, il citoplasma interno ribolle di masse dense e purpuree — nuovi virioni in assemblaggio, prodotti in serie su impalcature di nucleoproteine in una replicazione di scala industriale che preme contro la membrana dall'interno, gonfiandola in sottili rigonfiamenti dove l'attività è più intensa. Lontano, lungo la curvatura della cellula, i margini bianchi delle placche di calcite coccoliti si levano come contrafforti ceramici, disperdendo la poca luce disponibile in lampi prismatici mentre la cellula, nella sua bellezza geometrica assoluta, viene riscritta molecola per molecola dal programma virale che l'ha già condannata.

Sospeso nell'indaco assoluto a cento metri di profondità, ci si trova alla scala di una singola cellula di dinoflagellato — forse trenta micrometri — immersi nel massimo di clorofilla profondo, quella fascia precisa dove la luce solare, ridotta al due percento della sua intensità superficiale, sopravvive come un crepuscolo di puro blu a 475 nanometri, una luminanza così spectralmente stretta da sembrare quasi un colore piuttosto che una sorgente luminosa. Attorno a noi deriva una costellazione di cellule fitoplanctoniche — dinoflagellati che ardono di un caldo oro-olivastro contro il vetro freddo dell'oceano, catene di diatomee con pareti di silice trasparenti che captano i fotoni disponibili e li restituiscono come braci compresse, e la coccofera di un'*Emiliania huxleyi* ormai quiescente che scivola oltre di noi con le sue placche di calcite perfettamente incastrate, disperdendo la luce in scintille geometriche, l'unica luce dagli spigoli netti in questo mondo di bagliori biologici soffusi. Un fiocco di neve marina delle dimensioni di un edificio scende lentamente attraverso lo strato — un groviglio traslucido di filamenti di esoopolimeri, gusci di cocoliti ancora interlacciati nelle loro forme a ruota, pellet fecali densi e materia organica intrappolata nel muco — retroilluminato dal blu sovrastante così che le sue membrane più sottili sembrano quasi luminose. Più in basso, il blu si spegne per gradi percettibili in un indaco vero, poi in qualcosa di prossimo al nero assoluto, testurizzato solo dalle scintille bianche e remote di altre particelle di neve marina che catturano gli ultimi fotoni disponibili prima di spiralare nell'abisso.

Sospesi nell'ultimo millimetro oscuro dell'oceano aperto prima dell'alba, ci troviamo faccia a faccia con un *Ceratium tripos* che si estende davanti a noi come una cattedrale ambrata sospesa nel vuoto indaco: il suo corpo translucido è rivestito da placche dell'anfiesma disposte a nido d'ape, ciascuna cuciture che cattura i primi fotoni del crepuscolo come un filo di fuoco blu-bianco, mentre i tre corni cavi — uno apicale, due antapicali — si assottigliano in lance di vetro pallido rinforzate internamente da trabecolature delicate come merletto. Il flagello trasversale batte senza sosta nel solco del cingulum, producendo un fremito argenteo quasi invisibile che spinge la cellula attraverso un'acqua così viscosa a questa risoluzione da sembrare vetro liquido, mentre il flagello longitudinale si perde nell'oscurità sottostante come un filo di cristallo. Attorno alla cellula, decine di cocoliti staccati — piccole ruote di calcite di due o quattro micrometri — derivano nella diffusione browniana scintillando in fredde scintille predawn, tracce di un bloom invisibile che arma chimicamente quest'oceano di superficie contro l'acidificazione. Nel mezzo campo, a pochi centimetri reali ma percepito come una torre di vetro, un copepode di un millimetro incombe immobile con la gravità silenziosa di una massa geologica, le sue antenne trasparenti aperte come enormi remi congelati, promemoria brutale che questa bellezza microscopica esiste dentro una catena trofica che non conosce tregua.

Ci si trova immersi in una nebbia vivente di colore giada, una sospensione così densa di cellule di *Ostreococcus tauri* — ciascuna appena 0,8 micrometri di diametro, al limite tra particella e lunghezza d'onda luminosa — che il mezzo acquoso stesso è diventato una sostanza biologica, tinto di verde-smeraldo dalla clorofilla collettiva di miliardi di organismi invisibili a occhio nudo. Ogni cellula, quando deriva abbastanza vicino da essere distinta dal fondo, appare come una sfera traslucida quasi interamente occupata da un unico cloroplasto scuro, simile a un tuorlo di vetro verde che pulsa di autofluorescenza rossa quando la luce lo colpisce ad angolo giusto, per tornare poi a un fresco smeraldo mentre la cellula ruota nella corrente termica. La profondità non esiste come distanza percepita ma come saturazione cromatica: le cellule vicine sono lanterne nitide, quelle a soli due o tre micrometri di distanza sono già fantasmi dissolti nel bagliore collettivo, i loro contorni fusi nell'azzurro-verde ambientale che si estende in ogni direzione senza orizzonte né fondo. Il moto browniano è assoluto e onnipresente, un respiro probabilistico che agita l'intera nebbia, e la membrana di ciascuna cellula — un doppio strato lipidico di sette nanometri — cattura la luce diffusa come una bolla di sapone in miniatura, producendo un alone iridescente che trema e svanisce prima ancora di poter essere pienamente osservato. In questo ecosistema della scala submicrometrica, l'organismo non abita il mezzo: *è* il mezzo.
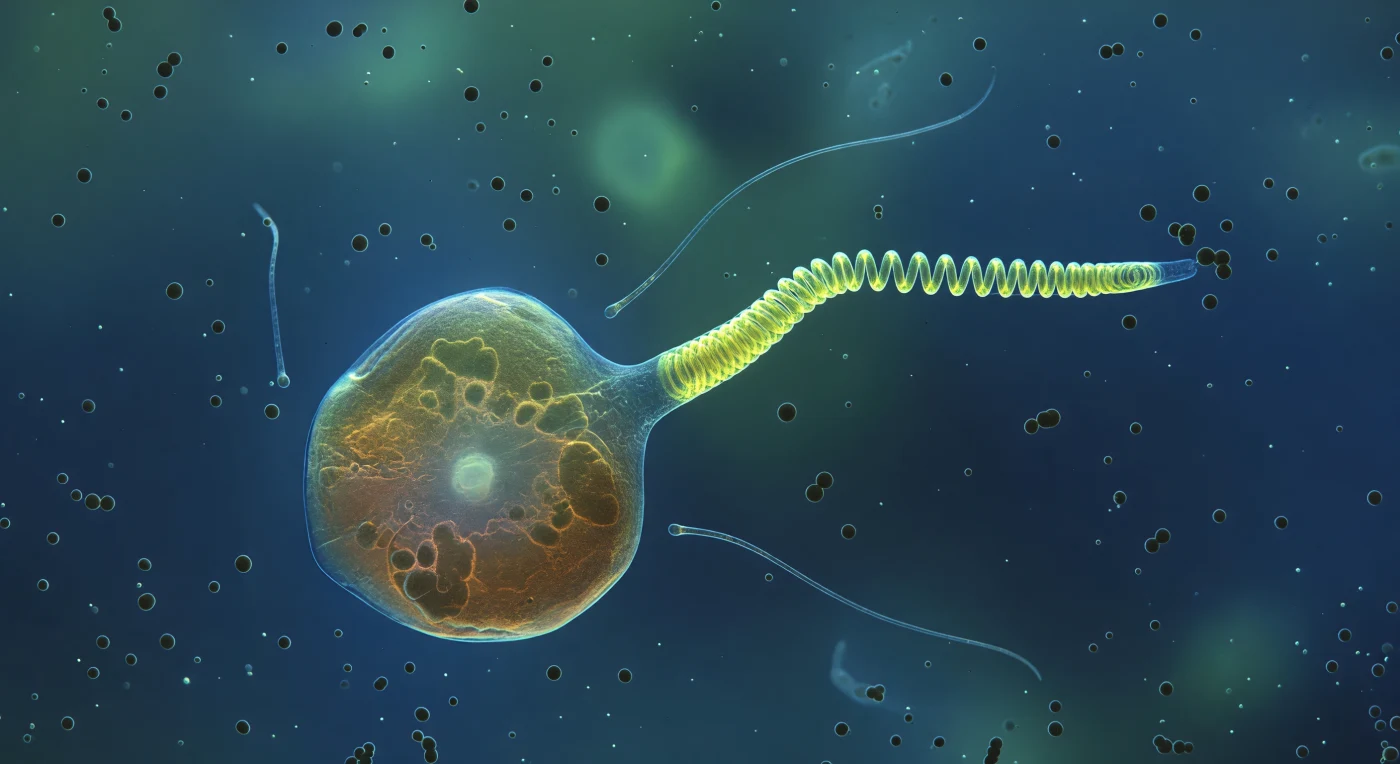
Sospesi nell'azzurro-verde gelido dell'oceano aperto, si assiste a uno degli eventi più rapidi del microcosmo planctonico: l'haptonema di una cellula di *Chrysochromulina* in piena retrazione, catturato nell'istante preciso in cui la struttura filamentosa passa da bastoncello rigido a spirale elicoidale, incandescente di giallo-verde fluorescente contro il fondo blu cobalto. La cellula stessa — un globo ambrato e semi-traslucido delle dimensioni di una piccola casa a questa scala — pulsa di vita interiore, con i cloroplasti che premono contro la membrana plasmatica e il nucleo pallido che brilla al centro come una lampada sepolta nell'ambra. L'haptonema non è un semplice prolungamento cellulare: è un organello unico degli aptofiti, distinto dai flagelli, capace di contrarsi in pochi millisecondi grazie a un sistema interno di microtubuli disposti in configurazione 6+0, accumulando energia elastica come una molla biologica per catturare batteri o rispondere a stimoli meccanici. Attorno alla punta che schiocca, sfere opache di un µm di diametro — cellule batteriche — derivano lente nel gradiente chimico emanato dalla cellula più grande, ignare o inerti di fronte alla violenza microscopica che le circonda. I due flagelli, quasi invisibili, si perdono come fili d'argento nel mezzo liquido mentre la luce diffusa illumina particelle submicroniche in sospensione, conferendo all'acqua quella luminosità lattiginosa che rivela la densità nascosta di un oceano vivo fino all'ultima molecola.

Dal parapetto di prua, l'oceano si divide sotto lo sguardo in due mondi separati da una linea quasi chirurgica: a sinistra, il blu-indaco profondo e trasparente dell'oceano aperto in cui la luce sprofonda verso il nulla; a destra, una massa d'acqua opaca e lattea, color turchese-calcare, che irradia una luminosità diffusa e perlacea come se la luce emergesse dall'interno della colonna d'acqua stessa. Quella luce interiore è prodotta da miliardi di coccolitofore — cellule di cinque-dieci micrometri, ciascuna corazzata di placchette di calcite cristallina — che disperdono i fotoni in tutte le direzioni come minuscoli prismi geometrici invisibili all'occhio umano ma collettivamente capaci di trasformare interi tratti di oceano in pietra liquida. Le windrow di schiuma organizzate dalla circolazione di Langmuir corrono parallele lungo il confine esatto dove le due masse d'acqua si tagliano in lenti vortici orizzontali, e un sula si tuffa con precisione proprio su quella soglia produttiva, sollevando uno schizzo bianco-latte che per un istante cattura il sole basso prima di collassare nella superficie pallida. Nell'aria fluttua una dolcezza sulfurea sottile — il dimetilsolfuro liberato dalle cellule in stress — e all'orizzonte il margine del bloom svanisce in una foschia luminosa dove decine di miliardi di placche di calcite sfumano il confine tra oceano e cielo.

Ci si trova immersi in una cattedrale compressa di calcite, dove ogni ruota di coccolite — larga appena tre micron — intreccia i suoi raggi cristallini con i vicini in un mosaico così denso da non lasciare vuoto alcuno, la luce ambrata radente che plasma ogni bordo sollevato in rilievo netto come bassorilievo su avorio. Questi dischi geometrici sono i gusci calcificati di *Emiliania*, *Gephyrocapsa*, *Calcidiscus* — organismi che un tempo fluttuavano nella zona fotica oceanica, ciascuno costruendo la propria armatura di placche trigonali con una precisione nanoscopica che la diagenesi impiegherà milioni di anni a cancellare. Guardando lungo la stratificazione laminare, le bande alternate di ooze a coccoliti compatti e di zone più scure ricche di minerali argillosi narrano i cicli glaciali come pagine di un archivio sedimentario: ogni strato sottile pochi decine di micron rappresenta secoli di pioggia lenta dal mare soprastante. Nelle sezioni più profonde della matrice, i bordi delle ruote cominciano a sfumarsi nella dissoluzione diagenetica, i cristalli che cedono la loro identità geometrica alla pressione di diecimila metri di colonna sovrastante compressa in dieci milioni di anni. Qui non vi è movimento, non vi è gradiente chimico né pulsazione vitale — soltanto la geometria ossessiva e magnificente dei morti, la simmetria di specie impressa nel cristallo e trasmessa attraverso il tempo profondo.
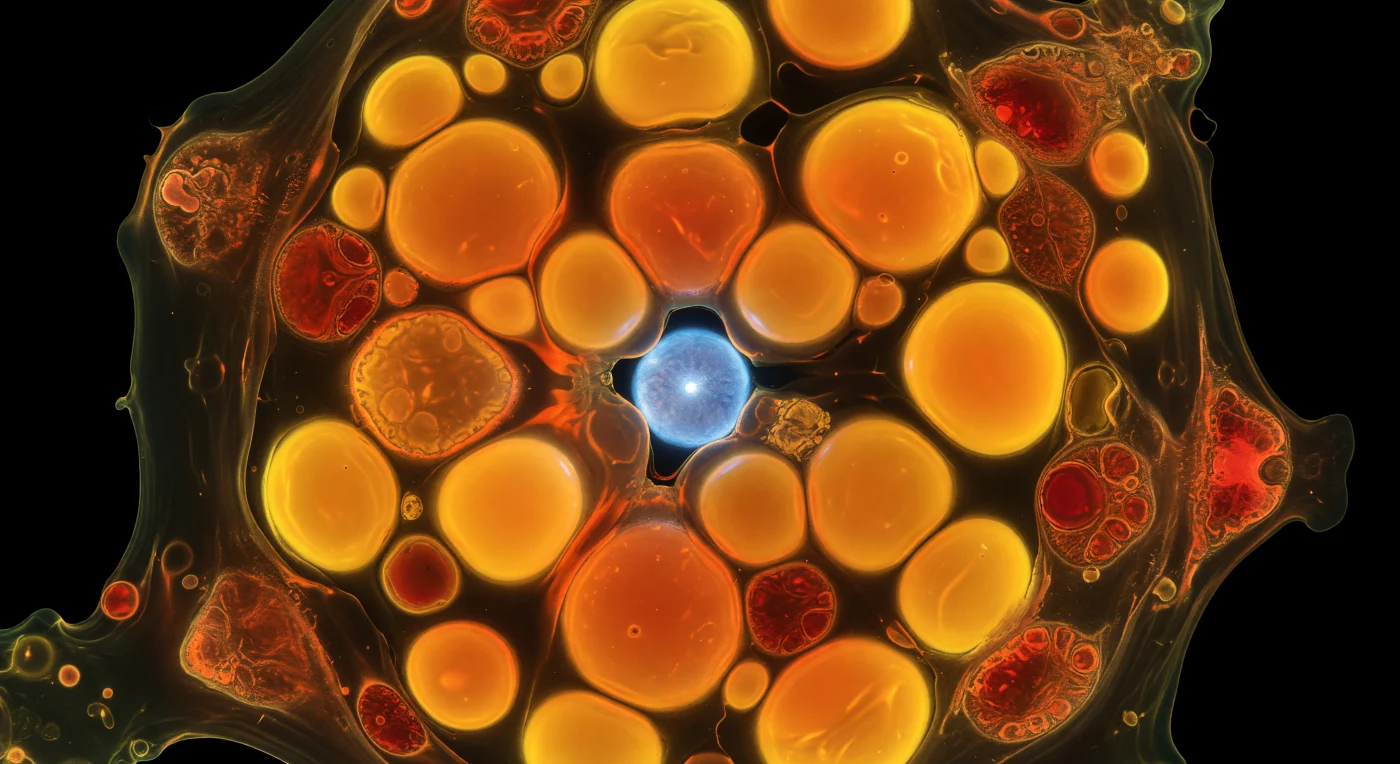
Ci si trova all'interno di una singola cellula di *Emiliania huxleyi* privata dell'azoto, immersi in un citoplasma denso e gelatinoso dove enormi gocciole lipidiche si affollano come pianeti d'ambra, ognuna che brucia dall'interno con una fluorescenza arancio-oro accecante grazie al Nile Red intercalato nelle molecole di lipidi neutri. Queste sfere perfettamente tese si deformano leggermente nei punti di contatto, proiettando aloni sovrapposti di zafferano e ambra profonda attraverso i viscosi canali di citoplasma che le separano, in un interno claustrofobico dove ogni fotone nasce, rimbalza e viene riemesso senza mai trovare uscita. Ai margini di questo paesaggio infuocato, i cloroplasti — spinti verso la periferia dalla massa lipidica in avanzamento — emettono una debole autofluorescenza cremisi, come braci che si spengono al bordo di un incendio, le loro membrane corrugate rivelando ancora, a fatica, le laminazioni dei tilacoidi dove la macchina fotosintetica gira al minimo, denutrita e reindirizzata verso l'accumulo di riserve. Più in profondità, attraverso un corridoio appena aperto tra le gocciole incandescenti, il nucleo si intravede a malapena — una sfera di blu elettrico lunare, colorata dal DAPI legato al DNA compattato — mentre all'esterno della membrana plasmatica regna il buio assoluto, un vuoto infinito che rende l'interno della cellula un mondo interamente autoilluminato, chiuso su se stesso come una lanterna sigillata nel cosmo.

Lo spettatore è immerso fino al petto in un oceano completamente nero, dove cielo e acqua si fondono in un'unica oscurità senza confini, e ogni movimento delle mani genera scie di fuoco freddo blu elettrico a 460 nanometri, prodotto dalla scarica simultanea di milioni di cellule di *Lingulodinium polyedra* — dinoflagellati unicellulari di sei-dodici micrometri, ciascuno dotato di scintilloni, tasche membranose contenenti luciferasi e luciferina che si innescano a cascata al minimo stimolo meccanico. Le tracce lasciate dalle dita persistono per due secondi interi, allargandosi da linee nitide in aloni cerulei che cartografano ogni vortice e corrente invisibile, mentre le creste delle onde portano un bagliore continuo poiché il moto orbitale delle particelle d'acqua agita senza sosta le cellule superficiali, rendendo leggibile la geometria nascosta del mare aperto. A cinquanta metri di distanza, la scia di una barca forma un fiume ininterrotto di luce bianco-azzurra che si estende fino ai limiti assoluti della visione, il suo centro così densamente luminoso da sembrare quasi solido. Il corpo del visitatore diventa esso stesso uno strumento di misurazione biologica: ogni respiro, ogni battito cardiaco genera nuove cascate luminescenti nelle cellule sensibilissime circostanti, trasformando i movimenti più impercettibili in una mappa vivente scritta in luce fredda contro il buio assoluto.
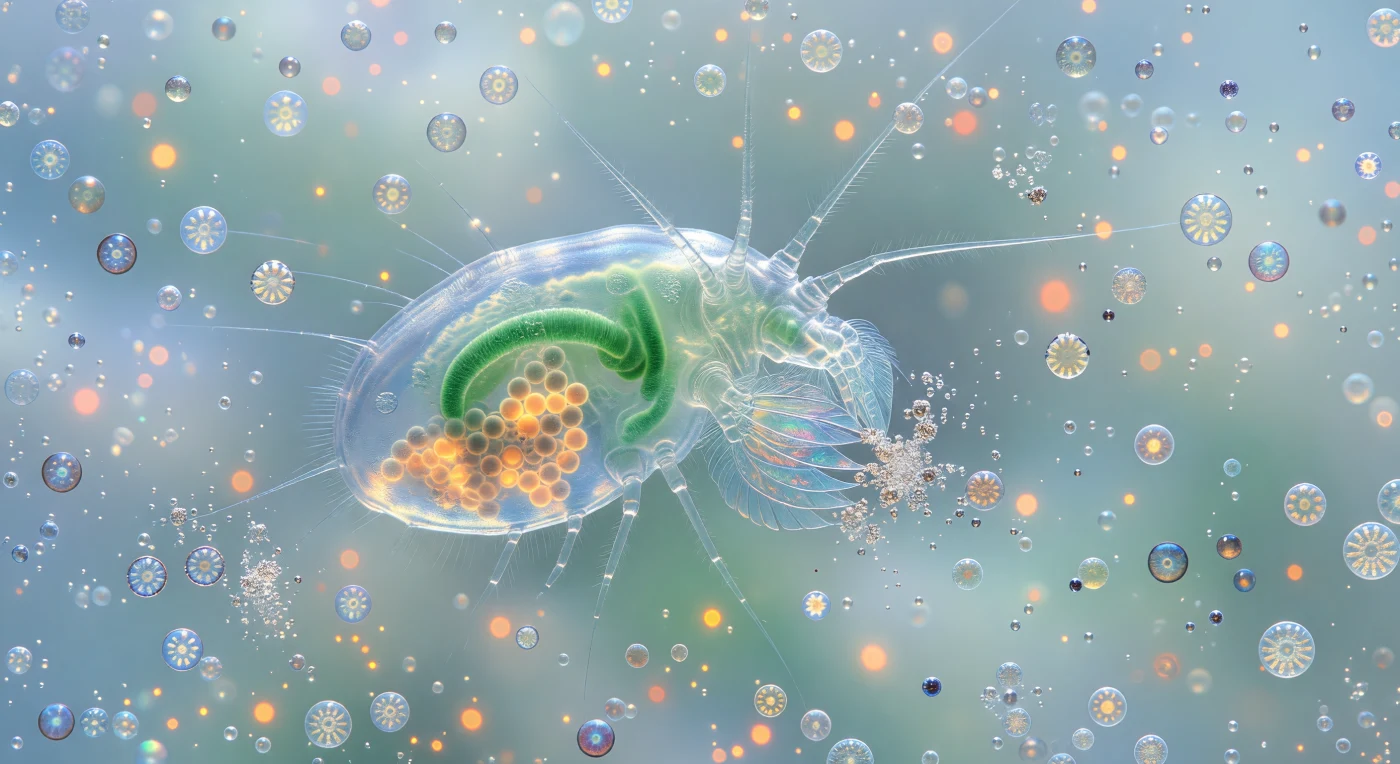
Ci si trova a due millimetri da una delle architetture più straordinarie dell'oceano: un copepode del genere *Calanus*, il cui corpo trasparente come vetro soffiato rivela, attraverso tre strati di cuticola chitinosa, il tubo intestinale color giada e gli ammassi di uova arancio-ambra che bruciano come braci dietro un vetro smerigliato. I massillipedi — appendici alimentari disposte come piume di vetro soffiato — tremano al margine del campo visivo, ogni seta sottile come un capello capace di intercettare singole cellule di *Emiliania huxleyi* mentre la corrente di alimentazione generata dal copepode le trascina in archi lenti ma inesorabili verso la bocca. L'acqua circostante non è vuota: è una sospensione di latte turchese, con decine di milioni di coccolithi staccati per millilitro che diffondono la luce disponibile in una nebbia luminosa nella quale le coccosfere intatte derivano come pianeti in miniatura, le loro placche di calcite che lampeggiano dall'argento all'oro pallido a seconda dell'angolo di incidenza. Ai margini dei massillipedi, ogni coccolite frantumato esplode in una raffica di dischetti bianchi da due micrometri, piccole detonazioni di luce che il vortice alimentare spazza via immediatamente; le cellule di *Emiliania* ancora intatte portano al loro interno una debole autofluorescenza rosso-arancio dei cloroplasti, costellazioni di calore metabolico che si muovono attraverso il freddo medium turchese come lanterne in una notte nebbiosa. La profondità alle spalle del copepode si dissolve in un'atmosfera infinita di biancoazzurro luminoso, il bloom così denso di calcite diffusa da funzionare come una nebbia in tutte le direzioni, rendendo il copepode stesso — con la sua geometria di alimentazione, le sue antenne come rami pallidi che si protendono nella foschia, il suo ventre di vetro illuminato dall'interno — un'enorme presenza architettonica che organizza attorno a sé tutta la luce disponibile in vettori di avvicinamento e distruzione scintillante.

Sospesi nella colonna d'acqua come osservatori neutri, ci troviamo a pochi micron di distanza da due cellule che rappresentano la stessa specie in stadi di vita radicalmente opposti: a sinistra, la cellula diploide si presenta come una piccola architettura minerale, la sua coccosfera di placche calcitee sovrapposte con geometria trigonale che intercetta e rifrange la luce diffusa dell'oceano in bagliori freddi di bianco e oro pallido, ogni coccolite un disco di lame cristalline assemblate con una precisione che sfida la scala biologica. A pochi corpi cellulari di distanza, la cellula aploide è nuda e quasi vulnerabile a confronto: la sua membrana traslucida di crema verdastra lascia intravedere il calore ambrato dei cloroplasti sottostanti, i cui pigmenti trasformano anche questi fotoni filtrati e diffusi in una debole autofluorescenza giada, mentre i due flagelli — fili biologici di appena qualche decina di nanometri di spessore — sono catturati nell'istante preciso del loro arco sinusoidale, come filamenti di vetro bagnato che catturano la luce ambientale. Intorno a entrambe le cellule, invisibili ma fisicamente reali, esistono aloni di gradiente chimico dove la CO₂ disciolto è localmente impoverita dalla fotosintesi attiva — il mezzo acquoso stesso è leggermente diverso al contatto con le membrane. Sullo sfondo ceruleo dell'abisso superficiale, coccolithe libere derivano come scintille bianche a distanze variabili, i più vicini ancora leggibili nella loro geometria, i più lontani ridotti a punti luminosi, creando una prospettiva di profondità che suggerisce una vastità paradossale in uno spazio misurabile in frazioni di millimetro.

Davanti a te si erge la faccia quasi verticale delle Bianche Scogliere di Dover, una parete abbagliante di gesso cretaceo che sale a un'altezza vertiginosa sotto il sole pomeridiano radente, la sua superficie così intensamente luminosa contro il cielo blu-grigio atlantico da sembrare emanare luce propria. Questa cattedrale di carbonato biogenico è composta da miliardi di cocoliti compressi — le minuscole placche di calcite che un tempo rivestivano le cellule di coccolitoforidi grandi appena cinque o dieci micrometri, microrganismi che vissero, calcificarono e affondarono in un mare cretaceo scomparso da sessantacinque milioni di anni, sedimentandosi lentamente sul fondale fino a formare strati di fango calcareo poi litificati in questa massa imponente di carbonato biogenico. Le fasce di selce grigio-bruna che tagliano la parete bianca in linee stratigrafiche quasi perfette sono fantasmi chimici di antichi processi diagenetici, ciascuna un momento compresso nel tempo profondo, in violento contrasto tonale con il gesso circostante come segni di inchiostro tracciati da una mano geologica su una pagina bianca. A metà parete, appena un centimetro di dimensione apparente a questa distanza, una singola folaga siede immobile su un cornicione stretto — testimone vivo e minuscolo che rende improvvisamente vertiginosa e reale l'altezza della scogliera, mentre dal basso salgono l'odore di sale freddo e gesso umido, il respiro minerale lento di un archivio di oceani invisibili fatto pietra.