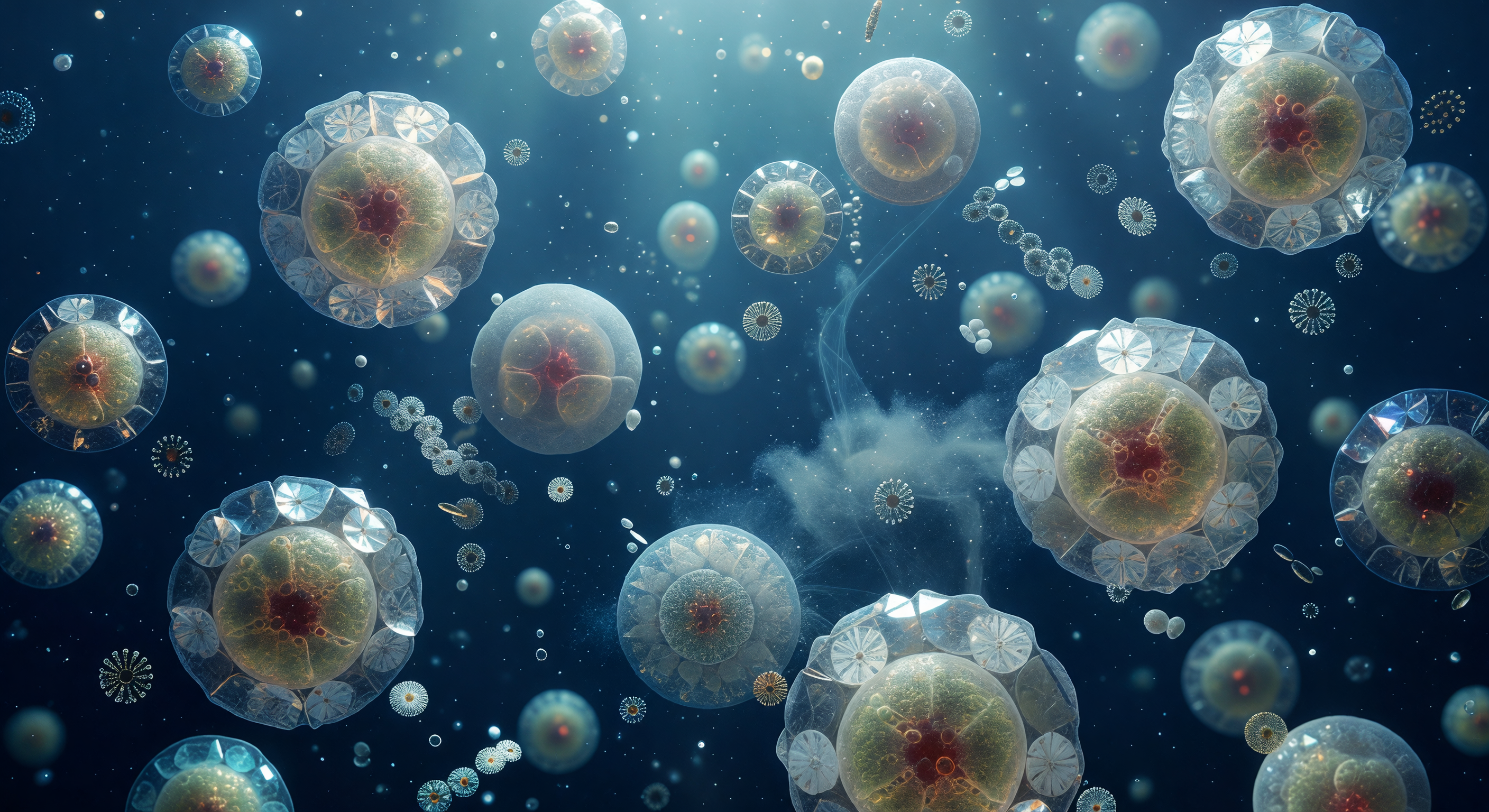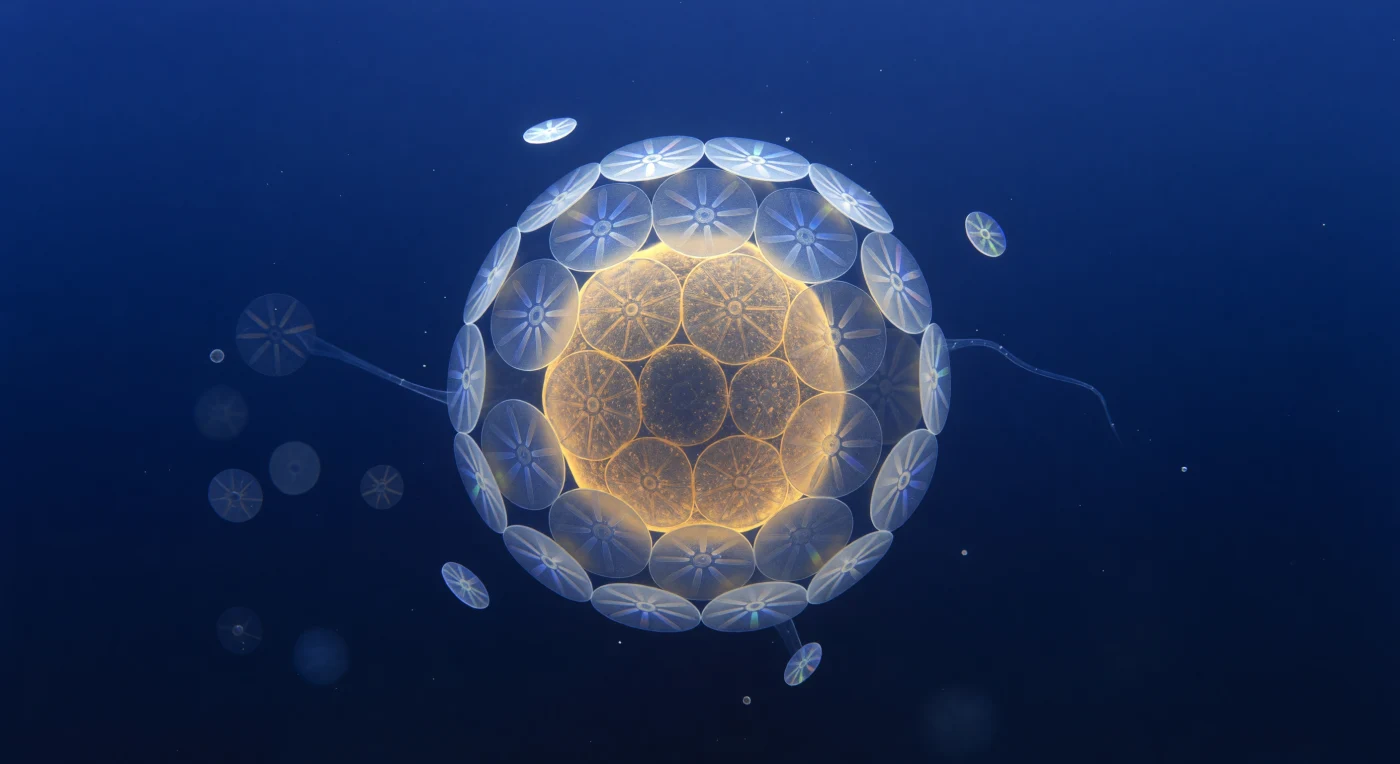
À cette distance infime, le regard est entièrement capturé par une sphère d'ambre translucide d'environ huit micromètres de diamètre — *Emiliania huxleyi* — dont les chloroplastes internes rayonnent une lumière dorée et mielleuse qui se diffuse en halos de safran à travers la membrane plasmique. L'armure qui l'entoure est une œuvre d'orfèvrerie minérale : vingt coccolithes de calcite cristalline s'emboîtent avec la précision d'une mécanique d'horlogerie, leurs rayons convergents fractionnant la lumière descendante à 480 nanomètres en éclats prismatiques fugaces — bleu glacé virant au violet, une lueur de vert menthe retenue un instant sur l'arête d'un cristal, puis disparue. Ces plaques calcaires, dont chacune représente environ la moitié de la largeur du corps du spectateur, sont le produit d'une biominéralisation intracellulaire extraordinaire : la cellule sécrète ses boucliers dans des vésicules de Golgi spécialisées avant de les extruder à sa surface, construisant ainsi l'une des architectures les plus géométriquement précises du vivant. Au-delà, dans l'ultramar profond du milieu environnant — un bleu comprimé sans équivalent terrestre, chargé de sa propre luminescence sourde — quelques coccolithes détachés dérivent librement, tournant imperceptiblement sous l'agitation thermique brownienne comme de minuscules disques prismatiques perdus dans un indigo qui se referme sur lui-même à cinquante longueurs de cellule.
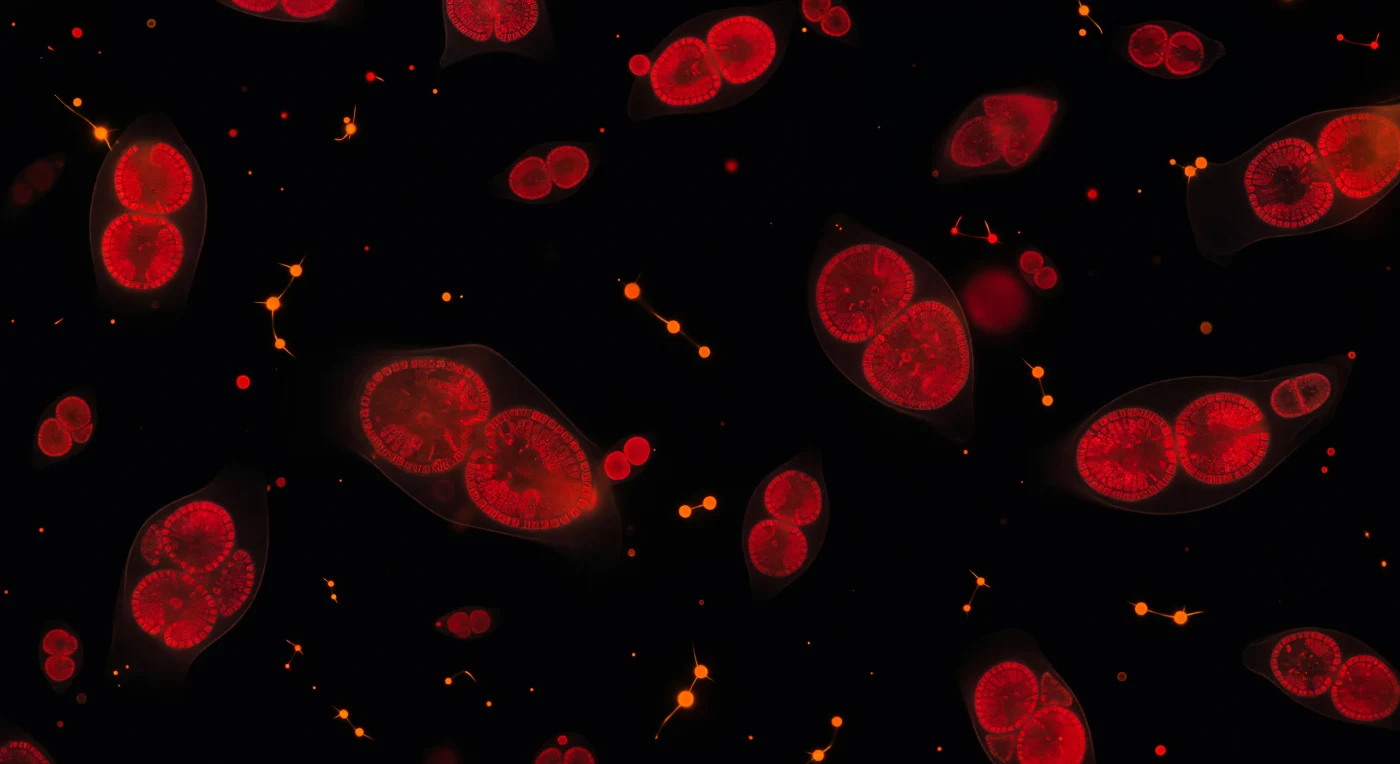
Dans l'obscurité absolue d'une goutte d'eau océanique, des dizaines de cellules phytoplanctoniques brûlent comme des braises cramoisies, leur autofluorescence chlorophyllienne émettant à 680 nm une lumière rouge saturée qui constitue l'unique source de couleur dans ce vide tridimensionnel — chaque photon perçu naît de l'intérieur même des cellules, sans aucun éclairage extérieur. À cette échelle de quelques microns, les chloroplastes bilobés se révèlent comme des continents écarlates aux contours réniformes, denses de membranes thylakoïdiennes empilées en feuillets lamellaires dont les plis les plus épais virent au bordeaux profond. Parmi les masses cramoisies des cellules eucaryotes, des cyanobactéries prokaryotes surgissent comme des étincelles orange vif — leur phycoérythrine brûlant d'une teinte tangerine nettement plus chaude que le rouge chlorophyllien — certaines isolées, d'autres disposées en paires ou en chaînettes formant de minuscules lignes de constellation dans le milieu noir. Le fluide invisible se trahit par de faibles auréoles rougeâtres autour des cellules les plus proches, là où des vésicules membranaires diffusent la lumière cellulaire en minces couronnes d'un micron d'épaisseur, confirmant que nous flottons dans un liquide et non dans le vide. Cette composition évoque un champ d'étoiles cosmiques compressé dans une infime fraction de goutte, où ces organismes photosynthétiques — piliers invisibles de la productivité océanique et pompes biologiques du carbone — sont les seuls repères de couleur, de chaleur et d'orientation dans un univers mesuré en millionièmes de mètre.

Vous vous tenez dans une eau qui n'est plus tout à fait de l'eau : la mer North-Atlantique autour de vous est devenue une suspension minérale vivante, opaque comme du lait de craie, dans laquelle dix millions de roues de calcite par millilitre diffusent la lumière du zénith jusqu'à ce qu'elle semble jaillir de la surface elle-même plutôt que du ciel. L'*Emiliania huxleyi* est à son apogée de floraison, et la transparence habituelle de l'océan a disparu à cinq centimètres sous vos yeux — en dessous, une blancheur vert lumineuse et impénétrable absorbe tout regard, produit de photons qui ont perdu tout souvenir de leur direction d'entrée. Des rubans crème parallèles rayent la surface tous les deux à quatre mètres : ce sont les windrows de Langmuir, signatures visibles de cellules contra-rotatives qui concentrent les coccolithes les plus légers en lignes de lait condensé, tandis qu'entre ces stries les petites facettes de houle captent le soleil de midi comme des éclats de porcelaine translucide. À l'horizon, la limite de la floraison tranche l'espace avec une netteté presque indécente — turquoise-craie à gauche, cobalt profond à droite — rappelant que cette météorologie biogénique de calcite, étalée à plat sur l'océan sur des centaines de kilomètres, est en train de réfléchir vers l'espace une fraction mesurable du rayonnement solaire, modifiant imperceptiblement le bilan énergétique de la planète.
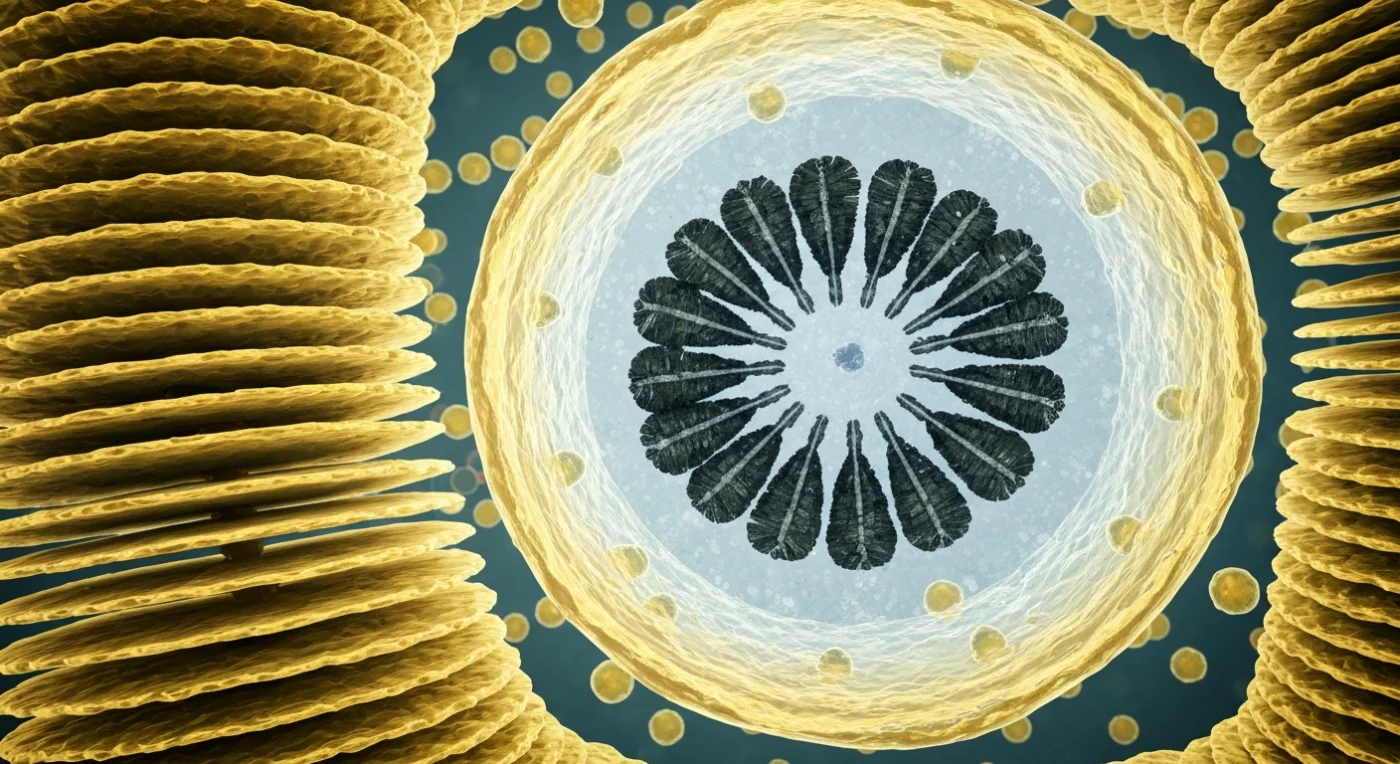
À l'intérieur même d'une cellule d'*Emiliania huxleyi*, le regard est immédiatement saisi par une architecture de membranes empilées en feuilles d'ambre translucide — les citernes du Golgi, chacune épaisse d'une trentaine de nanomètres à peine, s'élèvent en tiers parallèles dont les bords gonflent vers leur face trans en vésicules bourgeonantes qui se détachent lentement et dérivent dans le cytoplasme comme des lanternes portant leurs cargaisons de précurseurs calciques vers une chambre d'assemblage. Devant soi, la vésicule à coccolite s'impose comme une immense coupole membranaire, ambrée à sa paroi, baignée intérieurement d'une lueur froide bleu-gris au sein de laquelle une roue naissante de cristaux de calcite — sombre, facetté, disposée en anneau radial sur un disque de polysaccharides aussi fin que de la soie givrée — prend forme avec une précision qui semble usinée plutôt que biologique. Un quadrant du cercle demeure ouvert, les cristaux y sont plus courts, leurs terminaisons encore rugueuses, témoins d'une minéralisation en cours à laquelle des ions calcium arrivent en pulses invisibles à travers la membrane. Partout ailleurs, le cytoplasme est saturé — ribosomes grainant les surfaces du réticulum endoplasmique, filaments du cytosquelette se perdant dans la pénombre, mitochondries orangées passant au loin — un espace sans vide, sans silence, où chaque nanomètre est occupé et où la pierre se construit depuis la mer, membrane après membrane.

Devant vous, suspendu dans un vide absolu sans horizon ni pesanteur, un coccosphère se dresse comme un soleil conquis : quinze roues de calcite imbriquées forment une sphère presque parfaite, chacune embrasée par la biréfringence sous lumière polarisée croisée, révélant le classique motif en croix de Malte — quatre bras d'extinction veloutée et noire sur fond de blanc du premier ordre si dense qu'il semble posséder une pression interne. Aux bords épaissis des rayons et des boucliers distaux, l'interférence en couche mince fait basculer la couleur vers un or pâle et un ivoire orangé chaud, comme la lumière d'une bougie contre la neige. Les coccolithes libres qui dérivent alentour dans toutes les directions — chaque roue calcitique de trois micromètres, plate comme un métal battu mais ornée d'une architecture cristallographique précise — forment une ceinture de débris lumineux, certains de face révélant leur symétrie complète, d'autres vus par la tranche, minces comme des croissants de lune en rotation. Ces structures n'ont pas été fabriquées : elles ont été cultivées ion par ion, dans l'obscurité et le froid de l'océan, par un organisme unicellulaire dont le génome encode la géométrie du cristal avec une précision que nulle ingénierie humaine ne reproduit, à trois mille mètres au-dessus des sédiments où ses ancêtres ont bâti les falaises de craie.
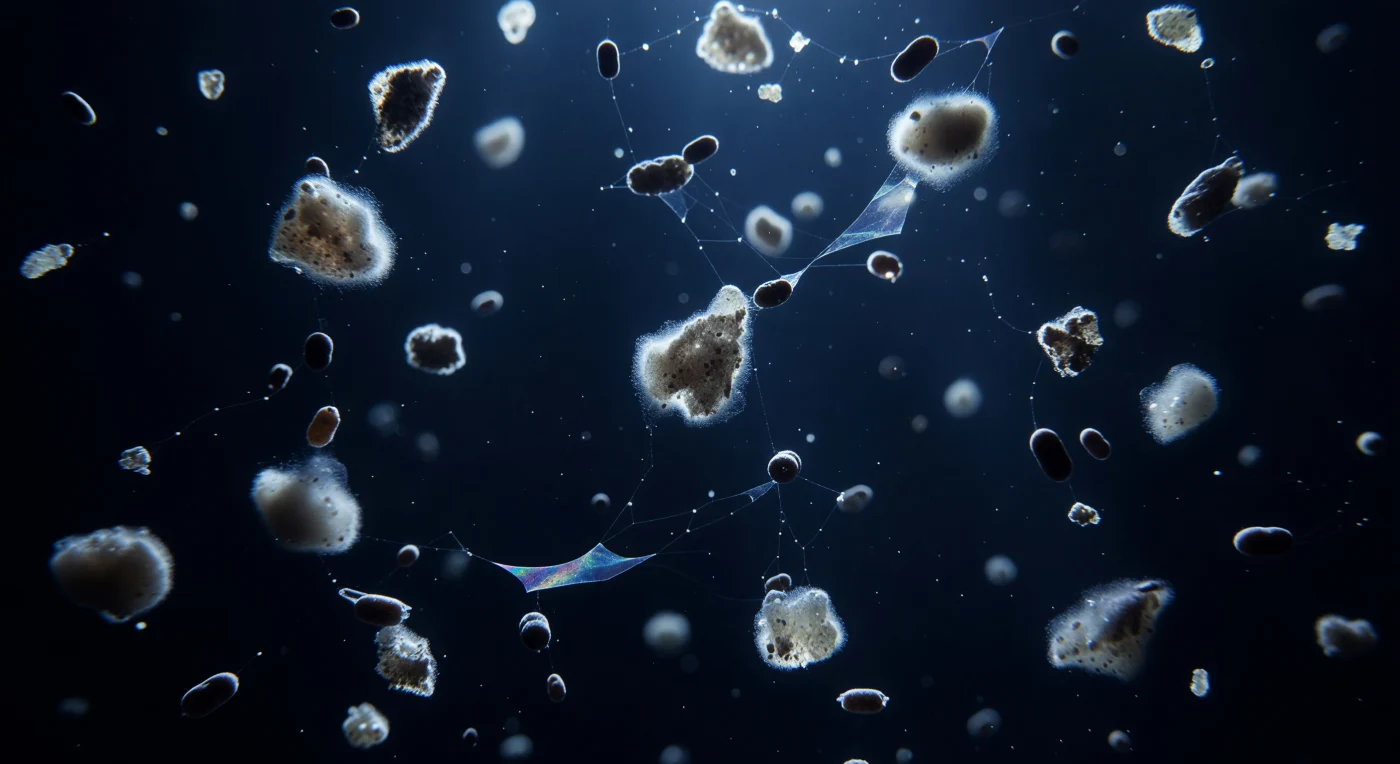
À deux cents mètres sous la surface, le spectateur flotte dans une obscurité quasi absolue, indigo profond, où seuls des photons résiduels filtrés depuis la zone euphotique percent encore l'espace en halo bleu-blanc froid autour de chaque agrégat de neige marine. Ces flocons — fragments de matière biologique compressée, coccolithes brisés, frustules de diatomées, mucus et débris cellulaires fusionnés — descendent avec une lenteur hypnotique, cottonneux et irréguliers, leurs bords lumineux révélant des cristaux de calcite qui dispersent les dernières longueurs d'onde entre 450 et 490 nanomètres comme autant de lanternes fantômes s'enfonçant vers l'abîsse. Entre eux, des pelotes fécales cylindriques brun sombre chutent trois à dix fois plus vite, perçant le champ de neige comme des torpilles compactes, tandis que des filaments de TEP — particules d'exopolymères transparents sécrétés par les cellules phytoplanctoniques — tissent entre les agrégats une toile iridescente à peine visible, ne se révélant qu'à leurs lisières par un reflet fantomatique. Cette scène est la pompe biologique à carbone à l'œuvre : chaque floc est une archive descendante de matière organique produite en surface, transportant vers les sédiments du carbone fixé par photosynthèse, dans une chute lente et continue qui façonne la chimie des océans depuis des centaines de millions d'années.
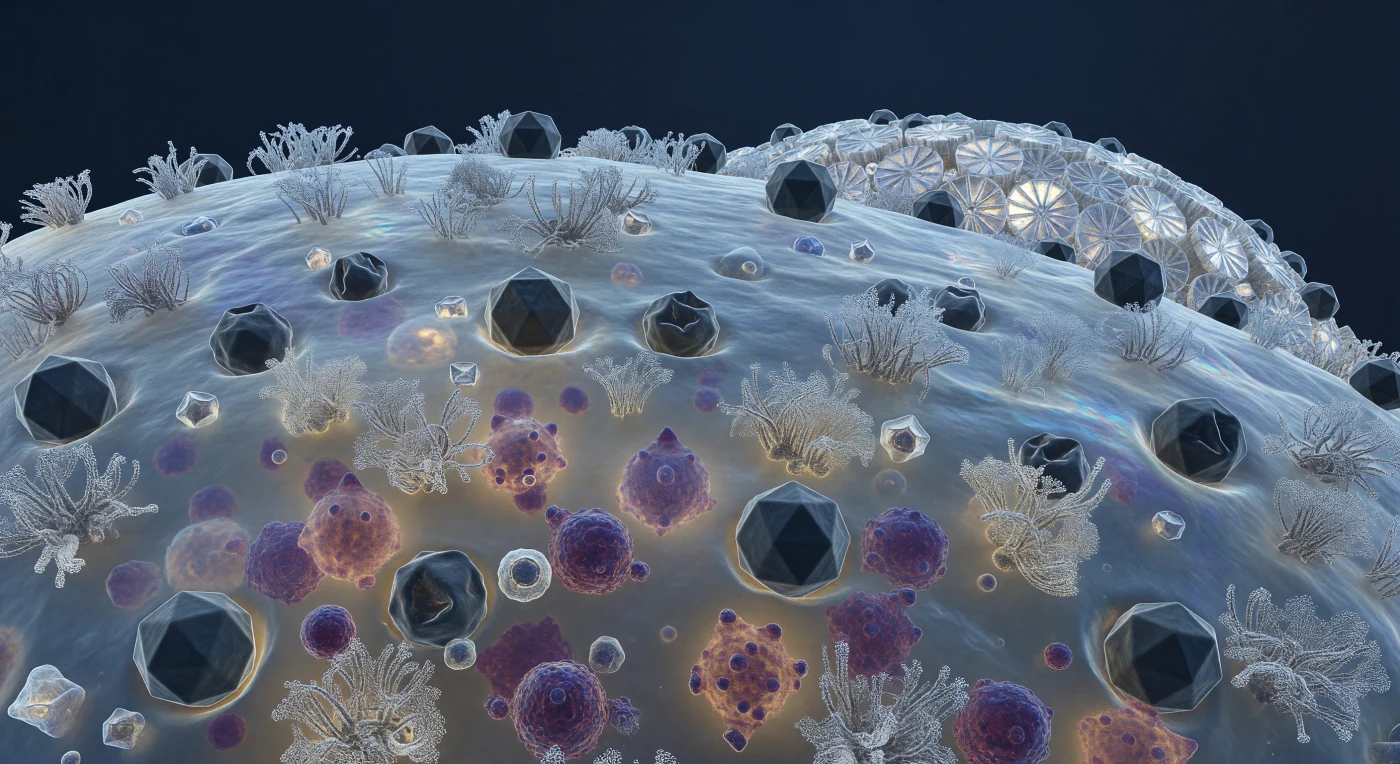
Le regard effleure une immensité courbe et tremblante — la membrane plasmique d'une coccolithophore, tendue comme une peau de tambour sur la pression intérieure de la cellule, ses domaines lipidiques irisés glissant du bleu ardoise au violet pâle sous l'effet d'une interférence en couche mince que l'œil perçoit sans pouvoir la saisir. Des forêts de glycoprotéines hérissent cette surface comme des récifs coralliens miniatures, et contre elles s'appuient, en douzaines d'endroits, des capsides icosaédriques du virus EhV : certaines géométriquement parfaites, leurs vingt facettes triangulaires captant une lumière froide et diffuse venue de nulle part, d'autres effondrées sur elles-mêmes, leur symétrie brisée après injection du génome viral, creusant dans la membrane une fossette de capitulation biologique. À travers la paroi translucide, le cytoplasme luit comme du verre ambré embrumé, et dans ce flou intérieur, de denses masses pourpres et magenta s'accumulent — de nouvelles particules virales en cours d'assemblage, envahissant compartiment après compartiment, appuyant contre la membrane de l'intérieur jusqu'à la faire bomber. Aux confins de cette surface assiégée, les plaques de calcite des coccolithes se dressent en contreforts céramiques blancs, leur géométrie en roue-et-rayons dispersant la lumière en éclairs prismatiques, tandis que la catastrophe moléculaire se déroule en silence, chaque angström de surface contestant la frontière entre la chimie de la cellule et le programme viral qui l'écrase.

Au cœur de l'océan subtropical, à cent mètres sous la surface, le regard s'ouvre sur un crépuscule d'une précision spectrale absolue : une lumière cobalt de 475 nanomètres, si pure qu'elle semble moins une illumination qu'une substance, baigne uniformément l'eau dans toutes les directions comme si l'océan lui-même en était la source. Dans cet indigo suspendu dérivent des dizaines de cellules — dinoflagellés aux armures amphiesmatiques légèrement prismatiques, chaînes de diatomées dont les frustules de silice captent les rares photons disponibles et les restituent en brèves étincelles froides — chacune brillant d'un or-olive chaud contre le verre bleu du milieu, leurs chloroplastes concentrant l'énergie lumineuse à peine 2 % de ce qu'absorbe la surface. C'est la couche de chlorophylle maximale profonde, une strate biologique qui s'organise à l'exacte frontière entre la lumière encore exploitable et les ténèbres en dessous : les organismes photosynthétiques s'y accumulent par chimiotaxie et flottabilité ajustée, exploitant jusqu'au dernier quantum utilisable. Au-dessous, à quelques longueurs de cellule, la neige marine descend en silence — agrégats translucides de brins d'exopolymères, de plaques de coccolithes encore parfaitement emboîtées en roues calcitiques géométriques, de matière fécale compacte — chaque flocon devenant à cette échelle un événement architectural, rétroéclairé par le bleu supérieur jusqu'à luire faiblement en ses membranes les plus minces avant de sombrer vers l'aphotique, là où la chaleur olive s'éteint graduellement et où ne subsiste bientôt plus que le noir absolu.

À l'échelle d'un grain de sable fin, suspendu dans le premier millimètre d'un océan ouvert à la lisière de l'aube, vous vous trouvez face à un *Ceratium tripos* qui emplit votre champ de vision comme une cathédrale d'ambre translucide — ses trois cornes creuses, renforcées de travées calcitiques aussi délicates que de la dentelle soufflée, captent les premiers photons roses et bleu d'acier qui se plient à travers l'interface eau-air tremblante au-dessus de vous, projetant des balayages prismatiques lents sur les plaques de l'amphiesma, dont chaque suture brille comme un fil de feu froid. Dans le sillon du cingulum, le flagelle transversal bat en ruban hélicoïdal continu — collectivement, ses coups produisent un frémissement argenté presque imperceptible, brève signature mécanique d'un organisme qui propulse son demi-millimètre de masse dans un milieu où la viscosité rend chaque déplacement comparable à une nage dans du verre refroidi. Autour de vous dérive une neige éparse de coccolithes détachés, minuscules roues de calcite de deux à quatre micromètres, chacune diffractant la lumière montante en étincelles froides dans l'indigo — vestiges d'une efflorescence invisible dont la calcite finira, en des millénaires, par sédimenter en craie au fond de l'océan. Dans le lointain intermédiaire, le copépode est immobile comme une tour de verre articulé, ses antennes déployées en rames transparentes gelées en plein mouvement, sa seule présence suffisant à rappeler que cette aube dorée, pour le *Ceratium*, est aussi une question de survie.

Le regard se perd dans un brouillard d'un vert de verre marin, dense et sans horizon, où chaque point lumineux est une cellule d'*Ostreococcus tauri* — le plus petit eucaryote photosynthétique connu, à peine 0,8 micromètre de diamètre, à la limite exacte entre particule et longueur d'onde visible. Si proches qu'elles se confondent avec le milieu lui-même, des milliards de ces sphères translucides teignent collectivement l'eau de leur chlorophylle, transformant le fluide interstitiel en une substance vivante d'un jade pâle qui s'épaissit vers le sarcelle là où la densité cellulaire augmente. Chaque cellule qui dérive à portée révèle son chloroplaste unique, volumineux, pressé contre la membrane comme un noyau sombre dans une bille de verre, avant de basculer sous l'effet du mouvement brownien et de se fondre à nouveau dans la lueur collective. La profondeur ne se lit pas en distance mais en saturation chromatique : les cellules proches sont des lanternes viridines distinctes, celles situées à deux ou trois micromètres déjà fantômes, leurs contours dissous dans le rayonnement ambiant de la suspension qui s'étend, tremblante et respirante, dans toutes les directions sans plancher ni plafond.
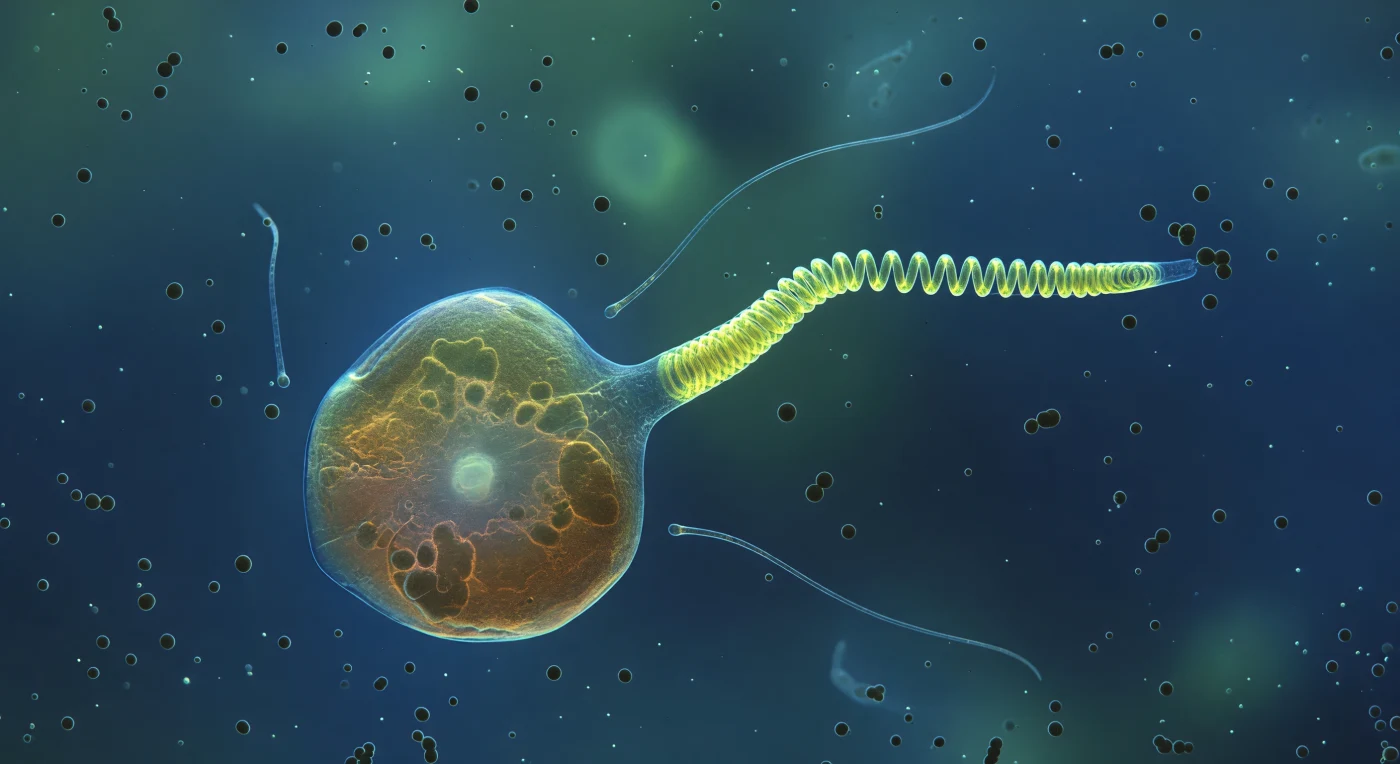
Au cœur de l'océan microbien, une cellule de *Chrysochromulina* emplit le champ visuel comme une maison de verre ambré suspendue dans une lumière bleue-verte diffuse, ses organites internes — lobes de chloroplaste sombres, noyau pâle — visibles par transparence à travers une membrane aussi fine qu'un film de savon. De l'un de ses pôles, l'haptonème jaillit en pleine métamorphose : son tiers proximal s'est déjà effondré en une spire hélicoïdale serrée d'un jaune-vert fluorescent presque incandescent, tandis que la portion distale, encore rigide, commence à fléchir à la zone de transition, toute la structure évoquant un filament de néon qui se noue sur lui-même en quelques millisecondes — un mécanisme de propulsion ou de capture dont la biophysique repose sur un réseau de microtubules internes capable de se contracter violemment sous l'afflux de calcium ionique. Autour de la cellule, deux flagelles quasi transparents dérivent comme des fils d'argent dans le milieu visqueux, pendant qu'une constellation de sphères matte de charbon — bactéries d'un micromètre — se rassemble dans le gradient chimique au voisinage de l'haptonème en train de claquer, attirées par les exsudats organiques que la cellule exhale en permanence. L'eau elle-même n'est pas vide : une diffusion douce et laiteuse trahit la présence de vésicules membranaires et de matière organique dissoute qui font reculer le fond jusqu'à un bleu cobalt presque noir, où les sphères bactériennes lointaines s'évaporent dans la lueur ambiante avant qu'aucun horizon ne soit jamais atteint.

Depuis le bastingage de proue, le regard plonge sur l'une des frontières naturelles les plus tranchées qu'offre la surface planétaire : à bâbord, un océan cobalt d'une transparence abyssale où la lumière s'enfonce en colonnes obliques sans jamais rencontrer d'obstacle ; à tribord, une masse d'eau opaque, calcaire, d'un turquoise pâle presque minéral, dont l'éclat diffus et nacré semble irradier de l'intérieur plutôt que de la surface — chaque litre contenant des dizaines de millions de coccolithophores, cellules de cinq à dix micromètres cuirassées de plaquettes de calcite qui diffusent la lumière en tous sens comme autant de prismes géométriques invisibles à l'œil nu. La limite entre les deux masses d'eau est quasi chirurgicale, à peine deux mètres de largeur, soulignée par des trainées de mousse parallèles organisées par la circulation de Langmuir en lents rouleaux hélicoïdaux affleurant la surface. Un fou de Bassan bascule soudainement en arrière et perce la zone productive dans une gerbe d'eau blanche qui flambe un instant sous le soleil rasant de l'après-midi avant que la surface ne se referme, lisse, sur l'oiseau disparu — pendant ce temps, l'air porte une légère douceur soufrée, le diméthylsulfure que libèrent les cellules en stress, preuve chimique d'une alchimie calcaire qui, accumulée sur des millions d'années, a bâti les falaises de craie de Douvres.

Au sein de la carotte sédimentaire, la section transversale révèle un monde compressé de lamines crème et ivoire qui s'étendent à l'infini de chaque côté, chaque bande représentant des siècles de sédimentation lente depuis les eaux de surface éclairées par le soleil. Vous existez à l'échelle d'un unique coccolithe — une roue de calcite trigonale d'une précision géométrique absolue, ses rayons cristallins encore intacts après dix millions d'années d'enfouissement, sa jante en relief projetant une ombre nette sous la lumière rasante ambrée qui traverse la matrice comme un soleil de fin d'après-midi filtré à travers de la pierre givrée. Autour de vous, la densité est écrasante : des milliers de roues similaires s'imbriquent comme un sol de mosaïque taillé à l'échelle nanométrique, leurs interstices comblés d'une boue coccolithique semi-translucide et cireuse, résidu compressé de membranes cellulaires et d'échafaudages polysaccharidiques qui furent autrefois vivants et photosynthétiques. Plus profond dans la matrice, les coccolithes plus anciens trahissent les premières signatures de la diagenèse — leurs contours s'estompent, leurs rayons se fondent dans une uniformité crayeuse — la calcite abandonnant progressivement son identité cristalline au poids des temps géologiques. Ce lieu est le silence absolu d'une floraison disparue : nulle diffusion chimique, nul mouvement brownien, seulement la géométrie obstinée et magnifique de l'armure calcaire qui survit à tout le reste de la biologie.
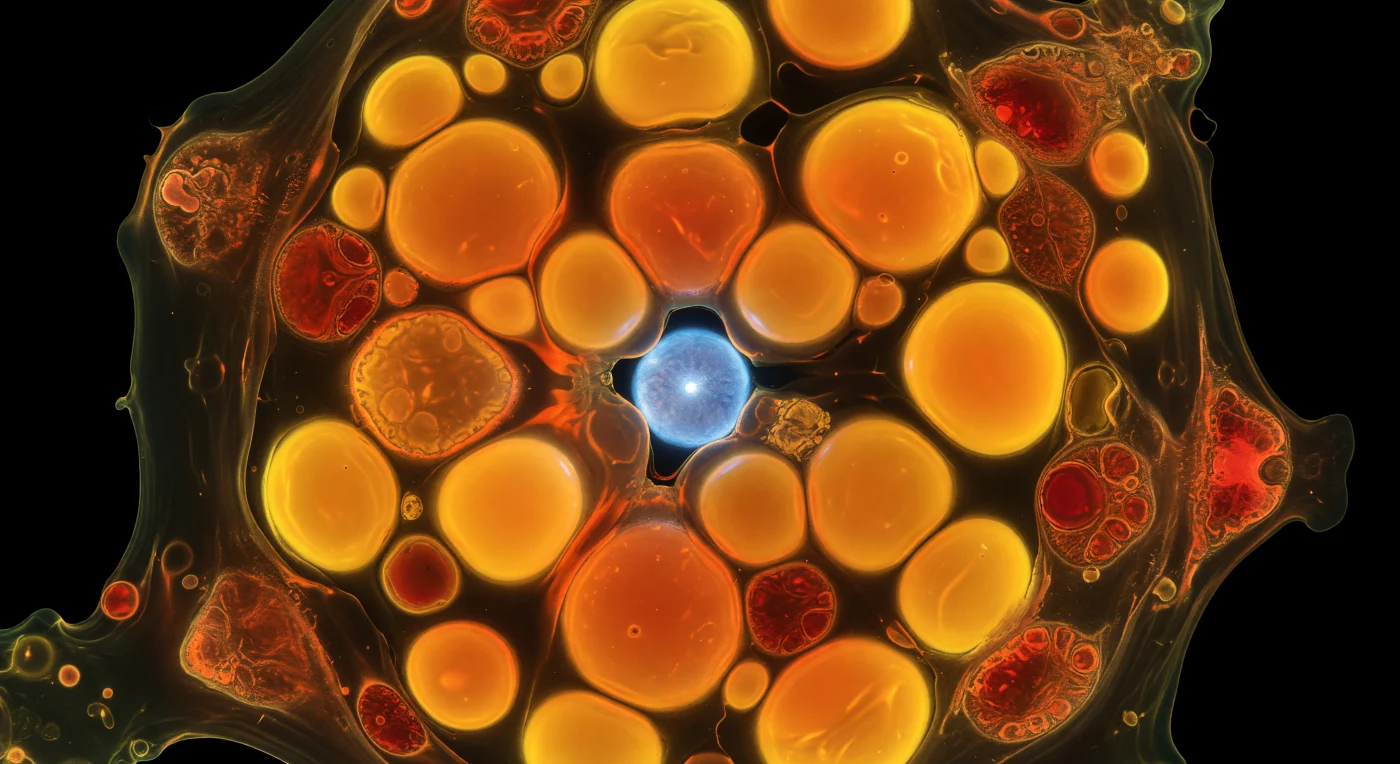
Dans l'obscurité absolue qui règne autour de cette unique cellule d'*Emiliania huxleyi* privée d'azote, le regard est immédiatement saisi par une constellation de sphères incandescentes : des gouttelettes lipidiques gonflées au-delà du raisonnable, chacune brillant d'un orange-or presque violent sous l'effet du Nile Red intercalé dans chaque molécule de lipide neutre, émettant leur propre lumière comme des lanternes closes. Ces globules huileux — dont les surfaces parfaitement tendues se déforment légèrement aux points de contact en lentilles aplaties — occupent la quasi-totalité du cytoplasme, résultat d'une redirection métabolique massive : face au manque d'azote, la cellule a détourné le carbone fixé par photosynthèse vers le stockage lipidique plutôt que vers la synthèse protéique. Repoussés à la périphérie par cette marée d'huile, les chloroplastes n'émettent plus qu'une autofluorescence rouge-cramoisi pâle et résignée, leurs empilements thylakoïdiens visibles comme de fines laminations concentriques dans des organites écrasés entre les globules. Au cœur de cet encombrement, à peine entrevu à travers un interstice entre deux sphères ardentes, le noyau brille d'un bleu électrique — le DAPI lié à l'ADN compacté — seul point froid et lunaire dans un univers intérieur qui brûle entièrement de lumière née de lui-même.

Les mains qui fendent l'eau noire déclenchent une déflagration froide à 460 nanomètres, une teinte bleu saturé si précise qu'elle semble synthétique, produite pourtant par des millions de *Lingulodinium polyedra* dont chaque cellule — une sphère de six à douze micromètres — libère sa luciférase en cascade dès que la pression mécanique de déplacement comprime les scintillons membranaires contre leurs voisins. Les sillages des doigts persistent deux secondes entières, s'élargissant de lignes tranchantes en auréoles diffuses qui cartographient la turbulence même, chaque tourbillon et remous rendu lisible en lumière vivante avant de se dissoudre vers le teal puis vers le néant, là où les cellules non perturbées dérivent invisibles et en attente. À cinquante mètres, le sillage d'une embarcation disparue forme un fleuve de lumière bleue et blanche d'une densité presque solide, ses rives nettes et son centre si intensément peuplé de décharges simultanées qu'il ressemble à une route incrustée dans l'eau noire, écrite par une coque qui a depuis longtemps quitté le champ de vision. Le corps lui-même devient générateur de lumière : chaque micro-ondulation produite par la respiration ou le battement cardiaque relance de nouvelles cascades dans les cellules sensibles alentour, de sorte que le simple fait d'exister dans l'eau trace en feu biochimique une carte en temps réel des plus infimes mouvements du vivant.
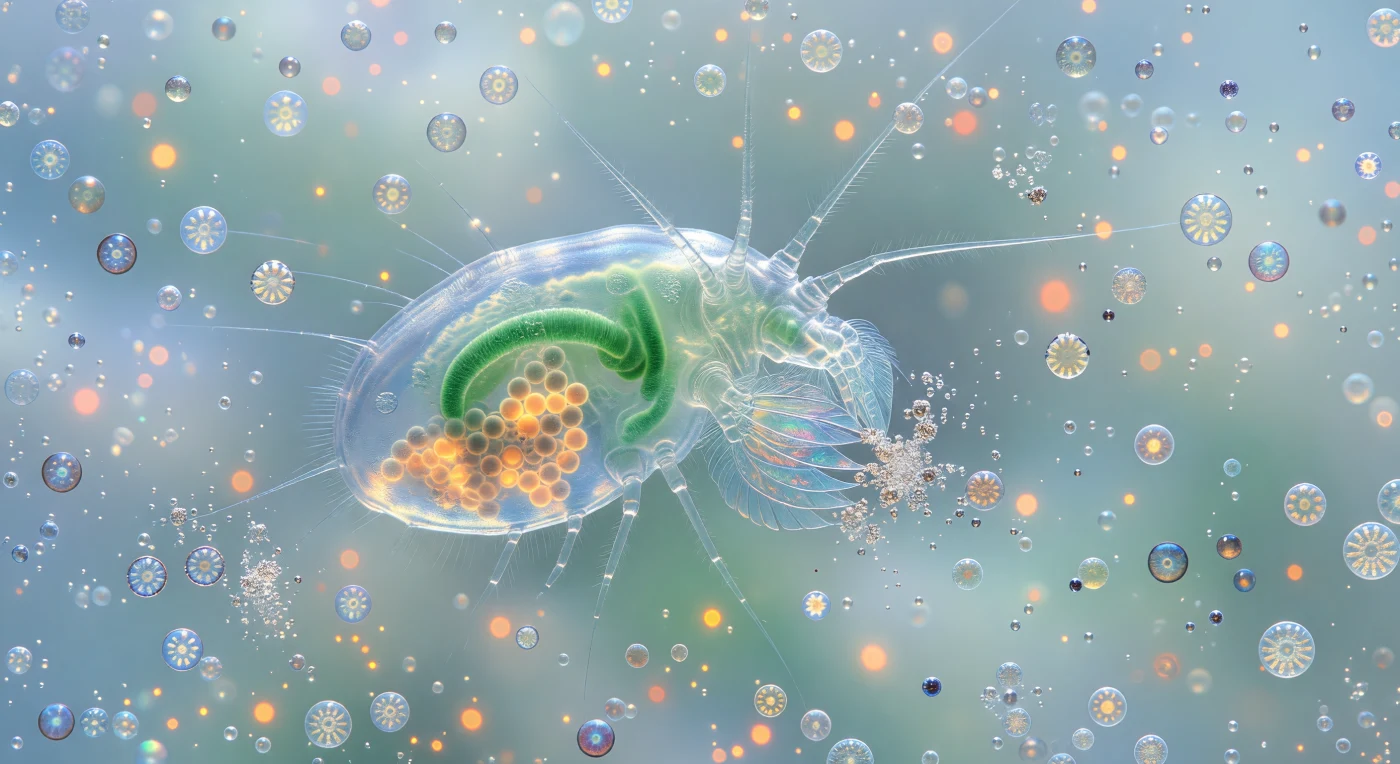
À deux millimètres de distance, le regard plonge dans la transparence absolue d'un copépode dont le corps vitrifié fonctionne comme une lanterne : le tube digestif jade et les grappes d'œufs ambré-orangé brûlent à travers trois couches de cuticule chitineuse, organes rétroéclairés par la lumière diffuse qui filtre depuis la surface en ondes bleu-vert et se plie en halos prismatiques sur chaque courbe de la carapace. Les maxillipèdes — rangées de soies en verre soufflé qui tremblent à la marge du champ visuel — capturent les cellules de coccolithophores une à une, et à leur point de contact les coccosphères broyées explosent en gerbes de glitter blanc, chaque sphère détruite libérant une volée de disques de calcite de deux micromètres qui flashent et tournent avant d'être emportés par le vortex alimentaire. L'eau environnante n'est pas vide : c'est une suspension de lait turquoise, dix millions de coccolithes détachés par millilitre transformant le milieu en brouillard lumineux où les coccosphères intactes dérivent comme des planètes blindées, leurs plaques de calcite captant la lumière en anneaux concentriques d'argent froid, tandis que les chloroplastes d'*Emiliania huxleyi* rayonnent une autofluorescence rouge-orangée visible comme des constellations de chaleur métabolique à l'intérieur de membranes translucides. Le copépode organise par sa seule géométrie d'alimentation tout l'espace lumineux alentour : ses antennes s'étendent dans le brouillard calcaire comme des branches pâles et réfractives, et derrière lui la colonne d'eau s'enfonce non dans l'obscurité mais dans une atmosphère bleu-blanc de plus en plus dense, chaque couche un peu plus brillante que la précédente à mesure que les coccolithes s'accumulent au-dessus — le monde entier réduit à texture, lumière, et destruction géométrique.

Vous flottez dans une colonne d'eau océanique d'un bleu profond et saturé, maintenu en suspension par les seules forces de la traînée visqueuse, le nombre de Reynolds si infime ici que toute notion d'élan devient absurde. À votre gauche, la cellule en phase C d'*Emiliania huxleyi* s'impose comme une architecture minérale baroque : sa coccosphère, composée de plaques de calcite crème disposées en symétrie imbriquée, intercepte les photons descendants et les renvoie en éclats prismatiques d'or pâle et de blanc froid, chaque coccolithe révélant des lames cristallines à géométrie trigonale, des rayons radiaux et de minuscules fenestrae d'une précision qui défie la matière vivante. À votre droite, séparée par quelques longueurs de cellule de colonne ouverte, la cellule haploïde en phase N offre un contraste de registre matériel saisissant : sa membrane nue, translucide et d'un vert crème légèrement irrégulier, laisse transparaître la chaleur dorée-ambrée de ses chloroplastes, dont les pigments convertissent même cette lumière filtrée en une douce lueur d'autofluorescence, pendant que ses deux flagelles — filaments biologiques à peine plus épais qu'une fraction de micron — sont figés en plein battement, chacun courbé en sinusoïde gracieuse contre le champ bleu. Ces deux cellules incarnent les deux faces d'un même cycle de vie : la diplophase calcifiée participant activement à la pompe biologique du carbone en précipitant du CaCO₃, tandis que la haplophase nue, plus mobile, explore chimiotactiquement son milieu, toutes deux baignant dans un médium dont les gradients imperceptibles de CO₂ et d'indice de réfraction trahissent l'activité métabolique intense de structures qui, agrégées par milliards, blanchissent des milliers de kilomètres carrés de surface océanique depuis l'espace.

Vous vous tenez au pied des falaises blanches de Douvres, le regard levé vers une paroi quasi verticale qui s'élève à une hauteur vertigineuse, sa surface calcaire d'un blanc aveuglant sous la lumière rasante de l'après-midi, si intense contre le ciel bleu-gris atlantique qu'elle semble irradier sa propre clarté. Ce que vous contemplez n'est pas de la roche ordinaire : chaque centimètre cube de cette craie cénomanienne renferme des millions de coccolithes, ces minuscules armures de calcite sécrétées par des algues unicellulaires vieilles de quatre-vingt millions d'années, compressées par le poids des océans disparus en une pâte biogénique qui constitue aujourd'hui une falaise de cent mètres. Les bandes sombres de silex qui strient horizontalement la paroi blanche sont les fantômes chimiques d'anciens fonds marins, chaque ligne marquant une pause dans la pluie silencieuse de coquilles calcifiées qui, génération après génération, s'accumulait sur le plancher d'une mer tropicale peu profonde. À mi-hauteur, à peine visible, un fulmar immobile sur une corniche révèle soudainement l'échelle réelle de cet édifice, rendant le vertige physique et presque insupportable. Vous êtes face à une archive de la vie microscopique rendue monumentale : la somme de milliards de cycles cellulaires, de photosynthèses, de calcifications et de chutes vers les abysses, solidifiée en ce mur silencieux et aveuglant.