
Der Blick richtet sich von unten nach oben durch einen Wald aus dreißig *Acetabularia acetabulum*-Stielen, die wie schlanke Jadestäbe aus dem weißen Kalkgestein emporwachsen – jeder Stiel ein einzelnes gigantisches Lebewesen, eine einzige Zelle von bis zu acht Zentimetern Höhe, deren dünne Wände die chloroplastenreichen Ektoplasmaschichten als dunkle Bänderung durchschimmern lassen. Die Schirmkappen an den Spitzen jedes Stiels sind flache, radiär segmentierte Scheiben – gametangiale Strahlen, angeordnet wie die Speichen eines gotischen Rosenfensters – und im Gegenlicht des schräg einfallenden Mittelmeermorgensonnenstrahls leuchten sie wie kleine Buntglaslanternen in Chartreuse und warmem Strohgelb auf. Das Wasser darüber schimmert in tiefem Coelanth-Türkis, durchzogen von kaustischen Lichtmustern, die langsam über den weißen Kalkboden wandern und den Zwischenraum zwischen den Stielen in kühlen Schatten tauchen, der von hellen, smaragdgrünen Lichtschlitzen durchbrochen wird. Was hier als Kolonie erscheint, ist in Wahrheit eine Gemeinde von Individuen, von denen jedes eine einzige, kernlose Zelle ist – der einzige Kern sitzt tief unten im Rhizoid, verankert in krustigen Kalziumkarbatatkristallen –, und die langsame Migration der Chloroplasten zur sonnenzugewandten Flanke hin ist die einzige Bewegung in dieser stillen, unterweltlichen Kathedrale.

Der Blick fällt senkrecht durch eine vollkommen reglose Wasseroberfläche, die wie ein optisches Glas wirkt und die Welt darunter in kristalliner Schärfe freilegt: ein Kontinent aus dicht gedrängten blaugrünen Kugeln, deren mehlig-blaugrüner Schimmer das gesättigte Chlorophyllgrün darunter sanft dämpft, während jede einzelne Sphäre einen harten weißen Lichtpunkt fängt — tausend Nadelstiche aus konzentriertem Mittagslicht über einem Teppich, der sich wie eine belebte Gebirgslandschaft aus Hügeln und Tälern im Millimetermaßstab entfaltet. Was hier als Terrain erscheint — mit Kammlinien, Schatten und topografischer Tiefe — ist in Wahrheit ein einziger lebender Organismus, dessen gesamte Oberfläche aus Rhizoiden bis zu den äußersten Verzweigungen von einer einzigen durchgehenden Plasmamembran umschlossen wird, ohne trennende Querwände: eine coenocytische Architektur, in der Millionen von Zellkernen gemeinsam durch dieselbe Cytoplasmamasse treiben. Kaustiknetzwerke aus gebrochenem Sonnenlicht wandern träge über den Algengrund, zeichnen die Mikrostruktur der Wasseroberfläche nach und verlöschen wieder, während am Rand des Beckens leuchtendes Orangerot der einkrustenden Schwämme den biologischen Regelmäßigkeiten der Sphären gegenübersteht. Die Paradoxie ist greifbar: was das Auge als Landschaft liest, ist Zelle.

Der Blick streift zentimeterknapp über den hellen Kalksand in zwölf Metern Tiefe und trifft auf eine Wand aus elektrischem Smaragdgrün, die sich lückenlos bis zum Horizont erstreckt: ein dichter Teppich aus *Caulerpa taxifolia*, jedes federartig gefiederte Thallus ein einziges riesiges Coenocyt, eine kernlose Vielfachzelle ohne innere Trennwände, deren gesamter Stängel, alle Stolonen und sämtliche Fiederblättchen von einem einzigen gemeinsamen Zytoplasma durchströmt werden. Die gepaarten, paddelflachen Pinnulen sind mit mechanischer Präzision entlang der Rachis angeordnet und fangen das diffus einstreuende, blau verschobene Sonnenlicht auf; wo es die hauchdünnen Randzonen von vorn beleuchtet, leuchten sie gelbgrün auf und geben den Blick frei auf eine glasige Vakuole und den granulierten, chlorophyllreichen Kortex darunter. Langsam ziehende Lichtkaustiken streifen über die Frondspitzen und verlieren sich im blaugrünen Halbdunkel zwischen den Stolonen, während eine einzelne, elfenbeinfarbene Gastropodenschale mit ihren Spiralrippen wie ein Fremdkörper auf dem Sand liegt – der einzige Gegenstand, der an menschliche Dimensionen erinnert, inmitten einer lebendigen Tessellation, die jede andere Struktur auslöscht. Diese invasive Alge überwuchert weite Teile des Mittelmeers mit einer Dichte und Gleichförmigkeit, die dem Meeresgrund jenen Artenreichtum raubt, der ein vielgestaltiges Benthos erst möglich macht.

You hover motionless just above a limestone crevice fracture, close enough that the trembling mercury sheet of the Caribbean surface fills your entire peripheral vision above, while fifteen *Valonia ventricosa* spheres occupy the crevice floor like pressurized glass baubles — each one a single cell two to four centimeters across, their taut walls pulled so tight they read less as biology than as blown borosilicate, shading from deep saturated emerald at the flanks to chartreuse where caustic threads of focused sunlight snake and bloom across their surfaces in continuous fluid reorganization. Each sphere is an individual coenocytic cell under extraordinary turgor pressure — its multilayered cellulose wall wound in opposing helical fiber arrays that lend the surface a faint silky crosshatch rather than a true mirror finish — and where the light strikes at near-normal incidence, the translucency of that wall reveals the interior as a single luminous jade volume, the massive central vacuole diffusing chlorophyll light outward so that each sphere glows as if self-illuminated, a dense green lantern with a darker ectoplasmic chloroplast rind pressed millimeter-thin against the inside of the glass. A bristle worm threads between two of the larger spheres in copper and rust iridescence, its body dwarfed by the cell mass it navigates — an animal composed of billions of cells picking its way through the architecture of just fifteen — while behind the cluster the crevice walls bear their crustose coralline algae in chalky pink granularity, the textural opposite of the glassy perfection pressing against them, and the entire scene holds suspended in a single sharp instant, every caustic filament crisp, every bristle a hair of light.
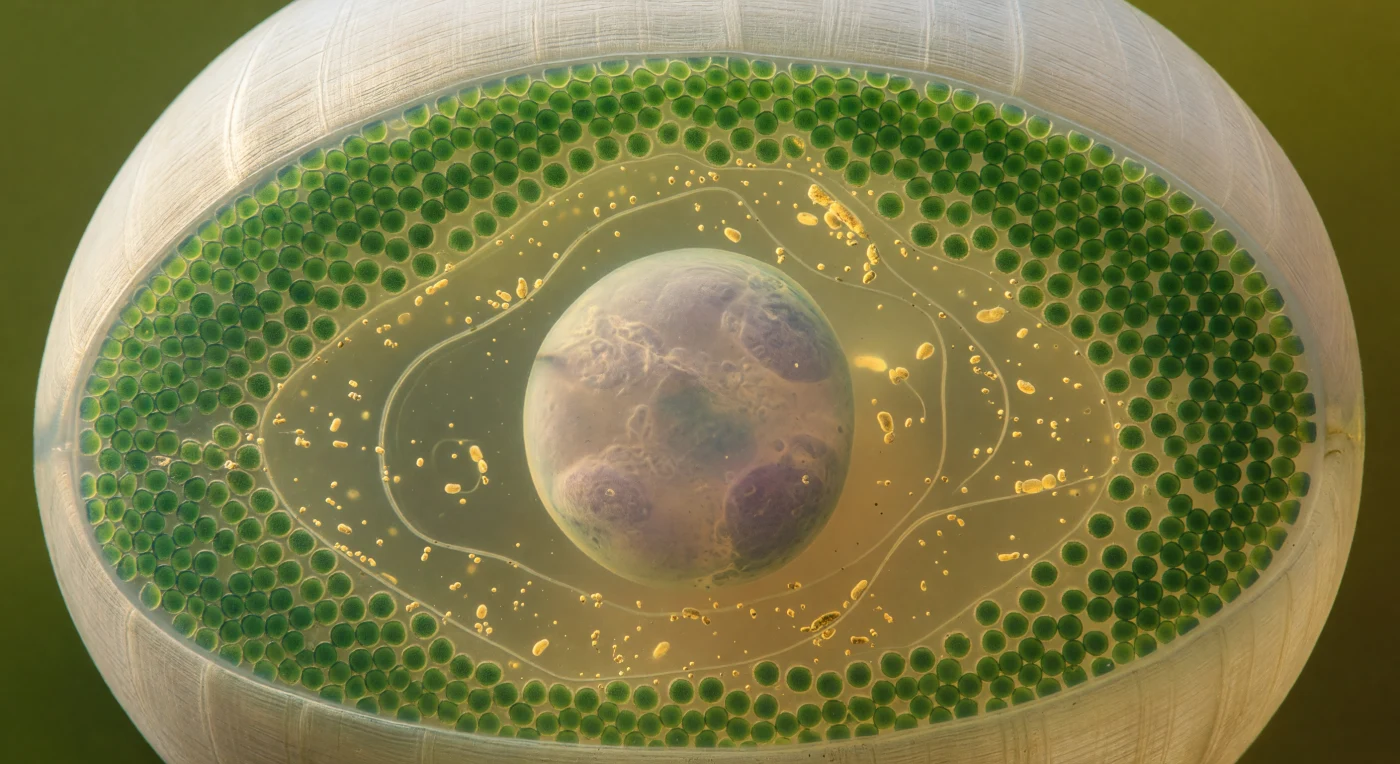
Im Inneren des Rhizoids einer einzigen lebenden Zelle schwebend, umgibt uns eine von warmem Bernsteingrün durchflutete Welt, in der die gekrümmte Zellwand aus gepresstem Cellulosemikrofibrillen-Geflecht wie das Innere einer kleinen Glaskugel um uns herum aufsteigt, dicht belegt mit Hunderten jadegrüner Chloroplasten, die wie ein leuchtendes Bleiglasmosaik gegen das von außen eindringende Sonnenlicht glühen. Im Zentrum dieses abgeschlossenen Raumes schwebt der Zellkern – eine blassgraue, ins Lavendel spielende Kugel mit einem dunkleren Nukleolus in ihrem Inneren –, ein einzelner kolossaler Kern, wie er nur in *Acetabularia* existiert, jener wenige Zentimeter großen Meeresalge, die als vollständiger Einzeller zu den faszinierendsten Organismen der Biologie zählt. Zwischen Wand und Kern fließt das Cytoplasma in trägen, geschwungenen Bahnen – goldene Granula und Stränge des endoplasmatischen Retikulums treiben in der Cyclosis-Strömung mit einer Langsamkeit, die eher geologischer Drift ähnelt als biologischer Bewegung. Das gesamte Licht stammt aus dem Gewebe selbst, gebrochen durch Chlorophyll und Zellsaft, und erfüllt den Raum mit einer botanisch-altertümlichen Leuchtkraft, als befände man sich im Inneren einer lebenden, pulsierenden Laterne.

Der Blick gleitet hinein in den Hohlraum eines einzigen lebenden Zellkorridors, dessen gebogene Innenwände aus dicht gepackten Chloroplasten in einem tiefen, satt leuchtenden Smaragdgrün strahlen – eine Wand aus lebendigem Buntglas, deren Licht kein Außen zu kennen scheint, sondern aus dem Material selbst quillt. Von Wand zu Wand spannen sich die Trabekel, jene zytoplasmastischen Stränge aus wasserheller Transluzenz, die den offenen Vakuolenraum in ein System aus gotischen Bögen und Strebebögen gliedern und sich in die grünlich schimmernde Tiefe des Stolons verlieren, bis die fernsten Fäden zu bloßen Lichtlinien im Dunkel verblassen. *Caulerpa* ist eine einzige ununterbrochene Zelle, die aus Holdfast, Stolon und aufrechten Fronden ein zusammenhängendes Zytoplasma ohne innere Querwände bildet – Tausende von Zellkernen teilen sich einen gemeinsamen Inhalt, der durch diesen Korridor als langsamer, kaum wahrnehmbarer Strom aus bernsteinfarbenen Organellen und Stärkekörnern treibt. Was einem gotischen Kirchenschiff gleicht, ist das Resultat eines einzigen biochemischen Lebens: Turgor, Zellwandarchitektur aus sich überkreuzenden Cellulosemikrofibrillen und die Mechanik des Zytoskeletts halten diesen Raum offen gegen den inneren Druckdes Lebens selbst.

Du schwebst Zentimeter über dem Boden der Welt, in Wasser, das sich unter fünf Kilometern Druck wie Glas um dich legt – und vor dir erhebt sich *Syringammina fragilissima*, ein einzelnes Lebewesen von der Größe einer Kinderfaust, das sich aus Tausenden agglutinierter Foraminiferenschalen und Mineralkörnern zu einer Architektur zusammengesetzt hat, die wie ein Karstgebirge im Miniaturformat wirkt, kohlrabenschwarz und tiefem Umber in den Zonen des schräg einfallenden LED-Lichts, absolut leer dort, wo es nicht hinreicht. Das harte blau-weiße Kegel-Licht des ROV schneidet messerscharfe Schatten in jede Vertiefung der porösen Oberfläche und macht sichtbar, was dieses Wesen ist: keine Kolonie, kein Tier, keine Pflanze, sondern eine einzige riesige Zelle, deren Zytoplasma sich in feinen Röhren durch das Sediment erstreckt und Körnchen für Körnchen zu einem Gehäuse zusammenfügt, das geologisch aussieht, wie Ruinen aussehen, wie Zeit selbst aussieht. In drei Körperlängen Entfernung erlischt das Licht vollständig, und was bleibt, ist keine gewöhnliche Dunkelheit, sondern das physische Gewicht von fünf Kilometern Meerwasser über dir. Durch den beleuchteten Kegel sinken winzige Partikel marinen Schnees in nahezu vollständiger Stille herab, und das Wesen darunter wartet – ohne Puls, ohne Bewegung – mit der Geduld von Stein in einem Abgrund, den sonst seit geologischen Zeiten nur Dunkel kennt.

Du stehst im genauen Mittelpunkt einer lebenden Kugel, und die Welt wölbt sich von dir weg in jede Richtung zugleich – die innere Oberfläche der Vakuolenmembran bildet einen vollständigen Horizont, der sich wie die Innenseite eines Planeten um dich schließt, nahe genug, dass man meint, ihn in wenigen Schritten erreichen zu können, und doch mit der Unausweichlichkeit einer Planetenkrümmung in alle Hemisphären entgleitend. Die gesamte Wand leuchtet: Ein dichtes, lückenloses Mosaik aus Chloroplasten, flach gegen das kortikale Ektoplasma gepresst, taucht die umschließende Sphäre in gesättigtes Smaragd- und Flaschengrün – kollektiv eine lebendige, leicht körnige Tapisserie, die mit dem inneren Licht photosynthetischer Pigmente pulsiert, während hinter dem grünen Mantel die kreuzweise verlegten Cellulosemikrofibrillen der Zellwand ein Fischgrätmuster aus Creme und Elfenbein weben, eine präzise textile Architektur unter gespannter Haut. Das blassstrohgelbe Vakuolenfluid, mit seiner ungewöhnlich hohen Kaliumkonzentration chemisch hochpräzise ausbalanciert, füllt den Innenraum mit einem Medium, das Licht kaum streut, sodass das grüne Wandleuchten dich von allen Seiten gleichzeitig erreicht und harte Schatten schlicht nicht existieren – nur eine allseitige, quellenlose Smaragdlumineszenz. *Valonia ventricosa* ist eine einzige Zelle, deren Turgor so exakt geregelt ist, dass die Sphäre starr wie geblasenes Glas steht, eine einzige Membran trennt dieses chemisch fremdartige Innere vom umgebenden Meer, und das gesamte Bauwerk verharrt in einer unwahrscheinlichen, monumentalen biologischen Stille.

Direkt vor dir erhebt sich der Stolon wie ein unter Druck gesetztes Rohr aus grünem Glas, seine Oberfläche nass-glänzend und lackartig, das Innere erfüllt von dicht gepackten Chloroplasten, die gegen die Wandung gepresst liegen – und das alles ist eine einzige, ununterbrochene Zelle. Von seiner Unterseite zweigen die Rhizoide fraktal in das Sediment hinab, je hundert Mikrometer breit, transluzent amber-weiß, ihre Wände so dünn, dass die anliegenden Sandkörner hindurchscheinen wie Felsen hinter einer Glasscheibe. Diese Sandkörner sind hier keine Partikel, sondern gewaltige Mineralbrocken – durchscheinende Quarzsphäroide, mattierte Feldspatplatten –, zwischen denen die feinen Rhizoidenden mit bemerkenswerter Präzision hindurchfädeln und sich der Topographie jedes einzelnen Korns anschmiegen. Das Licht wandelt sich von einer diffus-grünlichen Küstenradiation an der Oberfläche zu tiefem Bernstein-Braun in wenigen Zentimetern Tiefe, bis die feinsten Filamente nur noch als zarte Umrisse in einem letzten Lichtschimmer erkennbar sind, bevor sie in granularer Dunkelheit verschwinden. Was wie ein unterirdisches Wurzelsystem wirkt, ist in Wahrheit ein einziger coenocytischer Organismus ohne innere Zellwände – ein kontinuierliches Cytoplasma, das Meter weit reichen kann und dennoch nie aufgehört hat, eine Zelle zu sein.

Vor dir erheben sich drei grüne Säulen aus dem weißen Aragonitgrund — jede ein einziges Leben, jede eine einzige Zelle, jede in einem anderen Stadium ihrer langsamen Entfaltung. Die jüngste trägt noch zarte Haarwirtel aus Zytoplasma, die das schräg einfallende Licht in feine leuchtende Fäden zerlegen; die mittlere schwillt an ihrer Spitze zu einem unvollendeten Proto-Schirm, dessen Ränder im Gegenlicht wie flüssiges Gold aufglühen, während ihr Zentrum noch im Schatten reifer Form sucht; die älteste hat ihren vollständigen Reproduktionsschirm entfaltet, eine flache Scheibe aus fusionierten Gametangialstrahlen, deren aufgebogener Rand im Seitenlicht zu smaragdgrünem Buntglas wird und einen präzisen kreisrunden Schatten mit kaustischem Saum auf den Meeresgrund wirft. Jede dieser Strukturen — vom Rhizoidfinger, der in den Kalk greift, bis zur photosynthetischen Kortex, die hinter der kalkimprägnierten Zellwand grünlich schimmert — ist das Werk einer einzigen unteilbaren Zelle, die Wochen und Monate braucht, um diese Architektur aus sich selbst heraus zu errichten. Was hier wie eine botanische Abfolge in Zeitlupe wirkt, ist in Wahrheit das Wachstum dreier Individuen, die das Paradox des Lebens verkörpern: sichtbar, greifbar, monumental — und doch jedes für sich ein einziger Organismus ohne innere Grenzen.

Der Blick fällt auf einen acht Zentimeter hohen Busch aus *Halimeda*, dessen verzweigte Kalkkette sich wie ein versteinertes Korallenbäumchen aus dem hellen Sandboden erhebt – jedes scheibenförmige Segment eine breite, kreidige Raute aus mineralischem Aragonit, dessen matte, fein gegranulte Oberfläche mit ockergelben und goldbraunen Diatomeen-Epiphyten besetzt ist, die im schräg einfallenden Blaulicht wie bernsteinfarbene Funken aufleuchten. Was diesen Organismus zur Besonderheit macht, ist die Tatsache, dass er eine einzige lebende Zelle darstellt – ein coenozytisches Netzwerk ohne innere Trennwände, in dem ungezählte Zellkerne ein gemeinsames Cytoplasma teilen, das sich bis in jeden Ast und jede Gelenkverbindung erstreckt. Genau diese Verbindungspunkte zwischen den Segmenten offenbaren das lebendige Innere: Die vivid-grünen Nodien, an denen die Calcifizierung aussetzt, sind prall mit Chloroplasten gefüllte Zytoplasmabereiche, die im Gegenlicht ein tiefes, sattes Grün abstrahlen. Acht Meter Meerwasser dämpfen das Sonnenlicht zu einem kühlen Türkis-Aquamarin, das flache Reliefschatten über jede mineralische Unebenheit wirft und feines Karbonatmehl – abgeriebenes Material der Segmente selbst – als silberne Partikel durch die Wassersäule tanzen lässt. Im Hintergrund lösen sich die breiten Blätter des Seegrasbestands in ein weiches, lebendiges Bokeh aus Olivgrün und Bernsteingelb auf, das den Raum umschließt wie ein flüsternder, lichtdurchfluteter Vorhang.

Der Blick fällt mitten in eine Katastrophe, die sich in Zeitlupe entfaltet: Zehn Zentimeter über dem Riffboden hängt die eingerissene Hülle einer geplatzten *Ventricaria ventricosa* über einem Klumpen korallinischer Rubble wie das zusammengebrochene Zelt einer einzigen, zerstörten Zelle – eine ledrig-glänzende Membran aus mehrlagigen Cellulosemikrofibrillen, irisierend im schräg einfallenden Tropenlicht, die Ränder nach innen eingerollt und noch feucht vom entweichenden Zellsaft. Aus ihrem Inneren ergießt sich eine langsam treibende Konstellation von Tochterprotoplasten – jeder ein nahezu perfekter Kugelkörper zwischen Sandkorn- und Pfefferkornformat, dicht gepackt mit Chloroplasten, die jeden Sphere smaragdgrün im Kern und zitrinfarbig golden am Rand leuchten lassen, wo das Sonnenlicht durch die dünne Cytoplasmahülle bricht. Die nächstgelegenen Protoplasten sind scharf und fast greifbar nah, ihre Oberflächen zeigen ein körniges, wie Kopfsteinpflaster hinter Mattglas wirkendes Mosaik der darunter liegenden Chloroplasten; weiter hinten lösen sie sich in glühende grün-goldene Punkte auf, wie eine Nebula aus biolumineszenten Funken gegen das helle Preußischblau des offenen Wassers. Was sich hier abspielt, ist biologisch eine reproduktive Strategie – die explosive Fragmentierung eines Rieseneinzellers in Hunderte autonome Tochterzellen, von denen jede, sollte sie sich auf dem Riff niederlassen, ein vollständiger neuer Organismus werden kann –, doch die radiale Geometrie der Ausbreitung und die schiere Zahl der gleißenden Kugeln verleihen dem Ganzen das Wesen einer botanischen Supernova, einer grünen Sternenexplosion, die sich im Maßstab eines einzigen Atemzugs entfaltet.
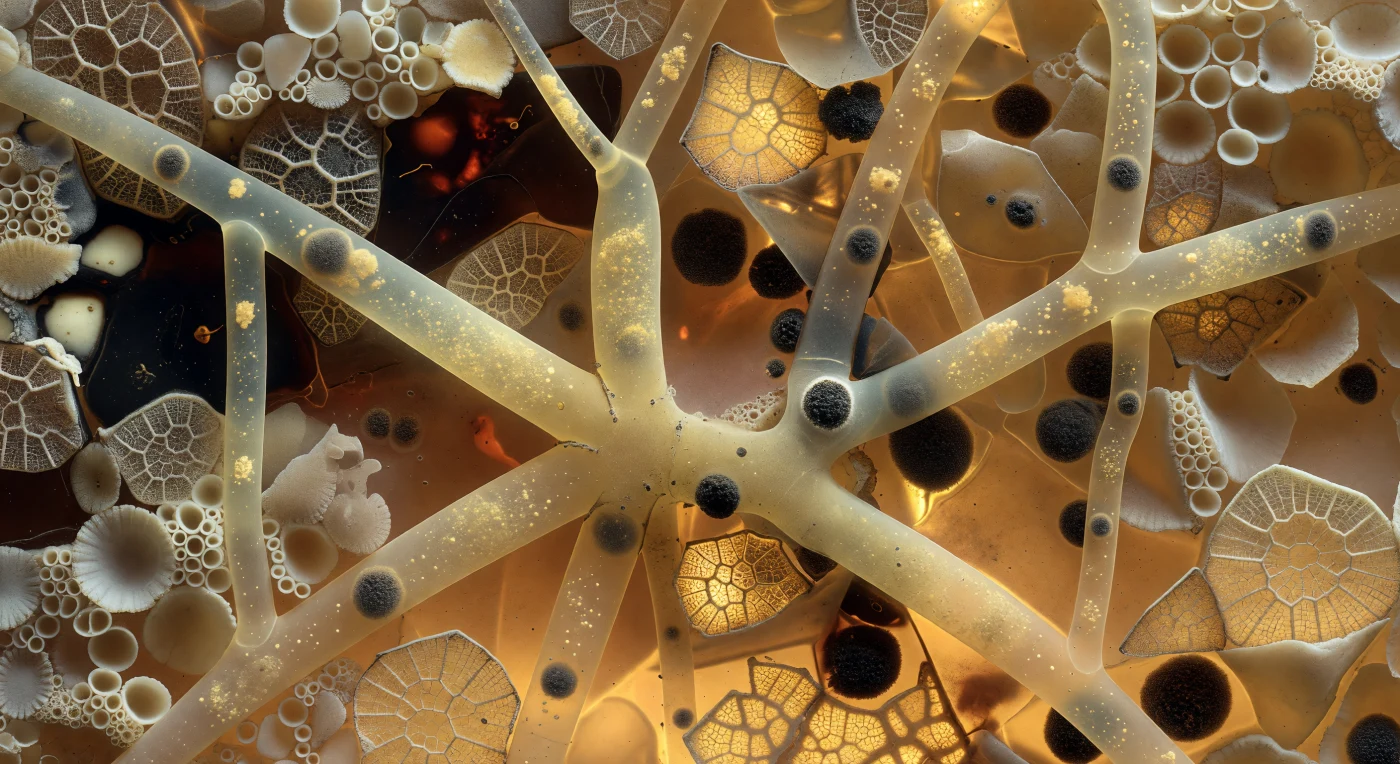
Du schwebst im Inneren eines Xenophyophoren-Tests, einem der größten bekannten Einzeller der Tiefsee, dessen Gehäuse aus fremdartigem Detritusmaterial – inkrustierten Foraminiferen-Schalen, Radiolarien-Gittern und dunkel glänzendem organischen Zement – zu einem mineralischen Mosaik zusammengefügt ist, das zugleich wie Geologie und wie Architektur wirkt. Das warme Bernsteinlicht, das von unten durch das Präparat fällt, taucht Schalen und Kieselgerüste in Töne von Ocker, gebrannter Sienna und tiefem Umbra, als stünde man in einem erleuchteten geologischen Dünnschliff, der aber noch atmet. Die Linellae – jene verzweigten Zytoplasmakanäle, die das gesamte Bauwerk durchziehen und vierzig bis achtzig Mikrometer messen – erscheinen dir hier als breite, transluzente Korridore aus warmem Bernsteinglas, in deren Inneren blassgelbes Zytoplasma mit kaum wahrnehmbarer Langsamkeit fließt. In unregelmäßigen Abständen sitzen darin dunkelgraue Zellkerne wie eingeschlossene Steine, ihr verdichtetes Chromatin schwer und gravitätisch gegen das schimmernde Strömen ringsum. Das Ganze ist ein einziger, weitverzweigter vielkerniger Zellleib – kein Gewebe, kein Kollektiv, sondern ungeteiltes Leben, das sich in seinen eigenen mineralischen Hallen verästelt.
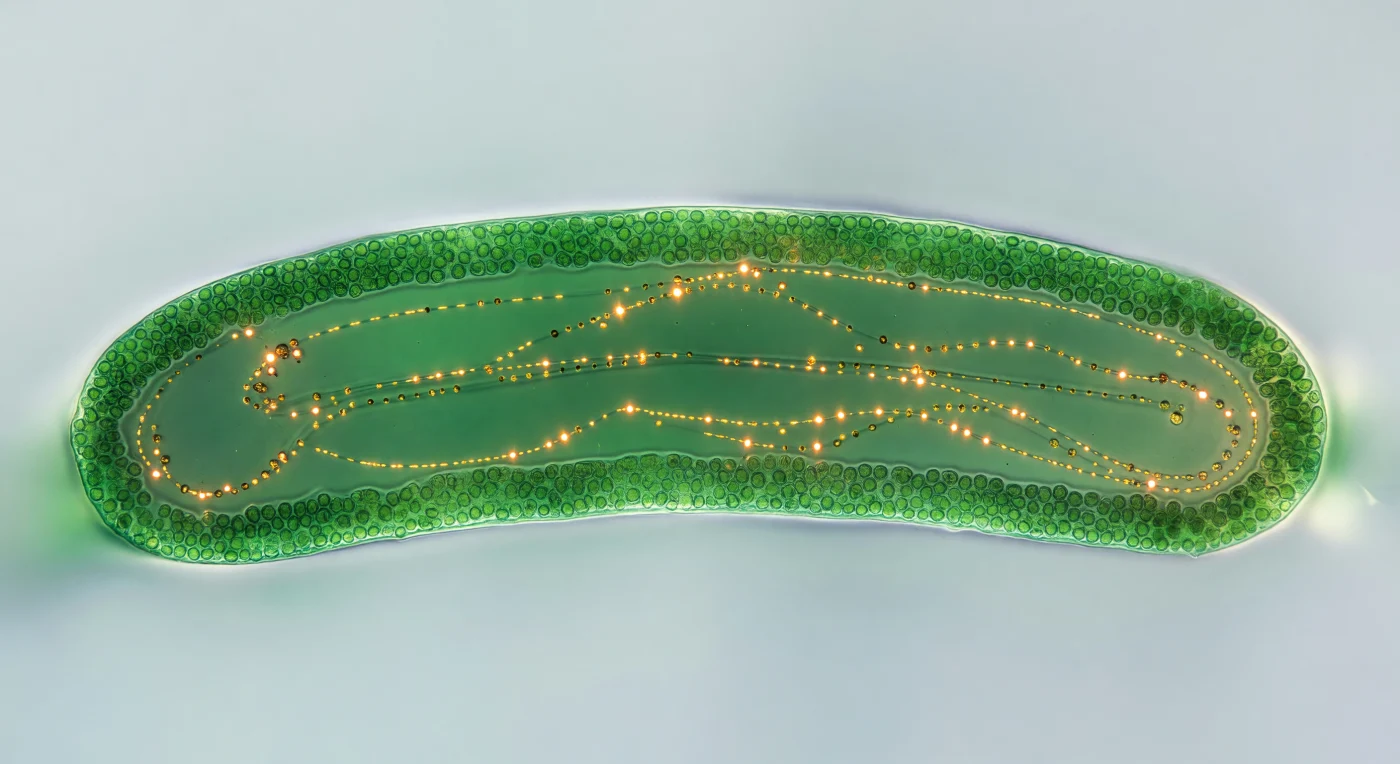
Direkt unter dir wölbt sich ein leuchtendes Grün, das den gesamten Blick ausfüllt — ein einzelnes Caulerpa-Stolon-Segment, gerade zwei Millimeter breit, das auf einer rückbeleuchteten Glasfläche in einer hauchdünnen Schicht Meerwasser ruht und von unten von kaltem, weißem Durchlicht in eine Art lebendes Kirchenfenster verwandelt wird. Der äußere kortikale Mantel, so dicht mit scheibenförmigen Chloroplasten gepackt, dass er wie eine massive Jadewand erscheint, leuchtet in gesättigtem Smaragdgrün und geht zur Mitte hin in ein dunkleres, kühleres Inneres über — den endoplasmatischen Korridor, einen flüssigen Tunnel, der das gesamte Lumen dieser einzigen, riesigen Zelle durchzieht, denn Caulerpa ist ein coenozytischer Organismus: kein Gewebe, keine Zellwände im Inneren, nur ein kontinuierliches Cytoplasma, das von einer einzigen Plasmamembran zusammengehalten wird. In diesem dunkleren Kanal driften bernsteinfarbene und goldene Granula auf langen, sanft geschwungenen Bahnen dahin — manche als scharfe, ruhende Lichtpunkte sichtbar, andere als kurze, ochrefarbene Bewegungsschlieren, die die unsichtbaren Aktinkabel verraten, an denen sie mit einer Geschwindigkeit von nur wenigen Mikrometern pro Sekunde entlanggleiten, der Cytoplasmaströmung folgend, die das Überleben dieser kolossalen Zelle sichert. An der äußersten Grenze des Stolons zeichnet ein schmaler, prismatischer Lichtbogen die Trennlinie zwischen Zellwand und Wasser nach, bevor das beleuchtete Glas ringsum in ein farbloses, strukturloses Weiß verblasst und die Zelle in ihrer eigenen Strahlkraft schweben lässt.

In der blauen Schwärze einen Meter unter der Mittelmeeroberfläche schweben drei Acetabularia-Stiele wie elfenbeinfarbene Miniaturkathedralen über dem Kalksteinsockel — jeder von ihnen eine einzige, ununterbrochene lebende Zelle, deren hauchdünne Schirmkappe aus radialen Segmenten wie Spitze aus Meeresglas aufgefächert ist. Zwischen den Blitzen pulsiert aus ihrem Inneren ein geisterhaftes Graugrün, das Nachleuchten des Chlorophylls, das kaum weiter reicht als ein Handbreit, bevor es in absolutem Blauschwarz erlischt. Dann durchzuckt ein Dinoflagellaten-Blitz die Wassersäule — ein chemisch-scharfes Blauweißlicht, das für den Bruchteil einer Sekunde die Rippenstruktur der Schirmkappen in harte Schatten und Eislicht zerschneidet, die Zellwände als lichtdurchlässige Hülle enthüllt und den granulären Nebel der Chloroplasten im Cytoplasma für einen Herzschlag sichtbar macht, bevor die Dunkelheit alles zurückfordert. Die Partikel im Wasser — eine langsame Galaxie organischen Treibguts — fangen jeden Blitz als winzige Einzelfunken auf und erinnern daran, dass diese Finsternis lebt und bevölkert ist, dass der einzige Takt dieses Ortes das panische Zucken unsichtbarer Organismen weit oberhalb ist, deren Schrecken hier unten das einzige Licht der Welt erzeugt.















