Wissenschaftliche Zuverlässigkeit: Hoch

Der Blick führt geradeaus in einen gewundenen Hohlraum, dessen Wände aus übereinander geschichteten, silbergrauen Smektit-Plättchen bestehen – dünn wie Rasierklingen, ihre Kanten werfen irisierende Lichtreflexe in Grau und zartem Lila an die unregelmäßige Decke –, während eisblanke Quarzblöcke mit internen Bruchflächen das schwache, quellenlose Leuchten zu prismatischen Splittern streuen und bernsteinfarbene Organikfilme alle Mineraloberflächen wie erstarrtes Harz überziehen. Kurz dahinter dominiert die Hyphe des arbuskulären Mykorrhizapilzes den Korridor: ein glasklares, lebendes Rohr mit einem Durchmesser von etwa einem Viertel der Porenwände, dessen transparente Membran in polarisiertem Licht einen Hauch Grünschimmer zeigt, während im Innern träge Lipidglobulen und cremefarbene bis dunklere Granula durch das Cytoplasma driften – Nährstofftransport in Zeitlupe, angetrieben durch Turgor und Cytoplasmaströmung. An den Porenwänden drängen sich in den Winkeln zwischen den Tonplättchen bakterielle Stäbchen in dichten Biofilmmatten zusammen, jedes Individuum etwa ein Fünftel so breit wie die Hyphe, gemeinsam jedoch Teil eines mikrobiellen Milieus, in dem Enzymausschüttung, Signalmoleküle und Mineralverwitterung auf engstem Raum ineinandergreifen. Drei dunkle Seitentunnel öffnen sich in der Ferne, ihre Eingänge von überstehenden Tonplättchen gerahmt, und hinter der nächsten Biegung verschluckt die absolute Dunkelheit des Bodens jede Textur – eine Schwärze, in der alle Orientierung ausschließlich chemosensorisch erfolgt, ohne einen einzigen Lichtstrahl.
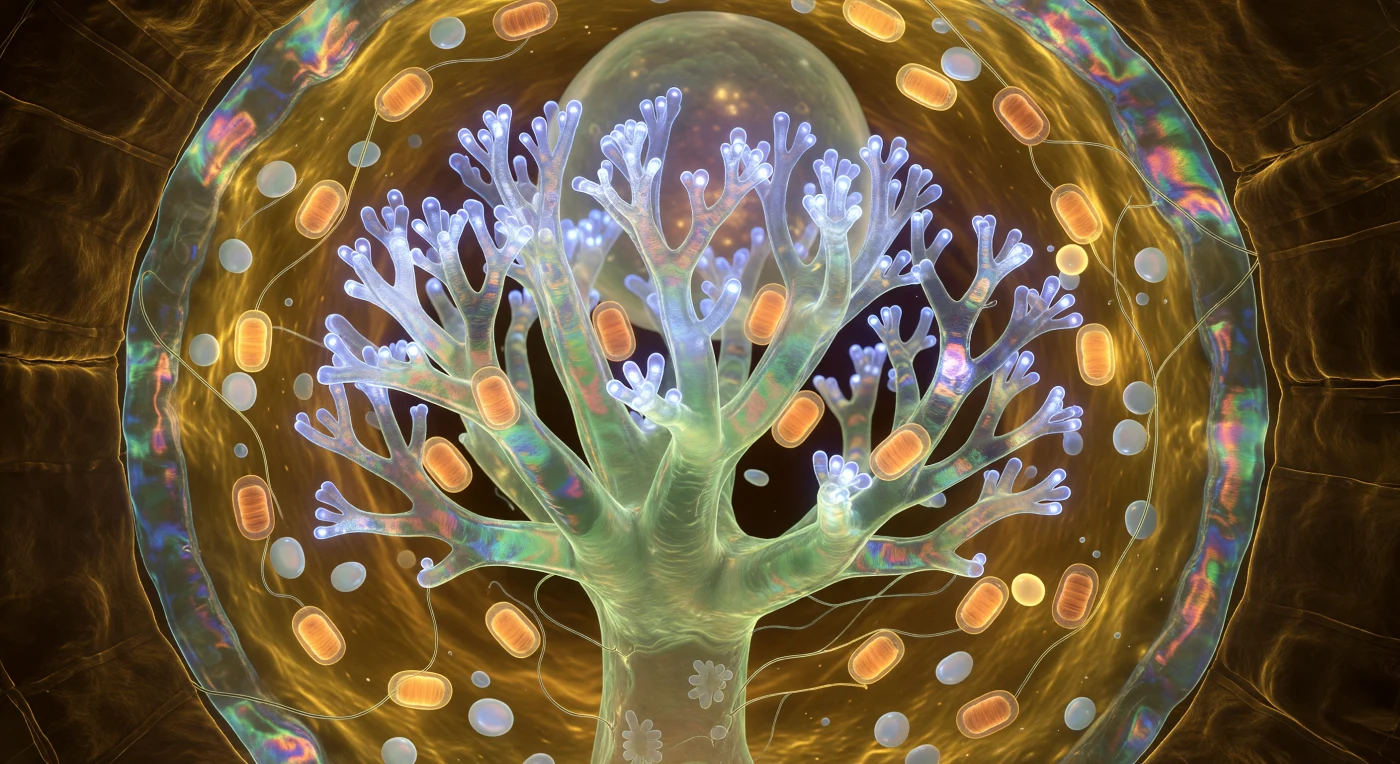
Du schwebst im Inneren einer einzigen lebenden Zelle, und dennoch umgibt dich eine Kathedrale: Der Arbuskel erhebt sich vor dir wie ein umgekehrter Korallenwald aus jade-elfenbeinfarbenem Gewebe, dessen Hauptstamm sich in immer feinere Äste aufzweigt, bis die terminalen Verzweigungen – kaum einen halben Mikrometer breit – in einem zitternden Schleier aus kobaltblau-weißem Licht verschwimmen, das von tausenden aktiver Phosphattransporter-Proteine erzeugt wird, die Schulter an Schulter in die periarbuskuläre Membran eingebettet sind. Diese Membran umhüllt jeden Ast mit der gespannten Logik einer Seifenhaut und schimmert von sich selbst heraus in bernsteingoldenen, blaugrünen und tiefrosafarbenen Interferenzfarben, ein Leuchten rein metabolischen Ursprungs, denn kein einziges Photon der Außenwelt dringt in diese Tiefe des Bodens vor. Zigarrenförmige Mitochondrien drängen sich um den arbuskulären Stamm wie bernsteingelbe Laternen und tauchen das gesamte viskoelastische Cytoplasma, in dem perlmuttartige Amyloplasten wie träge Flusssteine treiben, in ein warmes, goldenes Glühen. An jedem Rand deines Blickfelds erhebt sich die Zellwand als massives, dunkles Bernsteingewölbe, dessen überkreuzte Zellulosemikrofibrillen das blaue Licht des Arbuskels in flachen Winkeln einfangen und eine Topographie wie das Innere eines geschnitzten Holzgewölbes offenbaren – und im hauchdünnen apoplastischen Spalt zwischen äußersten Verzweigungen und Wirtsmembran vollzieht sich in diesem Augenblick ein molekularer Austausch, der Wälder trägt.

Im Querschnitt durch ein sandiges Bodengefüge erhebt sich vor dem Betrachter eine Welt von mineralischer Schwere und lebendiger Filigranität: bernsteinfarbene Glomus-Sporen wölben sich wie lackierte Findlinge aus dem Untergrund, ihre konzentrisch geschichteten Wandlamellen fangen das diffuse Licht in warmem Chiaroscuro, während eine cremefarbene Gigaspora-Spore mit warziger Oberfläche daneben still leuchtet und eine weinrote Scutellospora ihr halbmondförmiges Keimungsschild dem schwachen Lichtfall entgegenhält. Zwischen ihnen ragen Quarzkörner und Rosenfeldspatstücke wie Hochhäuser auf, ihr Inneres von blassen Lichtcaustics durchzogen, und dunkle Flocken zersetzter organischer Substanz bedecken den Bodengrund wie Scherben versteinerten Harzes. Über diese Minerallandschaft hinweg spannen sich transparente Hyphenfilamente — fast unsichtbare Silberfäden, die mehrere Sporen in seichten Katenarkurven miteinander verbinden und so das verborgene Transportnetz des Mykorrhizapilzes materialisieren. Diese Sporen sind die Überdauerungsorgane arbuskulärer Mykorrhizapilze (AMF), jener obligat biotrophen Organismen, die seit über 450 Millionen Jahren mit Landpflanzen koevolvieren und durch ihre weitverzweigten Hyphennetze Phosphat und Wasser gegen photosynthetischen Zucker tauschen. Was wie geologische Stille wirkt, ist in Wirklichkeit der ruhende Pol eines biologischen Systems von kontinentaler Reichweite — jeder Spore innewohnend das Potenzial, ein Netz zu entfalten, das Wurzeln verschiedener Bäume über Meter hinweg verknüpft.
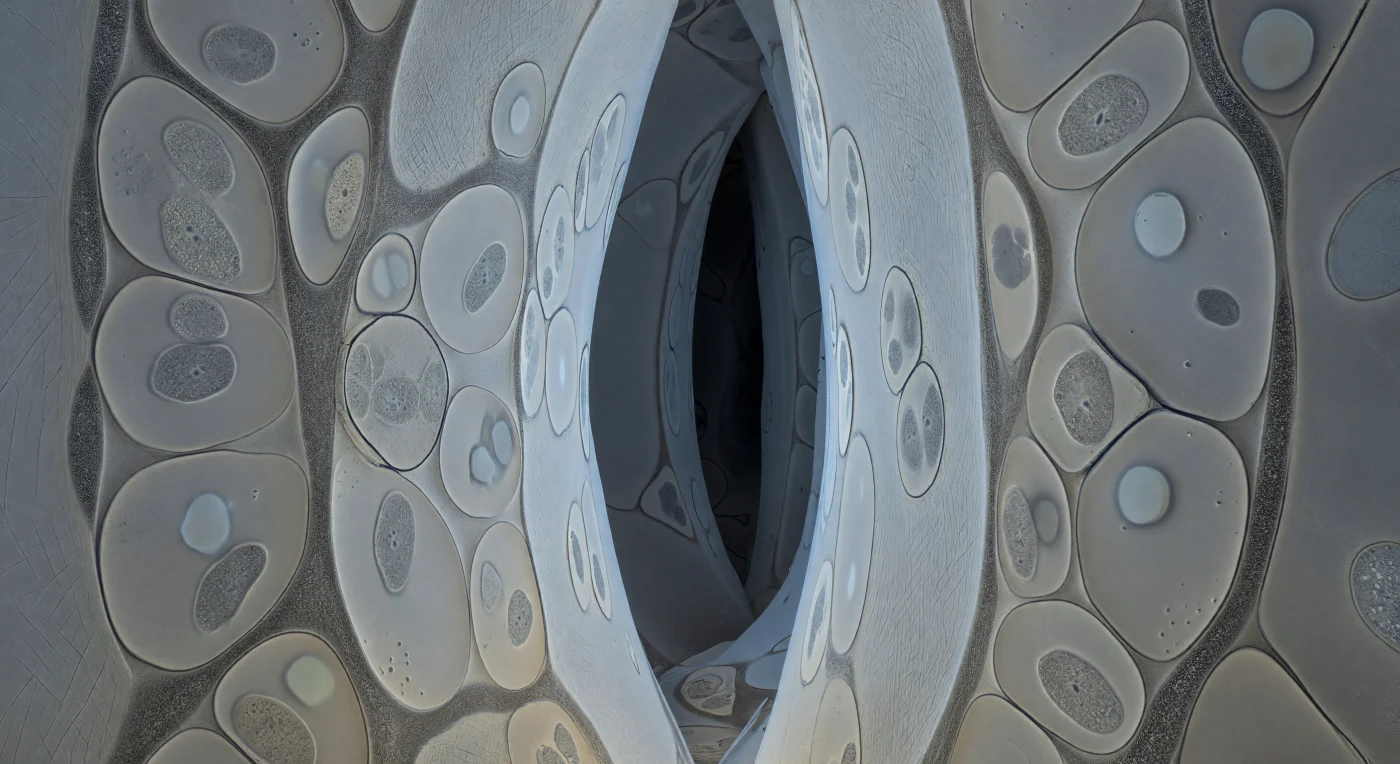
Du schwebst in einem Korridor, der dich von allen Seiten berührt: riesige Ebenen aus bleichcremeweißer Zellulose steigen in sanft gewellten Schichten auf, ihre Oberflächen bei näherer Betrachtung zart fibrillar, die Mikrofibrillen in gekreuzten Diagonalen verlaufend wie das Korn uralten gepressten Papiers. In jeden intercellulären Spalt drängen sich linsenfömige Hyphenquerschnitte, ihre Plasmamembranen als rasierscharfe graphitschwarze Linien gezogen, die eine Membranspannung einschließen, die man fast als physischen Widerstand spüren kann, während das blassgraue Cytoplasma im Inneren von punktförmigen Mitochondrien und kleinen luzenten Vakuolen bevölkert wird. Zwischen Pilzwand und Wurzelzellwand verläuft der 15–25 nm dünne interfaziale Matrixstreifen als feinkörniges Mittelgrau — weder Membran noch Leere, sondern ein ausgehandelter Schwellwert aus Glykoprotein-Netzwerk, an dem Phosphationen die Pilzzelle verlassen und Saccharose von der Pflanze eintrifft. Keine Lichtquelle dringt von außen ein; die Architektur besteht nur durch extremen Strukturkontrast, jeden Interface-Schatten in eine eigene Geometrie verwandelnd, während fernere Korridore in tiefem Schiefer zu dunklen Schlitzen verblassen. Diese enge, labyrinthische Welt — von der Pflanzenwurzel und dem Pilz gemeinsam gebaut und beständig umgebaut — ist der Ort, an dem der kohlenstoffbasierte Handel zwischen Baum und Erde in Echtzeit stattfindet, Molekül für Molekül, im absoluten Dunkel.
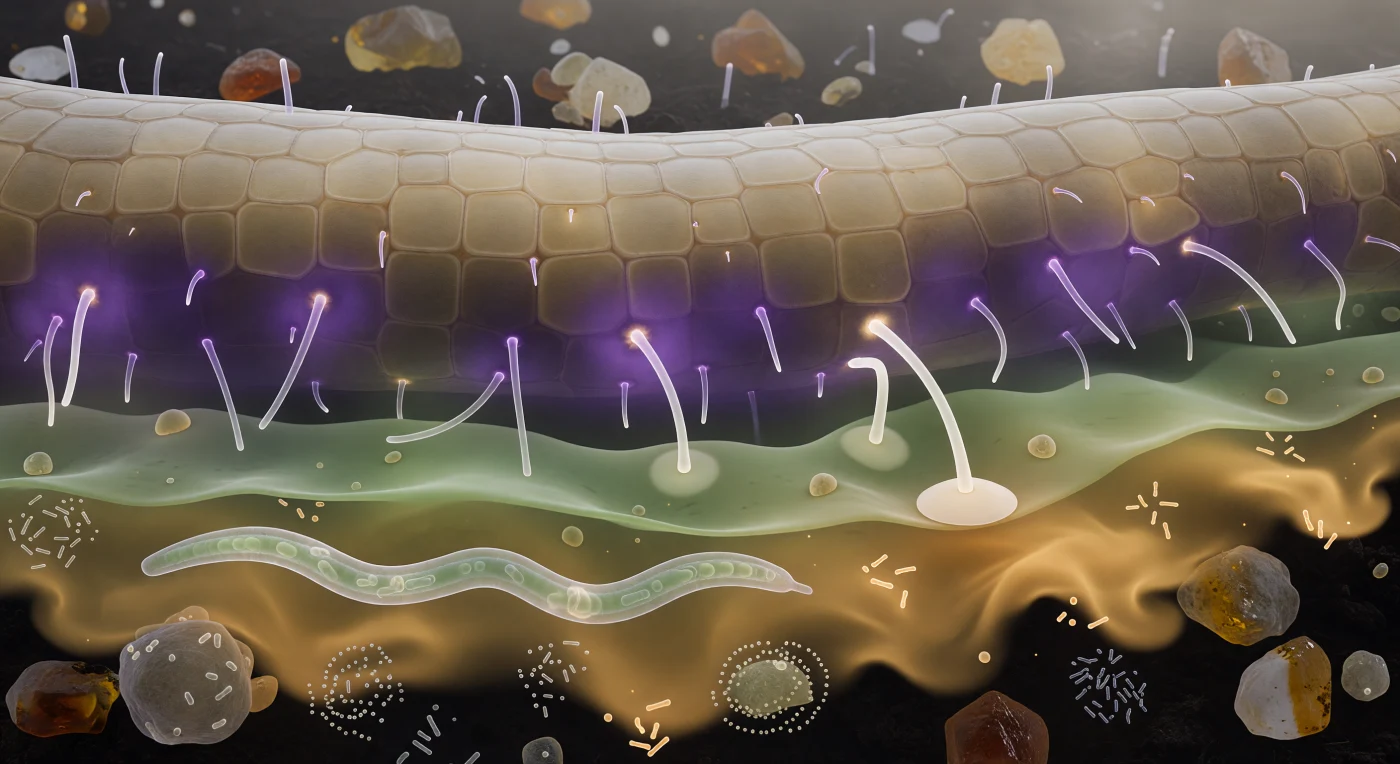
Vor dir wölbt sich die Wurzeloberfläche wie eine blasse Sandsteinwand, deren Epidermiszellen als leicht gewölbte, cremefarbene Kacheln eine subtile Mosaikstruktur bilden, durchbohrt von glasklaren Wurzelhaaren, die das chemische Leuchten der Rhizosphäre als kalte weiße Filamente in sich tragen. Zwischen dir und der Wurzel hat sich das unsichtbare Signalgeflecht in greifbare Atmosphärenschichten verwandelt: ein dichter Violettschleier aus Strigolactonen und Flavonoiden schmiegt sich eng an die Epidermis, dahinter staffeln sich grün-graue Aminosäuregradienten wie Aquarell in nassem Papier, und am weitesten driften bernsteinfarbene Zuckerexsudate in die Dunkelheit des Porenraums – Botschaften, mit denen die Pflanze Pilze, Bakterien und Nematoden gleichermaßen anlockt, zurückweist oder lenkt. Zwei Hyphenspitzen biegen sich messbar durch den grünen Chemogradienten auf die Wurzel zu, dem violetten Signal folgend wie ein Schiff einer Küstenlinie, und eine hat ihr Ziel bereits erreicht: Ihr verbreitertes Ende liegt als flaches Appressorium bündig auf einer Epidermiszelle, beginnt enzymatisch in die Zellwand einzudringen und leitet damit jene intime Symbiose ein, über die Kohlenstoff gegen Phosphat getauscht wird und die den Nährstoffhaushalt ganzer Wälder trägt. Im unteren Bildrand gleitet ein glasklarer Nematode in sinusförmigen Wellen durch spiralförmige Bakterienschwärme, die auf den Aggregatoberflächen pulsieren – eine Gemeinschaft von Organismen, die sich in absolutem Dunkel allein über Chemie orientieren und damit das unsichtbare Fundament terrestrischer Ökosysteme bilden.

Die Oberfläche, auf der man steht, ist kein Boden im gewöhnlichen Sinne: Es ist ein lebendiges Gewebe aus ineinandergreifenden Pilzzellen, dicht gewoben wie handgelegtes Keramikpflaster, cremeweiß an ihren Kernen und an den Nahtstellen von einem schwachen Schwefelgelb durchzogen, das die gesamte Fläche in einem kalten, perlmuttartigen Schimmer aufleuchten lässt. Hinter einem erhebt sich die Wurzelsäule wie die Bordwand eines gestrandeten Schiffes – ein massiver, glattgebogener Wall aus horn- bis dunkelbraunem Rindengewebe, dessen Krümmung so gewaltig ist, dass sie sich lange vor dem fernen Rand im Dunst auflöst, während an der Kontaktzone zwischen Mantel und Wurzelepidermis ein bernsteinfarbenes Glühen die unsichtbare Labyrinthstruktur des Hartig-Netzes verrät, das dort im Inneren sein stilles Werk tut. Zwischen den Zellfugen des Mantels haben sich Tonplättchen und eckige Mineralkörnchen festgesetzt – aus dieser Perspektive riesige Felsblöcke mit organischem Bernsteinfilm überzogen –, und sie pressen sich in die Vertiefungen des lebendigen Gewebes wie Sediment in Mauerfugen. Wenige Körperlängen voraus löst sich das Geflecht in einzelne Hyphen auf, die wie Glasfaserfilamente in den absoluten Schwarz des unkolonisierten Bodenporensystems hineinstrahlen: transparente Röhren, jede nur wenige Mikrometer breit, ihr brechendes Wandmaterial kaum von der Dunkelheit zu unterscheiden, und doch durch das schwache innere Leuchten der strömenden Organellen als helle, tastende Sonden gegen die Leere gezeichnet – das Nervensystem eines Waldes, noch bevor er weiß, dass er einen braucht.
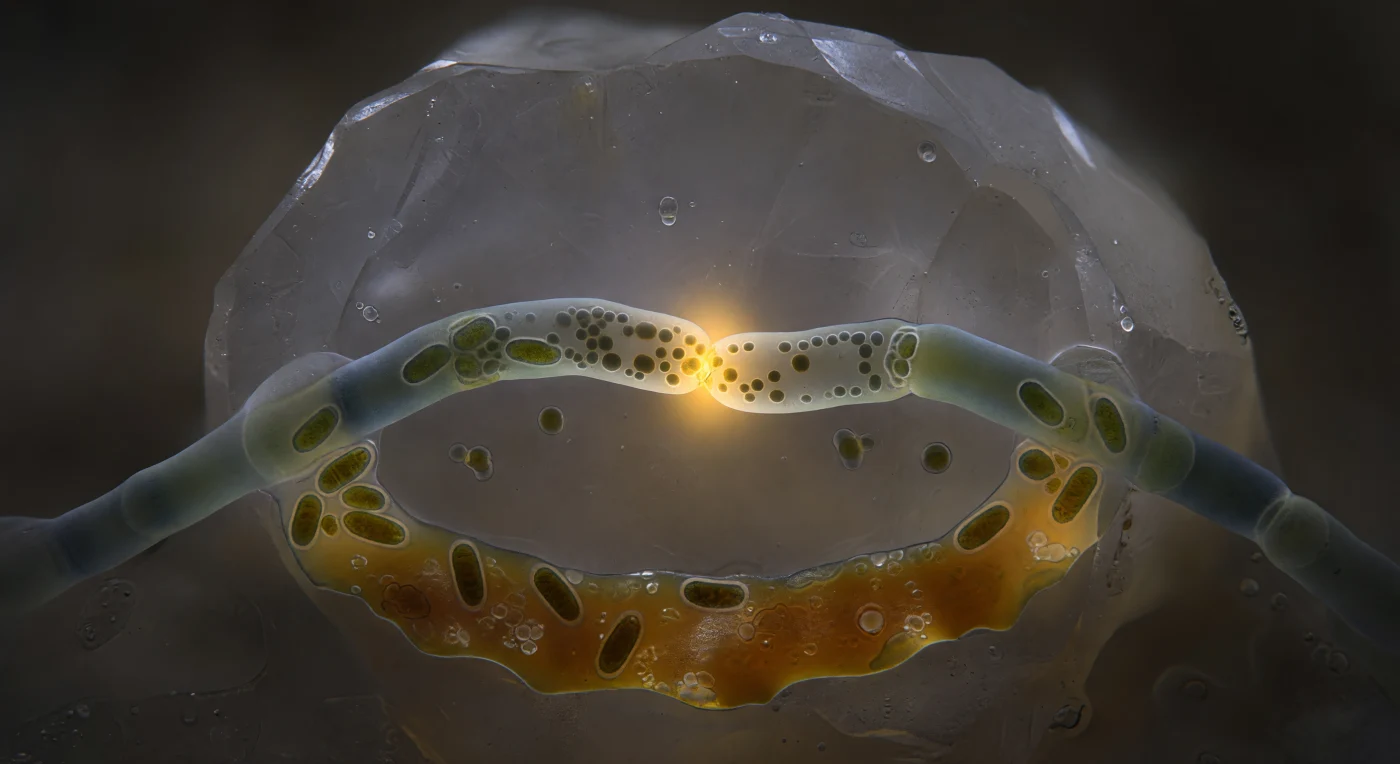
In diesem absoluten Dunkel eines Bodenporus, eng an eine Feldspatwand gedrängt, die wie eine glazial polierte Steilklippe aufsteigt, vollzieht sich einer der fundamentalsten Akte des Pilzlebens: die Anastomose, die Verschmelzung zweier Hyphen zu einem gemeinsamen Netz. Die beiden Schläuche aus Chitin-Glucan-Komposit wölben sich aufeinander zu, jeder kaum fünf bis sechs Mikrometer im Durchmesser, und an der einzigen Kontaktstelle — einem Fusionsporus von anderthalb Mikrometern Weite — haben sich ihre Zellwände ineinandergelöst, die Grenze zwischen zwei Individuen buchstäblich aufgehoben. Dieser Kontaktpunkt leuchtet in einem konzentrierten Bernstein-Gold, dem einzigen Licht in dieser sonst schwarzen Welt: Mitochondrien drängen sich dicht an den Porenrand, ihre Membranen als dunklere Striationen erkennbar, während ein viskoser Strom aus Lipidgranula und Zytoplasma pulsierend von der linken in die rechte Hyphe fließt — Organellen, Ressourcen, möglicherweise genetische Information, alles in einem einzigen kontinuierlichen Fluss. Was hier in einem Porus von vierzig Mikrometern Durchmesser geschieht, ist die mikroskopische Grundlage jener Netzwerke, die Bäume über Hektare miteinander verbinden: Kommunikation, gegenseitige Versorgung und kollektive Resilienz, zusammengebaut aus zahllosen solcher glühenden Berührungspunkte im Dunkeln des Bodens.

Der Blick fällt auf einen einzigen Bodenmakroaggregat, der das gesamte Bildfeld ausfüllt wie ein dunkler Planetenkörper — seine gewölbte Oberfläche aus humifizierter organischer Substanz, melaningeschwärzten Pilzresten und eingeschlossenen Quarz- und Feldspatkristallen erstreckt sich wie die erstarrte Geologie eines vulkanischen Mondes. Ein hauchdünner Glomalinfilm überzieht jede freiliegende Fläche in einem warmen Bernstein-Gold und versiegelt die Oberfläche hydrophob, sodass ein einzelner Wassertropfen kontaktwinkelsteil auf dem Aggregat sitzt und das dunkle Miniaturweltall wie ein konvexer Spiegel zurückwirft. Aus den Stressbrüchen, die die Oberfläche durchziehen, treten weiße Hyphalfäden hervor wie Seidennähte, die das komprimierte Mineral-Organik-Gefüge zusammenhalten — ein strukturelles Prinzip, das Glomalin, das glycoproteinreiche Sekret arbuskulärer Mykorrhizapilze, seit über 400 Millionen Jahren in Böden verankert. Im UV-Inset explodiert die gesamte Aggregatoberfläche in gelbgrüner Fluoreszenz, die das sonst unsichtbare Glomalingerüst in incandeszierendem Relief freilegt — entlang von Graten und Rissen am hellsten, in versenkten Becken dunkler werdend, als würde ein biologisches Kartierungssystem die kohlenstoffgespeicherte Architektur des Bodens sichtbar machen.
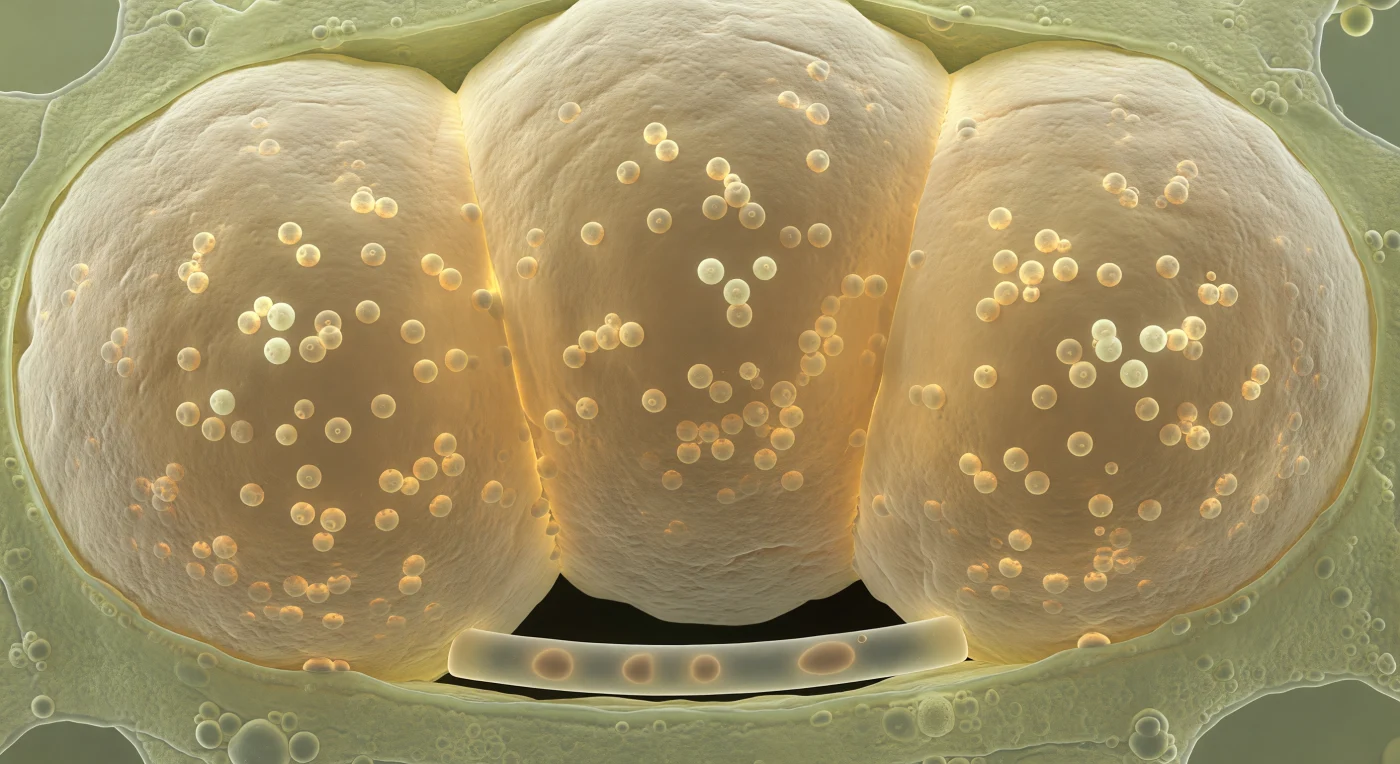
Du schwebst eingeklemmt zwischen drei gewaltigen Vesikeln, die das gesamte Volumen einer Wurzelrindenzelle ausfüllen – blassgelbe Bernstein-Ballons aus verdichteten Chitin-Glucan-Lamellen, deren äußere Wand rau und elfenbeinfarben texturiert ist, bevor sie nach innen in eine glasklare, lichtbrechende Glätte übergeht. In jedem Vesikel hängen Dutzende sphärischer Lipidtröpfchen von fünf bis zehn Mikrometern Durchmesser in einem milchig-viskosen Medium suspendiert, jedes mit einem eigenen goldenen Lichtreflex, als wären Tropfen kaltgepressten Öls in Bernstein eingefroren – dies sind die Fettstoffspeicher des arbuskulären Mykorrhizapilzes (*Glomeromycota*), in denen Triacylglyceride und andere Lipide akkumuliert werden, die als primäre Kohlenstoffwährung zwischen Pilz und Wirtspflanze zirkulieren. Die Vesikel haben sich gegenseitig und die Zellwand so stark gegen sich gedrückt, dass das Zytoplasma der Wirtszelle zu einem dünnen, blassgrünen Film an den Rändern zusammengequetscht wurde, fein granuliert von Ribosomen und Organellen, die kaum noch Raum haben. Zwischen zwei der Vesikel windet sich in Sichtweite eine einzelne intraradikale Hyphe von nur fünf Mikrometern Durchmesser – farblos, straff, von einem dünnen Wasserfilm glitzernd –, die dieses ölgesättigte Depot mit dem unsichtbaren externen Myzel verbindet und daran erinnert, dass dieser innere Tresor kein isolierter Raum ist, sondern ein Knoten in einem Netzwerk, das weit über die Wurzel hinausreicht.
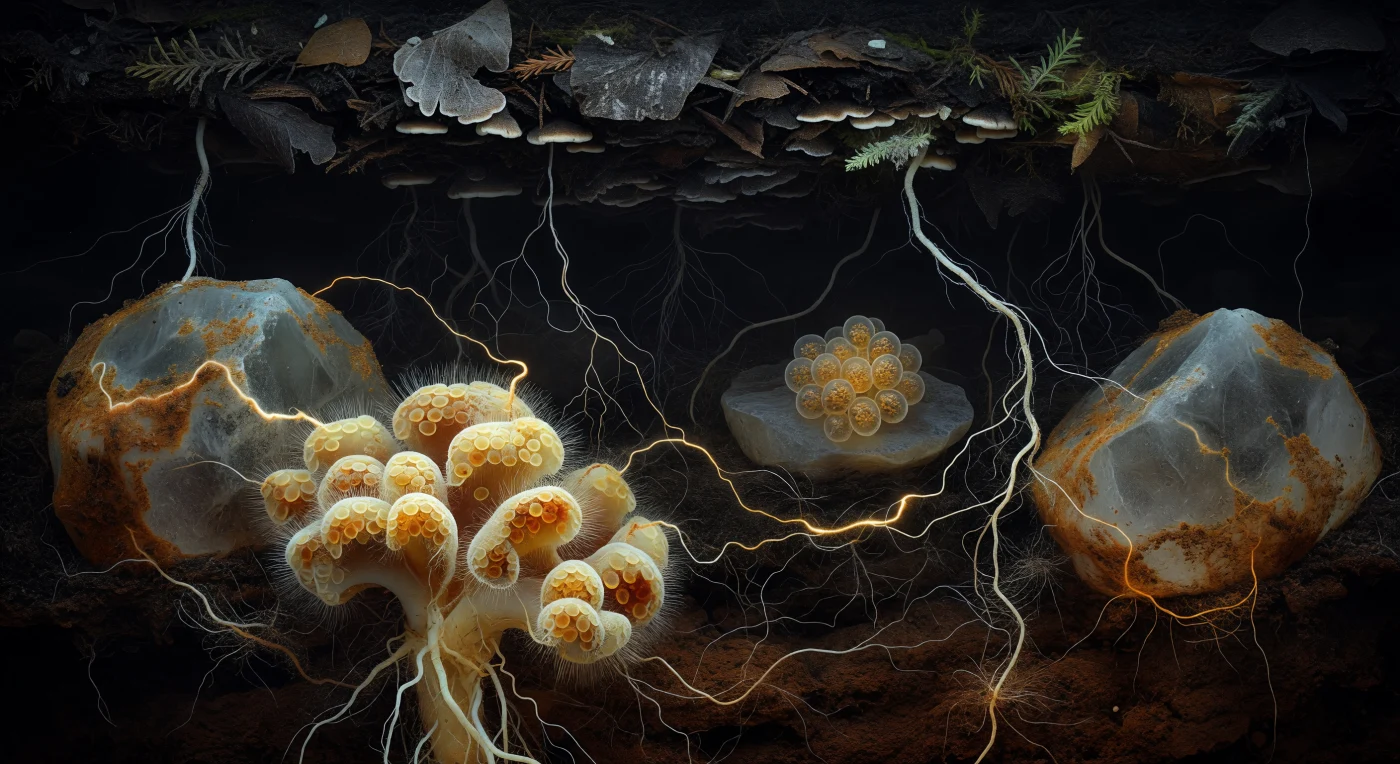
Im Innern des Waldbodens, vergraben unter dreißig Zentimetern humusreicher Dunkelheit, entfaltet sich eine Welt, die kein menschliches Auge je direkt erblickt hat: Zwischen zwei mächtigen Quarzkörnern — in dieser Perspektive so massiv wie Kathedralen — schwebt man in absoluter Schwärze, in der allein chemische Gradienten als fahles Leuchten sichtbar werden. Den Vordergrund beherrscht ein ektomykorrhizaler Wurzelspitzencluster wie eine barocke Korallenformation, sein Mantelgewebe in Butter-Gelb, Cremeweiß und Rostockra geschichtet, jede Zellfacette von einem feuchten Glanzfilm überzogen, während extraradikale Hyphen wie Haare in einer unsichtbaren Strömung nach außen strahlen — eine spezialisierte Symbiose, bei der der Pilz der Feinwurzel eine zweite Haut wächst, die deren Absorptionsfläche um das Hundertfache vervielfacht. Durch den Mittelgrund zieht sich das Gemeinsame Mykorrhizale Netzwerk wie dreidimensionaler Raureif: hauchfeine weiße Fäden, kaum breiter als ein gezogener Strich, weben sich durch die dunkle Bodenmatrix und verbinden Buchen-, Fichten- und Eichenwurzeln über Zehnzentimeter hinweg, während warmes Bernsteinleuchten in einigen Strängen den Fluss von Photosynthesezucker aus dem Kronendach verrät — ein aktiver Gütertransport, der Kohlenhydrate, Stickstoff und Phosphor zwischen konkurrierenden Bäumen verschiedener Arten umverteilt. Im Hintergrund verlieren sich die Fäden in der absoluten Schwärze des mineralischen Untergrundes, dort wo die fast schwarze Humusschicht in das rötlich-braune Mineralreich übergeht und das Netzwerk in Stille auflöst.

Vor dir wölbt sich der Querschnitt eines Rhizomorphen wie der freigelegte Grundriss eines vergrabenen Kabels – ein biologisch konstruiertes Rohr von 1,5 Millimetern Durchmesser, das in völliger Bodenfinsternis liegt und dennoch eine innere Architektur von erstaunlicher Präzision trägt. Der äußere Rand besteht aus melanisierten Zellen, deren Wände so dicht mit dunkelbraunem Schutzpigment durchsetzt sind, dass sie schwarzem Obsidian gleichen – eine biologische Rüstung, die Feuchtigkeit reguliert, mechanischen Druck abfedert und chemischen Angriff durch Bodenmikroorganismen abwehrt. Darunter öffnet sich die Medulla in eine Reihe großlumiger, dünnwandiger Leitungszellen, deren weite, mit Vakuolen gefüllte Innenräume den Ferntransport von Wasser, Zuckern und Stickstoffverbindungen zwischen Baumwurzel und äußerem Myzel ermöglichen – ein Versorgungsstrom, der sich unsichtbar und kontinuierlich durch den Boden zieht. Im axialen Kanal im Inneren der Struktur sammelt sich kondensiertes Wasser als feiner Feuchtigkeitsfilm, während nach außen hin feine Satellithyphen zwischen Quarzkörnern und organischen Partikelfilmen verschwinden, als versenkten sich Glasfasern in die Erde – unsichtbare Verbindungsleitungen eines Netzwerks, das ganze Baumgemeinschaften ernährt.

Im Abstand eines Staubkorns über der Bodenoberfläche entfaltet sich eine Landschaft von beinahe geologischer Wucht: Quarzkörner ragen als bernsteinfarbene Monolithe auf, ihre Flanken mit Eisenoxidfilmen in Rostbraun und dunklem Ocker überzogen, während schwarze organische Masse die Zwischenräume wie Teer verfüllt. Aus einer zentralen Läuferhyphe breitet sich ein lebendiges Flussdelta aus – jüngste Spitzen dicht mit Cytoplasma gefüllt, bleichweiß und transluzent wie Glasfasern, die durch nasses Obsidian getrieben werden, ältere Segmente dahinter perlschnurartig gegliedert durch große Vakuolen, in deren Bäuchen sich Lipidreserven als schwaches Gelblich verdichten. Einzelne Hyphen zwängen sich fadenförmig durch Engen von kaum acht Mikrometer, ihre Querschnitte leicht oval verformt, das cytoplasmatische Leuchten an der Verengung wie zusammengepresstes Licht; andere spannen sich frei über offene Makroporen wie Hängebrücken zwischen Kliffwänden. Auf cremefarbenen Kalzitkristallen verewigen sich ringförmige orange-gelbe Auflösungshöfe dort, wo Oxalsäure das Mineralgitter aufbricht – ein chemisch-warmes Schwefellicht gegen das biologisch-kalte Blauweiss der Hyphenspitzen. Weit im Hintergrund, kaum aufgelöst durch Schichten aus Partikeln und organischen Filmen, wölbt sich die blasse Wand einer Wurzelhaarzelle wie eine Klippe am Horizont: der stille Zielpunkt, auf den sich jede einzelne Spitze ausrichtet, als trüge das gesamte Netzwerk eine einzige, molekular kodierte Richtungserinnerung in sich.
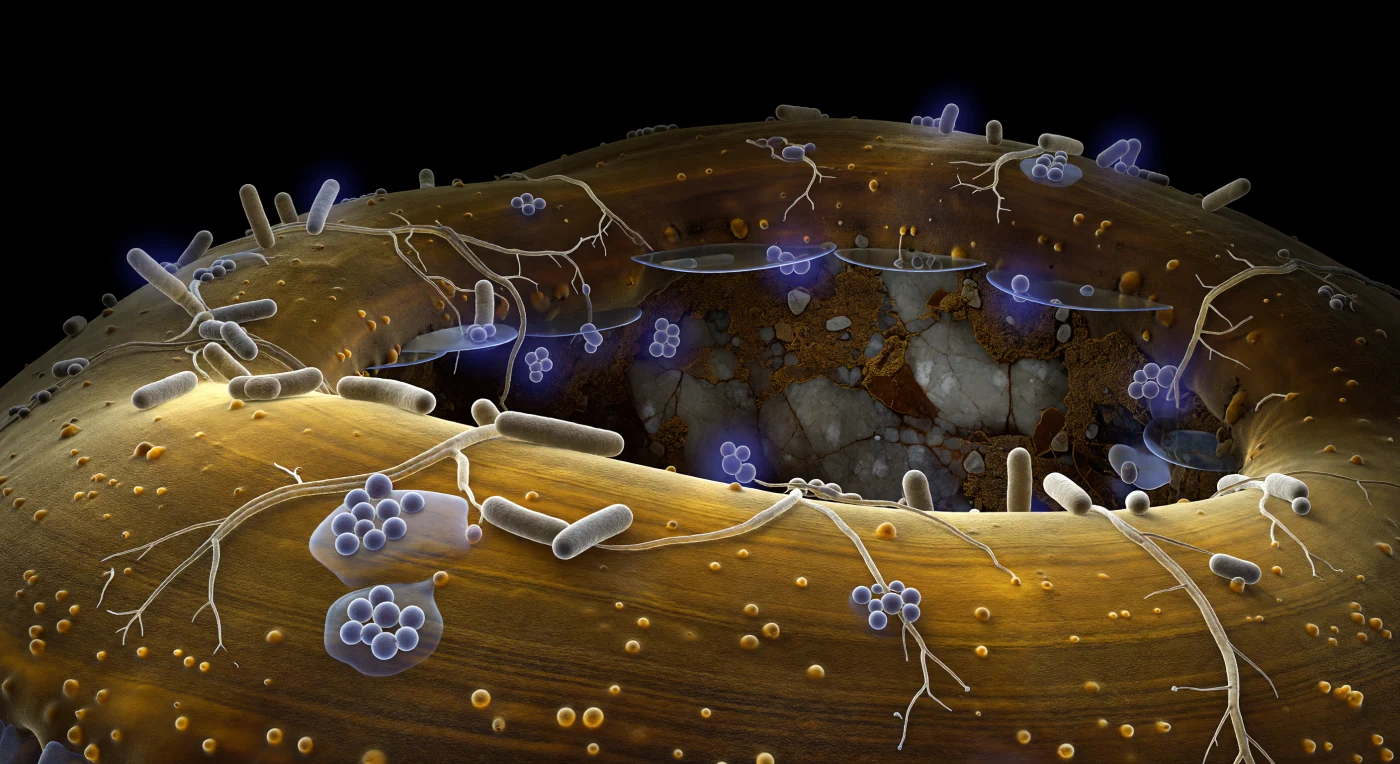
Die gewaltige, geschwungene Wand der ektomykorrhizalen Hyphe füllt das untere Bildfeld wie der Flankenabhang einer riesigen, honigfarbenen Klippe – ihre chitinöse Oberfläche schimmert von innen beleuchtet in warmen Bernstein- und Toffeétönen, da das Cytoplasma darunter ein schwaches, chemisches Licht aussendet, das die lamellierten Wandschichten wie poliertes Harz durchleuchtet. Überall auf diesem mikrobischen Küstenrelief heften sich Bacillus-Stäbchen und fein verzweigte Streptomyces-Fäden an die Hyphenoberfläche, gehalten von kaum sichtbaren Exopolysaccharid-Schlingen, die kurz aufleuchten, wenn das Zytoplasmaglühen den richtigen Winkel trifft – diese Bakterien der sogenannten Hyphosphäre gelten als „mycorrhiza helper bacteria", da sie das Pilzwachstum fördern, antibiotisch wirken und Nährstoffe mobilisieren. Einige Bakterienzellen sind von zarten violetten Diffusionshalos umgeben – in Falschfarbe dargestellte Signalmoleküle, die sich in konzentrischen Gradienten durch dünne Wasserfilme ausbreiten, bevor sie in der absoluten Dunkelheit des Bodenporus verblassen. Im Hintergrund zeichnet sich in undurchdringlichem Schwarz die kantige Oberfläche eines Feldspat-Mineralkorns ab, dessen sporadische glimmerartige Reflexe nur dann aufleuchten, wenn ein spiegelglatter Wassermeniskus das Cytoplasmaglühen über den Porenraum hinweg einfängt. Gravitationskräfte sind hier irrelevant; es sind Oberflächenspannung, chemische Gradienten und molekulare Adhäsion, die diese lebendige Architektur aus Pilzwand, Bakterienfilm und Bodenmineralik zusammenhalten.

In der absoluten Dunkelheit eines Bodenspalts irgendwo unter einer gemäßigten Wiese füllt der Orchideensamen dein gesamtes Blickfeld wie ein durchscheinendes Luftschiff aus — seine Samenschale eine einzige, seifendünne Membran aus gespenstischer Irisierung, die das fahle Licht der Porenwasserchemie in Silber und blassgrüne Interferenzfarben bricht, während dahinter der Embryo als lockere Ansammlung farbloser, kugeliger Zellen leuchtet, jede einzelne so warm und gedämpft wie eine Papierlaterne, ein Organismus in metabolischer Wartestellung. Die goldbraune Rhizoctonia-Hyphe, die von unten links eindringt, wirkt in diesem Maßstab wie ein massiver lackierter Zylinder aus Chitin — ockerfarben bis umber an den Septenknoten — und an der Eintrittsstelle zieht sich die Samenschale in einem engen, vernarbten Annulus zusammen, während im Inneren einer Embryozelle das Peloton den gesamten Zellraum ausfüllt: eine schwindelerregend dichte Spirale aus Hyphenfäden, aufgerollt wie eine Uhrfeder, deren äußerste Windungen die Zellwand sichtbar verformen und die von einer langsamen chemischen Wärme erleuchtet werden — dem molekularen Verhandlungsprozess zwischen Invasion und Allianz. Die unmittelbar benachbarten Embryozellen sind bereits im Begriff, sich zu verändern: ihre Membranen straffen sich, und ihre innere Leuchtkraft verschiebt sich von kühlem Silberweiß zu einem wärmeren Cremegold, den ersten Schritten der Differenzierung. Das schwarze Mineralgestein ringsum — Basalt und Quarz, ihre Oberflächen mit bernsteinfarbenen Humusfilmen überzogen — drängt wie brutalistisches Mauerwerk von allen Seiten heran und verstärkt den schwindelerregenden Maßstabskontrast zu dieser fragilen, transparenten Kugel des werdenden Lebens.

In der Dunkelheit unter dem frisch gestorbenen Baum öffnet sich eine Welt aus zersplitterndem Rindengewebe, schwebenden Sporen und einem Geflecht aus silbrigen Hyphen, die noch immer Nährstoffe zwischen den überlebenden Bäumen transportieren. Die Wurzelrinde über dem Betrachter zerfällt in schokoladenbraune und fast schwarze Fetzen, aus deren Rissen AMF-Sporen in Zeitlupe herausrollen – bernstein- und weinrot leuchtende Körper, die an Felsbrocken oder kleinen Häusern erinnern, ihre dicken Wände teilweise bereits geborsten und Lipidflüssigkeit in den umgebenden Wasserfilm freilassend. Glomalin, das klebrige Glykoprotein der arbuskulären Mykorrhizapilze, überzieht jeden Mineralkornspar wie eine halbdurchsichtige Harzschicht aus rohem Honig und macht die Quarzpartikel – hier in der Größe von Bürohochhäusern – zu schwach leuchtenden Laternen der chemischen Zersetzung. Während das saprotrophe Myzel mit seinen auffällig dickeren, cremefarbenen und verzweigungswütigen Hyphen die tote Rinde kolonisiert, nähern sich von links und rechts zwei mykorrhizale Netzwerke – eines blassgelb, eines cremeweiß –, angelockt von der Nährstoffdichte dieser biologischen Katastrophe. Was sich hier vollzieht, ist kein stiller Tod, sondern ein präziser ökologischer Umbau: Das Kohlenstoff- und Phosphornetz des Waldes reorganisiert sich im Verborgenen, Millimeter für Millimeter, durch chemische Signale und hyphal gewebte Solidarität.















